超小釕原子簇負載III-V族氮化物納米線光催化固氮反應
吳凱
北京大學化學與分子工程學院,北京 100871
氮元素是構成生命體的一種基本元素,廣泛存在于蛋白質、氨基酸及核苷酸中。由于穩定的氮氮三鍵的存在,絕大部分的有機體都無法直接利用大氣的主要成分氮氣。自然界中利用固氮細菌活化氮氣,是將氣態的游離氮分子轉變為可被動植物吸收的化合態氮的主要過程,也被認為是比肩光合作用的另一種重要生化過程1。人工固氮合成氨反應(N2+ 3H2→ 2NH3),也稱Haber-Bosch法,從發現距今已過百年。制備得到的氨氣接下來可以繼續轉化為硝酸,氮肥,含氮炸藥等重要化工原料,對人類社會的進步具有重大意義。不過,該方法基于鐵基催化劑,需要在高溫高壓條件下才能實現較快的動力學過程,每年會消耗世界能源總量的1%以上。作為一個放熱反應,開發較低工作溫度的高效氮氣活化催化劑,能在降低能源消耗的同時獲得熱力學的優勢,提高平衡轉化效率,是目前國際催化領域的熱點和前沿課題之一。
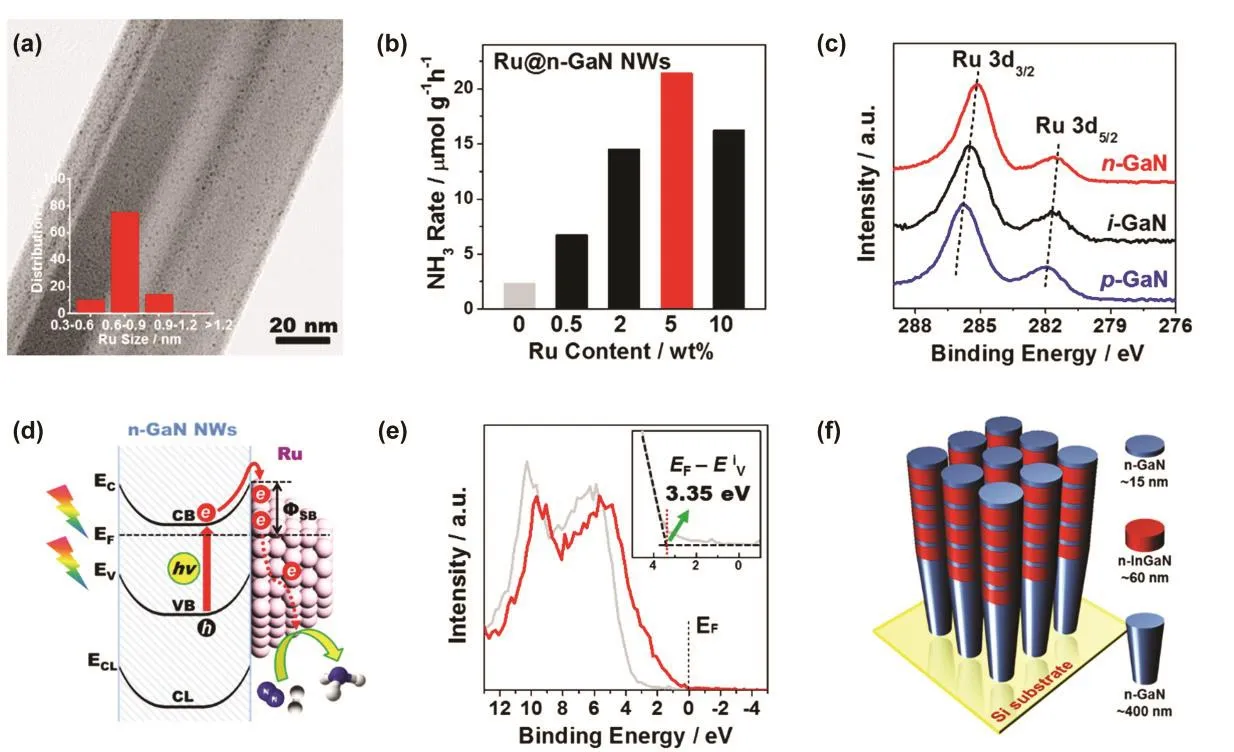
最近,加拿大麥吉爾(McGill)大學李朝軍教授與 Zetian Mi教授課題組聯合設計了一種超小釕原子簇負載的III-V族氮化物納米線陣列,實現了常溫常壓條件下的光驅動合成氨催化過程。利用5% Ru負載的n型氮化鎵納米線陣列,在10 °C紫外光輻照條件下,每小時每克催化劑能夠催化轉化 120 μmol的氨氣(2400 μmol?h?1?g?1),催化轉化效率是相同條件下參照催化劑的5倍2。在催化壽命測試中,該催化劑表現出良好的循環穩定性,8次循環后催化活性依然保持在80%以上。對催化劑結構表征表明,在5% (w,質量分數)負載量的條件下,氮化鎵表面的金屬Ru團簇尺寸均一,高度分散,粒徑僅僅為0.8 nm,遠遠低于傳統金屬Ru基催化劑(3–5 nm)。繼續增加金屬Ru的負載量到10% (w),團簇的尺寸依然保持在了1.5 nm左右,無明顯團聚發生。由于n型GaN半導體的功焓(4.1 eV)要小于金屬Ru的功焓(4.7 eV),當金屬Ru與n型GaN半導體復合時,部分電子會從GaN注入到金屬Ru,從而使金屬Ru帶有一定量的負電;另一方面,GaN的能帶在表面附近向上彎曲,達到平衡后,會在金屬與半導體的界面處形成Schottky能壘,高度經測定約為0.94 eV,其存在能夠顯著增強半導體的光致電荷分離效率。通過XPS測試可以發現,負載在n型GaN表面的Ru的電子束縛能要明顯低于負載在i型或p型GaN表面的Ru,表明載體與金屬之間的相互作用能夠明顯改變金屬催化中心的電子結構,從而進一步影響其催化活性。具有較低電子束縛能的金屬Ru團簇對于氮氣分子具有較強的 back donation作用,通過與氮氣分子進行配位,能夠有效的削弱其氮氮三鍵,是催化劑優異的低溫催化性能的根本原因。此外,通過向GaN中摻雜銦元素制備出三元InGaN材料,其禁帶寬度從之前的3.4 eV降低到2.3 eV。利用InGaN負載的Ru催化材料,能夠在室溫可見光照條件下,實現氮氣分子的活化。
該研究工作近期已在 Angewandte Chemie International Edition上在線發表3,該工作開發了具有高效氮氣活化反應性能的新型光催化劑,為常溫常壓合成氨氣催化體系的設計提供了新的思路。
(2) Zeng, H.; Terazono, S.; Tanuma, T. Catal. Commun. 2015, 59, 40.doi: 10.1016/j.catcom.2014.09.034
(3) Li, L.; Wang, Y.; Vanka, S.; Mu, X.; Mi, Z.; Li, C.-J. Angew.Chem. Int. Ed. 2017, doi: 10.1002/anie.201703301.

