荷斯坦奶牛乳腺干細胞的成神經誘導鑒定及催乳素對其增殖活性的影響
劉迎春,陳鈺萌,韓哲先,高 峰,周歡敏
(1.內蒙古農業大學生命科學學院,呼和浩特 010018; 2.內蒙古自治區生物制造重點實驗室,呼和浩特 010018;3.內蒙古農業大學動物科學學院,呼和浩特 010018)
動物的乳腺是一種能夠反復經歷發育、功能分化和退化的組織,早在胚胎期乳腺就己經開始發育[1]。奶牛的乳腺發育經過胚胎期、青春期前、青春期后、妊娠期、泌乳期及干乳期6個時期[2],這一過程是奶牛泌乳性能發揮的決定性過程。然而在乳腺的生長發育過程中,乳腺干細胞(Mammary stem cells, MSCs)對于青春期、妊娠期、泌乳期和泌乳衰退期的乳腺生長與重建具有重大意義[3]。乳腺干細胞由多種類型的上皮細胞組成,生長發育于動物的乳腺之中的一種處于靜止期的,未分化的細胞,其特點為自我增殖、自我更新和多向分化。其可以分化為所有類型的乳腺細胞[4],特別是具有向不同胚層來源細胞跨越分化的能力,跨越分化的研究,更有助于揭示細胞分化的機制。同時,乳腺干細胞的增殖對乳腺的生長、分化和再生也有十分重要的作用,尤其是在動物妊娠期、泌乳期和泌乳衰退周期中[5],是研究器官形成、細胞分化研究的理想模型。近年來的研究顯示[6],激素、生長因子、細胞因子及細胞外基質組分是干細胞分化增殖所必須的。乳腺的泌乳功能同樣依賴激素的調控,尤其是催乳素(Prolactin,PRL)的調控作用[7]。催乳素是一種蛋白質激素,由垂體前葉腺嗜酸細胞分泌,與其受體結合后,引發催乳素介導的細胞信號轉導通路[8],從而促進乳腺發育,發動并維持泌乳[9]。但是,催乳素如何促進奶牛乳腺干細胞向乳腺細胞發育分化,完成乳腺生長與重建的機理仍不清楚。由于干細胞在體外經化學誘導后具有跨胚層分化的能力[10],所以體外誘導法也是鑒定干細胞的常用方法。因此,本研究在已分離純化的荷斯坦奶牛乳腺干細胞基礎上,利用體外誘導法來誘導乳腺干細胞分化為神經細胞,旨在鑒定分離純化得到的荷斯坦奶牛乳腺干細胞具有跨胚層分化的能力,即多向分化潛能;并用催乳素刺激乳腺干細胞,以探討催乳素對其增殖的最適濃度,以期為催乳素調控乳腺干細胞在奶牛乳腺重建過程及泌乳性能的最大發揮提供理論依據。
1 材料與方法
1.1 材料
本實驗室提供的已分離純化的P3代荷斯坦奶牛乳腺干細胞[11]。DMEM/F12(SH30023.01B)、胎牛血清(FBS,SV30087.01)、PBS(SH30256.01B)均購自 HyClone 公司;青霉素(00212226)、鏈霉素(03032507)均購自華北制藥公司;胰蛋白酶(T4799)、催乳素(268615-1G)均購自 Sigma 公司;Insulin-Transferrin-Selenium(907606)購自Gibco公司;β-巰基乙醇(MB0338)購自BBI公司。尼氏染色試劑盒(DK0021)購自北京雷根生物公司;MTT (T0793)、二甲基亞砜(DMSO,0231)均購自Amresco公司。
1.2 方法
1.2.1乳腺干細胞的復蘇自液氮中取出P3代乳腺干細胞,迅速放到37 ℃水浴鍋中,鑷子夾住凍存管震蕩,直至凍存液溶解后拿出。75%酒精擦凈管口后,迅速移進超凈工作臺,吸出細胞凍存液,移到1.5 mL離心管,1 500 r·min-1離心5 min,棄除上清液,用干細胞培養液(DMEM/F12 +10%FBS +1%PS+EGF 20 ng·mL-1+ ITS 10 μL·mL-1)重懸細胞,將細胞接種到培養皿中,移入37 ℃、5%CO2培養箱培養。
1.2.2乳腺干細胞的傳代培養待細胞長到70%~80%融合時,酶消化法傳代培養。棄掉培育細胞時的細胞培養液,加適量的有雙抗(青霉素+鏈霉素)的PBS溶液清洗2遍后,棄掉,向培養皿中加入1 mL 0.25%胰蛋白酶消化細胞,待消化1~5 min,向培養皿中加入等體積培養液,停止消化。將上述細胞懸液轉移入1.5 mL的離心管中,1 500 r·min-1離心5 min,棄除上清,干細胞培養液重懸細胞,細胞計數(細胞計數板法,細胞數/mL=4個大格細胞總數/4×(104·mL-1)。
1.2.3乳腺干細胞成神經誘導 取上述傳代的細胞接種于12孔板中;顯微鏡觀察待細胞貼壁生長為50%~60%融合的時候,隨機分為對照組和試驗組,試驗組加入神經預誘導液(DMEM/F12 +10%FBS +1 mmol·L-1β-巰基乙醇),對照組加入普通培養液(DMEM/F12 +10%FBS +1%PS),置37 ℃、5%CO2培養箱中誘導24 h。24 h后,取適量PBS,清洗1遍,試驗組加入神經誘導液(DMEM/F12 +10%FBS +3 mmol·L-1β-巰基乙醇),對照組不變,置37 ℃、5%CO2培養箱中繼續培養,每天更換培養液1次,每天注意在熒光顯微鏡下觀察細胞生長形態的變化,并使用尼氏染色,試劑盒染色,鑒定神經細胞。
1.2.4乳腺干細胞誘導分化為神經細胞特異表達基因鑒定神經微管蛋白Ⅲ(β-TubulinⅢ)和神經元特異性烯醇化酶(NSE)為神經細胞的特異表達基因,利用Priemer 5.0軟件設計合成引物,并由生工生物工程(上海)有限公司合成(表1)。首先用RNAiso Plus裂解已誘導的乳腺干細胞,然后提取總RNA,并反轉錄為cDNA,通過PCR體系和1%瓊脂糖凝膠電泳進行鑒定。
表1神經細胞標記基因引物序列
Table1Theprimerssequenceofmarkergeneinneuralcell
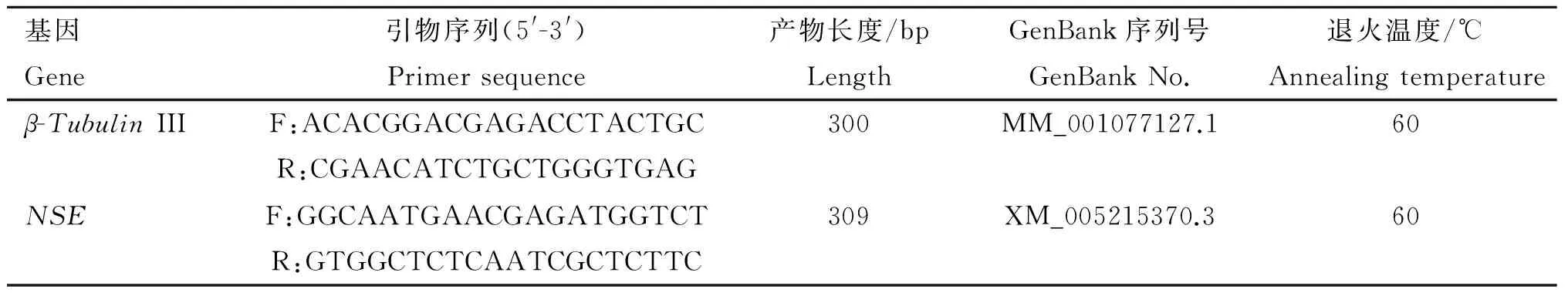
基因Gene引物序列(5'-3')Primersequence產物長度/bpLengthGenBank序列號GenBankNo.退火溫度/℃Annealingtemperatureβ-TubulinIIIF:ACACGGACGAGACCTACTGCR:CGAACATCTGCTGGGTGAG300MM_001077127.160NSEF:GGCAATGAACGAGATGGTCTR:GTGGCTCTCAATCGCTCTTC309XM_005215370.360
1.2.5乳腺干細胞活力的檢測按照2×103·孔-1的密度將細胞懸液接種于96孔培養板中,置于37 ℃、5%CO2飽和濕度的培養箱中培養,待干細胞生長貼壁后,隨機的分為對照組和催乳素處理組。設定催乳素0(對照組)、100、300、500、700 ng·mL-15個濃度梯度進行處理,每個濃度設定8個復孔,每個培養孔為1 個重復,置于37 ℃、5%CO2培養箱中繼續培養24 h;在培養結束前4 h,各培養孔加入 MTT(5 mg·mL-1) 20 μL; 4 h后,棄上清液,每孔加入二甲基亞砜(DMSO) 200 μL以溶解沉淀,振蕩10 min,用酶標儀在490 nm 波長處檢測各孔的吸光度值(OD)。
細胞相對增殖率(Relative growth rate,RGR)=(試驗組 OD490 nm/對照組 OD490 nm)×100%。
1.2.6數據分析采用SAS 9.4一般線性模型進行數據統計分析,以P<0.05為差異顯著。
2 結 果
2.1 乳腺干細胞的傳代與復蘇
將解凍后的乳腺干細胞培養2 d,顯微鏡下,觀察細胞貼壁后,有明顯鋪路石狀生長的細胞即為乳腺干細胞;高倍鏡下發現乳腺干細胞的細胞核較大,呈多核狀態,占細胞大部分位置,即核質比大,可見細胞有明顯的幼稚細胞的狀態(圖1)。
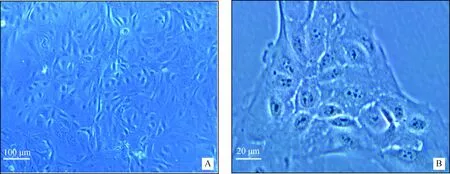
A.100×;B. 400×圖1 乳腺干細胞的傳代與復蘇(2 d)Fig.1 Passage and recovery of mammary stem cells (2 d)
2.2 乳腺干細胞成神經誘導
乳腺干細胞中加入神經預誘導液,放入CO2培養箱,培養24 h,有大部分乳腺干細胞都漂浮在培養基中,并且死亡,部分細胞開始慢慢變圓,也有堆積成細胞簇的現象,細胞兩極伸出細長突起,狀似雙極神經元細胞,尼氏染色呈陽性(圖2A),對照組細胞尼氏染色,可以從倒置顯微鏡中觀察到乳腺干細胞中有少許尼氏顆粒的存在,但沒有看到細胞明顯的分化成桿狀,樹突狀類型的神經細胞(圖2A′);更換正式神經誘導液,CO2培養箱中培養24 h,可以明顯的觀察到有桿狀,樹突狀的神經細胞,經尼氏染色呈陽性(圖2B),對照組尼氏染色后有少許尼氏顆粒的存在,仍沒有看到細胞明顯的分化(圖2B′);神經細胞繼續誘導24 h,有更多的細胞旁邊延伸出突起,細胞周圍出現微管樣結構有所增加,經尼氏染色呈陽性(圖2C),對照組尼氏染色后仍只有少許尼氏顆粒的存在,細胞未分化成桿狀,樹突狀類型的神經細胞(圖C′)。
A.誘導24 h;A′.未誘導24 h;B.誘導48 h;B′.未誘導48 h;C.誘導72 h;C′.未誘導72 h A. MSCs were induced 24 h; A′. MSCs were not induced 24 h; B. MSCs were induced 48 h;B′. MSCs were not induced 48 h; C. MSCs were induced 72 h;C′. MSCs were not induced 72 h圖2 乳腺干細胞成神經誘導(100×)Fig.2 Mammary stem cells(MSCs)were induced into neurocyte(100×)
2.3 乳腺干細胞誘導分化為神經細胞標記基因鑒定
RT-PCR法檢測神經細胞特異表達基因β-TubulinⅢ和NSE都呈現陽性結果,利用特異性引物擴增目的基因片段,電泳顯示條帶清晰且單一,無非特異擴增,圖3結果表明,β-TubulinⅢ的片段大小約為300 bp,NSE的片段大小約為309 bp,與設計的片段大小符合。

圖3 乳腺干細胞成神經誘導(基因檢測)Fig.3 Mammary stem cells were induced into neurocyte (Gene detection)
2.4 催乳素對乳腺干細胞增殖的影響
不同濃度催乳素對乳腺干細胞相對增殖率(RGR)的影響見表2。催乳素處理組(除700 ng·mL-1組外)RGR顯著高于對照組(P<0.05),100 ng·mL-1處理組顯著高于其他各組(P<0.05)。結果表明,與對照組相比較,催乳素組可顯著促進乳腺干細胞的增殖,其中100 ng·mL-1組的增殖活性最高。
3 討 論
乳腺干細胞是一種成體干細胞,具有多向分化潛能及自我更新能力[12]。研究發現,處于不同發育時期的動物乳腺中都存在一定比例的干細胞,正是這些干細胞對組織自穩態的維持和乳腺的生長與重建有很重要的作用[13],但是目前人們對乳腺干細胞的了解并不多。在乳腺干細胞存在于一部分基底細胞的前期認識基礎上[14],前人曾經嘗試回答乳腺干細胞的分化潛能問題。筆者將荷斯坦奶牛的乳腺干細胞在體外分離和培養并研究[15],檢測其多向分化潛能,這就是鑒定干細胞的一個重要的判斷標準。本試驗加入神經誘導液后,乳腺干細胞由緊密排列的鋪路石狀變為長梭型,且生長均一。隨著誘導時間不斷增長,能夠發現有類神經元細胞,經過尼氏染色后呈陽性。經過誘導后的乳腺干細胞可以表達一些神經元細胞或星形膠質細胞的特異標志物[16]:NSE和β-tubulinⅢ。RT-PCR技術鑒定基因的表達量,結果呈陽性表達。由此表明,在本研究條件下培養細胞,乳腺干細胞可表達其多向分化潛能,可以向多數不同的細胞組織定向分化。
表2不同濃度催乳素對奶牛乳腺干細胞相對增殖率的影響
Table2EffectofdifferentconcentrationsofprolactinonRGRofmammarystemcell

項目Item催乳素/(ng·mL-1)Prolactin0100300500700SEMP值PvalueRGR1.00±0.04c1.38±0.03a1.25±0.02b1.19±0.06b1.12±0.02bc0.05580.0546
同行數據肩標不同小寫字母表示差異顯著(P<0.05);相同或無小寫字母表示差異不顯著(P>0.05)
Values in the same row with different small letter superscripts mean significant difference (P<0.05), while with the same or no letter superscripts mean no significant difference (P>0.05)
乳腺的發育及泌乳都需要激素的調控。催乳素在促進哺乳動物的乳腺發育和維持泌乳等方面發揮重大作用[17-18]。催乳素對奶牛乳腺的發育及泌乳的研究已經取得了一些成果。E.H.Wall等[19]研究表明,給奶牛外源注射少量的催乳素,產奶量增加;P.Lacasse等[20]研究發現,無論單胃動物還是反芻動物,催乳素都可以促進其乳腺的發育和泌乳[21]。催乳素不僅可以通過激素系統間接地調節乳腺的發育,也可以通過與乳腺上皮細胞的催乳素受體結合直接調節乳腺的發育[22]。田青等[23-24]研究表明,胰島素、催乳素和氫化可的松能促進乳腺上皮細胞增殖。邢媛媛等[25]研究結果表明,低濃度催乳素能夠促進乳腺上皮細胞的增殖,而高濃度(1 000 ng·mL-1)催乳素對乳腺上皮細胞的增殖產生抑制效應。同時發現不同濃度的催乳素對乳脂和乳蛋白的合成調控有一定的關系,即低濃度時催乳素促進合成。100~300 ng·mL-1的濃度作用效果最好,而高濃度(1 000 ng·mL-1) 的催乳素對奶牛乳腺的乳脂和乳蛋白的合成產生一定的抑制作用。因為乳腺干細胞對于青春期、妊娠期、泌乳期和泌乳衰退期的乳腺生長與重建等都具有重要意義,筆者認為催乳素也會對乳腺干細胞的增殖產生一定的作用。將催乳素作用于乳腺干細胞,并利用 MTT 法檢測其對乳腺干細胞增殖活性的影響,旨在初步探討催乳素對于乳腺干細胞的作用意義。結果表明,催乳素能夠促進乳腺干細胞的增殖。另外,本試驗發現在選取不同濃度的催乳素刺激乳腺干細胞的情況下,100 ng·mL-1催乳素處理組乳腺干細胞增殖活性顯著高于0、300、500、700 ng·mL-1刺激組,說明低濃度時乳腺干細胞的活力較好,即且100 ng·mL-1為荷斯坦奶牛乳腺干細胞增殖的最適濃度。由此證明了催乳素可以促進乳腺干細胞增殖,為促進乳腺干細胞在體外繼續增殖,并分化為正常的乳腺細胞提供理論支持,這對于乳腺干細胞的臨床應用有重要意義。
本研究條件下可證明體外分離和培養的荷斯坦奶牛的乳腺干細胞具有多向分化潛能,且催乳素刺激后,增殖活性顯著增強,為進一步研究乳腺干細胞在體內外的分化和擴增提供基本的理論依據。以期為催乳素調控乳腺干細胞在奶牛乳腺重建過程及泌乳性能的最大發揮提供基礎理論依據。
4 結 論
在本研究條件下,體外分離培養的荷斯坦奶牛乳腺干細胞經特定誘導可以定向分化為神經樣細胞,具有分化神經細胞的能力,說明乳腺干細胞的多向分化潛能。催乳素可促進乳腺干細胞增殖,且100 ng·mL-1為增殖的最適濃度。
參考文獻(References):
[1]李慶章. 奶牛乳腺發育與泌乳生物學[M]. 北京: 科學出版社, 2014.
LI Q Z. Mammary gland development and lactation biology in dairy cows[M]. Beijing: Science Press, 2014. (in Chinese)
[2]HORIGAN K C, TROTT J F, BARNDOLLAR A S, et al. Hormone interactions confer specific proliferative and histomorphogenic responses in the porcine mammary gland[J].DomestAnimEndocrinol, 2003, 7(2): 124-138.
[3]STELWAGEN K, SINGH K. The role of tight junctions in mammary gland function[J].JMammaryGlandBiolNeoplasia, 2014, 19(1): 131-138.
[4]FU N Y, LINDEMAN G J, VISVADER J E. The mammary stem cell hierarchy[J].CurrTopDevBiol, 2014, 107: 133-160.
[5]KORDON E C, SMITH G H. An entire functional mammary gland may comprise the progeny from a single cell[J].Development, 1998, 125(10): 1921-1930.
[6]OHLSTEIN B, KAI T, DECOTTO E, et al. The stem cell niche: Theme and variations[J].CurrOpinCellBiol, 2004, 16(6): 693-699.
[7]FARMER C, PALIN M F. Exogenous prolactin stimulates mammary development and alters expression of prolactin-related genes in prepubertal gilts[J].JAnimSci, 2005, 83(4): 825-832.
[8]BERNARD V, YOUNG J, CHANSON P, et al. New insights in prolactin: Pathological implications[J].NatRevEndocrinol, 2015, 11(5): 265-275.
[9]WU W, CHEN Y H, UEDA E, et al. Different forms of prolactin have opposing effects on the expression of cell cycle regulatory proteins in differentiated mammary epithelial cells[J].OncolRes, 2006, 16(2): 75-84.
[10]INMAN J L, ROBERTSON C, MOTT J D, et al. Mammary gland development: Cell fate specification, stem cells and the microenvironment[J].Development, 2015, 142(6): 1028-1042.
[11]李帥民. 荷斯坦奶牛乳腺來源干細胞的初步分離及鑒定[D].呼和浩特:內蒙古農業大學, 2014.
LI S M. Reliminary isolation and identification of stem cells from Holstein mammary[D]. Hohhot: Inner Mongolia Agricultural University, 2014. (in Chinese)
[12]李吉霞, 葛秀國, 劉新峰, 等. 乳腺干細胞自我更新相關信號通路研究進展[J]. 天津農學院學報, 2013, 20(1): 41-45.
LI J X, GE X G, LIU X F, et al. Progress on self-renewal signaling pathways of mammary stem cells[J].JournalofTianjinAgriculturalUniversity, 2013, 20(1): 41-45. (in Chinese)
[13]WOODWARD W A, CHEN M S, BEHBOD F, et al. On mammary stem cells[J].JCellSci,2005, 118(Pt 16): 3585-3594.
[14]STINGL J, EIREW P, RICKETSON I, et al. Purification and unique properties of mammary epithelial stem cells[J].Nature, 2006, 439(7079): 993-997.
[15]VAN KEYMEULEN A, ROCHA A S, OUSSET M, et al. Distinct stem cells contribute to mammary gland development and maintenance[J].Nature, 2011, 479(7372): 189-193.
[16]王飛. 人胚胎神經干細胞體外誘導分化及其分化相關基因表達的研究[D].蘇州: 蘇州大學, 2003.
WANG F. Study on the inducing differentiation and expression of genes associated with differentiation of human embryonic neural stem cellsinvitro[D]. Suzhou: Suzhou University, 2003. (in Chinese)
[17]BOLE-FEYSOT C, GOFFIN V, EDERY M, et al. Prolactin (PRL) and its receptor: Actions, signal transduction pathways and phenotypes observed in PRL receptor knockout mice[J].EndocrRev, 1998, 19(3): 225-268.
[18]TWOROGER S S, RICE M S, ROSNER B A, et al. Bioactive prolactin levels and risk of breast cancer: A nested case-control study[J].CancerEpidemiolBiomarkersPrev,2015, 24(1): 73-80.
[19]WALL E H, CRAWFORD H M, ELLIS S E, et al. Mammary response to exogenous prolactin or frequent milking during early lactation in dairy cows[J].JDairySci, 2006, 89(12): 4640-4648.
[20]LACASSE P, LOLLIVIER V, DESSAUGE F, et al. New developments on the galactopoietic role of prolactin in dairy ruminants[J].DomestAnimEndocrinol, 2012, 43(2): 154-160.
[21]朱孟芝,董雅娟, 龔宜超, 等.體外誘導牛骨髓間充質干細胞向乳腺樣上皮細胞分化初步研究[J]. 中國畜牧獸醫, 2012, 39(1): 92-96.
ZHU M Z, DONG Y J, GONG Y C, et al. Preliminary study on differentiation of bovine BMSC into mammary gland-like epithelial cellsinvitro[J].ChinaAnimalHusbandry&VeterinaryMedicine,2012, 39(1): 92-96. (in Chinese)
[22]BINART N, HELLOCO C, ORMANDY C J, et al. Rescue of preimplantatory egg development and embryo implantation in prolactin receptor-deficient mice after progesterone administration[J].Endocrinology,2000, 141(7): 2691-2697.
[23]田青, 王洪榮. 胰島素、催乳素和氫化可的松對奶牛乳腺上皮細胞增殖和凋亡的影響[J]. 中國飼料, 2013(2): 8-12.
TIAN Q, WANG H R. Effects of insulin, prolactin and hydrocortisone on proliferation and apoptosis of mammary epithelial cells in dairy cows[J].ChinaFeed,2013(2): 8-12. (in Chinese)
[24]田青,王洪榮,王夢芝.氫化可的松對奶牛乳腺上皮細胞酪蛋白合成的影響[J].畜牧獸醫學報,2014,45(10): 1663-1670.
TIAN Q, WANG H R,WANG M Z. Effects of HYD on the synthesis of casein in mammary epithelial cells of holstein cowsinvitro[J].ActaVeterinariaetZootechnicaSinica, 2014, 45(10): 1663-1670. (in Chinese)
[25]邢媛媛, 李大彪, 李紅磊, 等. 催乳素對奶牛乳腺上皮細胞乳脂和乳蛋白合成相關基因表達的影響[J]. 動物營養學報, 2016, 28(8): 2439-2447.
XING Y Y, LI D B, LI H L, et al. Effects of prolactin on gene expressions involved in milk fat and milk protein synthesis in bovine mammary epithelial cells[J].ChineseJournalofAnimalNutrition, 2016, 28(8): 2439-2447. (in Chinese)

