化學實驗核心考點測試題(A卷)參考答案
1.A 2.C 3.A
4.D 提示:①電石與水反應生成乙炔,混有硫化氫,利用硫酸銅可除雜,然后用酸性KM n O4溶液檢驗乙炔的還原性,實驗合理,故正確;②C H3C H2B r與Na OH溶液共熱,發生水解反應,加硝酸至酸性,再利用硝酸銀檢驗,實驗合理,故正確;③淀粉與稀硫酸水浴共熱,發生水解生成葡萄糖,檢驗葡萄糖應在堿性條件下,故錯誤;④C2H5OH與濃硫酸加熱至170℃,發生消去反應生成乙烯,Na OH溶液可除雜,乙烯使高錳酸鉀溶液褪色,實驗合理,故正確;⑤苯與液溴反應,生成溴苯和H B r,然后加四氯化碳發生萃取,對上層溶液加硝酸銀生成淺黃色沉淀,實驗合理,故正確。
5.D
6.A 提示:高錳酸鉀與濃鹽酸反應生成氯氣,氯氣可氧化氯化亞鐵,生成氯化鐵,則觀察到c中溶液變棕黃色,故A正確;Na2S2O3與稀硫酸反應生成硫、二氧化硫,二氧化硫與溴水反應生成硫酸和H B r,則觀察到瓶c中溶液為無色,故B錯誤;硼酸與Na2CO3不反應,c中無現象,故C錯誤;常溫下Fe遇濃硝酸發生鈍化,則c中無現象,故D錯誤。
7.A 8.C 9.C 10.C 11.C 12.D 13.C 14.C 15.D
16.(1)增大反應物的接觸面積,加快反應速率 a、c
(2)Fe3+M g(OH)2、Ca(OH)2H2C2O4過量會導致生成Ba C2O4沉淀,產品的產量減少
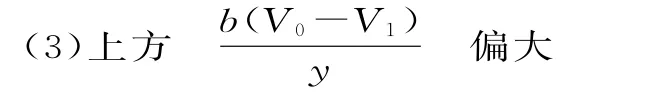
提示:(1)化學反應的速率與反應物的接觸面積有關,毒重石用鹽酸浸取前充分研磨,可以增大反應物的接觸面積,增大反應速率。溶液中質量分數=,實驗室用37%的鹽酸配制15%的鹽酸,需計算濃鹽酸的體積和水的體積,需要用量筒量取,濃鹽酸稀釋為稀鹽酸,需用燒杯作為容器稀釋,選擇a,玻璃棒攪拌加速溶解,選c。(2)根據流程和表3中數據可知,鐵離子完全沉淀時的p H為3.2,加入氨水,調p H為8,鐵離子和氨水反應生成氫氧化鐵和銨根離子,鐵離子完全沉淀,濾渣Ⅰ為氫氧化鐵,加入氫氧化鈉調節p H=12,鈣離子完全沉淀時的p H=13.9,鎂離子完全沉淀時的p H=11.1,鎂離子完全沉淀,鈣離子部分沉淀,濾渣Ⅱ含有氫氧化鎂和氫氧化鈣,溶液中主要含鈣離子、鋇離子。根據Ksp分析,Ksp越小,越容易形成沉淀,所以容易形成草酸鈣沉淀,加入草酸時應避免過量,防止草酸鈣沉淀完全后,過量的草酸會導致生成草酸鋇沉淀,產品的產量減少。(3)無論酸式滴定管還是堿式滴定管,“0”刻度都位于滴定管的上方,待鋇離子完全沉淀后,再加入酸堿指示劑,用bmol·L-1的鹽酸標準溶液滴定到終點,測得滴加鹽酸的體積為V1m L,則鹽酸的物質的量為V1×10-3×bmol,步驟Ⅰ中用鹽酸滴定到終點,測得滴加鹽酸體積為V0m L,加入的總鹽酸的物質的量為V0×10-3×bmol,Ba2++C r O2-4BaCrO4↓,則與Ba2+反應的C r O2-4的物質的量為V0×10-3×b-V1×10-3×b=(V0-V1)10-3b(mol),步驟Ⅱ中移取ym L氯化鋇溶液于錐形瓶中,所以氯化鋇溶液的濃度為
17.(1)分液漏斗 滴有品紅溶液的濾紙恢復紅色,滴有酸性KM n O4溶液的濾紙無變化
(5)使CO進入空氣,污染環境
提示:(1)盛裝濃硫酸的儀器是分液漏斗。因為SO2與品紅作用生成不穩定的無色物質,所以加熱時,濾紙②恢復紅色,但SO2與酸性KM n O4溶液發生了氧化還原反應,所以加熱時,濾紙③無變化。
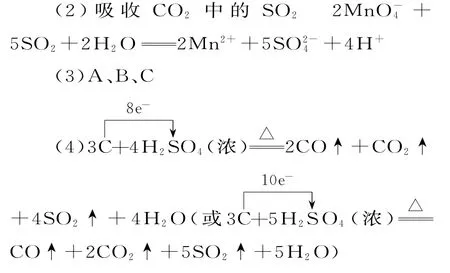
(2)B瓶中酸性KM n O4溶液的作用是吸收CO2中的SO2,該反應的離子方程式為2 M n O-4-5 SO2+2 H2O2 M n2++5 SO2-4+4 H+。
(3)在④號位置所放的濾紙是用來檢測二氧化碳中的二氧化硫是否完全被B瓶吸收,以防止其對C瓶中的反應的干擾,所以A、B、C均可,若從B中導出的氣體中有二氧化硫,④號位置所放的濾紙均會變色。
(4)解答此小題時,要抓住“蔗糖炭化后”及“反應生成的兩種碳的氧化物在相同條件下的體積比為2∶1”進行分析,即為碳與濃硫酸的再反應,若V(CO)∶V(CO2)=2∶1,則反應的化學方程式為2 CO↑ +CO2↑ +4 SO2↑ +4 H2O,若V(CO2)∶V(CO)=2∶1,則反應的化學方程
2017年,原國土資源部貫徹落實《中共中央國務院關于深化石油天然氣體制改革的若干意見》,穩步推進油氣勘查開采體制改革。積極開展頁巖氣區塊出讓工作,委托貴州省政府拍賣出讓正安頁巖氣勘查區塊;繼續推進新疆油氣勘查開采改革試點,委托新疆維吾爾自治區政府掛牌出讓柯坪南、溫宿、溫宿西三個油氣勘查區塊;實施煤層氣礦業權審批改革試點,將煤層氣委托審批下放試點從山西擴大到新疆、貴州等六省(區),山西省國土資源廳完成了10個煤層氣勘查區塊的招標出讓;經國務院批準,天然氣水合物成為我國第173個礦種。
(5)若在尾端沒有氣球b,產生的CO直接進入空氣,會污染環境。
18.(1)L i A l H4+2 H2OL i A l O2+4 H2↑
(2)①B M n O2+4 H++2 Cl-M n2++Cl2↑+2 H2O ②A 裝置D的硬質玻璃管中充滿黃綠色氣體 ③吸收多余的氯氣,避免空氣中的水蒸氣進入D中
(3)不合理 氫化鋁鋰遇水會爆炸性分解,且樣品中混有的L i H與水反應也會產生H2
19.(1)取代反應
(2)分液漏斗 30
(3)防止溫度過高濃硝酸分解,減少副產物間二硝基苯生成(或溫度較低反應速率慢,溫度過高反應物轉化率降低) 水浴加熱
(4)洗去殘留的Na OH及生成的鹽
(5)首先控制蒸餾溫度在80℃,收集該溫度下的餾分,除去苯,然后控制蒸餾溫度為211℃,收集該溫度下的餾分,得到純硝基苯
以免直形冷凝管通水冷卻時溫差過大而發生炸裂
(6)73.9%
提示:(1)苯環上的H原子被—NO2取代生成硝基苯,所以該反應為取代反應。
(2)混合酸應該盛放在儀器B所示的分液漏斗中,通過分液漏斗來控制加入混酸的速 率。0.552mol,解得x=30。
(3)根據題目信息可知,合成硝基苯的反應為放熱反應,從化學反應速率和化學平衡移動觀點來解釋溫度控制,同時濃硝酸受熱易分解生成NO2,溫度較高時副產物間二硝基苯也易生成。由于溫度低于100℃,所以可用水浴加熱方法控制溫度為50℃~60℃。
(4)先用水洗除去濃硫酸、濃硝酸,再用稀Na OH溶液將剩余的少量酸轉化為可溶性的鹽,這些鹽在蒸餾時不會變為氣體,便于后續分離提純硝基苯,最后水洗除去未反應的Na OH及生成的鹽。
(5)硝基苯中含有未反應的苯、副產物間二硝基苯,由于三者沸點差異較大,故采用蒸餾方法提純,首先應該在蒸餾溫度80℃下蒸餾除去苯,然后再在211℃蒸餾得到硝基苯。

