半滑舌鰨外周血T淋巴細(xì)胞的分離、鑒定及TCRβ基因免疫應(yīng)答分析
汪林慶 王 航 陳亞東, 楊 光 白 莉 孫璐明 沙珍霞,
(1. 福州大學(xué)生物科學(xué)與工程學(xué)院, 福州 350116; 2. 青島大學(xué)生命科學(xué)學(xué)院, 青島 266071; 3. 青島海洋科學(xué)與技術(shù)國家實(shí)驗(yàn)室海洋漁業(yè)科學(xué)與食物產(chǎn)出過程功能實(shí)驗(yàn)室, 青島 266235)
魚類是最早具有獲得性免疫系統(tǒng)的脊椎動(dòng)物,獲得性免疫功能依賴于T、B淋巴細(xì)胞2個(gè)亞群[1,2]。目前, 分離魚類免疫細(xì)胞比較常見的是密度梯度離心法[3,4], 但是對(duì)T、B淋巴細(xì)胞的分離和鑒定還缺乏有效的手段。根據(jù)B細(xì)胞表面凹凸不平, 而T細(xì)胞表面微絨毛多較光滑的細(xì)胞特性, 尼龍毛法成功應(yīng)用在哺乳動(dòng)物T、B淋巴細(xì)胞的分離上, 一些學(xué)者利用尼龍毛法在魚類上也成功分離了淋巴細(xì)胞[5,6]。T細(xì)胞受體(T cell receptor, TCR)是一種非常重要的T細(xì)胞抗原識(shí)別受體[7], 大多數(shù)T細(xì)胞的TCR由α和β肽鏈組成, 少數(shù)T細(xì)胞的TCR由γ和δ肽鏈組成[8]。
半滑舌鰨(Cynoglossus semilaevis)屬鰈形目(Pleuronectiformes)、舌鰨科(Cynoglossidae)、舌鰨屬(Cynoglossus), 是我國重要的海水養(yǎng)殖魚類, 但日益頻發(fā)的病害影響了養(yǎng)殖業(yè)可持續(xù)發(fā)展, 對(duì)半滑舌鰨免疫機(jī)制的解析是病害防治的根本途徑之一。鑒于多數(shù)魚類上尚缺乏有效的淋巴細(xì)胞分離、培養(yǎng)和鑒定技術(shù), 本文通過開展外周血T淋巴細(xì)胞的分離和鑒定, 以期為利用體外分離和短期培養(yǎng)的T淋巴細(xì)胞開展免疫基因功能研究提供細(xì)胞平臺(tái);同時(shí)通過對(duì)TCRβ基因的組織表達(dá)和免疫應(yīng)答趨勢(shì)進(jìn)行分析, 對(duì)半滑舌鰨獲得性免疫研究提供理論依據(jù)。
1 材料與方法
1.1 實(shí)驗(yàn)材料
半滑舌鰨購自日照東鑫現(xiàn)代漁業(yè)技術(shù)研究所,魚齡為1.5齡左右, 平均體重(310±5) g, 平均體長(zhǎng)(30.6±0.1) cm。健康實(shí)驗(yàn)魚在24℃水箱中暫養(yǎng)7d,以消除環(huán)境脅迫。
1.2 主要試劑
Hank’s緩沖液(Solarbio, 北京), 淋巴細(xì)胞分離液(Gibco, 美國), Ficoll-400(Solarbio, 北京), 瑞氏染液(Solarbio, 北京), 鼠抗人FITC-CD3單克隆抗體,鼠抗人FITC-CD19單克隆抗體, MTT (3-(4,5-dimethyl-2-thiazolyl)-2,5-diphenyl-2-H-tetrazolium bromide)(Sigma, 美國), 植物凝集素PHA (Sigma, 美國), 臺(tái)盼藍(lán), 尼龍毛。
DMEM完全培養(yǎng)基: DMEM基本培養(yǎng)基中添加15%FBS (胎牛血清, Gibco, 美國), 1 mmol/L的丙酮酸鈉, 50 mmol/L的 2-Me (2-巰基乙醇), 100 U/mL的青霉素, 100 U/mL的鏈霉素, 0.3 μg/mL的PHA,培養(yǎng)基pH為 7.0—7.3。
1.3 半滑舌鰨外周血淋巴細(xì)胞的分離
將人淋巴細(xì)胞分離液用Ficoll-400調(diào)整密度為1.080, 用于半滑舌鰨外周血白膜層細(xì)胞的分離。先將半滑舌鰨置于冰水中麻醉, 用70%酒精棉球擦拭體表, 使用肝素抗凝管抽取尾靜脈外周血, 立刻混勻, 在超凈工作臺(tái)中將全血與Hank’s緩沖液1∶3稀釋混勻, 取分離液各3 mL于15 mL離心管中, 再各取2 mL稀釋血液緩緩置于分離液液面上, 水平離心機(jī)1000 r/min離心20min, 收集白膜層細(xì)胞, 加入5倍體積的Hank’s緩沖液洗2次, 1000 r/min離心5min收集細(xì)胞沉淀, 重懸于DMEM完全培養(yǎng)基, 24℃培養(yǎng)箱培養(yǎng)3h后收集上層懸浮細(xì)胞, 0.2%臺(tái)盼藍(lán)活性計(jì)數(shù)。調(diào)整細(xì)胞濃度為6×105個(gè)/mL進(jìn)行后續(xù)培養(yǎng)。
1.4 淋巴細(xì)胞體外代謝活力的檢測(cè)
將密度為6×105個(gè)/mL懸浮淋巴細(xì)胞接種在含有0.3 μg/mL PHA的DMEM完全培養(yǎng)基中, 用96孔培養(yǎng)板培養(yǎng), 培養(yǎng)溫度為24℃。分別在0、6h、12h、18h、24h、36h、48h加入50 μL MTT溶液,繼續(xù)孵育4h。洗掉MTT溶液后, 每孔加150 μL DMSO, 平板搖床緩緩搖動(dòng)10min, 采用酶標(biāo)儀檢測(cè)570 nm波長(zhǎng)處每孔細(xì)胞的光密度, 重復(fù)3次。
1.5 淋巴細(xì)胞的進(jìn)一步分離
用1%HCl浸泡尼龍毛, 煮沸5—10min, 加蒸餾水沖洗直至溶液呈中性, 室溫晾干, 將尼龍毛梳理開, 使其無結(jié); 5 mL注射器移去活塞, 裝入0.4 g尼龍毛, 壓實(shí), 鋁箔包好管口高壓蒸汽滅菌。完全DMEM培養(yǎng)基流過注射筒并沒過尼龍毛, 封住下出口, 直立于24℃培養(yǎng)箱孵育≥45min。打開下出口流出培養(yǎng)基, 將收集的淋巴細(xì)胞稀釋到107個(gè)/mL, 加1 mL細(xì)胞懸液, 封閉出口, 再加2—3 mL DMEM完全培養(yǎng)基, 24℃培養(yǎng)箱直立孵育45min。打開下出口, 收集最初流出的非黏附細(xì)胞, 關(guān)閉出口加入0.7%冰冷生理鹽水, 震蕩, 套上活塞, 推出液體, 收集黏附細(xì)胞, 0.2%臺(tái)盼藍(lán)檢測(cè)細(xì)胞活性。
1.6 T樣、B樣淋巴細(xì)胞的鑒定
將收集的黏附細(xì)胞和非黏附細(xì)胞分別培養(yǎng), 并與50 μL鼠抗人FITC-CD3、FITC-CD19單克隆抗體混勻, 4℃靜置 30min, 洗棄上清, 流式細(xì)胞儀分別檢測(cè)其特異結(jié)合率, 與鼠抗人FITC-CD3結(jié)合的為T樣淋巴細(xì)胞, 與鼠抗人FITC-CD19結(jié)合的為B樣淋巴細(xì)胞。
1.7 T細(xì)胞的鑒定
分別收集黏附細(xì)胞和非黏附細(xì)胞, 用于RNA提取。RNA提取按照RNA提取試劑盒(天根, 北京)說明書進(jìn)行操作。cDNA第一條鏈的合成按照反轉(zhuǎn)錄試劑盒(寶生物, 大連)說明書進(jìn)行, 得到的cDNA在–20℃保存待用。根據(jù)已發(fā)表的半滑舌鰨轉(zhuǎn)錄組數(shù)據(jù)[9]中的TCR基因序列信息(XM_017043019.1), 設(shè)計(jì)特異性引物T1-F和T1-R (表 1)進(jìn)行PCR擴(kuò)增(目的片段長(zhǎng)度為760 bp左右), 經(jīng)測(cè)序驗(yàn)證獲得了TCRβ的基因序列, 根據(jù)測(cè)序得到的半滑舌鰨TCRβ基因序列設(shè)計(jì)qRT-PCR引物為qT1-F、qT1-R (目的片段長(zhǎng)度為216 bp)(表 1)。分別以非黏附細(xì)胞和黏附細(xì)胞為模板, 用T1-F和T1-R引物對(duì)、qT1-F、qT1-R引物對(duì)進(jìn)行PCR擴(kuò)增。
1.8 半滑舌鰨組織的收集
感染實(shí)驗(yàn)參照孫璐明等[10]方法略作修改, 采取實(shí)驗(yàn)室自行分離鑒定的鰻弧菌(Vibrio anguillarum),菌體為桿狀或弧狀, 單鞭毛, 革蘭氏陰性菌, 氧化酶陽性, 過氧化氫酶陽性, 葡萄糖發(fā)酵陽性, 對(duì)弧菌抑制劑敏感, 具有極強(qiáng)的致病性。在28℃, 2216E液體培養(yǎng)基中進(jìn)行擴(kuò)培。按照3.18×105CFU/g (半數(shù)致死量,LD50)對(duì)健康半滑舌鰨進(jìn)行腹腔注射; 對(duì)照組注射同等體積1×PBS緩沖溶液。在注射后的0、6h、12h、24h、48h、72h 6個(gè)時(shí)間點(diǎn)取樣, 每個(gè)時(shí)間點(diǎn)設(shè)置3個(gè)平行樣, 分別取肝、小腸、脾、頭腎、鰓、血液6種基本免疫組織; 另外隨機(jī)選3條健康魚分別收集肝、脾、頭腎、后腎、小腸、胃、血液、鰓、皮膚、肌肉、心臟、腦、卵巢13個(gè)組織, 所取組織迅速投入液氮中凍存, 用于RNA提取和cDNA制備。

表 1 半滑舌鰨TCRβ基因克隆和表達(dá)分析所用引物Tab. 1 Primers used for expression analysis and cloning of TCRβ in C. semilaevis
1.9 半滑舌鰨TCR基因?qū)崟r(shí)定量分析
以各組織cDNA為模板, 設(shè)計(jì)qRT-PCR引物為qT1-F、qT1-R (表 1), 以半滑舌鰨18S rRNA基因?yàn)閮?nèi)參, 設(shè)計(jì)引物為Cs18S-F、Cs18S-R (表 1)。用SYBR Green熒光定量試劑盒(天根, 北京)按照說明書在ABI PRISM 7500Fast實(shí)時(shí)定量擴(kuò)增儀上進(jìn)行qRT-PCR反應(yīng)。
1.10 統(tǒng)計(jì)學(xué)分析
使用SPSS19.0統(tǒng)計(jì)軟件對(duì)qRT-PCR檢測(cè)結(jié)果進(jìn)行分析。實(shí)時(shí)定量數(shù)據(jù)用3組重復(fù)平均值±標(biāo)準(zhǔn)誤(SE)表示, 使用2–ΔΔCt法計(jì)算相對(duì)表達(dá)量。采用單因素方差分析法中的Duncan法對(duì)多組樣本均數(shù)進(jìn)行兩兩比較分析,P<0.05時(shí), 認(rèn)為存在顯著性差異。
2 結(jié)果
2.1 半滑舌鰨外周血淋巴細(xì)胞的分離
外周血經(jīng)水平離心機(jī)離心20min后, 分為明顯的5層, 從下至上分別為紅細(xì)胞層、粒細(xì)胞層、分離液層、白膜層和血漿層(圖 1)。白膜層中包含淋巴細(xì)胞和單核/巨噬細(xì)胞。收集白膜層細(xì)胞, 洗滌兩次后接種到DMEM完全培養(yǎng)基中培養(yǎng)3h, 單核/巨噬細(xì)胞貼壁, 收集懸浮的淋巴細(xì)胞(圖 2)。在倒置顯微鏡下觀察, 淋巴細(xì)胞呈圓形, 直徑6—8 μm左右, 瑞氏染色發(fā)現(xiàn)核質(zhì)比較大, 細(xì)胞核呈圓形, 幾乎占據(jù)整個(gè)細(xì)胞, 具有典型的淋巴細(xì)胞形態(tài)特征(圖3), 0.2%臺(tái)盼藍(lán)檢測(cè)細(xì)胞活性, 活細(xì)胞百分率大于85%。

圖 1 密度為1.080 mg/mL的分離液分離效果Fig. 1 The result of separating blood of founder with density of 1.080 mg/mL
2.2 淋巴細(xì)胞體外代謝活力生長(zhǎng)曲線
實(shí)驗(yàn)結(jié)果表明, 在有絲分裂原PHA的刺激下,半滑舌鰨外周血淋巴細(xì)胞個(gè)體變大, 在體外可以增殖(圖 4), 在培養(yǎng)12—24h之后細(xì)胞細(xì)胞增殖迅速,隨后細(xì)胞不再增殖, 細(xì)胞數(shù)量慢慢減少, 24—48h后細(xì)胞數(shù)量保持相對(duì)穩(wěn)定。體外培養(yǎng)條件下淋巴細(xì)胞不貼壁, 呈懸浮狀態(tài), 細(xì)胞間相互黏連聚集呈葡萄串狀(圖 5)。

圖 2 100倍鏡下的懸浮淋巴細(xì)胞Fig. 2 Suspending lymphocytes under the microscope (100×)

圖 3 淋巴細(xì)胞瑞氏染色(100倍油鏡)Fig. 3 Lymphocyte Wright's staining (100-fold oil mirror)
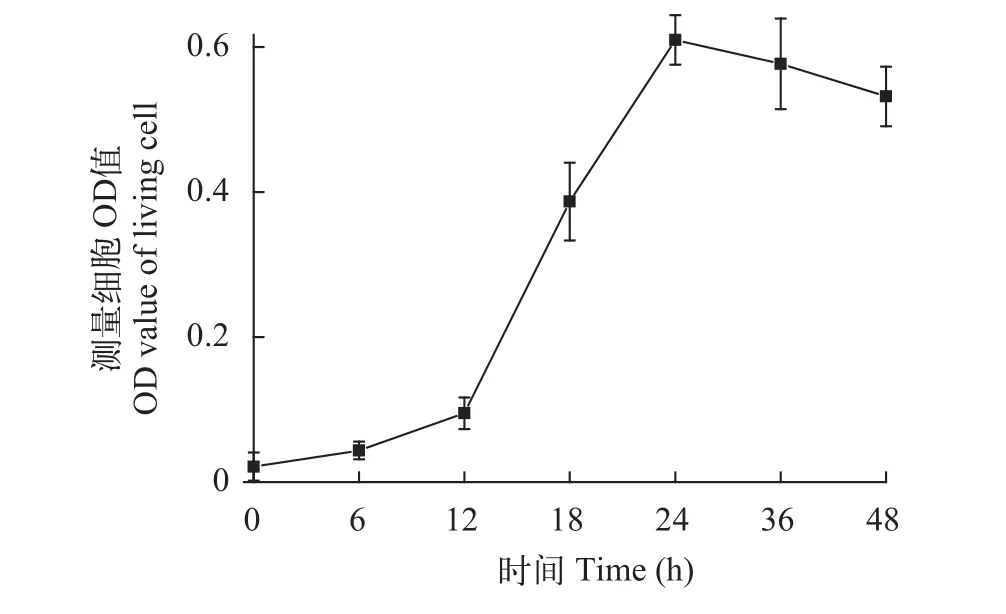
圖 4 半滑舌鰨外周血淋巴細(xì)胞生長(zhǎng)曲線Fig. 4 The growth curve of peripheral blood lymphocyte of C.Semilaevis
2.3 黏附細(xì)胞和非黏附細(xì)胞的鑒定
對(duì)黏附細(xì)胞和非黏附細(xì)胞采用流式細(xì)胞儀結(jié)合單克隆抗體進(jìn)行檢測(cè)。結(jié)果表明, 非黏附細(xì)胞與鼠抗人FTIC-CD3單克隆抗體的結(jié)合率為3.18%, 黏附細(xì)胞不與鼠抗人FTIC-CD3單克隆抗體結(jié)合,CD3分子在哺乳動(dòng)物中被證實(shí)是T淋巴細(xì)胞表面抗原, 因此可以認(rèn)為分離的半滑舌鰨外周血淋巴細(xì)胞中的非黏附細(xì)胞為T樣淋巴細(xì)胞。同樣, 黏附細(xì)胞和鼠抗人FTIC-CD19單克隆抗體的結(jié)合率為7.87%,非黏附細(xì)胞不與該抗體結(jié)合, 而CD19在哺乳動(dòng)物中被認(rèn)定為B淋巴細(xì)胞的表面抗原, 因此黏附細(xì)胞證明為半滑舌鰨B樣淋巴細(xì)胞。為進(jìn)一步確認(rèn)淋巴細(xì)胞的特性, 將分離的2種細(xì)胞分別用TCRβ基因克隆驗(yàn)證。由于TCRβ在T細(xì)胞表面特異表達(dá), 而在B細(xì)胞表面不表達(dá), 通過2對(duì)不同引物的擴(kuò)增(T1-F/R和qT1-F/R), 在非黏附細(xì)胞中分別獲得了760和261 bp左右的PCR擴(kuò)增產(chǎn)物, 在黏附細(xì)胞中檢測(cè)不到TCRβ基因的表達(dá), 表明收集的非黏附細(xì)胞是T淋巴細(xì)胞。
2.4 半滑舌鰨TCRβ基因在健康組織的表達(dá)
TCRβ基因在13個(gè)健康組織中均有表達(dá)(圖 6),在腸中相對(duì)表達(dá)量最高(12.22), 其次是胃(9.09)、脾臟(8.17), 在頭腎、后腎、皮膚和鰓中也有較高的表達(dá)量, 在肌肉和腦中的表達(dá)量相對(duì)低(肌肉0.13、腦0.57), 說明TCRβ基因在不同組織中存在表達(dá)差異性。
2.5 半滑舌鰨感染鰻弧菌后TCRβ基因在免疫組織中的表達(dá)
鰻弧菌感染半滑舌鰨后0、6h、12h、24h、48h、72h和96h,TCRβ基因在不同時(shí)間點(diǎn)6種免疫組織(肝、脾、頭腎、鰓、腸和血液)中呈現(xiàn)出不同的表達(dá)水平(圖 7)。結(jié)果表明: 在肝和脾中TCRβ基因的表達(dá)呈現(xiàn)相同的上調(diào)趨勢(shì), 其表達(dá)峰值出現(xiàn)在鰻弧菌感染后96h, 在肝中為對(duì)照組表達(dá)量的27.4倍;在脾臟中則是對(duì)照組的21.7倍; 在鰓中TCRβ基因表達(dá)上調(diào), 最大表達(dá)量出現(xiàn)在感染后72h, 是對(duì)照組的11.5倍, 96h時(shí)依然保持較高的表達(dá)水平; 在頭腎、血液和腸中的表達(dá)量變化不大, 在頭腎中下調(diào)或上調(diào)表達(dá)量在2倍左右; 在血液中表達(dá)的最低值出現(xiàn)在12h, 為對(duì)照組的0.02倍, 其表達(dá)的趨勢(shì)為先下降后上升, 48h基本恢復(fù)到正常表達(dá)水平。在腸中鰻弧菌感染后6h表達(dá)量增加了3倍, 但隨后的各時(shí)間點(diǎn)TCRβ基本處于下調(diào)表達(dá)狀態(tài)。

圖 5 淋巴細(xì)胞體外懸浮培養(yǎng)Fig. 5 Suspension culture of lymphocytes

圖 6 TCRβ基因在半滑舌鰨健康組織中的相對(duì)表達(dá)量Fig. 6 The relative expression of TCRβ gene in normal tissues of C. semilaevis
3 討論
3.1 T淋巴細(xì)胞的分離鑒定
采用密度梯度離心方法進(jìn)行魚類外周血淋巴細(xì)胞的分離已經(jīng)有很多成功的報(bào)道。早在20世紀(jì)80年代, Sakai[5]用18% Ficoll溶液分離得到金魚(Carassius auratus)和鱒(Salmo playtcephalus)淋巴細(xì)胞, Blaxhall[4]用Ficoll-paque或Percoll梯度離心法分離了河鮭(Satmo truttaL.)、鯉(Cyprinus carpio)外周血淋巴細(xì)胞。但是由于魚類的多樣性比較高,不同魚類所用分離液的密度有所不同。本實(shí)驗(yàn)對(duì)淋巴細(xì)胞分離方法進(jìn)行了改進(jìn), 建立了適用于半滑舌鰨外周血淋巴細(xì)胞的分離方法。這一結(jié)果與報(bào)道的物種如鯉、金魚等淋巴細(xì)胞分離結(jié)果相似。
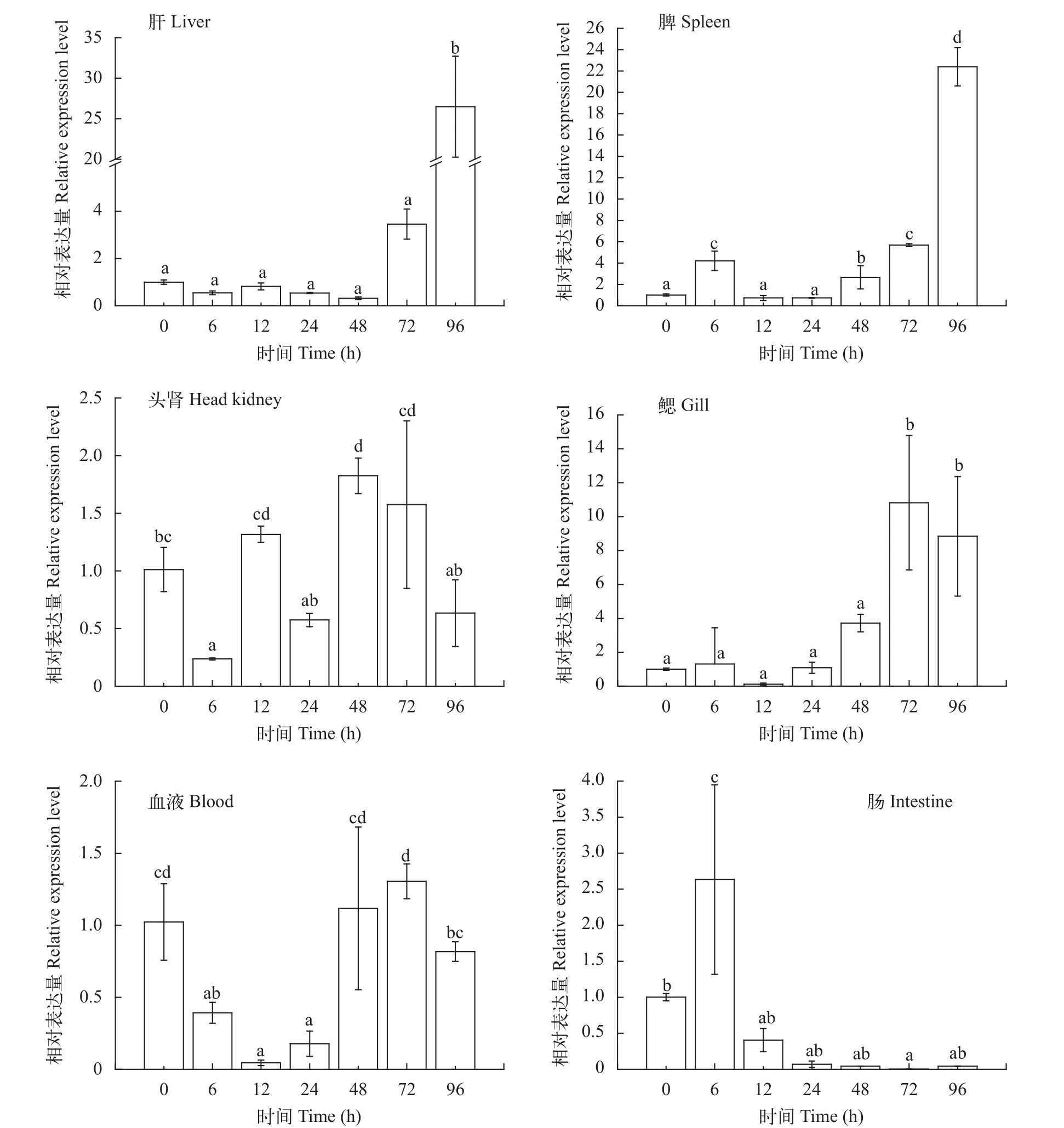
圖 7 鰻弧菌感染半滑舌鰨后不同時(shí)間點(diǎn)6種組織(肝、脾、頭腎、鰓、腸和血液)中TCRβ基因的相對(duì)表達(dá)水平Fig. 7 Relative expression of TCRβ gene in six tissues (liver, spleen, head kidney, gills, intestine and blood) of C. semilaevis at different time points after Vibrio anguillarum infection
體外培養(yǎng)的淋巴細(xì)胞不易傳代生長(zhǎng), 而適當(dāng)濃度的PHA (植物血凝素)可以促進(jìn)淋巴細(xì)胞體外生長(zhǎng), 使之成功分裂增殖。如Fujiwara等[11]用含有18 μg/mL PHA的M199培養(yǎng)液培養(yǎng)虹鱒(Oncorhynchus mykiss)外周血淋巴細(xì)胞可達(dá)6d并用于染色體組型實(shí)驗(yàn)。本文采用含有PHA終濃度為0.3 μg/mL的完全DMEM培養(yǎng)基, 對(duì)分離獲得的半滑舌鰨外周血淋巴細(xì)胞成功實(shí)現(xiàn)了體外培養(yǎng), 淋巴細(xì)胞在18h后增殖達(dá)到對(duì)數(shù)期, 且穩(wěn)定的增殖狀態(tài)可維持48h。
在魚類上, 目前由于缺少特異抗體, 對(duì)淋巴細(xì)胞的類群劃分還存在比較大的困難。但隨著基因組學(xué)的發(fā)展, 通過細(xì)胞表面特異基因的檢測(cè)已成為鑒定淋巴細(xì)胞的有效手段。魚類淋巴細(xì)胞表面標(biāo)記的研究處于初級(jí)階段, 利用現(xiàn)有的單抗分離的淋巴細(xì)胞往往并不是單一的細(xì)胞亞群[12—14]。尼龍毛法是分離魚類T、B淋巴細(xì)胞的有效手段, Tate[15]通過尼龍毛法收集了對(duì)PHA、ConA敏感的魚類非黏附細(xì)胞及對(duì)LPS敏感的黏附細(xì)胞。Xia等[5]用尼龍法分離鰻鱺(Anguilla japonica)淋巴細(xì)胞, 發(fā)現(xiàn)黏附性細(xì)胞具有B淋巴細(xì)胞有絲分裂反應(yīng)特性, 而非黏附性細(xì)胞有T淋巴細(xì)胞有絲分裂特性。本研究結(jié)果表明, 尼龍毛法同樣適用于半滑舌鰨外周血淋巴細(xì)胞的分離。目前, CD3[16,17]和CD19分別被認(rèn)定為B淋巴細(xì)胞T淋巴細(xì)胞的表面抗原分子[18—20]。通過蛋白序列比對(duì)得知, 半滑舌鰨CD3(NCBI:NO XP_008306806.1)與人CD3(NCBI:NO XP_016874032.1)蛋白序列相似性為29%; 半滑舌鰨CD19(本實(shí)驗(yàn)室未發(fā)表數(shù)據(jù))與人CD19(NCBI:NO XP_016874032.1)蛋白序列的相似性為44%左右。另外, 人類的CD3和CD19抗體已經(jīng)成功的應(yīng)用于多種水生動(dòng)物的淋巴細(xì)胞鑒定, 如中華鱉(Trionyx Sinensis)[21], 海星(Asteroidea)[22]等。根據(jù)T淋巴細(xì)胞表面特異CD3分子標(biāo)記和B淋巴細(xì)胞表面特異的CD19分子標(biāo)記, 利用流式細(xì)胞儀檢測(cè)到半滑舌鰨外周血中非黏附淋巴細(xì)胞和黏附淋巴細(xì)胞與鼠抗人FTIC-CD3單抗和鼠抗人FTIC-CD19單抗結(jié)合效率分別為3.18%和7.87%。且由于TCRβ在T細(xì)胞特異性表達(dá),而在B細(xì)胞不表達(dá), 本實(shí)驗(yàn)表明收集的非黏附細(xì)胞是T淋巴細(xì)胞, 黏附細(xì)胞是B淋巴細(xì)胞。目前應(yīng)用TCR的表達(dá)鑒定魚類的T細(xì)胞的方法在斑馬魚(Barchydanio reriovar)、大西洋鱈(Gadus morhua)等魚類上亦有報(bào)道[23,24]。
3.2 TCRβ基因的表達(dá)特征分析
T細(xì)胞受體(TCR)作為T細(xì)胞識(shí)別內(nèi)/外源性抗原的分子, 在免疫應(yīng)答和免疫調(diào)節(jié)中發(fā)揮著重要的作用。自20世紀(jì) 80 年代T細(xì)胞受體基因被先后發(fā)現(xiàn)和克隆以來[25,26], 關(guān)于T細(xì)胞受體與機(jī)體獲得性免疫[27]、自身免疫性疾病[28]、淋巴系統(tǒng)腫瘤[29]以及與病原分子[30]相互識(shí)別的關(guān)系得到了廣泛的研究。目前, 人和鼠的T細(xì)胞受體的研究較多, 而對(duì)魚類等動(dòng)物TCR分子結(jié)構(gòu)與功能研究較少。本研究表明,TCRβ在半滑舌鰨各個(gè)健康組織中都有表達(dá),在腸道中的表達(dá)最高, 在胃、頭腎、后腎和脾中的表達(dá)相對(duì)其他組織也較高。腸是最大的免疫器官,腸上分布著大量的腸相關(guān)淋巴組織(Gut associated lymphoid tissues, GALTs), 頭腎、脾臟是魚類的系統(tǒng)免疫器官, 也含有大量的T細(xì)胞, 故表達(dá)量較高。感染鰻弧菌后TCRβ在肝、脾、鰓中的表達(dá)量上調(diào)趨勢(shì)明顯, 且表達(dá)的峰值基本出現(xiàn)在72—96h。本研究結(jié)果說明TCRβ以在病原刺激后, 參與了機(jī)體的獲得性免疫應(yīng)答。TCRβ基因在鰻弧菌刺激后在腸中的表達(dá)變化幅度不大, 僅在感染6h后出現(xiàn)了小幅上調(diào)表達(dá), 12h后則呈現(xiàn)下調(diào)表達(dá)趨勢(shì), 可能與采用腹腔注射的感染方式有關(guān)。腸道是最早接觸病原菌的組織, 因此在腹腔注射導(dǎo)致腸道感染后的短時(shí)間內(nèi), 免疫細(xì)胞在腸道富集, 導(dǎo)致腸道中在感染后的6h內(nèi)TCRβ表達(dá)量提高; 隨后, 病原菌進(jìn)入其他組織, 激活其他免疫組織該基因的表達(dá)。這一點(diǎn)可以通過其他組織普遍在感染后的48h表達(dá)量上升得到印證, 感染鰻弧菌后TCRβ在肝、脾、鰓中的表達(dá)量上調(diào)趨勢(shì)明顯, 且表達(dá)的峰值基本出現(xiàn)在72—96h。
本研究通過密度梯度離心和短期細(xì)胞培養(yǎng)方法, 結(jié)合尼龍毛法、流式細(xì)胞儀成功分離、鑒定了半滑舌鰨外周血T樣淋巴細(xì)胞和B樣淋巴細(xì)胞, 并進(jìn)一步通過T細(xì)胞特異表面受體基因TCRβ表達(dá)對(duì)T細(xì)胞進(jìn)行了鑒定; 這為后續(xù)半滑舌鰨免疫學(xué)研究建立了奠定了良好的細(xì)胞學(xué)基礎(chǔ)。同時(shí)通過檢測(cè)TCRβ基因在健康組織中、病原刺激后不同的免疫組織中基因的表達(dá)變化趨勢(shì), 驗(yàn)證了TCRβ基因在機(jī)體獲得性免疫應(yīng)答中發(fā)揮的重要作用。
參考文獻(xiàn):
[1] Abbas A K, Lichtman A H, Pober J S. Antigen processing and presentation to T lymphocytes [J].Cellular and Molecular Immunology, 2003: 115—137
[2] Vantourout P, Hayday A. Six-of-the-best: unique contributions of γδ T cells to immunology [J].Nature Reviews Immunology, 2013, 13(2): 88—100
[3] Blaxhall P C. The separation and cultivation of fish lymphocytes [J].Fish Immunology, 1985, 11: 245—60
[4] Blaxhall P C, Hood K. Cytochemical enzyme staining of fish lymphocytes separated on a Percoll gradient [J].Journal of Fish Biology, 1985, 27(6): 749—755
[5] Sakai K. Separation of lymphycytes from the peripheral blood of rainbow trout (Salmo gairdnerii) and goldfish[J].Bulletin of the Japanese Society of Scientific Fisheries(Japan), 1981, 47(10): 1281—1288
[6] Xia C, Kusuda R. Studies on the heterogeneity of lymphocyte population in Eel,Anguilla japonica[J].Suisanzoshoku(Japan), 1993, 41(1): 119—123
[7] Yamamoto R, Uenishi H, Hatsuse H,et al. TRAV gene usage in pig T-cell receptor alpha cDNA [J].Immunogenetics, 2005, 57(3-4): 219—225
[8] Bonneville M, O'brien R L, Born W K. γδ T cell effector functions: a blend of innate programming and acquired plasticity [J].Nature Reviews Immunology, 2010, 10(7):467—478
[9] Zhang X, Wang S, Chen S,et al. Transcriptome analysis revealed changes of multiple genes involved in immunity inCynoglossus semilaevisduringVibrio anguillaruminfection [J].Fish & Shellfish Immunology, 2015, 43(1):209—218
[10] Sun L M, Yu M J, Chen Y D,et al. AKT-interacting protein gene cloning and its expression profile in response to pathogen infection in half smooth tongue sole (Cynoglossus semilaevis) [J].Acta Hydrobiologica Sinica, 2016,40(3): 467—473 [孫璐明, 于孟君, 陳亞東, 等. 半滑舌鰨AKT-ineracting protein基因的克隆及免疫應(yīng)答表達(dá)分析. 水生生物學(xué)報(bào), 2016, 40(3): 467—473]
[11] Fujiwara A, Nishida-Umehara C, Sakamoto T,et al. Improved fish lymphocyte culture for chromosome preparation [J].Genetica, 2001, 111(1-3): 77—89
[12] Verburg-van Kemenade B M L, Nowak B, Engelsma M Y,et al. Differential effects of cortisol on apoptosis and proliferation of carp B-lymphocytes from head kidney,spleen and blood [J].Fish & Shellfish Immunology, 1999,9(5): 405—415
[13] Scapigliati G, Mazzini M, Mastrolia L,et al. Production and characterisation of a monoclonal antibody against the thymocytes of the sea bassDicentrarchus labrax(L.)(Teleostea, Percicthydae) [J].Fish & Shellfish Immunology, 1995, 5(6): 393—405
[14] Romano N, Taverne-Thiele J J, Van Maanen J C,et al.Leucocyte subpopulations in developing carp (Cyprinus carpioL.): immunocytochemical studies [J].Fish &Shellfish Immunology, 1997, 7(7): 439—453
[15] Tate H. Immunosuppressive effect of infectious pancreatic necrosis virus on rainbow trout (Oncorhynchus mykiss)[J].The Japanese Journal of Veterinary Science, 1990,52(5): 931—937
[16] Bankfalvi A, Navabi H, Bier B,et al. Wet autoclave pretreatment for antigen retrieval in diagnostic immunohistochemistry [J].The Journal of Pathology, 1994, 174(3):223—228
[17] Kaiko G E, Horvat J C, Beagley K W,et al. Immunological decision-making: how does the immune system decide to mount a helper T-cell response [J]?Immunology, 2008, 123(3): 326—338
[18] van Zelm M C, Reisli I, van der Burg M,et al. An antibody-deficiency syndrome due to mutations in the CD19 gene [J].New England Journal of Medicine, 2006,354(18): 1901—1912
[19] Scheuermann R H, Racila E. CD19 antigen in leukemia and lymphoma diagnosis and immunotherapy [J].Leukemia & Lymphoma, 1995, 18(5-6): 385—397
[20] Chung E Y, Psathas J N, Yu D,et al. CD19 is a major B cell receptor-independent activator of MYC-driven B-lymphomagenesis [J].The Journal of Clinical Investigation, 2012, 122(6): 2257
[21] Guo Q. Studies on surface antigens of t lymphocyte in grass carp,Ctenopharyngodon idellusand Chinese oftshelled turtle,Trionyx sinensis[J].Acta Hydrobiologica Sinica, 2001, 25(5): 455—461 [郭瓊林. 草魚, 中華鱉T淋巴細(xì)胞表面抗原的研究. 水生生物學(xué)報(bào), 2001,25(5): 455—461]
[22] Leclerc M, Arneodo V J, Legac E,et al. Identification of T-like and B-like lymphocyte subsets in sea starAsterias rubensby monoclonal antibodies to human leukocytes[J].Thymus, 1993, 21(3): 133—139
[23] Haire R N, Rast J P, Litman R T,et al. Characterization of three isotypes of immunoglobulin light chains and T-cell antigen receptor a in zebrafish [J].Immunogenetics,2000, 51(11): 915—923
[24] Wermenstam N E, Pilstr?m L. T-cell antigen receptors in Atlantic cod (Gadus morhuaL.): structure, organisation and expression of TCR α and β genes [J].Developmental &Comparative Immunology, 2001, 25(2): 117—135
[25] Davis M M. T cell receptor gene diversity and selection[J].Annual Review of Biochemistry, 1990, 59(1): 475—496
[26] Lai E, Wilson R K, Hood L E. Physical maps of the mouse and human immunoglobulin-like loci [J].Advances in Immunology, 1989, 46: 1—59
[27] Sakuma H, Kohyama K, Jee Y,et al. Tracking of Vβ8.2-positive encephalitogenic T cells by complementarity-determining region 3 spectratyping and subsequent southern blot hybridization in lewis rats after neuroantigen sensitization [J].The Journal of Immunology, 2004,173(7): 4516—4522
[28] Puisieux I, Even J, Pannetier C,et al. Oligoclonality of tumor-infiltrating lymphocytes from human melanomas[J].The Journal of Immunology, 1994, 153(6): 2807—2818
[29] Farace F, Orlanducci F, Dietrich P Y,et al. T cell repertoire in patients with B chronic lymphocytic leukemia.Evidence for multiple in vivo T cell clonal expansions [J].The Journal of Immunology, 1994, 153(9): 4281—4290
[30] Miles J J, Borg N A, Brennan R M,et al. TCRα genes direct MHC restriction in the potent human T cell response to a class I-bound viral epitope [J].The Journal of Immunology, 2006, 177(10): 6804—6814

