碳酸鹽堿脅迫下尼羅羅非魚氨代謝兩種途徑時序研究
涂翰卿,趙金良,趙 巖,曹曉穎
(上海海洋大學,農業部淡水水產種質資源重點實驗室,上海 201306)
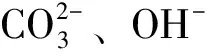
尼羅羅非魚(Oreochromisniloticus)是我國重要的淡水水產養殖品種,生長速度快,抗逆性好,對鹽、堿具有較強的耐受性,具備一定的鹽堿水養殖潛能[11-14]。前期研究表明,堿脅迫下尼羅羅非魚血氨濃度升高,相關組織內的谷氨酰胺合成酶、氨甲酰磷酸合成酶等氨代謝基因表達水平均與脅迫過程呈相應變化,推測即兩種氨代謝途徑共同參與調節血氨水平調節[15-16]。在此基礎上,通過檢測兩種代謝途徑主要產物尿素與谷氨酰胺的濃度的變化,關鍵酶的活性與基因表達量的變化,確認兩種氨代謝途徑的存在以及啟動時序,為羅非魚堿性水環境適應的研究提供基礎資料。
1 材料與方法
1.1 實驗材料
實驗所用尼羅羅非魚取自于上海海洋大學羅非魚種質資源試驗站,平均規格100 g,在室內淡水水族箱(0.6 m×0.5 m×0.4 m)內暫養2周,暫養期間正常喂食,定期換水,清理糞便,實驗前3 d停食,排空糞便,挑選具有良好體征活力強的個體進行急性堿脅迫實驗。
實驗用水為經過曝氣過夜處理的自來水與NaHCO3(分析純)按比例配制,配制完成后放置1 d使用。使用便攜式HI83200多參數水質分析儀測量修正堿度。
血氨測定試劑盒、尿素氮(BUN)測試盒(脲酶法)、谷氨酰胺測試盒購自南京建成生物公司;魚氨甲酰磷酸合成酶(CPS)酶聯免疫分析試劑盒、魚谷氨酰胺合成酶(GS)酶聯免疫分析試劑盒購自上海酶聯生物科技有限公司;Trizol購自Invitrogen公司;PrimeScript RT reagent Kit With gDNA Eraser、SYBR Premix ExTaq購自TaKaRa公司。熒光定量所用引物來自上海生工生物工程有限公司。
1.2 實驗方法
1.2.1 急性脅迫實驗
先對尼羅羅非魚進行堿度耐受性的預實驗,6 g/L堿以下尼羅羅非魚全部存活,所以設置了3個堿度組(2、4、6 g/L),每個組放置20尾,設置3個重復。實驗期間對水體pH進行調控維持在8.5左右,并保持溶氧在3 g/L以上。
1.2.2 樣品采集
分別于脅迫0、2、4、6、12、24、48、72 h,從3個堿度組各取3條魚,并采集水箱中的水樣4 ℃保存。通過擠壓魚腹部的方式收集尿液4 ℃保存。使用注射器從尾端靜脈抽血4 ℃靜置12 h后離心(3 000 r/min,4 ℃,10 min)取血清保存在-20 ℃冰箱。對魚進行解剖,取出腦、鰓、肝、腎等組織后放置在-80 ℃冰箱內保存。
1.2.3 血氨、尿素、谷氨酰胺濃度測定
使用試劑盒分別檢測血液中的氨濃度,肝、腦、鰓谷氨酰胺濃度,肝、腎、鰓組織及血液、尿液、水體中尿素濃度進行測定,使用Synergy H1酶標儀(Bio-tek,USA)檢測其吸光值。
1.2.4 GS、CPS酶活性測定
分別取腦、肝,稱重(0.5~1 g),按質量(g)︰體積(mL)= 1︰9 比例加入生理鹽水,低溫勻漿,4 ℃條件下離心(3 000 r/min,15 min),吸取上清液。使用試劑盒測定,用Synergy H1酶標儀讀取吸光值,換算其含量。
1.2.5 GS、GLS2、CPS1基因mRNA表達
GS、GLS2、CPS1基因的特異擴增引物參照文獻[16],由上海生工生物工程有限公司合成(表1)。鰓、肝、腎、腦組織在液氮中研磨碎,用Trizol提取總RNA,用RNase free ddH2O溶解,用OD-1000+分光光度計(Onedrop,國產)檢測RNA濃度和A260/A280值,ABS值在1.8-2.1之間的樣本保留。以總RNA為模板,按PrimeScript RT reagent Kit With gDNA Eraser 說明書操作反轉錄合成第一鏈cDNA。實時熒光定量PCR擴增參照SYBR Premix ExTaq說明書進行,擴增程序為:95 ℃ 預變性30 s;95 ℃ 變性5 s,58~62 ℃ 退火延伸30 s,40個循環;95 ℃ 熔解10 s,65 ℃ 退火5 s。根據結果調整擴增體系,使目的基因和內參基因擴增效率都接近100 %。擴增程序與標準曲線的擴增程序相同。最后采用2-ΔΔCt法對不同基因的表達量進行比較分析。

表1 引物信息Tab.1 The information of the primers
1.2.6 數據分析
實驗數據使用SPSS 22統計軟件分析,統計實驗數據的平均值和標準差,單因素方差分析進行顯著性檢驗,Duncan多重比較檢測各測量指標的差異,以P<0.05為差異顯著。
2 結果與分析
2.1 堿脅迫下血氨濃度的變化
脅迫開始后,實驗魚出現短時間不適反應現象,后逐漸消失,實驗過程中實驗魚均保持存活。血氨濃度隨著堿度、脅迫時間變化而升高,12 h到達峰值,24 h后維持高于初始水平(圖1)。
2.2 堿脅迫下尿素濃度變化
堿脅迫下,血液尿素濃度0~6 h快速升高,于6 h達到峰值,12 h后維持高于初始水平(圖2-a)。肝尿素濃度0~6 h快速升高,于6 h達到峰值,12 h后維持高于初始水平(圖2-b)。鰓尿素濃度在0~2 h快速升高, 6~12 h再次升高,于12 h到達峰值,24 h后維持高于初始水平(圖2-c)。腎尿素濃度在0~6 h快速升高,在6 h到達峰值,12 h后維持略高于初始水平(圖2-d)。尿液尿素濃度在0~6 h升高,在6 h到達峰值,12 h后恢復初始水平,水體尿素濃度未發生明顯波動(圖3)。
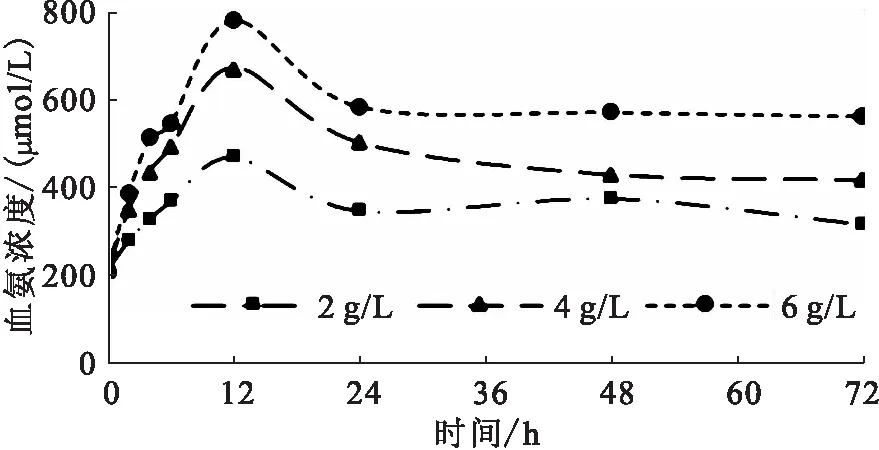
圖1 堿脅迫對尼羅羅非魚血氨濃度的影響Fig.1 Effect of alkalinity stress on ammonia concentration in serum of O.niloticus
2.3 堿脅迫下谷氨酰胺濃度變化
堿脅迫下,肝谷氨酰胺濃度0~6 h快速升高,于6 h到達峰值,24 h后維持高于初始水平(圖4-a)。腦谷氨酰胺濃度,在0~6 h快速升高后回落,12~72 h維持上升趨勢(圖4-b)。鰓谷氨酰胺濃度在0~2 h快速升高后回落, 6~24 h再次升高,于24 h到達峰值,48 h后維持高于初始水平(圖4-c)。
2.4 堿脅迫下CPS、GS活性變化
堿脅迫下,肝GS活性0~6 h快速升高,12 h后再次升高于24 h到達峰值(圖5-a)。鰓GS活性0~4 h快速升高,6 h后再次升高于24 h出現峰值(圖5-b)。肝CPS活性在0~2 h迅速升高,2 h到達峰值后回落,12 h后維持高于初始水平(圖5-c)。
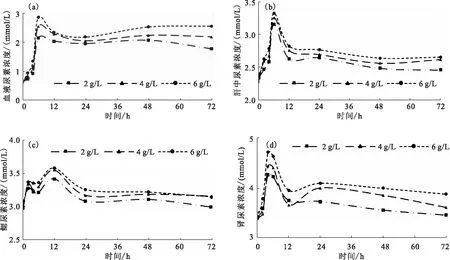
圖2 堿脅迫對尼羅羅非魚血液(a)、肝(b)、鰓(c)和腎(d)中尿素濃度的影響Fig.2 Effect of alkalinity stress on urea concentration in blood(a),liver(b),gill(c)and kidney(d)of O.niloticus

圖3 堿脅迫對尼羅羅非魚尿液中尿素與水體中尿素濃度的影響Fig.3 Effect of alkalinity stress on urea concentration in urinary of O.niloticus and urea in water
2.5 堿脅迫對尼羅羅非魚各基因在不同組織中的表達變化的影響
2.5.1 GS mRNA的相對表達變化
堿脅迫下,肝、腦GS基因的相對表達量隨時間的變化而升高,于24 h到達峰值,且不同堿度組間隨堿度提高而升高,其中6 g/L堿度組顯著高于其它堿度組(圖6)。
2.5.2 GLS2 mRNA的相對表達變化
堿脅迫下,鰓GLS2基因的相對表達量隨時間的變化而升高,于24 h達到峰值。不同堿度組間, 2~6 h差異不顯著,在12~24 h,6 g/L堿度組顯著高于其它組(圖7)。
2.5.3 CPS1 mRNA的相對表達變化
堿脅迫下,肝CPS1基因的相對表達量隨時間的變化而升高,于24 h到達峰值。在6 h、24 h,6 g/L堿度組顯著高于其它組,而其它時間點差異不顯著(圖8)。
3 討論
3.1 堿脅迫對血氨濃度變化的影響

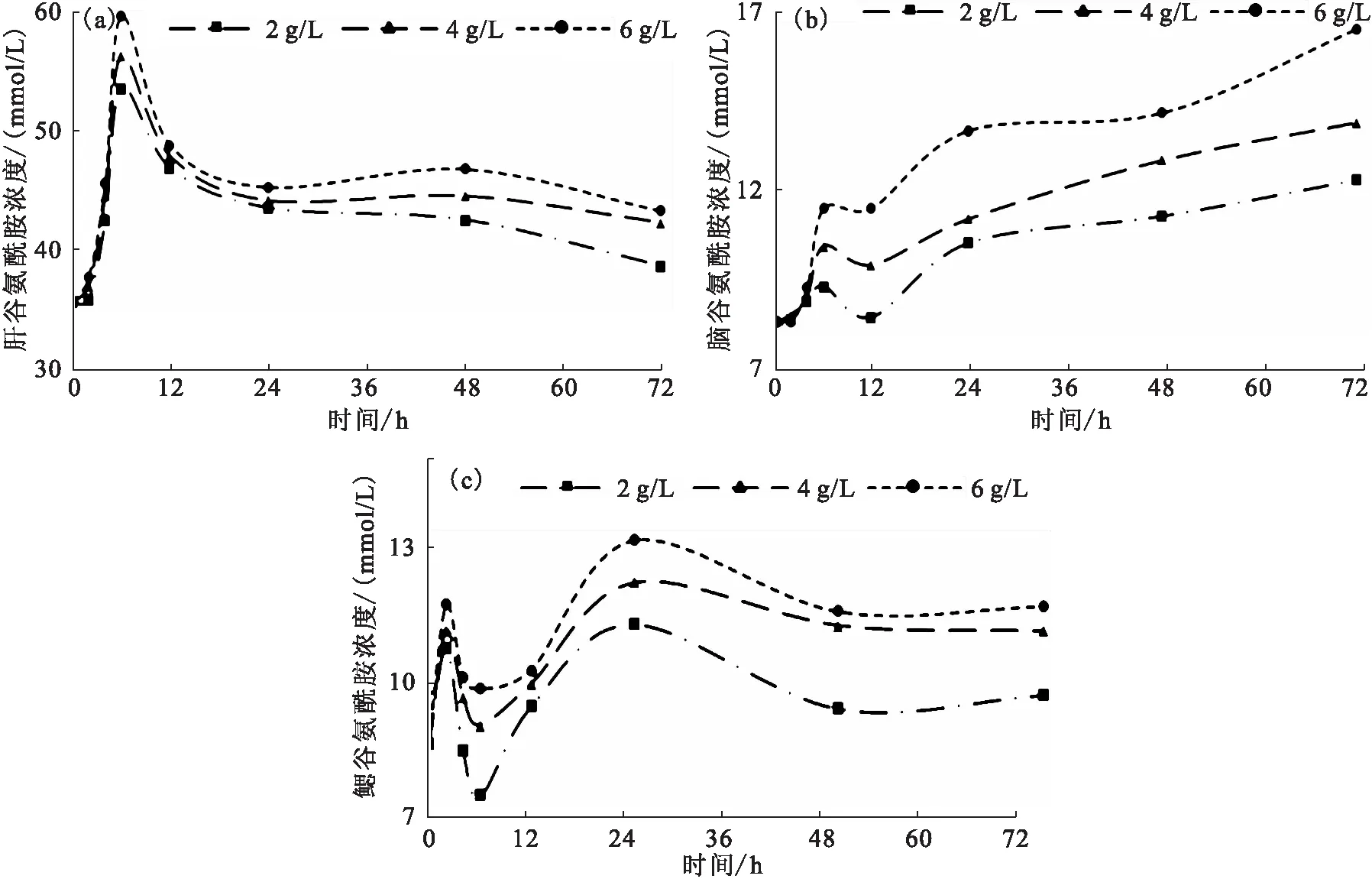
圖4 堿脅迫對尼羅羅非魚肝(a)、腦(b)和鰓(c)中谷氨酰胺濃度的影響Fig.4 Effect of alkalinity stress on glutamine concentration in liver(a),brain(b)and gill(c)of O.niloticus
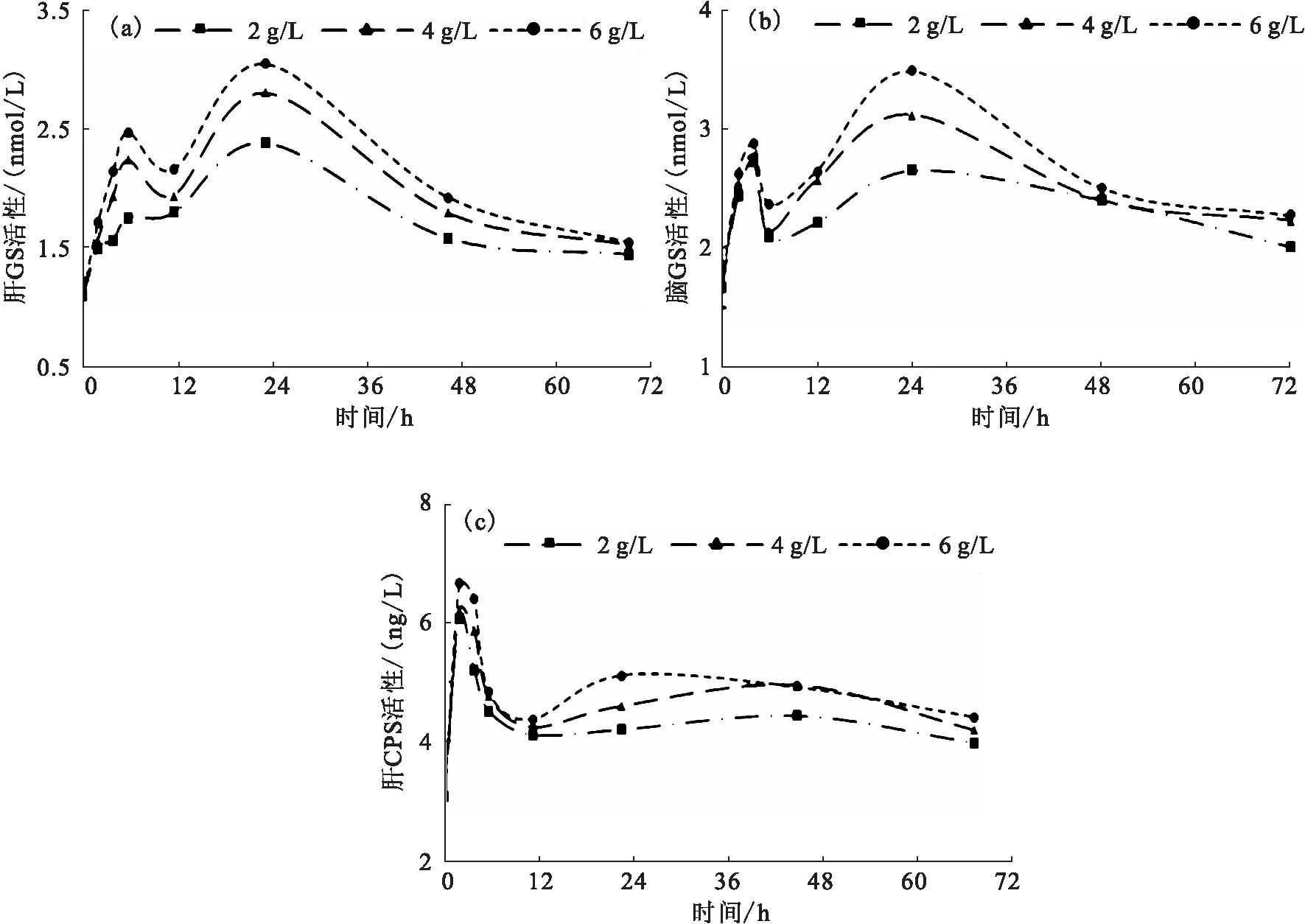
圖5 堿脅迫對尼羅羅非魚肝(a)、腦(b)中GS和肝中CPS(c)活性的影響Fig.5 Effect of alkalinity stress on GS activity in liver(a),brain(b)and CPS activity in brain(c)of O.niloticus
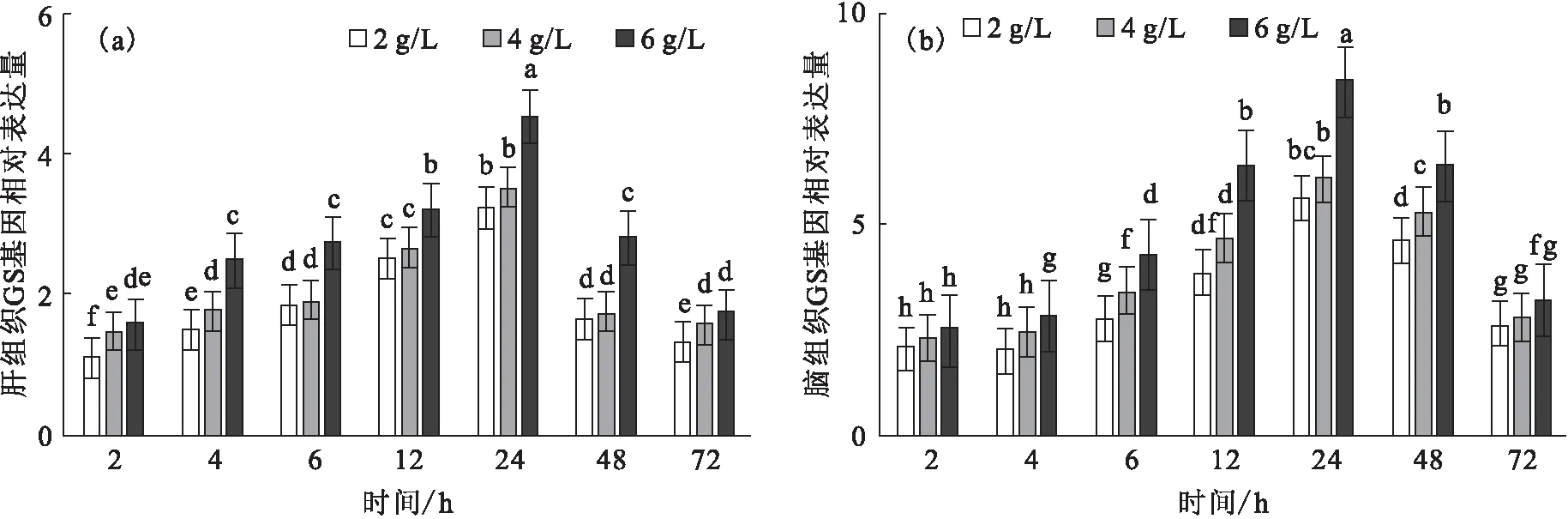
圖6 堿脅迫對尼羅羅非魚肝(a)和腦(b)GS基因的相對表達水平的影響Fig.6 Effect of carbonate alkalinity stress on relative expression of GS gene in liver(a)and brain(b)of O.niloticus注:標字母相同者表示差異不顯著(P>0.05),不同字母者表示差異顯著(P<0.05)。
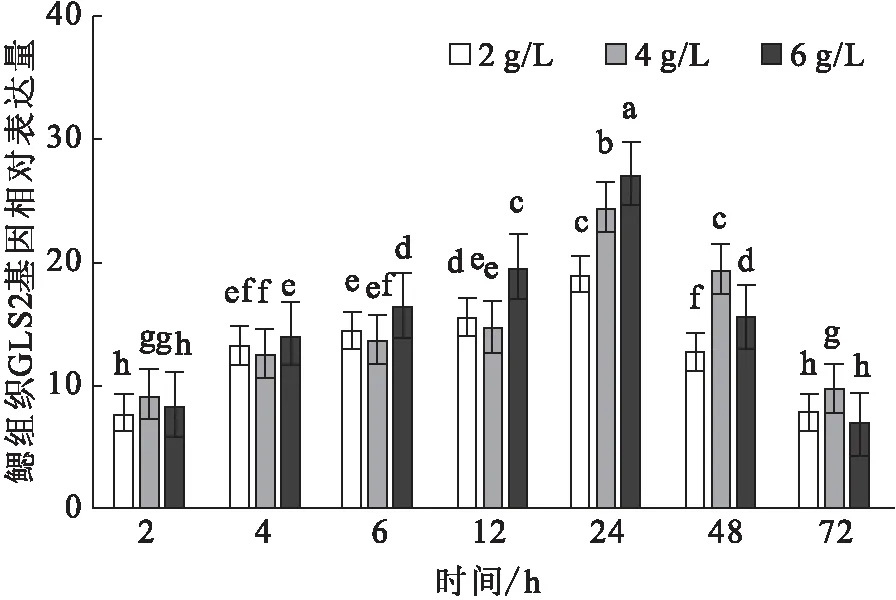
圖7 堿脅迫對尼羅羅非魚鰓中GLS2基因的相對表達水平的影響Fig.7 Effect of carbonate alkalinity stress on relative expression of GLS2 gene in gill of O.niloticus
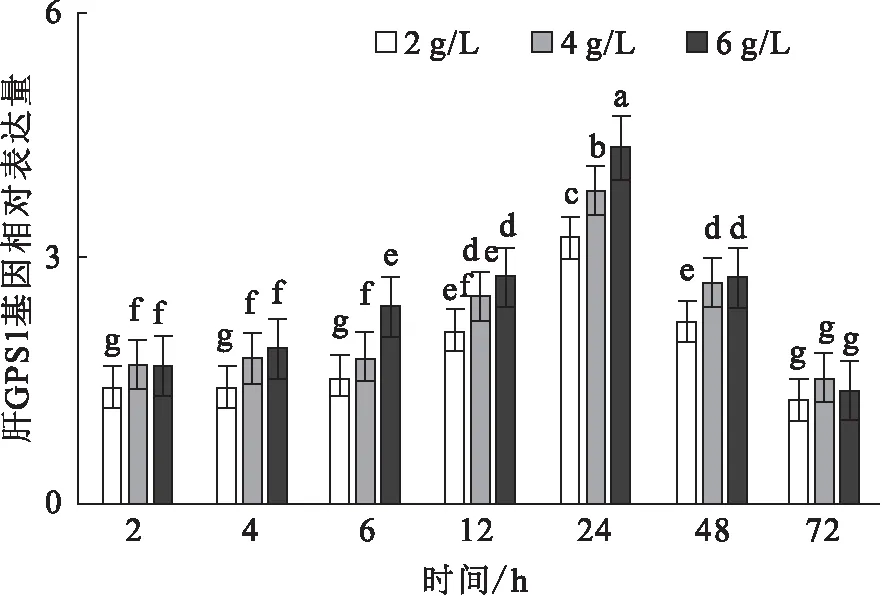
圖8 堿度脅迫對尼羅羅非魚CPS1基因的相對表達水平的影響Fig.8 Effect of carbonate alkalinity stress on relative expression of CPS1 gene in liver of O.niloticus
3.2 堿脅迫下氨的尿素代謝途徑的啟動
魚體內的氨經CPS催化產生氨甲酰磷酸等一系列生化反應,最終產生尿素[10],經血液循環到達腎臟后排出體外,此外鰓也是重要的排泄尿素的器官,存在專門處理尿素轉運的蛋白[22],如太平洋盲鰻的尿素主要依靠尿素轉運蛋白Ut從鰓中排出[23]。本研究中,脅迫開始后隨著血氨濃度的升高,尼羅羅非魚血液、肝、腎和鰓中尿素水平在0~6 h內即出現明顯升高,在生化水平上驗證了尼羅羅非魚體內氨的尿素代謝途徑開始發揮了作用。肝中CPS酶活在0~2 h活性明顯提升,及肝中CPS1基因的表達量也出現升高,在24 h出現最大值,這也從另一個側面印證了尼羅羅非魚氨的尿素代謝途徑能在0~6 h內迅速啟動。
已有研究表明大部分硬骨魚在鹽堿性水中以氨氮形式排泄60%~95%的含氮廢物,其余基本以尿素氮形式排出[24],如土耳其境內凡湖中的塔氏卡拉白魚(Chalcalburnustarichi)[25]、美國金字塔湖中的美洲鮭(Oncorhynchusclarkihenshawi)[26]。本研究中,水體中尿素濃度未發現明顯的變化,且不同堿度脅迫的情況下,肝臟中尿素水平也非常接近,表明尿素途徑可能并非是尼羅羅非魚降氨的主要途徑,而是原先正常的排氨途徑受到抑制情況下的一種快速且有限的補救手段,在青海湖裸鯉上也有類似發現[27]。
3.3 堿脅迫下氨的谷氨酰胺代謝途徑的啟動
本研究脅迫開始后,隨血氨的升高,肝谷氨酰胺濃度0~6 h快速升高,肝GS酶活性0~6 h快速升高,肝GS基因表達量也隨脅迫開始升高,且均隨堿度的提高而明顯升高,表明將氨轉化為谷氨酰胺的降氨機制開始啟動,并應對堿脅迫降氨作用中發揮了不同的效能。而鹽堿脅迫下GS基因表達量升高現象在青海湖裸鯉中也有發現[4]。谷氨酰胺對細胞膜具有很好的通透性,動物體內的氨即主要以谷氨酰胺的形式被運送到排泄部位[28],而魚體中谷氨酰胺會被運送到鰓,經由GLS重新分解成氨,沿血液-水的擴散梯度從鰓上皮排出[22,29],或借助轉運蛋白等載體排出[8]。在本研究中鰓GLS2基因的表達量隨時間的變化而升高,在24 h到達峰值,變化趨勢與肝中GS基因基本相似,則表明鰓將谷氨酰胺重新分解為氨排出體外的排氨機制也在迅速發揮作用。脅迫開始后腦GS基因的相對表達量的升高,腦GS酶活性的升高符合魚腦中具有高水平的GS活性,以保護其免受氨毒性的觀點[30]。馬加迪湖的羅非魚(Oreochromisalkalicusgrahami)在高氨氮環境中,能將體內過多的氨合成為谷氨酰胺儲存起來或用于其他代謝活動[31]在本研究腦谷氨酰胺濃度的持續升高的現象中得到印證。有的研究表明谷氨酰胺不僅是細胞外液中氨基酸的主要來源[32],還具有改進免疫細胞功能,提高應激反應能力等多種生理功能[33],同時近來的研究表明,魚類氨中毒死亡與星狀膠質細胞腫脹誘發的氧化損傷和免疫抑制有關[34],所以尼羅羅非魚在堿脅迫0~6 h內合成谷氨酰胺,可能并不只是為了降低體內氨的毒性效應,產生的谷氨酰胺還能夠參與調節尼羅羅非魚對脅迫的適應能力,保證機體存活。
4 結論
本研究表明在6 g/L以下堿脅迫的環境中,尼羅羅非魚能夠通過自身體內調節降低氨的濃度保證機體存活。在高堿脅迫下,原先通過鰓直接排氨途徑受到抑制,尿素代謝能力在0~6 h內快速提升,在12 h時到達最大效能后很快回落,因為堿度的提升而表現出明顯的增長,表明提高尿素合成只是其中一種補償機制。谷氨酰胺代謝能力在0~6 h內快速提升,在24 h到達最大效能,回落后依然持續在較高水平較長時間,且表現出隨堿度提升而增長,所以谷氨酰胺途徑應是尼羅羅非魚在堿脅迫下主要的降氨途徑。
參考文獻:
[1]中國農業部漁業管理局.2016中國漁業統計年鑒[M].北京:中國農業出版社,2016:1-2.
[2]王蘇民,竇鴻身.中國湖泊志[M].北京:科學出版社,1998:3-8,84-85.
[3]梁利群,任 波,常玉梅,等.中國內陸咸(鹽堿)水資源及漁業綜合開發利用[J].中國漁業經濟,2013,31(4):138-145.
[4]郭雯翡,么宗利,來琦芳,等.鹽堿脅迫下青海湖裸鯉鰓基因表達差異[J].海洋漁業,2012,34(2):137-144.
[5]Ip Y K,Chew S F,Randall D J.Ammonia toxicity,tolerance and excretion[J].Fish Physiol,2001,20(1):109-148.
[6]Tsui T K,Randall D J,Chew S,et al.Accumulation of ammonia in the body and NH3volatilization from alkaline regions of the body surface during ammonia loading and exposure to air in the weather loachMisgurnusanguillicaudatus[J].J Exp Biol ,2002,205(5):651-659.
[7]Benli A C K,K?ksal G,zkul A.Sublethal ammonia Exposure of Nile tilapia(OreochromisniloticusL.):Effects on gill,liver and kidney histology[J].Chemosphere,2008,72(9):1355-1358.
[8]Bolner K,Baldisserotto B.Water pH and urinary excretion in silver catfishRhamdiaquelen[J].J Fish Biol,2007,70(1):50-64.
[9]許友卿,李偉峰,丁兆坤.谷氨酰胺對水生動物免疫的影響及機理[J].動物營養學報,2012,24(3):406-410.
[10]Wood C M.Toxic response of the gill//Schlenk D,Benson W H.Target organ toxicity in marine and freshwater teleosts[M].London:Taylor & Francis,2001:1-89.
[11]Al-Amoudi M M.Acclimation of commercially cultured Oreochromis species to sea water-an experimental study[J].Aquaculture,1987 ,65(3-4):333-342.
[12]Lemarie G,Baroiller J F,Clota F,et al.A simple test to estimate the salinity resistance of fish with specific application toO.niloticusandS.melanotheron[J].Aquaculture,2004,240(1-4):575-587.
[13]么宗利,李思發,李學軍,等.尼羅羅非魚和以色列紅羅非魚耐鹽馴化初步報告[J].上海水產大學學報,2003,(2):97-101.
[14]邢憲利.鹽堿地池塘養殖羅非魚試驗[J].河北漁業,2010,(6):19-20.
[15]趙 巖,吳俊偉,孟 森,等.碳酸鹽堿度脅迫對尼羅羅非魚血清pH、游離氨濃度及相關基因表達的影響[J].南方農業學報,2016,47(6):1032-1038.
[16]吳俊偉,趙金良,趙 巖,等.高碳酸鹽堿脅迫對尼羅羅非魚氨代謝基因表達變化的影響[J].中國水產科學,2016 ,23(6):1290-1299.
[17]Wilkie M P,Wood C M.The adaptations of fish to extremely alkaline environments[J].Comp Biochem Physiol,1996,113(4):665-673.
[18]Parra J E G,Baldisserotto B.Effect of water pH and hardness on survival and growth of freshwater teleosts[M].USA:Science Publishers,2007 :135-150
[19]Binstock L,Lecar H.Ammonium ion currents in the squid giant axon[J].J Gen Physiol,1969,53(3):342-361.
[20]Cooper J L,Plum F.Biochemistry and physiology of brain ammonia[J].Physiol Rev,1987,67:440-519
[21]Wright P A,Wood C M.Muscle ammonia stores are not determined by pH gradients[J].Fish Physiol Biochem,1988,5(3):159-162.
[22]Wilkie M P.Ammonia excretion and urea handling by fish gills:present understanding and future research challenges[J].J Exp Zool,2002,293(3):284-301.
[23]Braun M H,Perry S F.Ammonia and urea excretion in the Pacific hagfish Eptatretus stoutii:evidence for the involvement of Rh and UT proteins[J].Com Biochem Phys A,2010,157(4):405-415.
[24]Wood C M.Ammonia and Urea Metabolism and Excretion[M].Boca Raton:CRC Press.1993:1-20.
[25]Danulat E,Kempe S.Nitrogenous waste excretion and accumulation of urea and ammonia inChalcalburnustarichi(Cyprinidae),endemic to the extremely alkaline Lake Van(Eastern Turkey)[J].Fish Physiol Biochem,1992,9(5-6):377-386.
[26]Wilkie M P,Wright P A,Iwama G K,et al.The physiological responses of the Lahontan cutthroattrout(Oncorhynchusclarkihenshawi),a resident of highly alkaline Pyramid Lake(pH 9.4),to challenge at pH 10[J].Exp Biol,1993,175(1):173-194
[27]衣曉飛,來琦芳,史建全,等.高堿環境下青海湖裸鯉氮廢物排泄及相關基因的表達規律[J].中國水產科學,2017,24(4):681-689.
[28]李少飛.中國對蝦氨氮代謝酶基因的cDNA克隆及其在氨氮解毒代謝過程中的作用[D].遼寧大連:大連海洋大學,2014.
[29]Evans D H,Piermarini P M,Choe K P.The multifunctional fish gill:dominant site of gas exchange,osmoregulation,acid-base regulation,and excretion of nitrogenous waste[J].Physiol Rev,2005,85(1):97-177.
[30]Wright P A,Steele S L,Hvitema A,et al.Induction of four glutamine synthetase genes in brain of rainbow trout in response to elevated environmental ammonia[J].J Exp Biol,2007,210(16):2905-2911.
[31]Jow L Y,Chew S F,Lim C B,et al.The marble gobyOxyeleotrismarmoratusactivates hepatic glutamine synthetase and detoxifies ammonia to glutamine during air exposure[J].J Exp Biol,1999,202(3):237-245.
[32]Kim M,Wischmeyer P E.Glutamine[J].World Rev Nutr Diet,2013,105 :90-96.
[33]Yin F G,Jiang W M,Guan S,et al.Glutamine and animal immune function[J].Food Agric Environ,2010,8(1):135-141.
[34]Ip Y K,Tay A S,Lee K H,et al.Strategies for surviving high concentrations of environmental ammonia in the swamp eelMonopterusalbus[J].Physiol Biochem Zool ,2004,77(3):390-405.

