磷脂復合物改善阿司匹林對大鼠胃腸道刺激性作用的研究
劉勃纓 ,姜雙瑜 ,李新悅 ,吳玉梅 ,張 瀛 ,徐松林
(1.天津中醫藥大學,現代中藥發現與制劑技術教育部工程中心,天津300193;2.天津中醫藥大學,天津市現代中藥重點實驗室-省部共建國家重點實驗室培育基地,天津300193;3.浙江海昶生物醫藥技術有限公司,杭州310000)
阿司匹林(asprin,ASP)又名乙酰水楊酸,具有解熱、鎮痛、抗癌、抗風濕作用[1],另外,阿司匹林能夠降低血小板黏附力,可以防止血栓形成和降低心腦血管疾病發病率,已常規用于冠心病及腦血栓的防治[2]。阿司匹林是傳統的非類固醇抗炎藥,它最大的問題是消化道的毒副作用[3-6],由于其酸性成分可透過胃黏膜上皮脂蛋白膜層,破壞脂蛋白膜的保護作用,使胃酸可逆地彌散到組織中損傷細胞,導致毛細血管破損而出血,這種嚴重的胃腸道不良反應限制了其在臨床的應用[7-10]。磷脂(phospholipid,PC)復合物是指藥物與PC以一定的配比關系結合而成的復合物[11]。磷脂是生命的基礎物質,它存在于人體的每一個細胞中,是細胞膜主要成分,在生物體內降解,無毒性、無免疫原性,可以降低阿司匹林對胃腸道的刺激[12-13]。本文通過大鼠胃腸道刺激性實驗來探究磷脂復合物對阿司匹林造成的胃腸道損傷的改善作用,從而為傳統的非類固醇抗炎藥的劑型研究提供新的方向。
1 材料與方法
1.1 藥物與試劑 阿司匹林普通腸溶片劑(浙江海昶生物醫藥技術有限公司,批號16112103-02,規格:81 mg);阿司匹林磷脂復合物(浙江海昶生物醫藥技術有限公司,批號:16122801,阿司匹林含量:42.7%);阿司匹林磷脂復合物膠囊(浙江海昶生物醫藥技術有限公司,批號16122802,規格:81 mg);生理鹽水(山東康寧藥業有限公司);多聚甲醛、甲醛溶液(天津市康科德科技有限公司)。
1.2 主要儀器 ASP200S自動真空組織脫水機,Leica EG1150H自動生物組織包埋機,Leica RM2255切片機,NikonCi-L顯微鏡。
1.3 實驗動物 清潔級雄性SD大鼠,體質量(220±20)g[天津中醫藥大學實驗動物中心,動物合格證號:SCXK(軍)2014-0001]。動物室溫度:(25±2)℃,相對濕度:(50±2)℃。健康雄性SD大鼠分為4組,每組10只,分別給予生理鹽水(2 mL)、阿司匹林片劑、阿司匹林磷脂復合物膠囊和阿司匹林磷脂復合物膠囊內容物,每次按300 mg/kg阿司匹林灌胃給藥。
1.4 實驗方法
1.4.1 動物處理 實驗前大鼠禁食12 h,每日灌胃1次,連續給藥14 d,后頸椎脫臼法處死動物并解剖取胃,向胃內注射多聚甲醛溶液2 mL。將胃浸入10%甲醛固定液中浸泡10 min,沿胃大彎開胃,生理鹽水洗凈胃內容物,所有胃組織均以10%甲醛固定液固定24 h,制作病理組織切片,照相,觀察胃部潰瘍的發生情況。
1.4.2 組織制片與觀察 解剖取材固定于10%甲醛固定液固定,組織經ASP200S自動真空組織脫水機脫水浸蠟,Leica EG1150H自動生物組織包埋機包埋,Leica RM2255切片機制片,HE染色,NikonCi-L顯微鏡觀察,HMIAS-2000高清晰度數碼顯微圖像分析系統采圖。
1.4.3 參考評價依據 根據胃黏膜的完整性及炎癥細胞的浸潤情況分為以下4種情況:正常(0分)胃黏膜結構完整,上皮細胞無缺損或脫落,排列整齊,胃底腺形狀規則,黏膜層偶見少量散在的炎癥細胞;輕度(1分)胃黏膜結構相對完整,上皮細胞無缺損或脫落,黏膜上皮及胃底腺整體排列較規則或局部欠規則,黏膜層上1/3可見較多炎癥細胞浸潤;中度(2分)胃黏膜結構不完整,黏膜上皮及胃底腺排列不規則,部分上皮細胞缺損或脫落壞死,黏膜層上2/3伴較多炎癥細胞浸潤;重度(3分)上皮細胞成片缺損或脫落壞死,黏膜層大于2/3甚至全層伴大量炎癥細胞浸潤,胃底腺結構紊亂。
1.5 統計學分析 采用SPSS17.0統計學軟件對數據進行相應的處理及分析,計量數據以分級評分表示,無損傷為0分,輕度1分,中度2分,重度3分。各組間的數據采用秩和檢驗分析方法進行分析,以P<0.05為差異有統計學意義。
2 結果
2.1 觀察結果 將病理切片分別置于低倍鏡和高倍鏡觀察胃的損傷情況,結果見圖1、2。
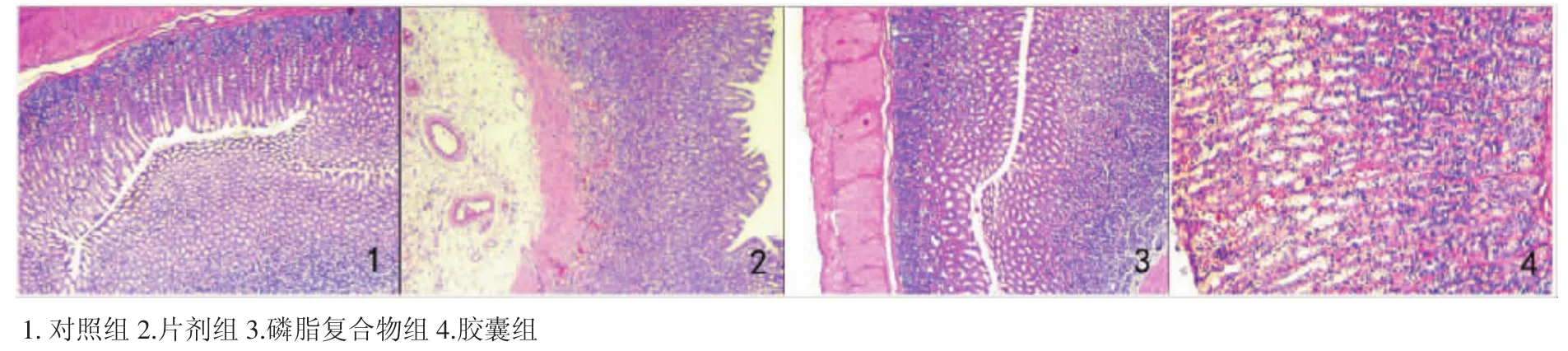
圖1 顯微鏡下觀察到的胃損傷圖像(×4)Fig 1 Images of the gastric injury observed with microscope(×4)

圖2 顯微鏡下觀察到的胃損傷圖像(×10)Fig 2 Images of the gastric injury observed with microscope(×10)
由圖1、2可知,對照組見胃黏膜結構完整,上皮細胞排列整齊,上皮細胞未見明顯缺損或脫落,胃底腺形狀規則,黏膜層偶見少量散在的炎癥細胞,黏膜肌層無增厚及向黏膜層擴張現象;4/10只動物黏膜下層至肌層間見輕度充血和水腫。
阿司匹林片劑組鏡下胃黏膜結構較完整,黏膜上皮排列規則,7/10胃底腺局部排列欠規則,黏膜層4/10輕度至重度以嗜中性粒細胞為主的炎癥細胞浸潤,7/10輕度至中度充血;9/10只動物黏膜下層至肌層間見輕度至中度充血和輕度水腫,8/10只動物輕度炎癥細胞浸潤。
阿司匹林磷脂復合物組鏡下胃黏膜結構較完整,黏膜上皮排列規則,4/10胃底腺形狀規則,黏膜層偶見少量散在的炎癥細胞,6/10輕度充血;4/10只動物黏膜下層至肌層間見輕度充血,8/10輕度水腫,2/10只動物輕度炎癥細胞浸潤。
阿司匹林復合物膠囊組鏡下胃黏膜結構較完整,黏膜上皮排列規則,4/10胃底腺局部排列欠規則,黏膜層3/10少量炎癥細胞浸潤,5/10輕度充血;9/10只動物黏膜下層至肌層間見輕度至中度充血,8/10輕度水腫,4/10只動物輕度炎癥細胞浸潤。
2.2 損傷情況 口服給藥14 d后胃潰瘍發生率見表1,由表可知,生理鹽水對照組胃潰瘍情況最低,阿司匹林普通片劑組胃潰瘍發生率最高,4組實驗對象具體胃損傷情況見表2。

表1 口服給藥14 d后各組胃損傷發生率Tab 1 Incidence of gastric injury after oral administration of 14 d in each group
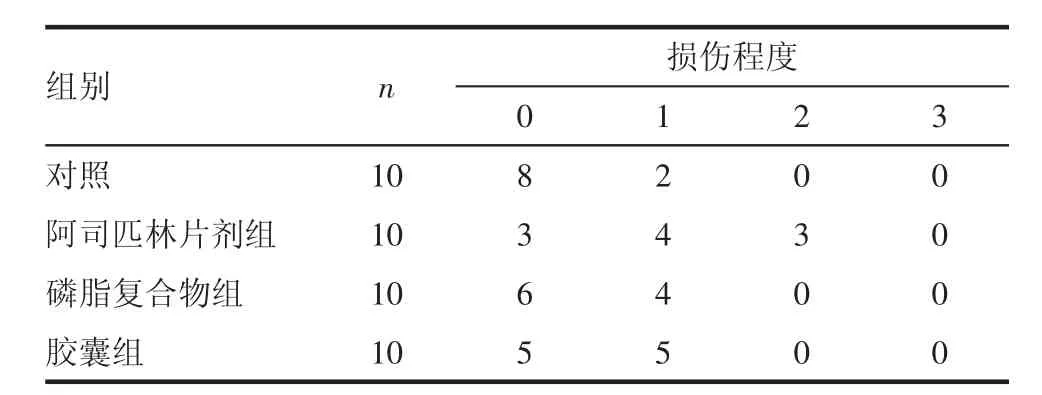
表2 各組胃損傷情況評分Tab 2 Gastric damage score in each group
由表1可知,對照組胃潰瘍發生率最低,阿司匹林磷脂復合物組和膠囊組相對較高,阿司匹林普通片劑組胃潰瘍發生率最高;采用秩和檢驗對表2所示的每組各級別損傷的樣本數進行統計分析,比較各組間差異,結果為阿司匹林普通片劑組與對照組生理鹽水相比,P<0.05,有統計學差異;阿司匹林磷脂復合物組和阿司匹林磷脂復合物膠囊組與對照組相比,結果均為P>0.05,沒有顯著性差異;阿司匹林片劑組與阿司匹林磷脂復合物組、阿司匹林磷脂復合物膠囊組相比,結果均為P<0.05,有統計學差異。說明阿司匹林磷脂復合物能有效降低阿司匹林對胃腸道的損傷。
3 討論
近年來,國內外相關文獻報道了多種類型的藥物與磷脂在一定條件下形成磷脂復合物后,使藥物的理化性質發生改變[14-16]。許建文等[17]對水飛薊賓-磷脂酞膽堿復合物的急性毒性的研究表明復合物的安全范圍很大,安全性好,其機制還有待進一步研究。目前,藥物磷脂復合物已應用于普通藥用劑型中,如已經用于糖漿劑、片劑、膜劑、膠囊劑、顆粒劑、口服液和適合局部用藥的乳劑、凝膠、水分散體等[18-20]。
本文通過兩周灌胃給藥后對大鼠胃部取材并制作病理切片,觀察阿司匹林藥物對胃腸道的損傷情況,通過與普通阿司匹林腸溶片比較可以發現,加工成阿司匹林磷脂復合物后對胃腸道的損傷明顯改善,這應該與磷脂本身的性質有關。活性成分通過與磷脂的極性基團相互作用而被固定,而磷脂的兩個長脂肪酸鏈不參與復合反應可自由移動,形成一個親脂性的表面[21],多個磷脂復合物分子有序排列形成一個球狀體將藥物中具有不良反應和刺激性的基團包裹起來,從而使得藥物的不良反應及刺激性明顯下降[17],確切的機制還有待研究。從實驗結果來看,阿司匹林磷脂復合物組胃組織無明顯病變,胃損傷情況與普通片劑組相比有顯著性差異(P<0.05),但將磷脂復合物制成膠囊對胃腸道保護作用沒有明顯提高,這可能是由于在給藥環節無法將整粒膠囊讓動物吞服,只能將膠囊內容物取出溶解再灌胃,從而失去膠囊這一劑型本身的優勢,進而影響實驗結果,但膠囊的劑型從生物利用度到患者順應性都有重要意義和研究空間。
[1]賀智勇,吳朝花,嚴俊麗,等.阿司匹林磷脂復合物的制備及其表征[J].中國藥房,2017,28(25):3562
[2]李成軍,馬丹丹,祝友朋,等.阿司匹林對大鼠胃潰瘍愈合的影響和機制[J].中國老年學雜志,2011,31(15):2898
[3]丁順,王昕.生姜對阿司匹林誘發胃潰瘍大鼠的胃粘膜保護作用研究[J].中國民族民間醫藥,2012,21(21):22
[4]顧同進,曹憶嶸.低劑量阿司匹林對黏膜損傷的防治[J].老年醫學與保健,2007,13(1):58
[5]練新飛,向定成.服藥時間對腸溶阿司匹林胃腸道副作用的影響[J].中國煤炭工業醫學雜志,2005,8(5):457
[6]Li J P,Guo J M,Hua Y Q,et al.The mixture of Salvia miltiorrhiza-Carthamus tinctorius (Danhong injection)alleviates low-dose aspirin induced gastric mucosal damage in rats[J].Phytomedicine,2016,23(6):662
[7]辛文妤,張雷明,王天,等.娑羅子提取物對阿司匹林致胃潰瘍作用的研究[J].中國藥物警戒,2010,7(6):321
[8]Mccarthy D M.Efficacy and gastrointestinal risk of aspirin used for the treatment of pain and cold[J].Best Pract Res Clin Gastroenterol,2012,26(2):101
[9]Saha L,Bhatia A,Chakrabarti A.Gastroprotective effect of bezafibrate,a peroxisome proliferator activated receptor agonist and its mechanism in a rat model of aspirin-induced gastric ulcer[J].Advanc Digest Med,2016,3(3):101
[10]Elshinnawy N A,Abdelmageid S A,Alshailabi E M.Evaluation of antiulcer activity of indole-3-carbinol and/or omeprazole on aspirin-induced gastric ulcer in rats[J].Toxicol Ind Health,2014,30(4):357375
[11]顧海濱.藥物磷脂復合物的研究進展[J].中國醫藥指南,2015,13(33):33
[12]翟光喜,婁紅祥,鄒立家,等.藥物磷脂復合物的研究進展[J].中國藥學雜志,2001,36(12):10
[13]郝海軍,張紅芹,賈幼智,等.采用制劑新技術提高中藥磷脂復合物的溶出度和生物利用度研究進展 [J].中草藥,2013,44(17):2474
[14]Semalty A,Semalty M,Singh D,et al.Development and characterizationofaspirin-phospholipidcomplexforimproveddrugdelivery[J].EpigenetPsychiatr,2010,35(2):79
[15]Tarnawski A S.Cellular and molecular mechanisms of gastrointestinal ulcer healing[J].Digest Dis Sci,2005,50(1):S24
[16]Giraud M N,Sanduja S K,Felder T B,et al.Effect of omeprazole on the bioavailability of unmodified and phospholipid-complexed aspirin in rats[J].Aliment Pharm Therap,2015,11(5):899
[17]許建文,張光軍,陳正躍.水飛薊賓-卵磷脂復合物制備工藝比較[J].中國生化藥物雜志,2002,23(5):245
[18]凌沛學,湯漩,王鳳山,等.藥物與磷脂復合物研究近況[J].中國藥學雜志,2005,40(6):401
[19]丁冬梅,張振海,蔣艷榮,等.中藥磷脂復合物的研究進展[J].中國中藥雜志,2013,38(13):2046
[20]李瑾,朱美娟,周凱,等.丹酚酸B磷脂復合物的制備和質量評價[J].廣州化工,2016,44(21):26
[21]廉潔,王伯初.藥物磷脂復合物工藝評價標準及應用研究進展[J].生物技術通訊,2006,17(5):830

