肝臟原發胃腸道間質瘤1例
王彥坤 李卿 劉暉 呂福東
患者男性,74歲,主因“發現肝內占位4年余,右上腹疼痛半年余”于2016年12月23日經門診以“肝占位”收治于首都醫科大學附屬北京佑安醫院。患者4年前體檢發現肝臟占位性病變,大小約4 cm,考慮肝囊腫,未特殊處置。患者提供外院腹部超聲示:肝左葉低回聲團塊,大小為45 mm×40 mm,邊界清;肝右葉可見厚壁無回聲,大小為129 mm×122 mm,內透聲差。本院增強CT(圖1)及MR檢查均示:于肝右葉查及囊實性占位1處,大小為129 mm×122 mm,考慮轉移的可能性大。實驗室血液檢查以及免疫學檢查結果均提示無明顯異常。患者于本院2018年1月11日行肝占位切除術。術后病理大體檢查腫物大小為5.5 cm×5 cm×5 cm,切面灰白、實性、質硬,鏡下腫瘤細胞呈梭形,漩渦樣排列,細胞排列較密集,輕度異型性,核分裂像<5個/50HF,部分見圍血管現象。免疫組織化學結果示:HBsAg(-),HBcAg(-),CK19(-),CD34(-),Hepa(-),GPC-3(-),Ki-67(15%+),P53(-),CK7(-),CgA(-),Syn(弱+),S100(-),HMB-45(-),Vimentin(+++),SMA(弱+),CK20(-),Villin(-),Desmin(-),EMA(-),CD117(+++)(圖2A),CD31(-),Dog-1(+++)(圖2B)。病理診斷為肝臟原發胃腸道間質瘤(gastrointestinal stromal tumors,GIST),高危險度(圖3)。
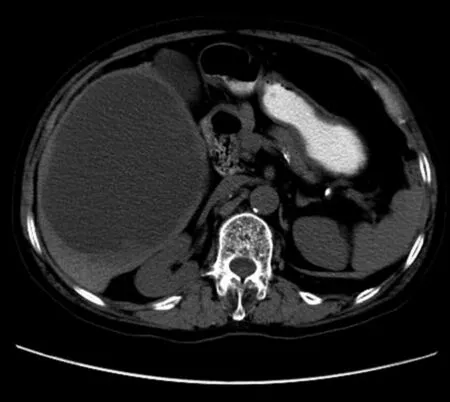
圖1 CT顯示肝右葉巨大類圓形低密度灶
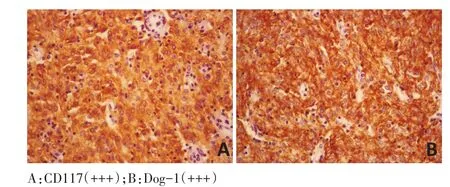
圖2 免疫組織化學陽性檢測結果(×400)
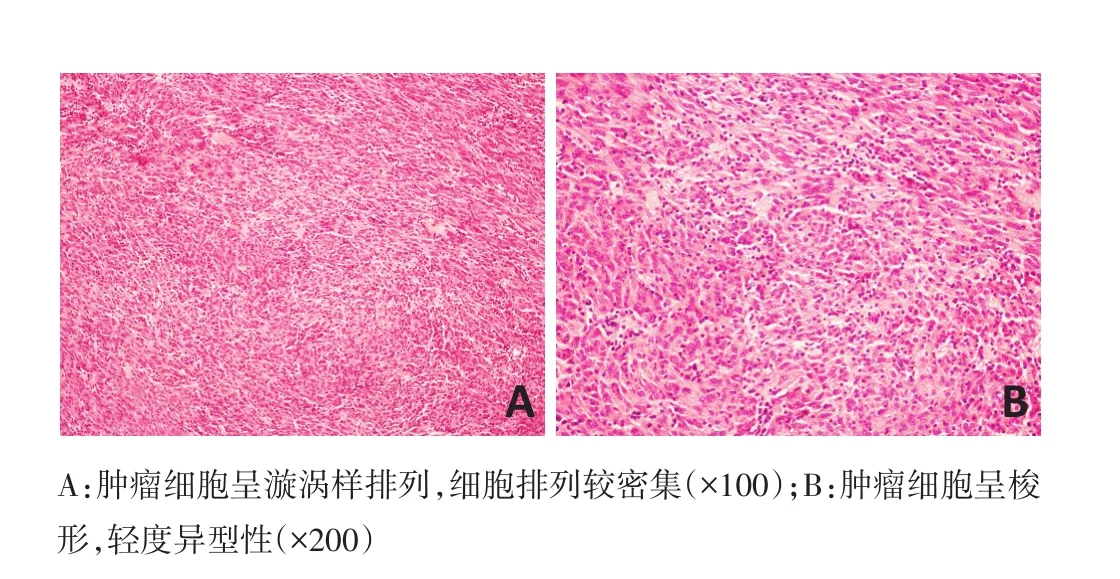
圖3 腫瘤組織的形態學結果(H&E染色)
小結GIST是一類起源于胃腸道間葉組織的腫瘤,占消化道間葉腫瘤的比例較高。GIST大部分發生于胃(50%~70%)和小腸(20%~30%),結直腸約占10%~20%,食管占0~6%,腸系膜、網膜及腹腔后罕見。GIST患者20%~30%為惡性,首次就診時約11%~47%發生轉移,轉移部位主要在肝和腹腔;原發于肝臟較為罕見。
GIST是一組主要來源于胃腸道間質組織的惡性腫瘤,含有梭形細胞、上皮樣細胞,高表達CD117。最初由Kindblom等[1]于1998年根據腫瘤的分化特征提出,為獨立來源于胃腸道間質干細胞(cajal細胞)的腫瘤。GIST的免疫組織化學染色CD117和CD34多為陽性,但引起GIST的原因尚不清楚。GIST可以起源于能夠分化慢起搏細胞的未分化的間質細胞。惡性GIST易通過血液轉移至肝臟。肝臟內若腫瘤組織形態符合GIST,并且有肝外原發性的GIST,則肝臟病變屬于繼發性GIST;否則,如同本例,結合患者提供的所有既往病例資料以及于本院行胃、腸和腹腔臟器的B超、CT、MR等影像學檢查和血液檢查均未能發現肝外的GIST,因此本病例應診斷為肝臟原發GIST,高危險度。
近年來隨著免疫組織化學、分子生物學及電鏡技術的不斷發展,對該病的認識不斷深入[2-4],發現這類腫瘤完全具有自身的形態、免疫和遺傳學特征,目前普遍接受GIST的診斷概念是胃腸道的非上皮性、非肌源性、非神經性腫瘤,病變多由c-kit基因突變引起,細胞形態主要由梭形和上皮樣細胞組成,免疫組織化學CD117、CD34陽性,主要發生于胃腸道,其次是腸系膜、腹腔、盆腔、卵巢,也可罕見于肝臟、胰腺、前列腺、膀胱和陰道等,均具有與GIST形態學、免疫表型及分子遺傳學的相同特征,統稱為胃腸道外間質瘤(extra-gastrointesti?nal stromal tumors,EGIST)。肝臟原發性間質瘤罕見,既往報道較少。廖輝軍等[5]報道1例原發性肝臟間質瘤并頸部淋巴結轉移的病例討論,在術前術中均排除胃腸道轉移可能,結合免疫組織化學CD117、CD34、Dog-1表達陽性且PDGFRA和c-kit基因無突變,確診為肝臟原發性間質瘤。本例肝臟原發性的GIST的特點是類圓形占位,逐步發展為中間壞死伴囊腔形成,腔內可伴有出血,超聲引導下細針穿刺或肝活檢行病理檢查和免疫組織化學染色是早期診斷的關鍵。
目前,盡管有國際現行的臨床診療指南可供參考,如美國國家綜合癌癥網絡(NCCN)和歐洲醫學腫瘤學會(ESMO),但尚不清楚這些是否適用于亞洲患者群體的臨床情況。2014年,來自亞洲的多個國家和地區(韓國、日本、中國、中國臺灣等)多個學科領域的專家,通過對GIST及相關的研究進行全面回顧和分析并分享經驗和觀點,從而達成了一定的共識[6]。腫瘤直徑1~35 cm不等且病理學診斷,胃腸道間質細胞的腫瘤大部分起源于胃(60%),30%源于小腸,罕見于網膜、腸系膜、骨盆及腹膜后腔。免疫組織化學染色中c-kit蛋白表達CD117(94%~98%),CD34陽性(60%~80%),血小板生長因子受體PDGFRA突變(5%~7%),SMA陽性(30%~40%)以及S-100表達陽性。DOG-1的表達不同于KIT/PDGFRA突變的GIST和野生型GIST。有研究指出[7-8],外科治療的基礎上根據病理分級的不同持續服用伊馬替尼,預后較好,且高劑量的伊馬替尼對亞洲人群更適用。
[1]Kindblom LG,Remotti HE,Aldenborg F,et al.Gastrointestinal pace‐maker cell tumor(GIPACT):gastrointestinal stromal tumors show phenotypic characteristics of the interstitial cells of Cajal[J].Am J Pathol,1998,152(5):1259‐1269.
[2]蘇韜,薛衛成.胃腸道間質瘤的TNM分期系統簡介[J].中華病理學雜志,2011,40(2):141‐142.
[3]王棟,夏立強,郝洪波,等.胃腸道間質瘤影像學表現與病理對照分析[J].實用醫學影像雜志,2009,10(6):372‐375.
[4]Miettirnen M,Majid M,Lasota J.Pathology and diagnostic criteria of gastrointerstinal stromal tumors(GISTs):a review[J].Eur J cancer,2002,38(5):39‐51.
[5]廖輝軍,聶劍宏,吳新軍.原發性肝臟間質瘤并頸部淋巴結轉移1例并文獻復習[J].中國普通外科雜志,2017,26(1):116‐120.
[6]Koo DH,Ryu MH,Kim KM,et al.Asian consensus guidelines for the diagnosis and management of gastrointestinal stromal tumor[J].Cancer Res Treat,2016,48(4):1155‐1166.
[7]Liu Z,Tian Y,Liu S,et al.Clinicopathological feature and prognosis of primary hepatic gastrointestinal stromal tumor[J].Cancer Med,2016,5(9):2268‐2275.
[8]Lim KT,Tan KY.Current research and treatment for gastrointestinal stromal tumors[J].World J Gastroenterol,2017,23(27):4856‐4866.

