腦小血管病影像學表現與血管性認知功能障礙相關性研究
張學艷,樊峰萍,苑聰聰,張 麗,趙曉紅,周 瑾
(河北省保定市第一中心醫院,河北 保定 071000)
腦小血管病(CSVD)是指不同病因引起的主要累及顱內小動脈、微動脈、前毛細血管及小靜脈的一組病變,臨床表現主要包括靜灶性腦梗死(無癥狀性腦梗死)、各種腔隙綜合征、認知功能障礙等,其影像學表現包括腔隙性腦梗死(LI)、腦白質變性(WML)、腦微出血(CMB)、血管周圍間隙擴大(VRS)。隨著醫學影像技術的迅猛發展,磁共振新序列的產生(如SWI)及神經影像檢查在人群中的普及和廣泛應用,使CSVD檢出率也大大提高。當前CVSD在腦血管病中占據重要地位,已成為國內外學者的研究熱點。近年來CVSD中LI、WML、CMB的臨床重要性越來越引起臨床關注,尤其是其與認知功能的關系方面,越來越多的報道顯示三者均與認知功能障礙有關,目前CSVD被認為是導致血管性認知功能障礙(VCI)的重要原因之一[1],而VCI是僅次于阿爾茲海默病(AD)導致老年人認知功能障礙的重要因素。在AD人群中,CSVD患病率占30%,其發病率之高、危害之大,越來越引起業內人士的高度關注。2008年第六屆世界卒中大會及歐洲卒中會議提出“小卒中,大麻煩”的論點,并強調早期識別和防治VCI的重要性[2]。LI、WML、CMB、VRS均可導致認知功能損害,它們既可單獨存在,也可同時存在,當同時存在時其相互作用可進一步加重認知功能損害。本研究分析了CSVD影像學表現與VCI之間的關系及CVSD相關危險因素,旨在為CSVD所致的VCI的早期預測診斷及防治提供理論依據。
1 臨床資料
1.1一般資料 收集2013年3月—2014年12月在我院神經內科門診及住院的CSVD患者60例,入組標準:年齡40~80歲,腦梗死發病10 d~6個月;符合LI綜合征臨床表現,但不伴有失語或意識障礙;腦MRI符合LI改變;頸部血管狹窄<50%;發病前無精神病史,無情緒障礙;簽署知情同情書。排除難控性高血壓(持續血壓≥220/120 mmHg,1 mmHg=0.133 kPa)者;有心房纖顫病史者;半年內心肌梗死病史者;頸部血管狹窄>50%者;其他病因腦梗死如動脈夾層、Moyamoya病、血管炎、CADASIL、FABRY和線粒體腦肌病者;有嚴重肝、腎疾病或惡性腫瘤者;有腦出血病史者;活動性出血性疾病者;嚴重出凝血障礙者。另選20例年齡40~80歲,經影像學檢查無異常的正常人為對照組。
1.2研究方法 對入選者進行一般資料收集,包括年齡、性別、身高、體質量、受教育年限,既往有無高血壓、冠心病、糖尿病、腦卒中等病史及心腦血管病家族史。將經MRI+MRA+DWI+SWI證實的CVSD患者按具體病情分為單純LI組、LI+WML組、LI+CMB組、LI+WML+CMB組,統計各組蒙特爾認知評估量表(MoCA)、簡易精神狀態量表(MMSE)評分,并與對照組進行比較,分析各組MMSE評分與MoCA評分相關性,采用Logistic回歸模型分析LI+WML+CMB組與對照組相關危險因素。
1.2.1影像學檢查方法 入選者均采用GE Signa 3.0T EXCITE HDMR系統,NV8通道頭顱線圈進行檢查,DWI和SWI圖像后處理在ADW 4.2工作站上進行。病灶判斷標準:由一名專業中樞組影像科醫師閱片,LI多分布在半卵圓區、側腦室旁白質、內囊、基底節、丘腦、腦干等部位,影像學表現為T1W1為低信號、T2W1為高信號、直徑小于15 mm的腔隙灶;WML為腦白質區的片狀T2WI或FLAIR高信號、T1WI偏低信號,邊界模糊;CMB在磁共振梯度回波成像(GRE)或磁敏感加權成像(SWI)序列上表現為2~10 mm的小灶樣、圓形、卵圓形、性質均一的低信號且周圍無水腫。
1.2.2神經心理功能評價方法 由1名神經內科醫師經過培訓后對研究對象進行MoCA、MMSE評估, 評估環境需保持安靜,僅測試者與研究對象兩人進行,量表評定時間間隔應超過30 min,每個量表用時約10 min,測試由一人獨立完成。MMSE量表包括定向力(10分)、記憶力(3分)、注意力和計算力(5分)、回憶能力(3分)、語言能力(9分)五部分內容。判定標準:①認知功能障礙,最高分為30分,分數27~30分為正常,分數<27分為認知功能障礙。②癡呆劃分標準,文盲≤17分,小學程度≤20分,中學程度(包括中專)≤22分,大學程度(包括中專)≤23分。③癡呆嚴重程度分級,MMSE評分≥21分為輕度,10~20分為中度,≤9分為重度。MoCA量表包括視空間及執行能力(5分)、命名(3分)、注意力(3分)、計算力(3分)、語言(3分)、抽象(2分)、延遲回憶(5分)、定向力(6分)8項,如受教育年限≤12年則加1分,最高分30分,≥26分為正常。
1.2.3危險因素評估及定義 高血壓診斷標準:連續2次在非同一天測量血壓收縮壓≥140/90 mmHg(1 mmHg=0.133 kPa),或卒中后2周血壓仍≥140/90 mmHg。糖尿病診斷標準:空腹血糖≥7.0 mmol/L,或餐后血糖≥11.1 mmol/L,或葡萄糖耐量試驗2 h血糖≥11.1 mmol/L,或糖化血紅蛋白≥6.5%。高血脂癥診斷標準:總膽固醇≥6.22 mmol/L,或高三酰甘油≥2.26 mmol/L,或低密度脂蛋白≥4.14 mmol/L,或受試者報告的經醫生診斷的高血脂癥。吸煙史定義為吸煙量≥10支/d,≥20年,或≥20支/d,≥10年;嗜酒史定義為乙醇攝入量≥60 g/d。

2 結 果
2.1CVSD各組與對照組一般資料比較 CVSD各組除高血壓和腦卒中次數與對照組比較差異有統計學意義外(P均<0.05),其余指標比較差異均無統計學意義(P均>0.05)。見表1。
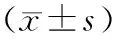
表1 CVSD各組與對照組一般資料比較
注:性別女=0,男=1;吸煙、飲酒、高血壓、高血脂、高Hcy血癥、冠心病、糖尿病、家族史無=0,有=1;①與對照組比較,P<0.05。
2.2CVSD各組與對照組MMSE評分和MoCA評分比較 單純LI組、LI+WML組、LI+CMB組、LI+WML+CMB組MMSE評分和MoCA評分均明顯低于對照組(P均<0.05),且單純LI組、LI+WML組、LI+CMB組間MMSE評分和MoCA評分比較差異均無統計學意義(P均>0.05),但3組均明顯高于LI+WML+CMB組(P均<0.05)。見表2。
2.3CVSD各組不同等級認知功能障礙情況 4組均以輕度認知功能損害為著,LI組、LI+WML組、LI+CMB組輕度認知功能損害發生率比較差異無統計學意義(P>0.05),但3組均明顯低于LI+WML+CMB組(P<0.05)。見表3。
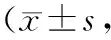
表2 CVSD各組與對照組MMSE評分和MoCA評分比較分)
注:①與對照組比較,P<0.05;②與LI+WML+CMB組比較,P<0.05。

表3 CVSD各組不同等級認知功能障礙情況比較 例(%)
注:①與LI+WML+CMB組比較,P<0.05。
2.4CVSD各組及對照組MMSE評分中各項目評分比較 CSVD各組時間定向、注意計算、語言理解及圖像描述評分均明顯低于對照組(P均<0.05),LI+CMB組、LI+WML+CMB組短程記憶評分和LI+WML組、LI+WML+CMB組語言表達評分明顯低于對照組(P均<0.05)。見表4。
2.5MMSE評分與MoCA評分相關性 Pearson相關分析顯示,LI組、LI+WML組、LI+CMB組、LI+WML+CMB組、對照組MMSE評分與MoCA評分均呈正相關(r=0.915,0.677,0.893,0.871,0.572,P<0.05)。
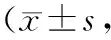
表4 CVSD各組及對照組MMSE評分中各項目評分比較分)
注:①與對照組比較,P<0.05。
2.6LI+WML+CMB組與對照組相關危險因素Logistic回歸模型分析顯示,高血壓(P=0.009,OR=31.087)、糖尿病(P=0.049,OR=16.849)與CSVD密切相關。見表5。

表5 LI+WML+CMB組與對照組相關危險因素的Logistic回歸模型多因素分析
3 討 論
隨著人口老齡化的到來, VCI作為繼AD之后的第二大癡呆類型越來越引起人們的重視,而CSVD在VCI的發生發展中起著重要作用,其中約一半的VCI是由CSVD引起的[3]。因CSVD起病隱襲,過去人們只重視由其引起的軀體癥狀,忽視了CSVD也是引起VCI的重要因素,導致VCI的發生,嚴重影響患者的生活質量。CSVD多指腦小動脈及微動脈的血管病變,微小動脈是指直徑在30~800 μm(多數在100~400 μm)、沒有側枝吻合的解剖終末動脈,此類動脈病變病理學表現多為纖維素樣或淀粉樣變性、出血、閉塞等,并不是動脈粥樣硬化。CSVD引起腦實質損害的機制非常復雜,現在仍不十分明確。Greenberg等[4]研究認為在各種危險因素及遺傳因素作用下,導致小血管內皮細胞破壞,引發小血管疾病,使腦血流量降低、少突膠質細胞凋亡、血腦屏障破壞以及炎癥反應,從而引起一系列的病理改變;此外腦小動脈及微動脈大多為終末動脈,不與其他動脈形成吻合,很容易出現低灌注和缺血性損傷,影響與神經細胞的物質能量交換,導致相應腦組織持續緩慢性損傷,逐步造成認知功能障礙[5]。
目前CSVD尚無規范的診斷標準,因現有的影像學技術不能在活體組織中觀察到顱內小血管,且病理資料難以獲得,CSVD的診斷主要依靠其定義、臨床表現及影像學特點。本研究結果顯示單純LI組、LI+WML組、LI+CMB組、LI+WML+CMB組均有認知功能障礙發生,且以輕中度認知功能障礙為主,其中LI+WML+CMB組最為顯著,認知功能損害主要以語言理解、言語表達及圖像描述等執行功能損害為重,其次計算、記憶力也有一定程度下降。說明LI、WML、CMB、VRS均可導致認知功能損害,它們既可單獨存在,也可同時存在,當同時存在時,其相互作用可進一步加重認知功能損害。
LI多分布在半卵圓區、側腦室旁白質、內囊、基底節、丘腦、腦干等部位,在CT上呈低密度,在磁共振T1加權像為低信號,且與腦脊液影像非常接近,在液體衰減反轉恢復序列(FLAIR)上呈邊緣高信號環影,可區別于VRS。影像學的LI直徑在DWI上為3~20 mm的高信號病灶;病理學的LI最大直徑定義為15 mm,而最小直徑的標準尚未達成共識,研究多選擇的病灶界值是3 mm,必須強調的是LI不能等同于CSVD。CSVD主要累及顱內細小動脈,其病理改變并非動脈粥樣硬化,影像上可表現為LI。但并非所有LI都是CSVD的影像學表現,其中的病因及發病機制不同,部分LI的病因是由大動脈粥樣硬化血栓形成致血管狹窄及遠端低灌注或心源性/動脈-動脈微栓子栓塞所致。LI作為腦梗死的一種常見類型,主要是由高血壓、糖尿病等因素導致腦內小動脈的結構發生變化,腦血流自動調節機制受損,最終引發腦梗死。其特點為梗死體積小、多發,可在沒有明顯神經系統局灶體征情況下出現明顯的認知功能障礙[6]。LI的部位與VCI關系密切,如內囊后角的病灶與執行功能受損相關聯,額葉的病灶與記憶障礙及執行功能、編碼、管理信息功能障礙相關聯;枕葉腔隙灶與視覺障礙相關;顳葉病灶與記憶、語言、聽覺及情感障礙相關;丘腦前部的病灶與遺忘相關聯。研究表明,LI的數目、體積、部位在癥狀性腦卒中中是處理速度及執行功能損害的獨立預測因子[7]。本研究發現,單純LI組MMSE評分及MoCA評分均低于對照組,說明LI的發生在一定程度上對老年人認知功能障礙確實存在一定影響,其可能的發病機制是LI破壞了與信息處理速度、記憶及執行功能相關的額葉-皮質下環路[8]。
Hachinska[9]于1986年最早提出WML的概念,在很長的一段時間里被人們所忽視,然而隨著近年來對WML不斷深入的研究,人們逐漸意識到WML患者并非無癥狀,它不但與認知功能障礙密切相關,還影響著腦卒中的發生、發展、治療及預后。WML是發生在側腦室旁、半卵圓中心的腦白質脫髓鞘性病變,可能與高血壓密切相關[10]。在CT上呈低密度,邊界模糊;磁共振T1加權像呈稍低信號,T2加權或FLAIR序列呈高信號[11]。WML機制目前尚不明確,內皮細胞功能障礙、血腦屏障通透性增加、炎性反應、頸靜脈回流受阻等在WML中發揮著重要作用[11]。Wen等[12]研究表明腦白質疏松可增加多發性腦梗死患者認知功能損害的風險,其機制可能為腦室旁邊緣環路及投射纖維受損,減慢神經信號傳導及處理速度,從而導致認知功能障礙。Jokinen等[13]的研究顯示,早期WML對認知功能影響相對較小,明顯的WML才會引起嚴重的認知功能障礙。WML能預測CSVD及VCI的嚴重程度。
CMB是指顱內微小血管周圍含鐵血黃素、脫氧血紅蛋白和鐵蛋白等沉積所致的一種腦實質亞臨床損害,多數無臨床癥狀,且腦CT及MRI很難檢測出來。隨著影像學技術的發展,尤其是磁共振梯度回波成像(GRE)或磁敏感加權成(SWI)序列的出現,使CMB的檢出率大大提高,因其與認知功能密切相關,并能增加腦出血風險,近年來逐漸引起人們的廣泛關注并成為國內外學者研究的熱點話題。CMB在T2-GRE或SWI上表現為直徑為2~5 mm的圓形、卵圓形低信號影,周圍無水腫。不同部位CMB的病理機制不同,高血壓性腦血管病所致的CMB多發生在基底節-丘腦區,腦淀粉樣血管病所致的多發生在腦葉。Seo等[14]研究顯示,VCI患者中CMB發生率高達84.9%,且CMB是VCI的獨立預測指標。CMB導致VCI的機制尚不明確,可能是通過直接損傷腦組織,使皮質-皮質下聯系纖維及白質傳導通路受損[15];也可能是CMB本身導致腦組織低局部灌注和長期慢性缺血,間接引起臨近腦組織功能紊亂,干擾神經元生物電活動所致。Goos等[16]研究結果顯示,CMB數量越多,認知功能損害越嚴重,CMB常常與WML、LI并存,且其與腦白質損害的嚴重程度及LI數目有關,三者相互作用,共同促使血管性認知功能障礙的發生及發展。本研究結果顯示,LI+WML+CMB組MMSE評分和MoCA評分均明顯低于其他組,說明當LI、WML、CMB同時存在時可進一步加重認知功能的損害。
MMSE量表是國際上公認的、普遍使用的、最具影響的認知功能障礙篩查工具之一,包括定向力、記憶力、注意力和計算力、回憶能力、語言能力五部分內容,受教育程度對其影響較小[17-18]。本研究結果顯示MMSE評分與MoCA評分呈正相關性,故通過MMSE評分進一步對認知功能各項進行研究,結果顯示以語言理解、言語表達及圖像描述等執行功能損害為重,其發病機制主要包括前額葉-皮質下環路受損和長聯絡纖維受損兩種學說。
目前關于CSVD的危險因素的研究結果不甚相同。本研究結果顯示,高血壓、糖尿病與CSVD密切相關。高血壓是CSVD的重要危險因素之一,其發病機制可能是高血壓導致動脈硬化及血管自主調節功能喪失,影響腦組織血液灌注,引起LI、WML、CMB,從而進一步導致認知功能減退,預防卒中復發及認知功能障礙的有效措施之一即積極平穩的控制血壓。高血糖在CSVD導致VCI的發生、發展過程中起到同樣重要作用,其可能的發病機制為高血糖破壞血腦屏障,并通過神經毒性、氧化應激反應及長期高血糖所致無氧代謝及酸中毒導致代謝紊亂,破壞信號分子,導致腦組織、顱內大血管及微血管廣泛性損傷,加之糖尿病患者胰島素受體介導的神經營養作用減弱或消失,神經元功能紊亂,進一步導致認知功能下降。
綜上所述, LI、WML、CMB均可導致認知功能障礙,三者并存時最為明顯,且以輕度認知功能障礙為主,其認知功能損害以時間定向、注意計算、短程記憶、語言理解、言語表達及圖像描述為主;高血壓、糖尿病均與可導致血管性癡呆的CSVD密切相關,積極控制血壓及血糖有助于降低CVSD發生率,為防治VCI提供了一定依據。
[參考文獻]
[1] Ihara M. Management of cerebral small vessel disease for the diagnosisand treatment of dementia[J]. Brain Nerve,2013,65(7):801-809
[2] Hachinski V. World Stroke Day 2008:“little strokes, big trouble”[J]. Stroke,2008,39(9):2407-2408
[3] Zhang AJ,Yu XI,Wang M. The clinical manifeastations and pathophysilogy of cerebral small vessel diease[J]. Neurosci Bull,2010,26(3):257-264
[4] 曹金強,吉訓明. 腦小血管疾病[J]. 罕少疾病雜志,2011,18(6):42-46
[5] 張微微. 腦小血管病的新進展[J/CD]. 中華腦血管病雜志:電子版,2008,2(4):210-213
[6] Grau-Olivares M,Arboix A Bartrés-Faz D,et al. Neuropsychological abnorm alities associated with lacunar infarction[J]. J Neurol Sci,2007,257(1/2):160-165
[7] Edwards JD,Jacova C,Sepehry AA,et al. A quantitative systematic review of domain-specific cognitive impairment in lacunar stroke[J]. Neurol,2013,80(3):315-322
[8] 周瑞,胡芙君,尹虹祥,等. 腦梗死患者病灶部位與認知損傷的相關性研究[J]. 神經損傷與功能重建,2009,4(3):203-204
[9] Hachinski VC,Potter P,Merskey H. Leuko-araiosis:an ancient term for an new problem[J]. J Neurol Sci,1986,13(4):533-534
[10] Vannorsdall TD,Waldstein SR,Kraut M,et al. White matter abnormalities and cognition in a community sample[J]. Arch clin Neuropsychol,2009,24(3):209-217
[11] 霍迪,豐宏林. 腦白質疏松的相關研究新進展[J]. 醫學綜述,2015,21(2):269-271
[12] Wen HM,Mok VCT,Fan YH,et al. Effect of white matter changes on cognitive impairment in patients with lacunar infarcts[J]. Stroke,2004,35(8):1826-1830
[13] Jokinen H,Gouw AA,Madureira S,et al. Incident lacunes influence cognitive decline:the LADIS study[J]. Neurol,2011,76(22):1872-1878
[14] Seo SW,Hwa Lee B,Kim EJ,et al. Clinical significance of microbleeds in subcortical vascular dementia[J]. Stroke,2007,38(6):1949-1951
[15] Imamine R,Kawamura T,Umemura T,et al. Does cerebral small vessel disease predict future decline of cognitive function in elderly people with type 2 diabetes[J]. Diabetes Res Clin Pract,2011,94(1):91-99
[16] Goos JD,Kester MI,Barkhof F,et al. Patients with Alzheimer disease with multiple microbleeds:relation with cerebralpinal fluid biomarkers and cognition[J]. Stroke,2009,40(11):3455-3460
[17] Ciesielska N,Sokoowski R,Mazur E,et al. Is the Montreal Cognitive Assessment (MoCA) test better suited than the Mini-Mental State Examination (MMSE) in mild cognitive impairment (MCI) detection among people aged over 60? Meta-analysis[J]. Psychiatr Pol,2016,50(5):1039-1052
[18] Zhang H,Zhang XN,Zhang HL,et al. Differences in cognitive profiles between traumatic brain injury and stroke:A comparison of the Montreal Cognitive Assessment and Mini-Mental State Examination[J]. Chin J Traumatol,2016,19(5):271-274

