不同血液透析方式對終末期糖尿病患者微炎癥狀態、胰島素抵抗和β2微球蛋白水平的影響及意義
何揚彪
(金華市中醫醫院 腎病風濕免疫科,浙江 金華 321000)
糖尿病腎病(diabetic nephropathy,DN)是指由糖尿病(diabetes mellitus,DM)本身引起的腎臟損傷,臨床特征為蛋白尿、漸進性腎功能損害、高血壓、水腫等,若不及時治療,最終可發展為腎衰竭[1-2]。近年來,維持性血液透析(maintenance hemodialysis,MHD)在DN患者中的應用逐漸增加,而隨著患者生存時間的延長,多種慢性并發癥的表現逐漸突出,其中,心血管疾病(cardiovascular disease,CVD)成為長期透析患者的主要并發癥和致死原因[3]。研究顯示,胰島素抵抗(insulin resistance,IR)、微炎癥狀態作為CVD的危險因素,與DN患者血液凈化的效果密切相關[4]。鑒于此,本研究對比研究了高通量血液透析(high-flux hemodialysis,HFHD)和低通量血液透析(low-flux hemodialysis,LFHD)對DN患者微炎癥狀態、IR和β2微球蛋白(β2-MG)水平的影響及安全性,旨在為臨床治療提供參考。
1 資料和方法
1.1一般資料選擇2014年1月—2016年12月在我院就診的DN患者60例,納入標準:(1)均為2型DM,符合WHO制定的DM診斷和分型標準;(2)病因為DN所致終末期腎衰,腎小球濾過率(GFR)低于15mL/min,需行MHD治療;排除標準:(1)合并急性心血管事件、急性感染、惡性腫瘤等疾病或除DN以外的其他腎臟疾病;(2)近期有輸血、激素、免疫抑制劑或抗炎類藥物治療史;(3)試驗期間原有疾病加重或患新病。根據治療方法不同將本組患者分為HFHD組和LFHD組,每組30例。其中,HFHD組男19例,女11例;年齡47~75歲,平均59.32±10.57歲;病程9~22年,平均16.84±3.19年。LFHD組中男17例,女13例;年齡46~78歲,平均60.08±10.63歲;病程9~21年,平均16.79±3.22年。2組一般資料差異無統計學意義(P>0.05)。
1.2方法血液透析均采用反滲水和碳酸氫鹽透析液,流量為500 mL/min,每周透析3次,每次4 h;采用動靜脈內瘺建立血管通路,治療時血流量200~250 mL/min,肝素或分子肝素抗凝。HFHD組選用高通量聚砜膜透析器(德國費森尤斯公司生產),膜面積1.3 m2,超濾系數40 mL·h-1·mmHg-1·m-2;LFHD組選用低通量聚砜膜透析器,膜面積1.3 m2,超濾系數5.5 mL·h-1·mmHg-1·m-2。兩組患者均常規補充鐵劑、葉酸、碳酸鈣補充劑、皮下注射促紅細胞生成素(EPO)糾正貧血等治療,血壓偏高者予以ACEI/ARB類和(或)CCB類藥物控制血壓,血糖升高者口服降糖藥或皮下注射胰島素。
1.3觀察指標分別于首次透析前、透析3個月后抽取患者的外周靜脈血,常規離心,分離血清,置于-20℃冰箱保存,待檢。(1)炎癥指標:超敏C反應蛋白(hs-CRP)采用免疫散射比濁法檢測,白細胞介素6(IL-6)和腫瘤壞死因子-α(TNF-α)采用雙抗夾心ELISA法測定;(2)IR:采用全自動生化分析儀檢測空腹血糖(FPG),放射免疫分析法測定空腹胰島素(FINS),應用穩態模型(Homa)評估IR指數(HOMA-IR),HOMA-IR=FPG×FINS/22.5;(3)β2-MG:采用膠乳增強免疫透射比濁法測定;(4)統計并發癥及不良反應情況。
1.4統計學分析采用SPSS 21.0軟件進行數據統計,計量資料采用t檢驗,計數資料采用χ2檢驗;P<0.05為差異有統計學意義。
2 結果
2.1透析前后患者微炎癥狀態、IR及β2-MG水平比較透析后,HFHD組hs-CRP、IL-6、TNF-α、HOMA-IR和β2-MG水平均較透析前明顯下降,且各指標顯著低于LFHD組;差異均有統計學意義(P<0.05);LFHD組各項指標在透析后無明顯改變,與透析前比較,差異不具有統計學意義(P>0.05),見表1。
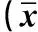
表1 兩組透析前后微炎癥狀態、IR及β2-MG水平比較±s)
注:與透析前比較,△P<0.05;與LFHD組同期比較,*P<0.05。
2.2并發癥及不良反應情況透析期間,患者出現低血壓、頑固性高血壓、失衡綜合征、出血、酮尿癥重度、皮膚瘙癢等不良反應;HFHD組不良反應總發生率26.67%,顯著低于LFHD組(56.67%),差異有統計學意義(χ2=5.554,P<0.05)。
3 討論
DN是DM最重要和最常見的并發癥之一,隨著我國老齡化程度的加深以及人們飲食習慣的改變,DM的發病率不斷增加,DN亦呈增長趨勢,已成為僅次于腎小球腎炎的第二大誘發終末期腎病的疾病原因[5]。研究發現,DN患者普遍存在IR和微炎癥狀態[6]。IR可促進脂肪細胞產生和釋放游離脂肪酸(FFAs)增多,前者可通過產生大量的細胞因子如IL-6、TNF-α等,促進血管硬化;而FFAs可誘導血管舒縮的急性改變,導致內皮損傷;此外,IR可導致脂質異常改變,引起血管炎性改變。微炎癥狀態可增加DN患者發生CVD并發癥的幾率,因為微炎癥時血漿蛋白組成發生變化、血管內皮和脂蛋白結構和功能的變化以及由此引起的血小板、中性粒細胞、單核細胞表面配位體的改變,共同促進血管內皮細胞的損傷[7]。已有研究證實,微炎癥狀態、IR是造成DN病情惡化和CVD等并發癥發生的重要影響因素[8]。因此,逆轉IR和清除炎癥因子對于DN的臨床治療具有重要的價值。
目前,血液透析在DN患者的應用逐漸增加,主要利用半透膜的原理,清除體內毒素和過多水分,補充體內需要物質,糾正電解質和酸解平衡紊亂,其中主要包括LFHD和HFHD兩種模式。LFHD主要清除小分子毒素,不能有效清除IL-6、TNF-α、β2-MG等中、大分子毒素[9]。本研究結果顯示,LFHD組各項指標在透析后無明顯改變(P>0.05),反而有上升趨勢,考慮可能是在透析過程中由于血液動力學改變、壓力和機械因素,激活了氧化應激反應,促發炎性反應所致。HFHD是利用高通量血液濾器的大孔徑透析膜和較高的超濾系數,依靠彌散、對流和吸附的方式清除溶質,其中彌散作用主要清除小分子毒素,對流作用可清除低分子蛋白,可通過對流和吸附作用清除炎癥介質,增加中、大分子清除率;此外,高通量透析器具有良好的生物相容性,可減少透析患者的補體激活及炎性反應,更好地提高HFHD的安全性,減少不良反應的發生[10]。
本研究結果表明,透析后,HFHD組hs-CRP、IL-6、TNF-α、HOMA-IR和β2-MG水平均較顯著低于LFHD組;而透析期間,HFHD組不良反應總發生率顯著低于LFHD組。可見,與LFHD相比,HFHD在改善DN患者微炎癥和IR狀態、提高腎功能、減少透析并發癥等方面更具優勢。但由于本研究樣本量較少,且觀察時間較短,HFHD能否長期持續改善DN患者的IR、微炎癥狀態,仍需大樣本、長程的研究證實。

