一個響應土壤缺鐵擬南芥突變體的分離及鑒定①
王立賽,閆明科,王 晗,沈仁芳,蘭 平*
?
一個響應土壤缺鐵擬南芥突變體的分離及鑒定①
王立賽1,2,閆明科1,2,王 晗1,沈仁芳1,蘭 平1*
(1土壤與農業可持續發展國家重點實驗室(中國科學院南京土壤研究所),南京 210008;2中國科學院大學,北京 100049)
鐵是植物生長發育必需的一種微量元素,但土壤中植物可直接吸收利用的鐵非常有限。缺鐵使作物生長受限,進而影響人類膳食健康。植物體能通過調節一系列基因表達的變化來響應缺鐵,但目前對該調控系統的研究仍不完善。()是擬南芥中一個強烈響應缺鐵的基因,本研究將該基因啟動子連接熒光素酶報告基因并轉化擬南芥,進一步通過T-DNA的隨機插入得到一個響應缺鐵信號的突變體庫。通過篩選該突變體庫,我們得到一個強烈響應缺鐵信號的突變體L22-8。和野生型相比,正常情況下L22-8地上部和地下部內源的表達量均顯著增高,缺鐵處理時其地上部表達量仍高于野生型,而地下部則不明顯。定量結果顯示,和等植物鐵代謝關鍵調控因子的表達發生了顯著變化,但植株總鐵、磷、鋅的含量較野生型并沒有顯著區別,表明該T-DNA的插入雖影響了植株對缺鐵脅迫的響應,但并不直接作用于植株對鐵的吸收、轉運上。反向PCR分析發現L22-8的T-DNA插入位點位于和之間,且這兩個基因的轉錄表達在正常生長條件下均略低于Col-0。基因互補實驗發現僅有能部分互補L22-8的熒光信號,表明基因的表達影響了對缺鐵脅迫的響應。本研究進一步擴展了植物吸收利用鐵的分子調控網絡,為分子育種工作提供了指導。
土壤;缺鐵脅迫;突變體鑒定;分子調控
鐵是動植物生長必需的、需求量最大的微量營養元素[1],在高等植物的光合作用和呼吸作用等多種生命活動中起非常重要的作用[2],同時也是許多功能蛋白的重要輔助因子[3]。植物缺鐵會導致作物產量和品質的降低,危害人體的營養健康,如人體貧血的一個常見原因就是鐵元素的缺乏。雖然鐵在地殼中的含量豐富,但因為鐵元素大多以Fe3+的形式存在,在中性和堿性土壤中的溶解度極低,從而限制了土壤中鐵的有效性,使得植物生長易受缺鐵的限制[4-5],隨著土壤鹽堿化程度加劇,植物缺鐵現象愈發普遍。因此,闡明植物體內鐵平衡機制、通過育種工作提高植物體內鐵含量有益于促進農業發展和人體健康[6-7]。植物在長期的進化過程中,演化出一套完整的鐵吸收、轉運的分子調節系統。根據植物對鐵吸收機制的不同,分為兩大類:非禾本科植物所采用的機理Ⅰ,及禾本科植物所采用的機理Ⅱ[8]。其中機理Ⅰ又可分為3個組成部分,即H+-ATPase泵系統、Fe3+還原系統和Fe2+轉運系統。一些H+-ATPase(HA)基因,如擬南芥中的基因的表達,能通過H+-ATPase作用將H+分泌到質外體[9]。功能缺失突變體的分析發現是引起缺鐵誘導根際酸化的主要成員[10]。H+的分泌可以降低土壤pH,提高土壤中鐵等營養元素的溶解性[11],通過根細胞質膜上的鐵離子螯合還原酶(ferric-chelate reductase oxidase,FRO)和與之偶聯的NADPH脫氫酶,如擬南芥中的Fe3+螯合還原酶將Fe3+還原為Fe2+[12],再通過一系列鐵轉運蛋白(iron-regulated transporter,IRT),如擬南芥中的IRT1將還原的Fe2+轉運到細胞內[13],之后通過其他的一些轉運載體運送到植物各個細胞器或器官中供機體利用。采用機理Ⅱ的禾本科植物可在根部合成高鐵載體(Phytosiderophores,PS)如麥根酸類物質(mugineic acid, MA)并分泌到土壤中,這類物質對Fe3+具有很高的親和性,可以促進低鐵環境下根際鐵的活化。Fe3+-PS螯合物經YS1(YELLOW STRIPE 1)和YSL(YELLOW STRIPE1-like)轉運載體吸收至胞內,再釋放出Fe3+供代謝利用[14]。
近年來的轉錄組和分子遺傳學分析鑒定得到了一系列與植物鐵吸收利用相關的基因和蛋白,如非禾本科植物鐵吸收的重要調控基因和。首次在番茄中被鑒定出來,其編碼一個bHLH轉錄調控因子[15];當環境中鐵濃度過低時表達增強,過高時則在轉錄后水平上受到抑制[16]。擬南芥中的(FER-like iron deficiency-induced transcription factor)是番茄基因的同源基因,主要在根部受缺鐵脅迫誘導表達,且只在缺鐵脅迫下,才能激發上下游基因的相互作用[7]。FIT可以與bHLH蛋白家族(AtbHLH38、AtbHLH39、AtbHLH100、AtbHLH101)形成異源二聚體,有效誘導和基因的表達,從而提高植物對缺鐵脅迫的耐受性[17-18]。有研究證實,bHLH轉錄調控因子ROREYE(PYE)在缺鐵條件下對根的生長起重要作用,PYE負調控植物體內鐵平衡相關基因的表達[19]。bHLH34、bHLH104與bHLH105能夠形成同源二聚體或異源二聚體,激活和的轉錄表達,進而激活下游鐵吸收及轉運相關基因的表達,bHLH104與bHLH105可與鐵吸收負調控因子E3泛素連接酶BTS相互作用,以此防止植物對鐵的過量吸收[6,20-21]。雖然前期研究已經得到了FIT等眾多鐵代謝相關的調控基因和蛋白,但仍有很多響應土壤鐵含量變化的基因功能未被闡明,特別是一些用來維持植物體內鐵穩態的負調控因子,仍需進一步探索[3,7,14]。
編碼細胞色素P450 (CYTOCHR-OMEP450)蛋白,能夠強烈響應缺鐵脅迫。細胞色素P450基因家族成員、()、()均屬缺鐵脅迫上調基因,且擬南芥基因在缺鐵脅迫下響應最為強烈,有研究表明基因通過其啟動子部位的IDE1-like序列(iron deficiency-responsive element)響應鐵缺乏的早期反應[22]。為尋找到更多早期響應缺鐵脅迫的調控因子,本文以模式植物擬南芥為研究材料,首先分離出基因的啟動子,再連接報告基因,構建成pCAMBIA2300-::基因表達載體,通過轉化擬南芥得到T-DNA隨機插入突變體庫,然后通過確定突變體的T-DNA插入位點,找到影響基因轉錄表達的上游基因。探索可能存在的調控基因表達的新的調控因子,并探討新調控因子的基因功能。旨在完善植物缺鐵響應的分子調控網絡,并為促進植物高效利用土壤中鐵元素打下理論基礎。
1 材料與方法
1.1 植物材料與突變體庫的建立
供試材料為擬南芥(L.) Columia -0生態型(Col-0)。以擬南芥Col-0基因組DNA為模板,擴增目的基因啟動子(1149bp),所用引物:F:5’- AAGGTTTTCT-CTGATTGGAAATTG-3’, R:5’-ACGCGATTGAA-GAGTAGTGTCTGTC-3’,兩條引物5’ 端分別帶有Ⅰ與Ⅰ酶切位點。如圖1,PCR產物經酶切后連接pCAMBIA2300-載體,構成目的基因表達載體pCAMBIA2300-::。實驗中所用酶均為Thermo Scientific產品。

圖1 載體構建
通過農桿菌轉化法得轉基因株系,抗性(卡那霉素,Kanamycin)篩選得到單拷貝純合株系,通過熒光觀察從中選取一到兩株符合缺鐵表達特性的穩定表達株系作為母本,再次進行T-DNA插入突變,篩選過程中尋找特殊熒光變化的株系,構建突變體庫。
1.2 材料處理與方法
1.2.1 種子處理及培養條件 擬南芥種子表面消毒:首先使用75% 酒精洗滌2 ~ 3 min;再經 Tween (0.5%,/),NaClO (0.5%,/)的混合水溶液震蕩洗滌10 min,最后使用滅菌超純水洗5 ~ 6遍。播種前4 ℃春化1 ~ 2 d,根據不同實驗項目播種到正常或缺鐵培養基上,生長于恒溫培養箱中(22 ℃,60 μmol/(m2·s),16 h光照,8 h黑暗)。正常及缺鐵處理培養基:ES培養基(5 mmol/L KNO3, 2 mmol/L Ca(NO3)2, 2 mmol/L MgSO4, 2.5 mmol/L KH2PO4, 70 μmol/L H3BO3, 14 μmol/L MnCl2, 0.2 μmol/L Na2MoO4, 1 μmol/L ZnSO4, 0.5 μmol/L CuSO4, 10 μmol/L NaCl, 40 μmol/L Fe-EDTA,10 g/L蔗糖,0.918 g/L MES,8 g/L瓊脂,用1 mmol/L NaOH 調節pH 至5.5;缺鐵處理(即ES培養基中除不添加Fe-EDTA,添加100 μmol/L Ferrozine螯合培養基中的多余鐵元素,其他均一致),121 °C高溫滅菌20 min。種子抗性篩選培養基用1/2MS(Duchefa Biochemie公司)+ Kanamycin (50 mg/L)。
1.2.2 熒光檢測及篩選 將在正常培養基上生長10 d的擬南芥幼苗分別轉移至正常和缺鐵培養基表面繼續培養3 d,均勻噴灑熒光底物D-Luciferin(1 mmol/L D-Luciferin+0.01% TritonX-100)處理3 min后,通過化學發光儀(Tanon-5200,中國)拍攝熒光信號。
1.2.3 轉錄水平基因表達量檢測 將在正常培養基上生長10 d的擬南芥幼苗移至正常和缺鐵培養基上繼續生長3 d,地上部與地下部分開取材。用Trizol法提取樣品RNA,并使用Nanodrop2000及電泳檢測RNA濃度及質量。采用PrimeScript RT reagent Kit (TaKaRa) 將RNA反轉為cDNA,用于基因轉錄表達的半定量及定量檢測。用TaqMix酶(康維)進行半定量的PCR擴增檢測,用實時定量PCR儀(Thermo PIKOREAL96)對基因表達進行定量檢測,內參基因選用(),基因相對表達量用2-△△Ct公式計算。半定量、定量檢測所需引物:-RT-S: 5’-CCAGCTAACGACATCTACAACG-3’,-RT-A: 5’-GTAGTCGGTCTTGCTATCCATG-3’;-F: 5’- GTGCTGAAGGTGGAGACGAT-3’,-R: 5’- AACACGAAGACCGAACGAAT-3’。同時將,,,作為缺鐵處理的標記基因。
1.2.4 甲基化分析 通過在線甲基化分析及引物設計軟件(MethPrimer)分析插入T-DNA片段最可能發生甲基化的片段并設計引物。取正常培養基上生長10 d的Col-0及L22-8擬南芥幼苗用CTAB法提取DNA,經甲基化變性試劑盒EZDNA Methylation-Gold kit對Col-0和L22-8基因組DNA進行亞硫酸氫鹽變性,并用軟件設計的引物擴增。擴增條帶經凝膠回收(Axygen AxyPrep DNA Gel Extraction Kit)后連接pEASY-Blunt Zero克隆載體,分別取Col-0和L22-8的6個克隆進行測序分析。引物序列:-Fb:5’-TTTAATTTTAAAAGTTTAATATTGGT-GA-3’,-Rb: 5’-CAAAATCCATACATA-AACTACTTTTT-3’。
1.2.5 插入位點的鑒定 根據pCAMBIA2300載體選取EcoRⅠ與EcoRⅤ同時酶切Col-0與L22-8株系DNA,通過T4連接酶將酶切片段連接成環,在pCAMBIA2300載體上設計引物擴增環狀DNA片段得L22-8特異條帶,擴增引物:p2300-LB-S:5’- TGCCTCGTCCTGGAGTTCAT-3’,p2300-LB-A:5’- AGCGTTGGCTACCCGTGATA-3’。膠回收(Axygen AxyPrep DNA Gel Extraction Kit)目標片段連接到pEASY-Blunt Zero克隆載體,測序后比對確定T-DNA插入位點。
1.2.6 植物總磷、總鐵、總鋅含量測定 將在正常培養基上生長21 d的擬南芥幼苗轉移至正常及缺鐵培養基繼續生長5 d,取地上部,105 ℃殺青30 min,70 ℃烘干至恒重,用HNO3-H2O2消煮[23]至澄清的消解液,用電感耦合等離子發射光譜儀(ICP)對P、Fe、Zn元素含量進行檢測。總共進行3個生物學重復。
1.2.7 數據處理 應用Excel 2007進行數據的處理并統計分析,TTEST檢測以<0.01為極顯著差異,用“**”表示,以<0.05為顯著差異,用“*”表示。圖表用Origin 8.0生成。
2 結果與分析
2.1 L22-8的發現及檢測
在轉基因篩選單拷貝純合株系過程中發現突變體L22-8。如圖2A顯示,L22-8表現為在正常生長條件下熒光信號強烈高于其他純合株系(如L10-9等)。進一步分析發現,L22-8在缺鐵處理下雖然仍會被強烈誘導,但無論在正常生長條件下還是缺鐵處理下L22-8熒光信號均強烈高于L10-9(圖2B)。半定量檢測結果表明,外源基因轉錄表達在正常和缺鐵處理下的地上部與正常生長條件下的地下部均明顯高于L10-9(圖2C)。
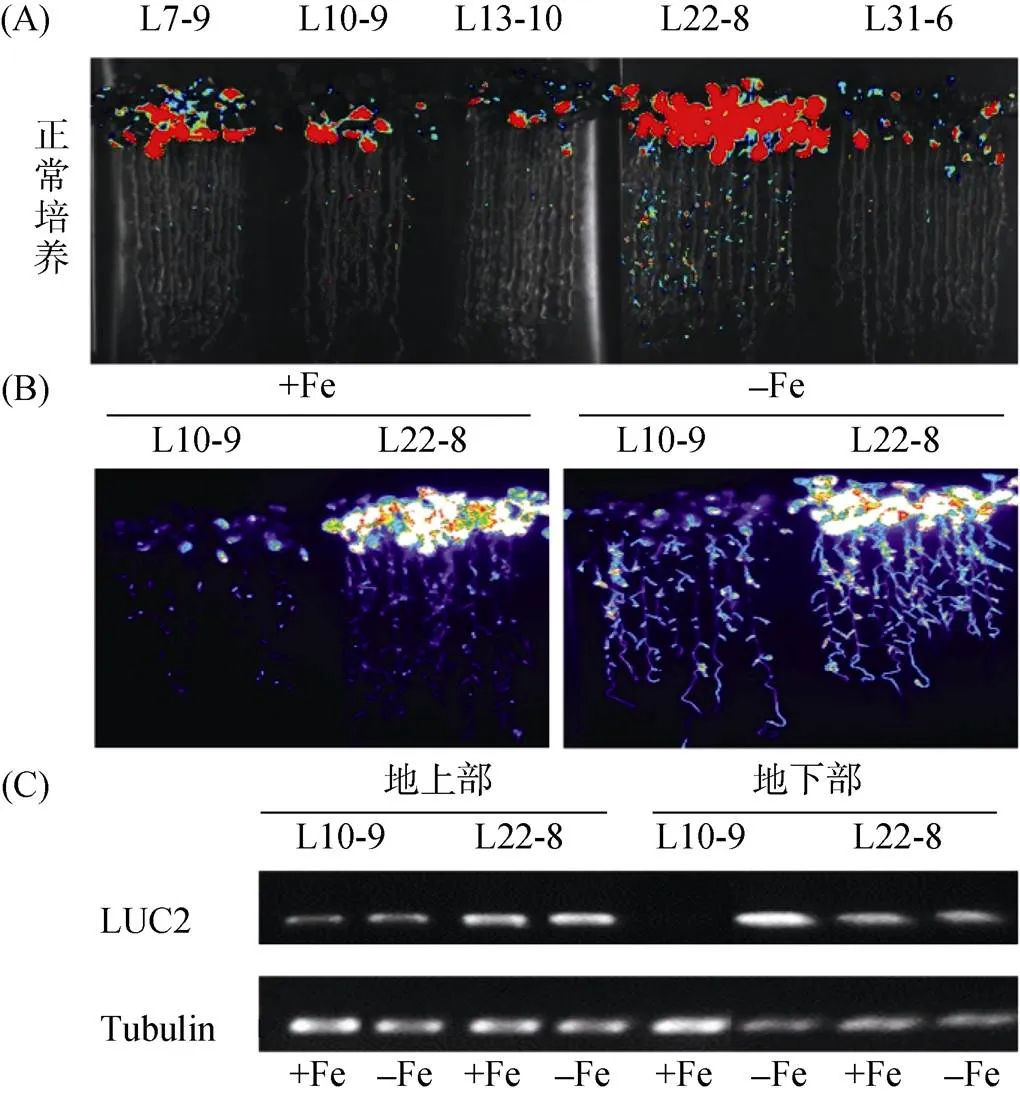
圖2 突變體的獲得及進一步驗證
2.2 突變體內源基因CYP82C4的表達差異
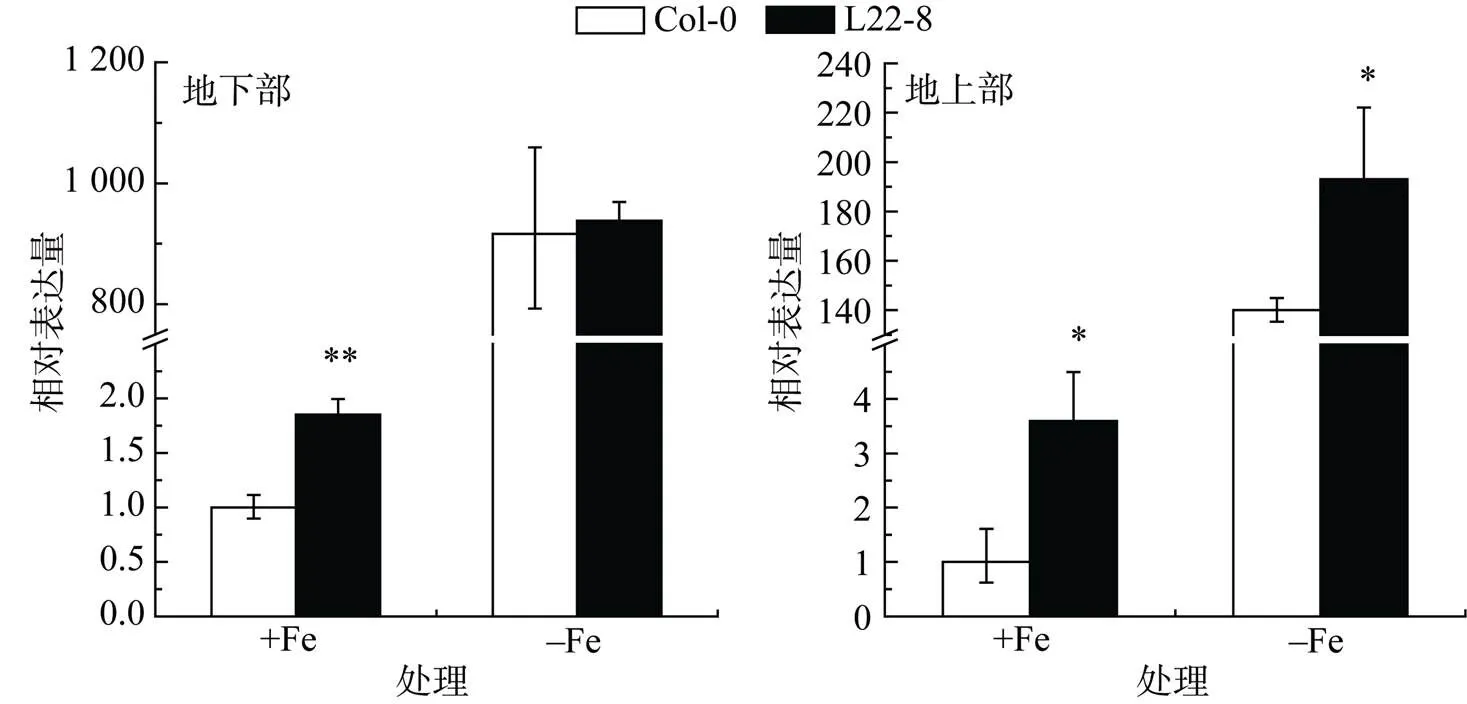
為確定突變體L22-8內源基因是否發生變化,我們使用實時定量PCR對轉錄表達進行了檢測。圖3顯示,地下部基因的表達量表現為,正常生長條件下,L22-8高于Col-0,但缺鐵處理下,L22-8與Col-0沒有表現出顯著差異。地上部基因的表達量表現為,無論正常生長條件下還是缺鐵處理下,L22-8均顯著高于Col-0。
2.3 幾種響應缺鐵脅迫標記基因的定量檢測
為確定缺鐵響應標記基因的表達在L22-8中是否發生改變,通過實時定量PCR方法對植株地下部幾種響應鐵缺乏主要的標記基因的轉錄表達進行了檢測。結果如圖4顯示,突變體L22-8缺鐵處理下的表達量明顯高于Col-0,而在缺鐵處理條件下受調控的鐵吸收相關Marker基因與在L22-8中的表達量沒有發生顯著差異。在正常生長條件下,L22-8中與的表達量均沒有表現出與Col-0的顯著不同,僅的表達量略高于Col-0。但無論在正常生長條件還是缺鐵處理下,L22-8株系中與互作的轉錄因子和的表達量,均明顯高于Col-0。
(*,** 代表t-test檢驗的顯著性差異,*:P<0.05,**:P<0.01,下同)

圖4 Fe Marker基因的檢測
2.4 突變體P、Fe、Zn元素的測定
L22-8株系基因及響應缺鐵脅迫標記基因表達量的改變可能影響植株對鐵元素的吸收及積累。因為P、Zn元素對Fe元素起拮抗作用,我們同時對L22-8及Col-0地上部總Fe、總P、總Zn含量進行了測定。如圖5結果表明,無論在正常生長條件下還是缺鐵處理下,突變體L22-8株系的總Fe、P、Zn含量與野生型相比均沒有表現出顯著性差異,說明突變體雖影響了某些響應缺鐵脅迫基因的表達,但并不影響植株對環境中鐵元素的積累。
2.5 甲基化對熒光信號的影響分析
從前面的研究結果得知,L22-8雖影響到內源基因及幾種鐵響應Marker基因的轉錄表達,但在元素測定上并未表現出差異,而DNA甲基化對基因的表達起到一定調控作用[24]。為確定L22-8熒光信號的變化是否與T-DNA中基因啟動子的甲基化改變有關,我們對該啟動子序列進行了甲基化分析。圖6測序比對結果表明,在軟件分析的可能發生甲基化的5個CpG位點中,L22-8基本與Col-0測序結果一致,均未發現有甲基化發生。表明,L22-8熒光信號的增強不是由甲基化變化導致。
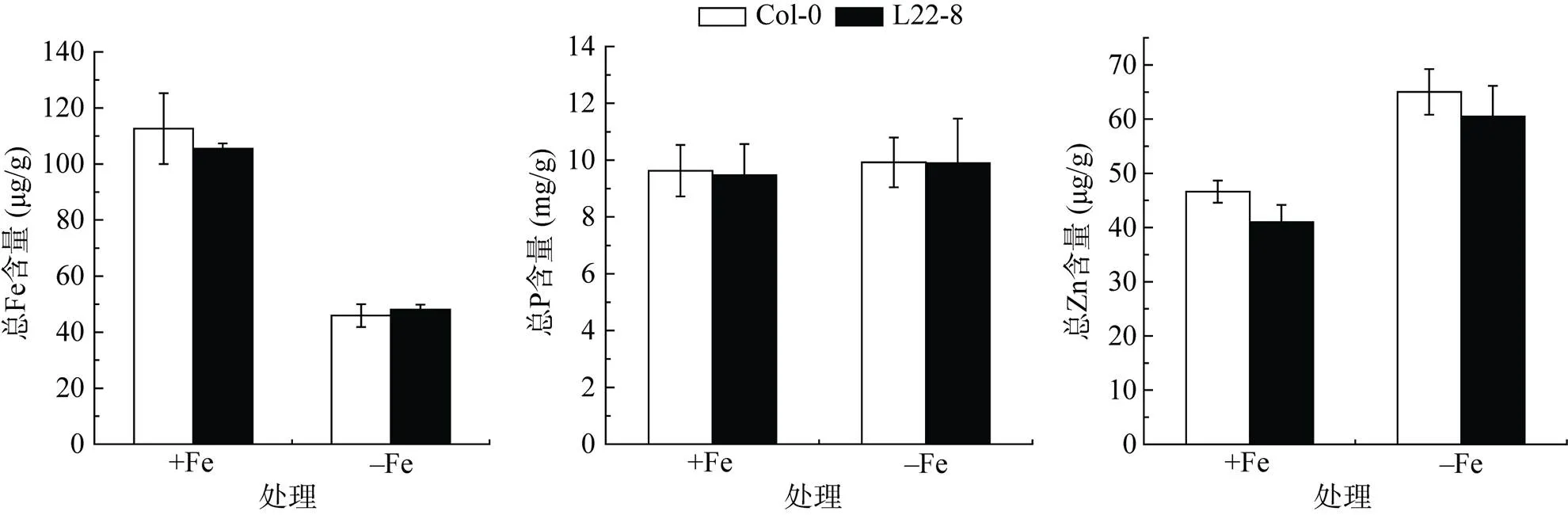
圖5 總Fe、P、Zn元素含量檢測

圖6 甲基化分析
2.6 突變體L22-8株系T-DNA插入位點的鑒定及相關基因表達檢測
運用反向PCR方法,鑒定了突變體L22-8株系的T-DNA插入位點。圖7A顯示,T-DNA插入于和之間。為了確定T-DNA插入是否影響到側翼基因的轉錄表達,對側翼基因的表達進行了實時定量PCR檢測。圖7B顯示,正常生長情況下L22-8的和兩個基因的表達量顯著降低,而缺鐵處理下未發生顯著性改變,且發現兩個基因均不響應缺鐵脅迫。
2.7 互補實驗純合株系的獲得與熒光檢測
為確定導致L22-8熒光信號變化的基因,分別轉化L22-8獲得兩個基因的單拷貝純合互補株系,記為L5-1~6、L6-1~6,并進行熒光檢測。結果如圖8所示,基因的多數互補株系熒光信號強烈,表明該基因未產生互補作用;基因互補株系的熒光信號明顯弱于L22-8株系,起到部分互補作用。表明L22-8株系可能通過影響側翼基因的作用進而影響到目標基因的表達。

圖8 正常生長條件下側翼基因互補株系的熒光檢測
3 討論
為促進植物對土壤中鐵元素的吸收、利用,近年已實踐應用了多種措施,如新的鐵螯合劑的使用,不同耕作措施的實施及基因改造等[22]。植物鐵調控機制的研究表明,除了眾多缺鐵響應基因參與植物鐵平衡調控外,許多調控植物生長的信號分子也參與調控缺鐵過程,如:乙烯、NO、生長素、茉莉酸等[25-28],植物體內擁有一個十分復雜的鐵平衡調控網絡。盡管我們已經在植物鐵吸收、運輸等分子機制方面取得重要的進展,但植物體內應該存在有新的調控因子并需要我們的探索,特別是負調控因子的探索。例如雖然我們已知FIT是正調控缺鐵脅迫的核心調控因子,但受FIT調控響應缺鐵脅迫的基因僅占眾多鐵響應基因的一部分[7,29],仍有很多鐵響應基因的調控因子尚不清晰。
本文通過分離基因的啟動子,再連接報告基因構成基因的表達載體pCAMBIA2300-::以轉化擬南芥,進而通過T-DNA隨機插入得到了一個響應缺鐵信號的擬南芥突變體庫;通過篩選突變體庫我們得到了一個強烈響應缺鐵信號的株系L22-8;根據對突變體T-DNA插入位點的確定,進一步探討影響基因表達可能存在的新的調控因子。通過篩選突變體找到突變基因并進行基因功能研究的正向遺傳學方法是將表型與其潛在的基因聯系起來的最成功的策略之一[30],是發現基因、研究基因功能非常有效的手段。而T-DNA插入突變篩選突變體庫的方法,因其T-DNA序列已知,具有插入突變體易定位的優點,且帶有報告基因的T-DNA則更易篩選檢測[31]。2016年Shinde等[32]研究中就運用正向遺傳學方法篩選突變體,用作為報告基因,取得良好的研究結果,亦適用于本研究。本研究通過篩選T-DNA插入突變體庫,發現了突變體L22-8,并證明由于T-DNA的插入影響了目標基因的表達,使得L22-8在正常生長條件下就表現出缺鐵反應,且在缺鐵處理條件下發現L22-8地下部基因的表達量未發生變化,但地上部的表達量卻顯著高于Col-0。我們推測這可能是因為缺鐵處理下在地下部的本底表達量就已經很高,使得地下部未表現出差異,而在表達量變化較低的地上部則能表現出顯著性差異,或可能由于T-DNA的插入影響了L22-8的地下部對缺鐵脅迫的部分響應,降低了變化幅度。此外,通過實驗證明由于T-DNA的插入影響了幾種關鍵缺鐵響應標記基因的轉錄表達,如和等。而FIT可與AtbHLH38、AtbHLH39等形成異源二聚體,有效地誘導和基因的表達[17-18],由本研究結果推測基因可能在bHLH38、bHLH39與FIT形成異源二聚體的過程中發揮作用,參與調控因子之間的信號傳導。研究結果分析得知L22-8株系中受FIT調控的下游鐵吸收相關基因與的表達量并沒有表現出明顯的不同,僅正常生長條件下L22-8的表達量表現為略高于Col-0。地上部總鐵含量與野生型沒有顯著差異,暗示基因組中可能存在的互作基因,共同參與對缺鐵脅迫的調控。結合已有的研究結果[20]進一步證明,基因并不是響應缺鐵脅迫的關鍵基因,這也是本研究中并未發現L22-8出現顯著異常表型的原因之一。轉基因互補實驗證明側翼基因對L22-8株系的熒光信號起到一定的互補作用,影響到基因的表達。基因又名,屬BZIP家族,在鹽脅迫環境中會被誘導表達。BZIP家族中BZIP19、BZIP23與BZIP24同屬BZIP家族中的F組,啟動子具有相同的結構域[33]。有研究表明、基因在響應缺鋅脅迫時會顯著被誘導,但未發現對缺鋅脅迫的明顯響應[34]。缺鐵時植物通過提高的表達間接性增強植株對Zn的積累,過量的Zn會導致植株的生理性Fe缺乏[35-36]。本研究結果表明,基因組中可能存在的互作基因影響了其對缺鋅脅迫的響應,而鋅信號的變化導致基因表達發生變化,從而間接對響應缺鐵脅迫造成影響,即其并不直接對基因響應缺鐵脅迫起上游調控作用。這可能導致了研究結果中L22-8插入位點雖影響了側翼基因的表達,但側翼基因在實驗中的培養時間內對缺鐵脅迫并沒有明顯響應的現象。
綜上所述,我們篩選到了一個強烈響應缺鐵信號的突變體L22-8,并進一步分析發現,可能是T-DNA的插入導致鋅信號響應基因的表達發生變化,而進一步引起L22-8對缺鐵信號的響應,但具體的作用方式和機制還需后續實驗進一步探索。
[1] 周曉今, 陳茹梅, 范云六. 植物對鐵元素吸收、運輸和儲存的分子機制[J]. 作物研究, 2012, 26: 605-610
[2] Saleeba J A, Guerinot M L. Induction of ferric reductase activity in response to iron deficiency in[J].Biometals, 1995, 8: 297-300
[3] Kobayashi T, Nishizawa N K. Iron uptake, translocation,and regulation in higher plants[J]. Annual Review of Plant Biology, 2012, 63: 131-152
[4] 吳慧蘭, 王寧, 凌宏清. 植物鐵吸收、轉運和調控的分子機制研究進展[J]. 植物學通報, 2007, 24(6): 779-788
[5] 顏路明, 郭祥泉. 鹽堿脅迫對香樟幼苗離子吸收與分配的影響[J]. 土壤, 2015, 47(6): 1176-1180
[6] Li X L, Zhang H M, Ai Q, et al. Two bHLH transcription factors, bHLH34 and bHLH104, regulate iron homeostasis in[J].Plant Physiology, 2016, 4: 2478-2493
[7] Colangelo E P, Guerinot M L. The essential basic helix-loop-helix protein FIT1 Is required for the iron deficiency response[J]. Plant Cell, 2004, 16: 3400-3412
[8] 李俊成, 于慧, 楊素欣, 等. 植物對鐵元素吸收的分子調控機制研究進展[J]. 植物生理學報, 2016, 52(6): 835-842
[9] Santi S, Cesco S, Varanini Z, et al. Two plasma membrane H+- ATPase genes are differentially expressed in iron- deficient cucumber plants[J].Plant Physiology And Biochemistry, 2005, 43(3): 287-292
[10] Santi S, Schmidt W. Dissecting iron deficiency - induced proton extrusion inroots[J].New Phytologist, 2009, 183(4): 1072-1084
[11] 王媛華, 段增強, 湯英, 等. 不同施肥處理對堿性設施土壤酸化的影響[J]. 土壤, 2016, 48(2): 349-354
[12] Robinson N J, Procter C M, Connolly E L, et al. A ferric-chelate reductase for iron uptake from soils[J]. Nature, 1999, 397(6721): 694-697
[13] Eide D, Broderius M, Fett J, et al. A novel iron-regulated metal transporter from plants identified by functional expression in yeast[J]. Proceedings of the National Academy of Sciences, 1996, 93: 5624-5628
[14] Nozoye T, Nagasaka S, Kobayashi T, et al. Phytosiderophore efflux transporters are crucial for iron acquisition in graminaceous plants[J]. Journal of Biological Chemistry, 2011, 286: 5446-5454
[15] Ling H Q, Bauer P, Bereczky Z, et al. The tomato fer gene encoding a bHLH protein controls iron-uptake responses in roots[J]. Proceedings of the National Academy of Sciences, 2002 , 99(21): 13938-13943
[16] Brumbarova T, Bauer P. Iron-mediated control of the basic helix-loop-helix protein FER, a regulator of iron uptake in tomato[J]. Plant Physiol., 2005, 137: 1018-1026
[17] Yuan Y X, Wu H L, Wang N, et al. FIT interacts with AtbHLH38 and AtbHLH39 in regulating iron uptake gene expression for iron homeostasis in[J]. Cell Research, 2008, 18: 383-397
[18] Wang N, Cui Y, Liu Y, et al. Requirement and functional redundancy of Ib subgroup bHLH proteins for iron deficiency responses and uptake in[J]. Molecular Plant, 2013, 6: 503-513
[19] Long T A, Tsukagoshi H, Busch W, et al. The bHLH transcription factor POPEYE regulates response to iron deficiency inroots[J]. Plant Cell, 2010, 22: 2219-2236
[20] Selote D, Samira R, Matthiadis A, et al. Iron-binding E3 ligase mediates iron response in plants by targeting basic helix-loop-helix transcription factors[J]. Plant Physiology, 2015, 167: 273-286
[21] Zhang J, Liu B, Li M S, et al. The bHLH transcription factor bHLH104 interacts with IAA-LEUCINE RESISTA-NT3 and modulates iron homeostasis in[J]. Plant Cell, 2015, 27: 787-805
[22] Murgia I, Tarantino D, Soave C, et al. Arabidopsis CYP82C4 expression is dependent on Fe availability and circadian rhythm, and correlates with genes involved in the early Fe deficiency response[J]. Journal Plant Physiology, 2011, 168: 894-902
[23] 魯如坤. 土壤農業化學分析方法[M]. 北京: 中國農業科技出版社, 1999: 331-336
[24] Xu W, Yang T Q, Dong X, et al. Genomic DNA methylation analyses reveal the distinct profiles in castor bean seeds with persistent endosperms[J]. Plant Physiology, 2016, 171(2): 1242-1258
[25] Wu J J, Wang C A, Zheng L Q, et al. Ethylene is involved in the regulation of iron homeostasis by regulating the expression of iron-acquisition-related genes in oryza sativa[J]. Journal of Experimental Botany, 2011, 62(2): 667-674
[26] Chen W W, Yang J L, Qin C, et al. Nitric oxide acts downstream of auxin to trigger root ferric-chelate reductase activity in response to iron deficiency in[J]. Plant Physiology, 2010, 154(2): 810-819
[27] Blum A, Brumbarova T, et al. Hormone influence on the spatial regulation of IRT1 expression in iron-defiecent[J]. Plant Signal Behavior, 2014, 9(4): e28787
[28] Maurer F, Mueller S, Bauer P. Suppression of Fe deficiency gene expression by jasmonate[J]. Plant Physiology and Biochemistry, 2011, 49(5): 530-536
[29] Mai H J, Pateyron S, Bauer P. Iron homeostasis in Arabidopsis thaliana: Transcriptomic analyses reveal novel FIT-regulated genes, iron deficiency marker genes and functional gene networks[J]. BMC Plant Biology, 2016, 16: 211
[30] 陸才瑞, 鄒長松, 宋國立. 高通量測序技術結合正向遺傳學手段在基因定位研究中的應用[J]. 遺傳, 2015, 37(8): 765-776
[31] 司曉嬌. 鹽芥突變體庫的構建及突變體的篩選[D]. 濟南: 山東師范大學, 2014: 14-16
[32] Shinde S, Villamor J G, Lin W D, et al. Proline coordination with fatty acid synthesis and redox metabolism of chloroplast and mitochondria[J]. Plant Physiology Preview, 2016, 172(2): 1074-1088
[33] Jakoby M, Weisshaar B, Droge-Laser W, et al. bZIP transcription factors in[J]. Trends in Plant Science, 2002, 7: 106-111
[34] Assuncao A G L, Herrero E, Lin Y F, et al.transcription factors bZIP19 and bZIP23 regulate the adaptation to zinc deficiency[J]. Proceedings of the National Academy of Sciences, 2010, 107: 10296-10301
[35] Sinclair S A, Kramer U. The zinc homeostasis network of land plants[J]. Biochimica et Biophysica Acta-gene regulatory mechanisms, 2012, 1823: 1553-1567
[36] Haydon M J, Kawachi M, Wirtz M, et al. Vacuolar nicotianamine has critical and distinct roles under iron deficiency and for zinc sequestration in[J]. Plant Cell, 2012, 24: 724-737
Screening and Characterization of anMutant in Response to Iron Deficiency
WANG Lisai1,2, YAN Mingke1,2, WANG Han1, SHEN Renfang1, LAN Ping1*
(1 State Key Laboratory of Soil and Sustainable Agriculture, Institute of Soil Science, Chinese Academy of Sciences, Nanjing 210008, China; 2 University of Chinese Academy of Sciences, Beijing 100049, China)
Iron is an essential nutrient for plant growth, but also a limiting factor for crop production due to its low solubility and availability in soil. The expression of a variety of genes would be induced under iron deficiency, while to many of these genes, the mechanisms remains unclear.() is one of the iron starvation induced gene and regulated byin. In this study, the promotor ofwas linked to Luciferase to screen the T-DNA insertion mutant library for genes in response to iron deficiency in. After screening, a line L22-8 was identified to remarkably intensify the fluorescence ofin both iron sufficient and deficient conditions. Real time qPCR analysis showed that the expression levels of endogenouswas increasedin root and shoot under normal growth condition, and in shoot underiron deficiency condition, but not the shoot in shortage of iron. The expression of several Fe-marker genes, such as,and, et al., were also significantly changed. These results indicated that the T-DNA insertion of L22-8 affected the molecular response ofto iron deficiency stress andmay play an important role in the formation of heterodimer ofwithand. The T-DNA insertion site of the L22-8 strain was detected to be located betweenandby reverse PCR, and the transcriptional expression of these two genes was slightly lower in mutant than Col-0 under normal conditions. Complementary analysis confirmed thatcould partially recover the L22-8 fluorescence signal, suggesting its role in regulating the response ofto iron deficiency stress. In addition, the contents of total Fe, P and Zn in shoot of L22-8 had no differences compared with Col-0, indicating that there maybe exsit someotherinteractive genes ofinOur results further extend the molecular regulation network of iron uptake and utilization in plant, and provide guidance for molecular breeding.
Soil;Iron-deficiency stress; Mutant characterization; Molecular regulation
國家重點研發計劃項目(2016YFD0200308)和國家重點基礎研究發展計劃(973計劃)項目(2015CB150501)資助。
(plan@issas.ac.cn)
王立賽(1990—),女,山東德州人,碩士研究生,主要從事植物營養分子生物學研究。E-mail:1527951097@qq.com
10.13758/j.cnki.tr.2018.03.006
Q945.1
A

