玉米SRO基因家族的鑒定及表達分析
趙秋芳,馬海洋,賈利強,陳曙,陳宏良
?
玉米SRO基因家族的鑒定及表達分析
趙秋芳,馬海洋,賈利強,陳曙,陳宏良
(中國熱帶農業科學院南亞熱帶作物研究所/農業部熱帶果樹生物學重點實驗室,廣東湛江 524091)
【目的】SRO(similar to rcd one)是植物所特有的一類小蛋白家族,其在植物的生長發育,及應對非生物脅迫中發揮著重要功能。基于玉米全基因組數據庫,鑒定玉米SRO家族基因,分析其序列、基因定位、蛋白結構及其系統進化關系,同時解析在玉米組織表達特異性及其在高鹽和干旱脅迫下的表達變化,為闡明SRO基因在玉米生長和逆境響應中的功能研究奠定基礎。【方法】利用擬南芥SRO家族基因為探針,在玉米全基因組查找并下載玉米SRO基因序列,并從MaizeGDB中獲取玉米SRO基因相關信息,包括CDS、氨基酸序列及染色體位置等。通過生物信息學工具(GSDS2.0、Expasy-protparam、SOPMA、Plant-mPLoc、EMBL-EBI、MEME)對獲得序列的基因結構、蛋白質分子量、等電點、二級結構、亞細胞定位、保守結構域、保守基序原件等進行預測和分析。同時利用Clustalx(1.83)和MEGA 6.0軟件進行同源序列比對并構建系統進化樹。運用實時熒光定量PCR技術分析玉米組織表達特異性及其在高鹽和干旱脅迫下的表達變化情況。【結果】從玉米全基因組共鑒定6個SRO家族基因,分別命名為。分布于第1、4、5和9染色體,包含25個內含子。序列分析發現CDS序列長度在1 2151 791 bp;編碼氨基酸數目為404596 aa;分子量為45.2366.78 kD;等電點為7.019.17。亞細胞定位分析發現ZmSRO1a/ZmSRO1b/ZmSRO1c/ZmSRO1d定位于葉綠體,ZmSRO1e則定位于過氧化氫酶體,ZmSRO1f定位于細胞核。系統進化樹分析發現ZmSROs分為3個亞類,Ⅰa亞類包括ZmSRO1a/ZmSRO1b/ZmSRO1c,Ⅰb亞類包括ZmSRO1f,Ⅰc亞類包括ZmSRO1d/ZmSRO1e。保守結構域分析結果顯示ZmSRO1a/ZmSRO1b/ZmSRO1c/ZmSRO1d/ZmSRO1e包含PARP和RST結構域,缺少WWE結構域,ZmSRO1f包含WWE和PARP催化中心,RST結構域缺失。ZmSROs蛋白共找到5個保守基序,命名為基序15。ZmSRO1a/ZmSRO1b/ZmSRO1c包含所有保守基序,ZmSRO1d/ZmSRO1e缺少保守基序3,ZmSRO1f缺少保守基序5。組織表達分析發現在根系特異性表達。高鹽脅迫下,玉米根系中在1 h時顯著上調表達,地上部中均下調表達,而在處理6 h顯著上調表達。干旱脅迫下,玉米根系在1 h顯著上調表達,在24 h顯著上調表達;地上部中均下調表達。【結論】玉米SRO家族基因包含6個成員,被劃分為3個亞類,6個在玉米根系中特異性表達,且可以不同程度地響應干旱和高鹽脅迫。
玉米;SRO基因;非生物脅迫;基因表達
0 引言
【研究意義】玉米(L.)是世界重要的糧食作物之一,在世界糧食總產量中處于第一位,同時也是重要的飼料和工業原料[1]。但實際生產中玉米常常會因受到諸多不利環境因素的影響而大面積減產,比如干旱、鹽脅迫和低溫等。SRO(similar to rcd one)是植物所特有的一類小蛋白家族,其在植物的生長發育及應對鹽、干旱、重金屬等非生物脅迫中發揮著重要作用。對玉米SRO家族基因進行全面的生物信息學、組織特異性表達及鹽、干旱脅迫條件下表達進行分析,有利于更深入了解SRO家族基因的功能,并對玉米抗逆基因挖掘和抗逆育種具有重要意義。【前人研究進展】SRO是植物所特有的類RCD-ONE蛋白家族,它們通常包含高度保守的PARP(poly (ADP ribose) polymerase catalytic;PS51059)催化中心和C末端的RST(RCD1-SRO-TAF4;PF12174)保守結構域[2]。目前對SRO蛋白家族的研究主要集中在擬南芥中。據報道,在擬南芥中共鑒定出6個SRO同源基因,分別為、[2-3]。AtSRO1與AtRCD1(radical-induced cell death 1)同源性最高,除具有PARR和RST保守結構域外,還具有N端的WWE(PS50918)結構域,屬于亞家族A[4],AtSRO2-5僅包含PARP和RST結構域,缺少WWE結構域,屬于亞家族B[5]。以往研究表明,PARP-RST結構域是植物所特有的,而WWE-PARP結構域廣泛存在于生物體中,且高度保守[6-7]。是植物中首個被鑒定的SRO家族基因,擬南芥中突變體表現出對鹽、寒害、紫外線、MV、以及CO毒害和激素(ABA/JA/ETH)的耐受性的增加,同時影響擬南芥的生長,表現為株高減少、早花、連坐葉片、限制根系生長和生殖發育等[1,5,8-14]。同樣參與到非生物脅迫的應激反應,但是與之間有些不同,突變體增強鹽脅迫下的擬南芥的滲透調節能力,而突變體則表現出對鹽脅迫敏感表型[13]。此外,有研究表明可以響應鹽脅迫[15],和的轉錄子也受到O3引起的氧化脅迫誘導[5]。目前SRO家族基因在水稻、小麥、番茄、蘋果、陸地棉等作物中有部分研究,其作用和功能也已日益清楚。水稻OsSRO1c蛋白可以與水稻干旱轉錄因子SNAC1和DST直接作用,通過調節氣孔關閉和過氧化氫累積來響應干旱和氧化脅迫[16-17]。小麥在干旱、高鹽和H2O2脅迫條件下均上調表達,可以通過調節植物體內的氧化還原平衡來提高植物生長和抵抗逆境脅迫的能力[18]。番茄與序列相似,且在鹽脅迫條件下上調表達,特別是在根系中[19]。蘋果中鑒定出6個SRO家族基因,其中被認為是重要的非生物脅迫調節因子,可以增強其耐受鹽、干旱、及氧化脅迫的能力[20]。呂有軍等[21]在陸地棉中鑒定出12個SRO基因,它們的表達存在組織特異性,且明顯受冷處理和鹽處理的誘導,、、也受到不同程度脅迫處理的誘導。【本研究切入點】隨著研究的深入,植物SRO家族基因功能被越來越多的人所認識,其在植物生長,特別是應答各種非生物脅迫中的作用被日益重視,但是該家族基因在玉米中鮮見報道。【擬解決的關鍵問題】本研究以玉米全基因組數據為基礎,鑒定SRO家族成員,分析基因結構、亞細胞定位、蛋白保守結構域及系統進化關系等信息,明確玉米SRO家族基因在各個組織中的表達特異性和脅迫條件下的表達模式,為解析SRO蛋白功能和抗逆調控作用奠定基礎,同時也為玉米抗逆基因挖掘和抗逆育種提供理論參考。
1 材料與方法
1.1 試驗材料及處理方法
供試玉米材料為B73,玉米不同組織器官(根、莖、葉、雄穗和雌穗)取自B73自交系,采樣時期為玉米抽穗期,采樣時間為2017年5月23日。取樣完成后,液氮速凍,-80℃保存,備用。非生物脅迫于2017年6月8日開始,具體試驗如下:選取B73生長飽滿的種子,表面消毒殺菌后,28℃催芽2 d,轉入1/2 Hoagland培養液中培養7 d后,正常營養液培養至玉米3葉1心,選取生長一致玉米幼苗各12株進行干旱和高鹽脅迫處理,每個處理4株,3次重復。干旱脅迫:幼苗置于20% PEG-6000溶液中培養;高鹽脅迫:幼苗置于200 mmol·L-1NaCl溶液中培養,并于處理后0、1、6和24 h采集玉米幼苗和根系樣品,液氮速凍,-80℃冰箱保存備用。
1.2 玉米SRO基因家族的鑒定及序列分析
以擬南芥全基因組數據庫(TAIP)中6個擬南芥SRO蛋白序列為探針,在玉米基因組數據庫MaizeGDB(https://www.maizegdb.org/)和Phytozome12.0(https:// phytozome.jgi.doe.gov/pz/portal.html)搜索玉米SRO家族候選成員,并利用Pfam和SMART對候選基因進行進一步確認玉米SRO家族基因,同時獲得其CDS、氨基酸序列及染色體位置信息。
1.3 玉米SRO基因的生物信息學分析
運用Expasy protparam tool(http://web.expasy.org/ protparam/)在線工具分析玉米SRO基因家族成員的分子量和等電點;分別運用在線工具plant-mploc(http://www.csbio.sjtu.edu.cn/bioinf/plant-multi/)和SOPMA(https://npsa-prabi.ibcp.fr/cgi-bin/npsa_automat. pl?page=npsa_sopma.html)對SRO進行亞細胞定位和蛋白的二級結構預測。利用GSDS2.0(http://gsds.cbi.pku. edu.cn/)在線工具繪制玉米SRO基因結構圖,分析其外顯子和內含子結構。利用EMBL-EBI(http://www. ebi.ac.uk/interpro/)分析氨基酸序列的蛋白質保守區,并用IBS1.0軟件繪制蛋白保守結構域圖。利用MEME(http://meme-suite.org/tools/meme)在線工具對玉米SRO蛋白的保守基序進行預測,參數中預測數目設置為5,長度設置為6—50,其他參數均為默認設置。從水稻基因組獲取已知的水稻SRO家族蛋白序列,利用Clustalx(1.83)進行同源序列比對,并利用MEGA6.0軟件,采用相鄰連接法(Neighbor-Joining,NJ)構建擬南芥、水稻、玉米SRO蛋白家族的系統進化樹,校驗參數BootStrap重復為1 000次,其他參數均為默認值。
1.4 玉米SRO基因家族表達
采用華越洋植物RNA快速提取試劑盒提取玉米樣品總RNA,使用Roche第一鏈cDNA合成試劑盒將提取的總RNA反轉錄cDNA。根據玉米SRO基因序列,采用Oligo 7軟件設計定量引物,上海生工生物工程有限公司合成,引物序列詳見表1。實時熒光定量PCR反應在Roche lightCycler480中進行,試劑盒為Thermo Fisher scientific,反應體系10 μL包括SYBR Green Master MIX(2×),5 μL、上下游引物(10 μmol·L-1)各1 μL、cDNA 1 μL和ddH2O 2 μL。反應條件為50℃ 2 min,95℃ 3 min;95℃ 15 s,58℃ 15 s,72 ℃ 30 s,45個循環,3次重復。采用2-ΔΔCt方法進行數據計算,基因的相對表達量使用(平均值±標準差)表示。

表1 ZmSROs實時熒光定量PCR分析所用引物
2 結果
2.1 玉米SRO基因的鑒定及序列分析
從玉米基因組數據庫中共鑒定到6個SRO家族基因,并按照You等[17]方法進行命名,其基因序列信息見表2。6個分別分布于第1、4、5和9染色體,其中和位于第1染色體,位于第4染色體,和位于第5染色體,位于第9染色體。玉米SRO家族基因編碼區長度為1 215—1 791 bp;編碼氨基酸數目為404—596 aa;分子量為45.23—66.78 kD;等電點為7.01—9.17,均大于7,均為堿性蛋白。亞細胞預測定位4個ZmSROs定位于葉綠體,ZmSRO1f定位于細胞核,ZmSRO1e則定位于過氧化氫酶體中(表2)。
通過對6個ZmSROs蛋白的二級結構預測(表3),結果表明,ZmSROs蛋白的二級結構以α-螺旋和無規則卷曲結構為主,擴展鏈結構和β-轉角結構所占比例較小。其中ZmSRO1a、ZmSRO1b、ZmSRO1c和ZmSRO1f的無規則卷曲結構所占比例最大,為38.76%—46.55%,其次為α-螺旋結構,為28.22%—30.54%;ZmSRO1d和ZmSRO1e的α-螺旋結構所占比例最大,分別為47.10%和43.62%,其次為無規則卷曲結構分別為30.36%和32.25%。
2.2 玉米SRO基因結構、蛋白保守結構域及進化樹分析
6個s的基因結構圖見圖1。均含有5個內含子和6個外顯子,和均包含3個內含子和4個外顯子,而僅包含2個內含子和3個外顯子。
利用EBL-EBI在線分析發現,根據SRO蛋白序列中所包含的保守功能區域,可以將ZmSROs蛋白分為2類,A類為ZmSRO1a/ZmSRO1b/ZmSRO1c/ ZmSRO1d/ZmSRO1e共5個蛋白,均包含PARP催化中心和C-末端的RST結構域,缺少WWE結構域,但是由于蛋白質氨基酸序列長度不同,其保守結構域出現的位置也不相同。ZmSRO1a/ZmSRO1b/ZmSRO1c的PARP和RST結構域分別位于第235—466 aa和第486—572 aa,而ZmSRO1d和ZmSRO1e蛋白的PARP和RST結構域分別位于第147—384 aa和第373—448 aa;B類為ZmSRO1f包含WWE和PARP催化中心,C-末端的RST結構域缺失,其中WWE位于第75—129 aa,PARP催化中心位于第189—404 aa(圖2)。

表2 玉米SRO基因家族的序列信息
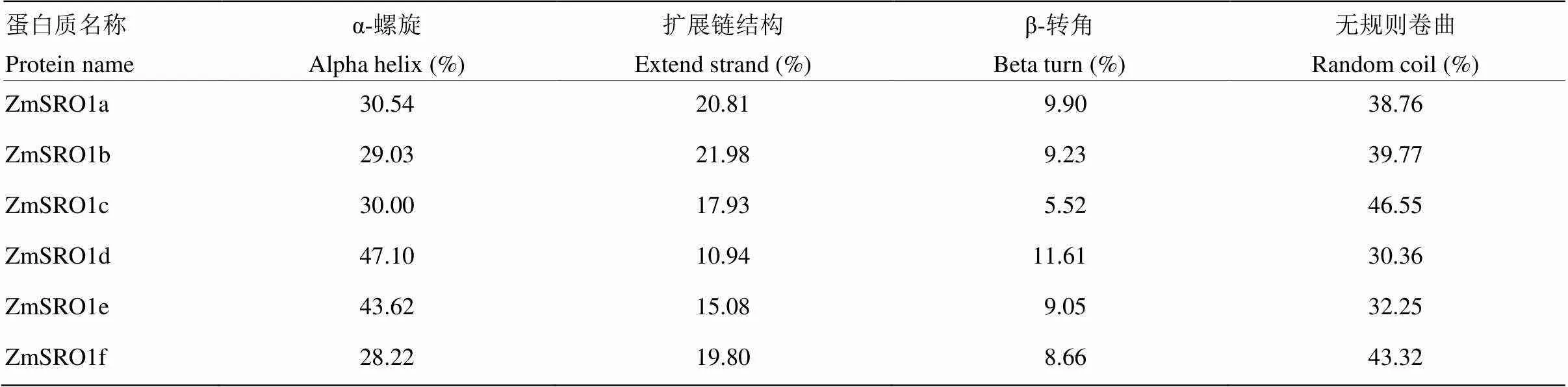
表3 玉米SRO蛋白的二級結構
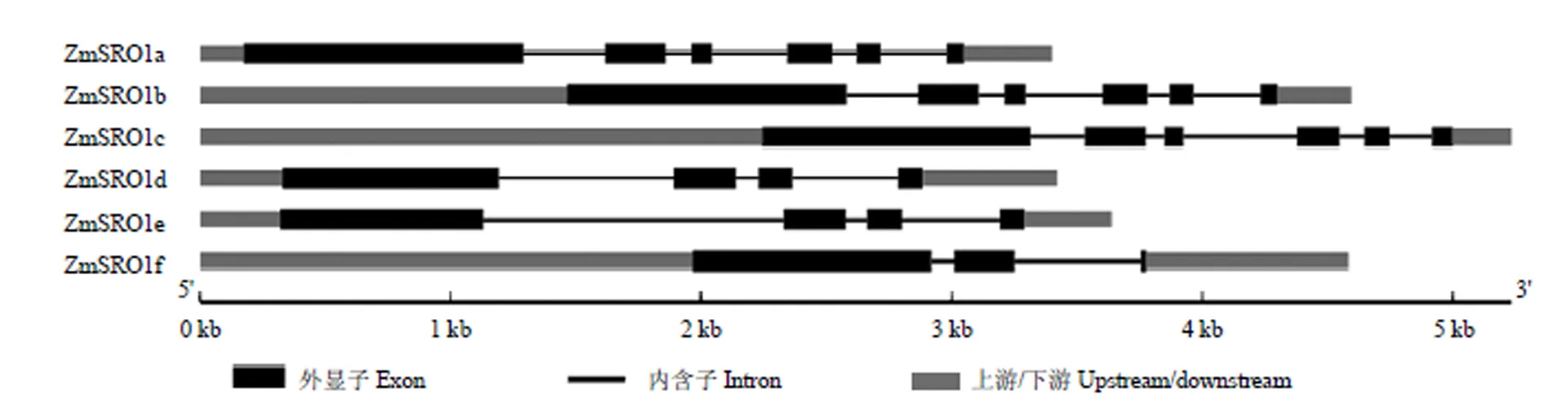
圖1 ZmSROs基因結構圖
利用MEME在線工具預測ZmSROs蛋白的保守基序,由圖3可知,ZmSROs蛋白共找到5個保守基序,ZmSRO1a/ZmSRO1b/ZmSRO1c包含保守基序1—5,ZmSRO1d/ZmSRO1e缺少保守基序3,ZmSRO1f缺少保守基序5。結合ZmSROs蛋白結構域分析可以看出,保守基序1位于PARP催化中心,保守基序5位于RST保守結構域中。
利用MAGA6.0構建玉米、擬南芥、水稻SRO蛋白家族的系統進化樹(圖4),SRO家族蛋白可以被分為Ⅰ和Ⅱ兩類,其中Ⅰ類由可以被分為Ⅰa、Ⅰb、Ⅰc 3個亞類,Ⅱ類可以被分為Ⅱa和Ⅱb 2個亞類。在玉米和水稻中僅存在第Ⅰ亞類,缺少第Ⅱ亞類。按照水稻的亞家族分類,可以將ZmSROs分為3個亞類,ZmSRO1a/ZmSRO1b/ZmSRO1c同源性最高,均屬于Ⅰa亞類,ZmSRO1d/e屬于Ⅰc亞類,ZmSRO1f屬于Ⅰb亞類,玉米和水稻均為禾本科植物親源關系較近,其SRO蛋白序列同源性非常高,進化關系非常接近。
2.3 玉米SRO基因在不同組織的表達分析
利用qRT-PCR技術分析了6個在玉米根、莖、葉、雄穗和雌穗中的表達(圖5),6個在玉米根系相對表達量顯著高于其他組織部位,說明6個均在根系中有特異性表達,而在雌穗和雄穗中的表達量較低,幾乎不表達。結果表明,可能在玉米根系發育過程中起重要作用。
2.4 玉米SRO基因在逆境脅迫的表達分析
為了明確玉米SRO基因對逆境脅迫下的應答機制,分析了SRO基因在鹽脅迫和干旱脅迫下根系和地上部的表達模式(圖6和圖7)。在根系中,200 mmol·L-1NaCl處理下,除外,其余5個處理1 h時顯著上調表達,1 h相對表達量分別為0 h的13.5、17.1、5.4、31.1和27.9倍,隨后6和24 h后表達量下降,表明玉米根系中的5個基因均可以迅速響應鹽脅迫信號,而對鹽脅迫信號沒有響應。20%PEG處理下,在1 h表達量為0 h處理的3.6倍,顯著上調表達;在24 h的表達量為0 h的2.7倍,顯著上調表達,表明玉米根系中和可能響應干旱脅迫。鹽脅迫條件下玉米地上部的表達均下調,表達差異不大而在處理6 h顯著上調表達,為0 h的3.06倍,說明玉米地上部可能對鹽脅迫有響應。干旱脅迫處理下,均下調表達,而和表達差異不顯著,變化趨勢與鹽脅迫處理類似。
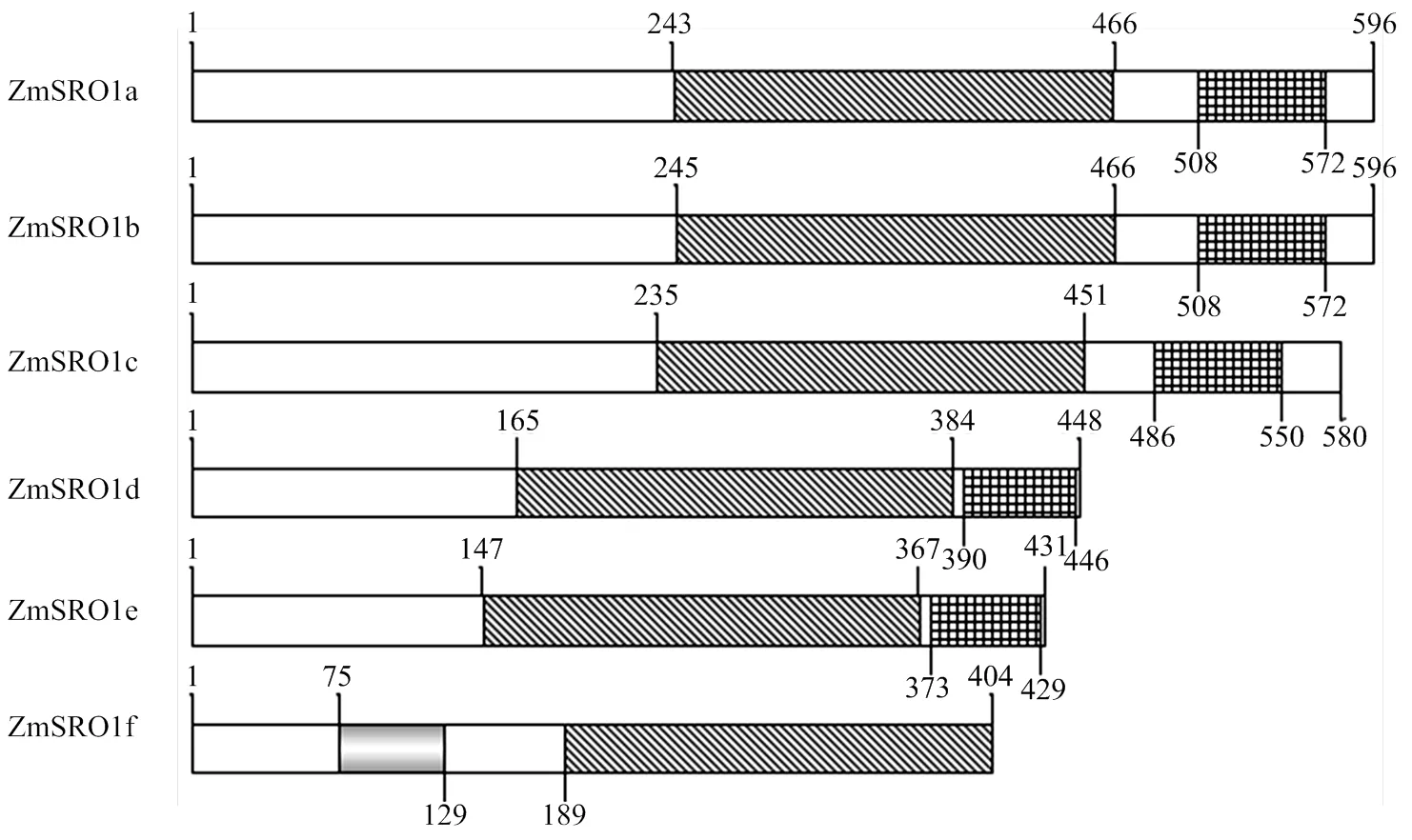
灰色區域、黑色斜紋網格區域和黑色豎紋區域分別表示ZmSROs蛋白的WWE、PARP和RST結構域
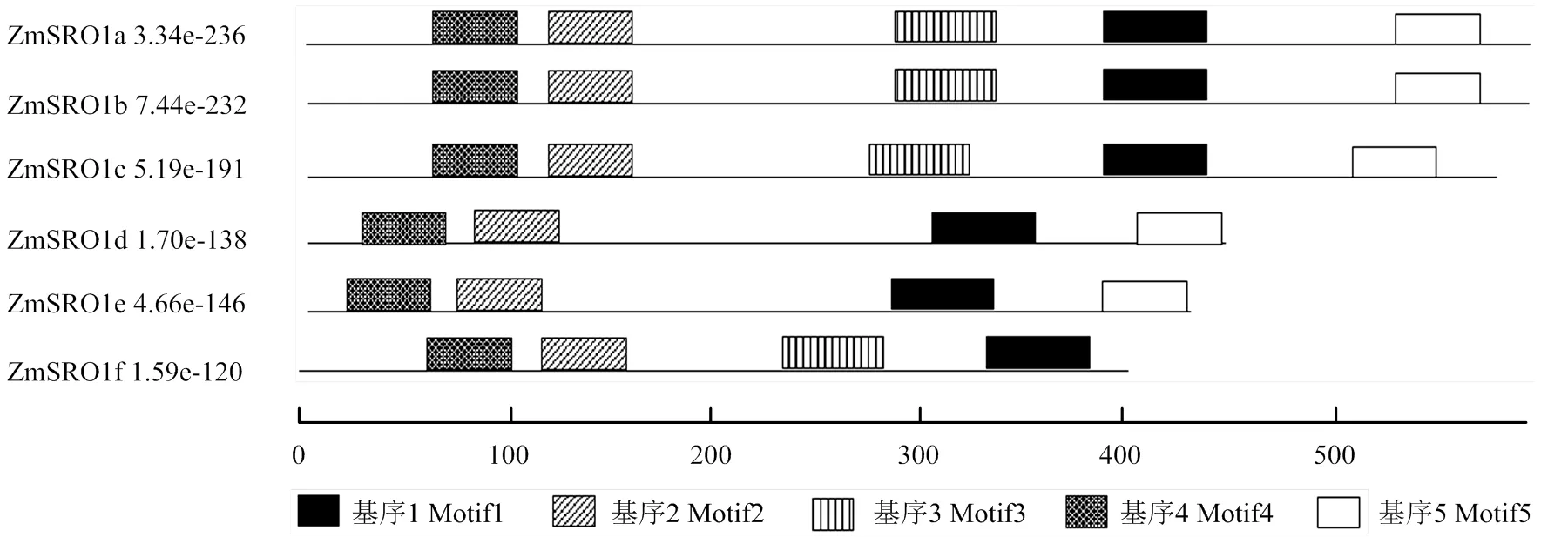
圖3 ZmSROs蛋白保守基序分布
3 討論
由于全球氣候變化,極端氣候條件頻發,以及土壤質量下降和鹽漬化的加劇,使得干旱和鹽害等非生物脅迫成為影響植物生長和產量的主要限制因子。玉米作為世界重要糧食作物,玉米產業發展也時刻面臨著非生物脅迫等逆境環境的危害,因而挖掘重要的抗逆基因,選育抗逆玉米新品種,以提高玉米自身的抗逆能力顯得尤為重要。研究發現許多植物特有的轉錄因子可以影響植物生長發育,并響應外界環境變化[22],如NAC、AP2/ERF、WRKY、Dof和ARF等[23-27]。SRO是最近被發現的陸生植物特有蛋白家族,其在植物生長發育以及響應非生物脅迫方面具有重要作用。目前,擬南芥[2-3]、水稻[16-17]、小麥[18]、番茄[19]、蘋果[20]等植物中的SRO家族已被分離鑒定,并對其功能進行了初步研究,但SRO基因家族在玉米中的研究仍鮮見報道。本研究從玉米全基因組中共鑒定出6個,依次命名為,系統進化樹分析發現,玉米和水稻SRO蛋白相似性非常高,親緣關系相近。根據植物SRO蛋白可以被分為2類(Ⅰ和Ⅱ),Ⅰ類被進一步分為Ⅰa、Ⅰb、Ⅰc 3個亞類,系統進化樹分析表明AtSRO1、AtRCD1、OsSRO1a/ OsSRO1b和ZmSRO1a/ZmSRO1b/ZmSRO1c屬于Ⅰa亞類,OsSRO1d/OsSRO1e和ZmSRO1f屬于Ⅰb亞類,OsSRO1c和ZmSRO1d/ZmSRO1e屬于Ⅰc亞類,Ⅱ類蛋白也可以被分為Ⅱa和Ⅱb 2個亞類,其中AtSRO2/AtSRO3屬于Ⅱa,AtSRO4/AtSRO5屬于Ⅱb亞類(圖4)。Ⅱ類蛋白是雙子葉植物所特有的[17],玉米和水稻中均不存在Ⅱ類的SRO蛋白。根據其包含蛋白家族結構域可將ZmSROs分為2類,A類包括ZmSRO1a/ZmSRO1b/ZmSRO1c/ZmSRO1d/ZmSRO1e,均包含PARP催化中心和C-末端的RST結構域,缺少WWE結構域,而B類僅包括ZmSRO1f,包含PARP催化中心和WWE結構域,缺少C-末端的RST結構域(圖2),以往研究表明水稻OsSRO1d中也缺少RST結構域,其原因可能是OsSRO1d的RST結構域中被額外插入18個氨基酸序列,使得在結構域分析時RST結構域未被分析出來[17]。蛋白保守基序預測顯示ZmSRO1f缺少保守基序5,結合蛋白保守結構域分析保守基序5恰好位于RST保守結構域內(圖4和圖5),而ZmSRO1f僅含404個氨基酸,其氨基酸數目較少可能是RST保守結構域缺失的原因。
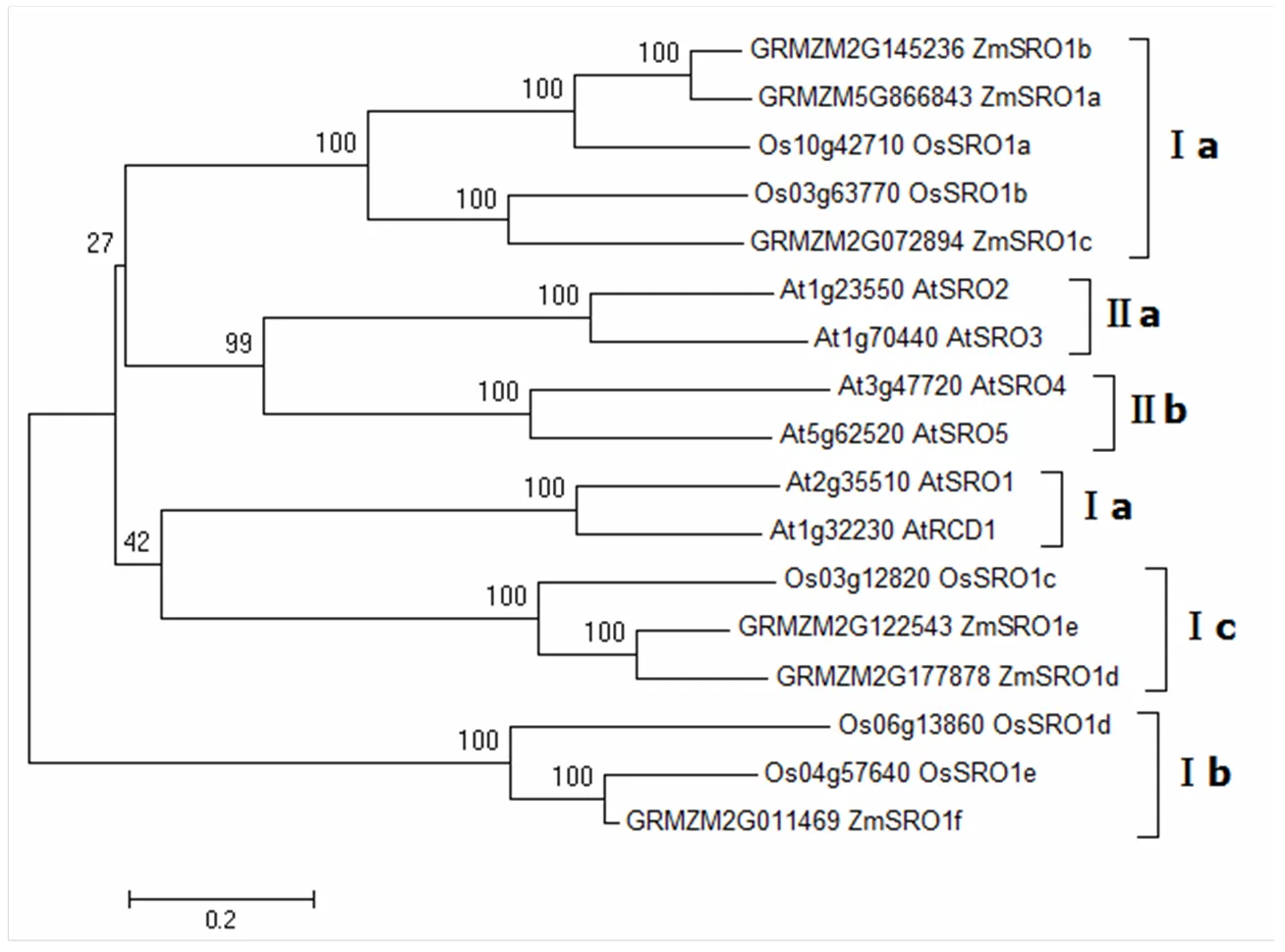
圖4 玉米、擬南芥、水稻的SRO蛋白家族的系統進化樹
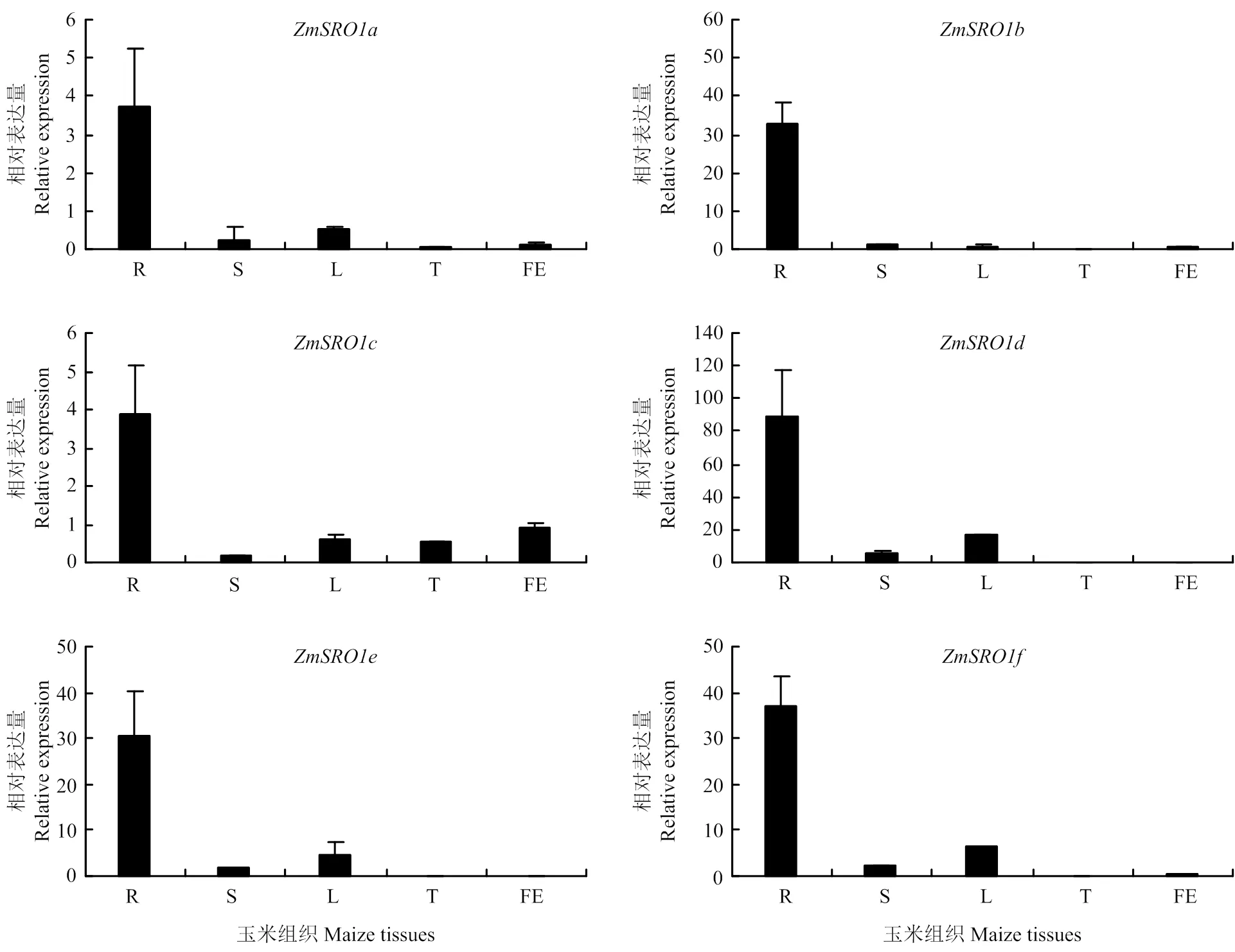
R:玉米根;S:莖;L:葉片;T:雄穗;FE:雌穗 R: root; S: stem; L: leaf; T: tassel; FE: female ear
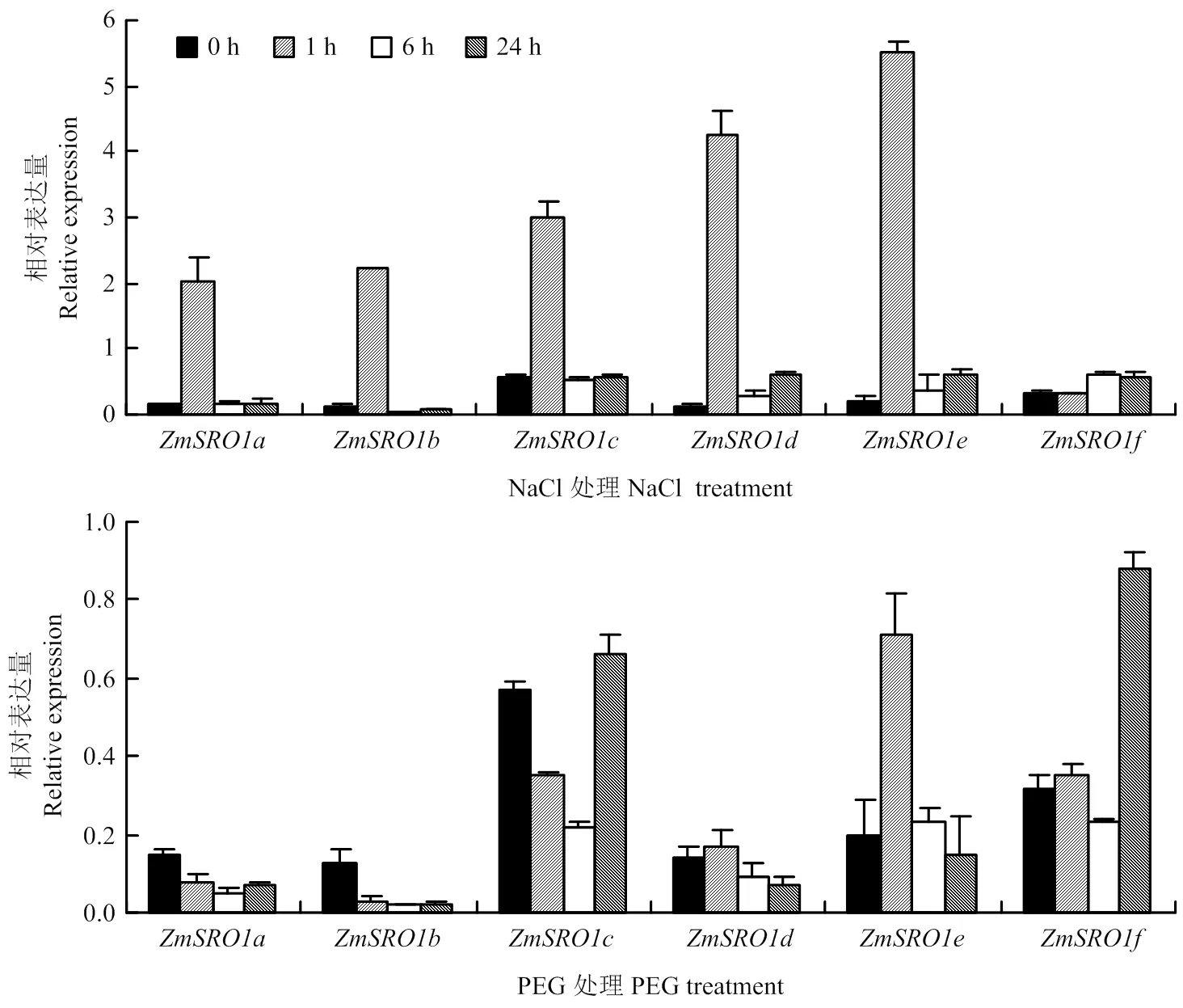
圖6 脅迫條件下ZmSROs在玉米根系的表達
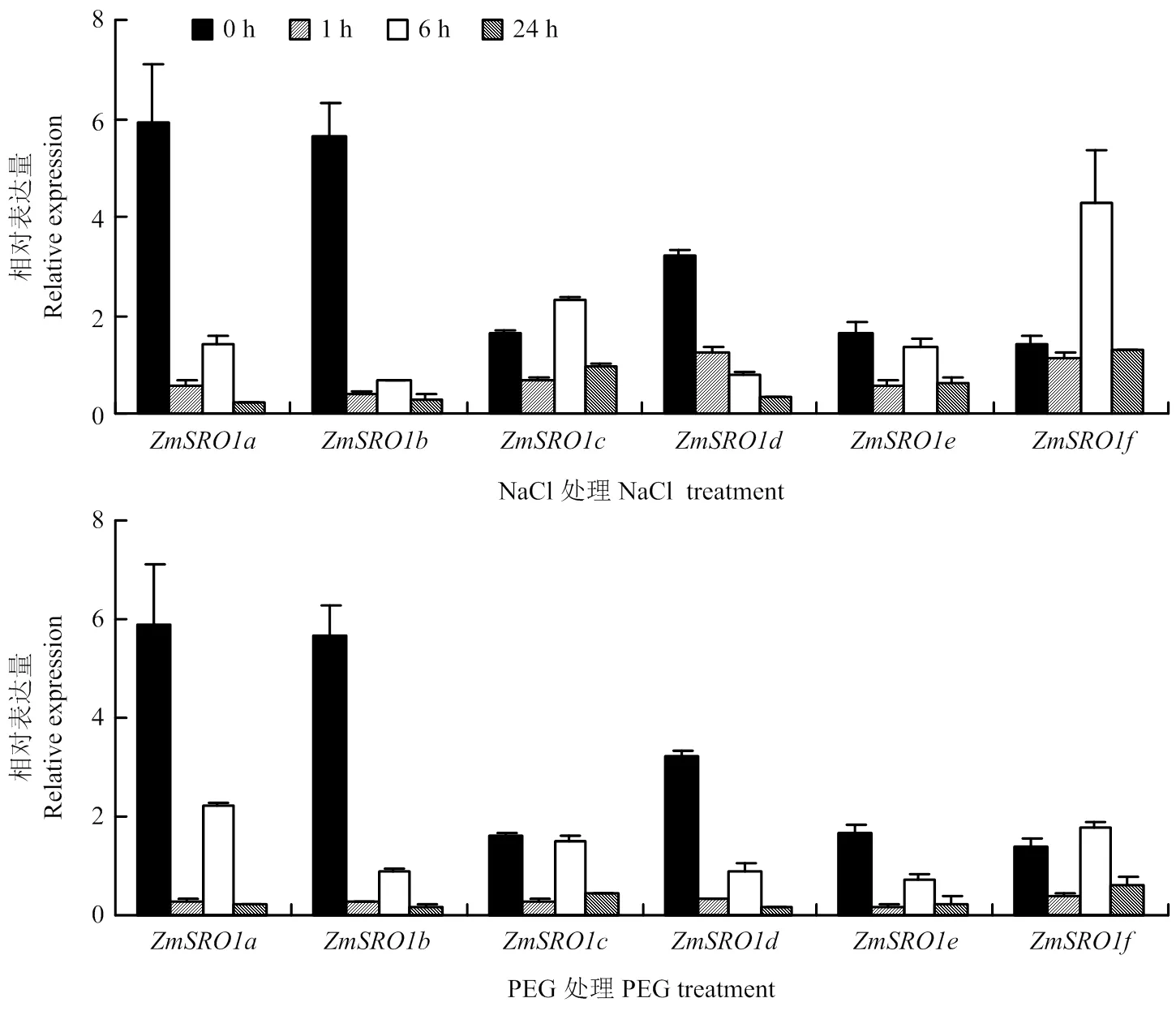
圖7 脅迫條件下ZmSROs在玉米地上部的表達
SRO基因可以調控植物生長發育,因此其在植物不同組織部位的表達情況也備受關注。有研究表明蘋果中SRO家族基因存在組織特異性表達,在果實中的表達顯著高于其他組織,而其余在根、莖和花中的表達量較高,而在葉片和果實中的表達量低,同時在花中表達量最高,說明可能在蘋果花發育過程中發揮重要作用[20]。水稻中和呈現組成性表達,和呈現組織特異性表達,在水稻三葉苗期和分蘗期表達量高,在葉片、鞘和4—5 cm幼穗中表達量低,在子房發育和胚乳成熟階段表達量高,而在胚胎發育早期的表達量較低[17]。本研究結果顯示在根系中表達量顯著高于其他組織,暗示在玉米根系發育中發揮作用。另外在雄穗和雌穗中的表達量均較低,幾乎不表達,表明其對玉米的生殖生長階段作用較小(圖6)。
SRO家族不僅影響植物的生長進程,而且在許多植物中均證實SRO家族可以響應植物的非生物脅迫。如在ABA和JA處理下顯著上調表達[17],小麥中可以通過調節植物體內的氧化還原平衡來提高其耐干旱、高鹽和H2O2脅迫的能力[18]。番茄在番茄根系中,鹽脅迫條件下顯著上調表達[19]。蘋果表達量在100 μmol·L-1ABA和4℃處理下分別上調14和37倍,而在20%PEG處理下,、和分別上調18、17和14倍,說明可以響應ABA和寒害脅迫,、和響應干旱脅迫[20]。本研究中,玉米根系中5個基因均在200 mmol·L-1NaCl處理1 h顯著上調表達,表明根系中這些基因可以迅速響應鹽脅迫信號,另外和在干旱條件下顯著上調表達,說明和響應干旱脅迫(圖6)。相較根系SRO基因的表達量變化,地上部SRO基因表達量普遍呈現下調現象(圖7),綜上所述,可能在玉米根系響應干旱和高鹽脅迫中發揮作用。
4 結論
從玉米全基因組中鑒定到6個SRO家族基因,均含有SRO蛋白特有的PARR催化中心結構域。系統進化樹分析ZmSROs被分為3個亞類,其中ZmSRO1a/b/c屬于Ⅰa亞類,ZmSRO1f屬于Ⅰb亞類,ZmSRO1d/e屬于Ⅰc亞類。在玉米根系特異性表達。玉米根系中的受鹽脅迫誘導上調表達,和受干旱脅迫誘導上調表達,同時地上部受鹽脅迫誘導上調表達,其余基因在干旱和鹽脅迫均下調表達。
[1] 齊濤. 中國玉米國際競爭力研究[D]. 楊凌: 西北農林科技大學, 2011.
Qi T. The international competitiveness of cron in china [D]. Yangling: Northwest agriculture and forestry university, 2011. (in Chinese)
[2] Jaspers P, Blomster T, Brosché M, Saloj?rvi J, Ahlfors R, Vainonen J P, Reddy R A, Immink R, Angenent G, Turck F, Overmyer K, Kangasj?rvi J. Unequally redundant RCD1 and SRO1 mediate stress and developmental responses and interact with transcription factors., 2009, 60(2): 268-279.
[3] 李保珠, 趙翔, 趙孝亮, 彭雷. 擬南芥SRO蛋白家族的結構及功能分析. 遺傳, 2013, 35(10): 1189-1197.
LI B Z, ZHAO X, ZHAO X L, PENG L. Structure and function analysis ofSRO protein family., 2013, 35(10): 1189-1197. (in Chinese)
[4] Aravind L. The WWE domain: a common interaction module in protein ubiquitination and ADP ribosylation., 2001: 26: 273-275.
[5] Jaspers P, Overmyer K, Wrzaczek M, Vainonen J P, Blomster T, Saloj?rvi J, Reddy R O, Kangasj?rvi J. The RST and PARP-like domain containing SRO protein family: analysis of protein structure, function and conservation in land plants., 2010, 11: 170.
[6] Otto H, Reche P A, Bazan F, Dittmar K, Haag F, Koch-Nolte F. In silico characterization of the family of PARP-like poly (ADPribosyl) transferases (pARTs)., 2005, 6: 139.
[7] Hassa P O, Haenni S S, Elser M, Hottiger M O. Nuclear ADPribosylation reactions in mammalian cells: where are we today and where are we going?, 2006, 70(3): 789-829.
[8] Ahlfors R, Lang S, Overmyer K, Jaspers P, Brosche M, Tauriainen A, Kollist H, Tuominen H, Belles-Boix E, Piippo M, Inze D, Palva T, Kangasjarvi J.RADICAL-INDUCED CELL DEATH1 belongs to the WWE protein-protein interaction domain protein family and modulates abscisic acid, ethylene, and methyl jasmonate responses., 2004, 16: 1925-1937.
[9] Ahlfors R, Brosché M, Kollist H, Kangasj?rvi J. Nitric oxide modulates ozone‐induced cell death, hormone biosynthesis and gene expression in., 2009, 58(1): 1-12.
[10] Katiyar-Agarwal S, Zhu J, Kim K, Agarwal M, Fu X, Huang A, Zhu J K. The plasma membrane Na+/H+antiporter SOS1 interacts with RCD1 and functions in oxidative stress tolerance in., 2006, 103: 18816-18821.
[11] Fujibe T, Saji H, Arakawa K, Yabe N, Takeuchi Y, Yamamoto K T. A methyl viologen-resistant mutant of Arabidopsis, which is allelic to ozone-sensitive rcd1, is tolerant to supplemental ultraviolet-Birradiation., 2004, 134: 275-285.
[12] Overmyer K, Tuominen H, Kettunen R, Betz C, Langebartels C, Sandermann H, Kangasj?rvi J. Ozone-sensitivemutant reveals opposite roles for ethylene and jasmonate signaling pathways in regulating superoxide- dependent cell death., 2000, 12(10): 1849-1862.
[13] Teotia S, Lamb R S. The paralogous genes RADICALINDUCED CELL DEATH 1 and SIMILAR TO RCD ONE 1 have partially redundant functions duringdevelopment., 2009, 151(1): 180-198.
[14] Teotia S, Lamb R S. RCD1 and SRO1 are necessary to maintain meristematic fate in., 2011, 62: 1271-1284.
[15] Borsani O, Zhu J H, Verslues P E, Sunkar R, Zhu J K. Endogenous siRNAs derived from a pair of natural cis-antisense transcripts regulate salt tolerance in., 2005, 123: 1279-1291.
[16] You J, Zong W, Li X, Ning J, Hu H, Li X, Xiao J, Xiong L. The SNAC1-targeted gene OsSRO1c modulates stomatal closure and oxidative stress tolerance by regulating hydrogen peroxide in rice., 2012, 64(2): 569-583.
[17] You J, Zong W, Du H, Hu H, Xiong L. A special member of the rice SRO family, OsSRO1c, mediates responses to multiple abiotic stresses through interaction with various transcription factors., 2014, 84(6): 693-705.
[18] Liu S, Liu S, Wang M, Wei T, Meng C, Wang M, Xia G. A wheat SIMILAR TO RCD-ONE gene enhances seedling growth and abiotic stress resistance by modulating redox homeostasis and maintaining genomic integrity., 2014, 26(1): 164-180.
[19] Babajani G, Effendy J, Plant A L. Sl-SROl1 increases salt tolerance and is a member of the radical-induced cell death 1-similar to RCD1 gene family of tomato., 2009, 176(2): 214-222.
[20] Li H, Li R, Qu F, Yao J, Hao Y. Identification of the SRO gene family in apples (Malus×domestica) with a functional characterization of MdRCD1., 2017, 13(5): 94.
[21] 呂有軍, 楊衛軍, 趙蘭杰, 姚金波, 陳偉,李燕,張永山. 陸地棉SRO基因家族的鑒定及表達分析. 作物學報, 2017, 43(10): 1468-1479.
Lü Y J, YANG W J, ZHAO L J, YAO J B, CHEN W, LI Y, ZHANG Y S. Genome-wide identification and expression analysis of SRO genes family inL.., 2017, 43(10): 1468-1479. (in Chinese)
[22] Riechmann JL, Heard J, Martin G, Reuber L, Jiang C, Keddie J,Adam L, Pineda O, Ratcliffe OJ, Samaha RR, Creelman R, Pilgrim M, Broun P, Zhang JZ, Ghandehari D, Sherman BK, Yu G.transcription factors: genome-wide comparative analysis among eukaryotes., 2000, 290:2105-2110.
[23] Olsen AN, Ernst HA, Leggio LL, Skriver K. NAC transcriptionfactors: structurally distinct, functionally diverse., 2005, 10:79-87.
[24] Du H, Huang M, Zhang Z, CHENG S. Genome-wide analysis of the AP2/ERF gene family in maize waterlogging stress response., 2014, 198(1): 115-126.
[25] Chen L, Song Y, Li S, Zhang L, Zou C, Yu D. The role of WRKY transcription factors in plant abiotic stresses., 2012, 1819(2): 120-128.
[26] NOGUERO M, ATIF R M, OCHATT S, THOMPSON R D. The role of the DNA-binding One Zinc Finger (DOF) transcription factor family in plants., 2013,, 32-45.
[27] Wang Y, Deng D, Shi Y, MIAO N, BIAN Y, YIN Z. Diversification, phylogeny and evolution of auxin response factor (ARF) family: insights gained from analyzing maize ARF genes., 2012, 39(3): 2401-2415.
(責任編輯 李莉)
Genome-wideIdentification and Expression Analysis ofGenes Family in Maize
ZHAOQiufang, MAHaiyang, JIA Liqiang,CHENShu, CHENHongliang
(South Subtropical Crops Research Institute, Chinese Academy of Tropical Agricultural Science/Key Laboratory of Tropical Fruit Biology, Ministry of Agriculture, Zhanjiang 524091, Guangdong)
【Objective】The SRO (similar to rcd one) is a group of plant-specific proteins which have important functions in plant growth and development, and response to abiotic stress. Based on maize genome information, the SRO family genes were identified, and the sequences, gene localization, protein structure and their evolutionary relationships were analyzed. Meanwhile, the SRO family genes tissue-specific expression profiles and expression pattern under salt and drought stresses ofwere analyzed. This research can lay a foundation for researching the function of SRO family genes in the growth and response mechanisms of stress in maize. 【Method】The Arabidopsis SRO protein sequences were used as queries to identify SRO in maize genome and download all the SRO gene sequences, which information regarding the maize SRO genes, including CDS sequences , amino acid sequences and chromosome location were obtained from MaizeGDB. The gene structure, protein molecular weight, isoelectric point, secondary structure, subcellular localization, conserved domain, and conserved element were also prospected and analyzed by GSDS2.0, Expasy-protparam, SOPMA, Plant-mPLoc, EMBL-EBI, MEME bioinformatics tools. Meanwhile the homologous sequence alignment and phylogeny were analyzed by Clustalx (1.83) and MEGA6.0 software. The expression levels of ZmSROs genes in different maize tissues and under high salt and drought stresses were analyzed by real-time fluorescence quantitative PCR. 【Result】Six SRO family genes were identified from Maize genome, and designatedto.were mapped on 1, 4, 5 and 9 chromosome, and contained two to five introns. The CDS of 6varied in length from 1,215 to 1,791 bp, and their predicted protein products ranged from 404 to 596 aa, with corresponding molecular masses of 45.23 kD and 66.78 kD, and with predicted isoelectric points in the range of 7.01 to 9.17. Subcellular localization analysis showed that ZmSRO1a/ZmSRO1b/ZmSRO1c/ZmSRO1d were located in the chloroplast, ZmSRO1e was located in the peroxisome, and ZmSRO1f was located in the nucleus. Phylogentic analysis revealed that ZmSROs can be divided into three subgroups. Subgroup Ⅰa contains ZmSRO1a/b/c, subgroups Ⅰb contains ZmSRO1f, and subgroup Ⅰc contains ZmSRO1d and ZmSRO1e. Conservative structure domain analysis showed that ZmSRO1a/ZmSRO1b/ZmSRO1c/ZmSRO1d/ZmSRO1e contain the PARP and RST domain, lack the WWE domain. ZmSRO1f contains the PARP and WWE domain, lacks the RST domains. A total 5 motif were identified from ZmSROs proteins,named motif 1—motif 5. ZmSRO1a/ZmSRO1b/ZmSRO1c contain all of motif,ZmSRO1d/ZmSRO1e lack the motif 3,ZmSRO1f lacks the motif 5. Different tissues expression assay showed that allhad specific expressions in root. The expression ofin root were significantly up-regulated under high salinity treatment for 1 h.were down-regulated in shoots, However, the expression ofin shoot was significantly up-regulated under high salinity treatment for 6 h.in root was up-regulated under drought stress for 1 h and that ofwas up-regulated for 24 h. Meanwhile, the expressions ofin shoot were down-regulated under drought stress and that ofandhad no significant changes in shoot. 【Conclusion】Maize SRO family contains six genes, and ZmSROs genes could be classified into threes subgroups. Six ofgenes had specific expressions in root and could respond to high salt and drought stresses in varying degrees.
; SRO gene; abiotic stress; gene expression
2018-02-28;
2018-05-09
國家自然科學基金(31501818)、中國熱帶農業科學院基本科研業務費專項資金(1630062017006、1630062017015和1630062015003)
趙秋芳,E-mail:qiufangzhao@163.com。通信作者賈利強,E-mail:lqjia@mail.zaas.ac.cn
10.3864/j.issn.0578-1752.2018.15.0016

