阿莫西林克拉維酸鉀片含量測定方法的改進
張靜巖 張煒 任風芝 張雪霞 王海燕 孟令茹
摘要:為解決實際應用中克拉維酸鉀峰與后相鄰雜質的分離度達不到要求的問題,建立了一種同時測定阿莫西林克拉維酸鉀片中阿莫西林和克拉維酸鉀含量的新方法,采用反相高效液相色譜法(RP-HPLC), Ultimate AQ-C18色譜柱(4.6 mm×250 mm,5 μm),以pH值為4.4的0.05 mol/L磷酸二氫鈉緩沖液為流動相,柱溫為35 ℃,流速為1.0 mL/min ,檢測波長為220 nm 。結果表明:阿莫西林和克拉維酸鉀兩主峰與相鄰雜質得到完全基線分離,分離度大于1.5;克拉維酸鉀對照品溶液質量濃度為0.050 0~0.500 1 mg/mL時與峰面積的線性關系良好(r=0.999 8),平均回收率(n=9)為100.14%,RSD值為0.24%;阿莫西林對照品溶液質量濃度為0.100 0~1.000 1 mg/mL時與峰面積的線性關系良好(r=0.999 9),平均回收率(n=9)為100.45%,RSD值為017%。與原有的《中華人民共和國藥典》方法相比,新的阿莫西林克拉維酸鉀片含量測定方法專屬性好,準確度高,操作簡便快捷,結果可靠,可作為一種質量控制方法。
關鍵詞:色譜分析;阿莫西林;克拉維酸鉀;含量測定;高效液相色譜法
中圖分類號:R9781+1文獻標志碼:Adoi: 10.7535/hbgykj.2018yx04013
阿莫西林克拉維酸鉀片是葛蘭素史克(GSK)公司研制的由阿莫西林三水化合物和克拉維酸鉀組方的復方制劑,屬于國家基本藥物[1-2]。其中阿莫西林為廣譜青霉素類抗生素,克拉維酸鉀為競爭性廣譜β-內酰胺酶抑制劑,兩者合用,可保護阿莫西林免受β-內酰胺酶的水解,使對阿莫西林耐藥并產生β-內酰胺酶的細菌仍然對阿莫西林敏感,從而不影響阿莫西林的殺菌效果[3-4],臨床上廣泛應用于敏感菌引起的上呼吸道感染、下呼吸道感染、泌尿系統感染、軟組織及皮膚感染以及其他感染。國家食品藥品監督管理總局(CFDA) 明確規定在2018年底前需完成對“阿莫西林克拉維酸鉀片”及其原研制劑的一致性評價工作[5-9]。目第4期張靜巖,等:阿莫西林克拉維酸鉀片含量測定方法的改進河北工業科技第35卷前,本實驗室對該藥品進行了含量、雜質和溶出曲線等對比研究。《中華人民共和國藥典》(以下簡稱《藥典》)2015版[10]所述方法在含量測定部分指出,記錄色譜圖譜應與標準圖譜一致,但對分離度并未有具體的要求,而在實際應用中發現克拉維酸鉀峰與后相鄰雜質的分離度達不到要求。本文在《藥典》2015版分析方法及相關文獻\[10-20\]的基礎上,對阿莫西林克拉維酸鉀片含量的測定方法進行了改進,采用水相柱對樣品組分進行分離,通過色譜條件優化實現純緩沖鹽相作為流動相,從而達到綠色環保檢測的要求,操作簡便,且最終的分離度符合要求,效果較好。
1主要儀器與試藥
Aglient 1260高效液相色譜儀(安捷倫科技有限公司提供);色譜柱Ultimate AQ-C18(4.6 mm×250 mm,5 μm,月旭科技(上海)股份有限公司提供);BP211D電子天平(德國賽多利斯集團提供)。
克拉維酸化學對照品(批號為130429-201307,含量為95.0%(質量分數,下同),中國藥品生物制品檢定所提供);阿莫西林化學對照品(批號為130409-201011,含量為85.8%,中國食品藥品檢定研究院提供);阿莫西林克拉維酸鉀系統適用性對照品(批號為130588-201202,中國食品藥品檢定研究院提供);阿莫西林克拉維酸鉀片 (規格為0.375 g,批號為170201,170202,170203,自制);水為超純水;磷酸二氫鈉(批號為20140728,優級純,天津市永大化學試劑開發中心提供)。
2方法與結果
2.1色譜條件
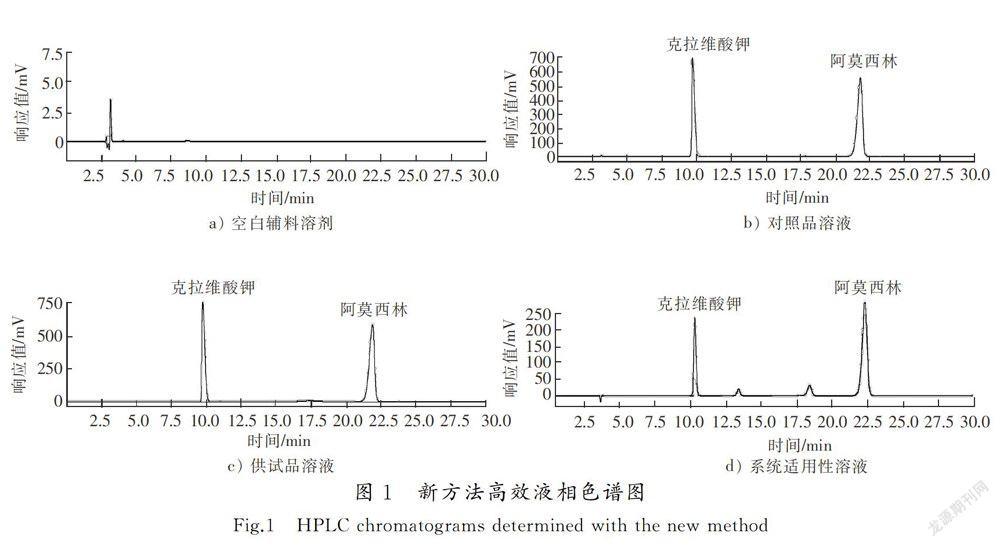
色譜柱為Ultimate AQ-C18(4.6 mm×250 mm,5 μm),流動相為005 mol/L磷酸鹽緩沖液(0.05 mol/L磷酸二氫鈉溶液,取磷酸二氫鈉7.8 g,加水900 mL使之溶解,用10%磷酸溶液或氫氧化鈉溶液調pH值至(4.4±0.1),加水稀釋至1 000 mL),檢測波長為220 nm,進樣體積為20 μL,柱溫為35 ℃,流速為1.0 mL/min,分離度不低于2.0,色譜圖見圖1。
2.2溶液的配制
阿莫西林克拉維酸鉀系統適用性對照品溶液的配制:精密稱取適量阿莫西林克拉維酸鉀系統適用性對照品,加流動相溶解并稀釋制成0.8 mg/mL的溶液。
對照品溶液的配制:精密稱取適量克拉維酸對照品和阿莫西林對照品,加水超聲溶解,制成含克拉維酸0.25 mg/mL和含阿莫西林0.50 mg/mL的溶液。
供試品溶液的配制:另取阿莫西林克拉維酸鉀10片,研細,精密稱取適量,加水超聲溶解,制成含克拉維酸0.25 mg/mL和含阿莫西林0.50 mg/mL的溶液,用0.45 μm的微孔濾膜過濾,棄去初濾液,取續濾液作為供試品溶液。
2.3專屬性試驗
分別精密吸取阿莫西林克拉維酸鉀系統適用性對照品溶液、阿莫西林克拉維酸對照品溶液、供試品溶液,以及高溫、光照、酸堿和氧化的強制降解樣品溶液各20 μL,注入液相色譜儀,按“2.1”項所述方法進行分析,記錄色譜圖。結果發現,在該色譜條件下,所有強降解產物與兩主峰分離度良好,未見輔料干擾,克拉維酸保留時間為9.82 min,阿莫西林保留時間約為21.75 min,輔料無吸收峰。表明該方法的專屬性良好。
2.4線性范圍考察
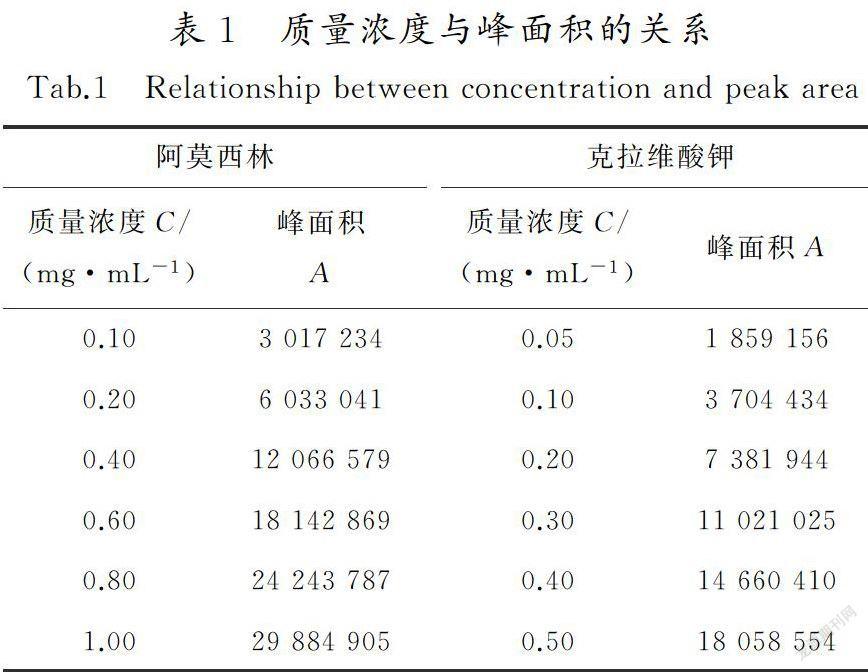
取克拉維酸對照品26.32 mg、阿莫西林對照品58.28 mg,精密稱定,用超純水配制成含克拉維酸0500 1 mg/mL和含阿莫西林1.000 1 mg/mL的對照品儲備液。準確移取儲備液1,2,4,6和8 mL,分別置于10 mL量瓶中,用超純水稀釋定容至刻度,搖勻,得到克拉維酸質量濃度分別為005,010,020,030,040,050 mg/mL和阿莫西林質量濃度分別為010,020,040,060,080,100 mg/mL的標準品溶液。分別吸取20 μL進樣,記錄色譜圖。以對照品峰面積A為縱坐標,質量濃度C為橫坐標進行線性回歸,得到克拉維酸的線性方程為A=36 136 625.041 1C+112 292.364 4(r=0.999 8) ,表明克拉維酸在質量濃度為0.050 0~0.500 1 mg/mL時與峰面積的線性關系良好;阿莫西林的線性方程為A=29 999 898.274 0C+64 788.391 8(r=0.999 9),表明阿莫西林在質量濃度為0100 0~1000 1 mg/mL時與峰面積的線性關系良好。結果見表1。
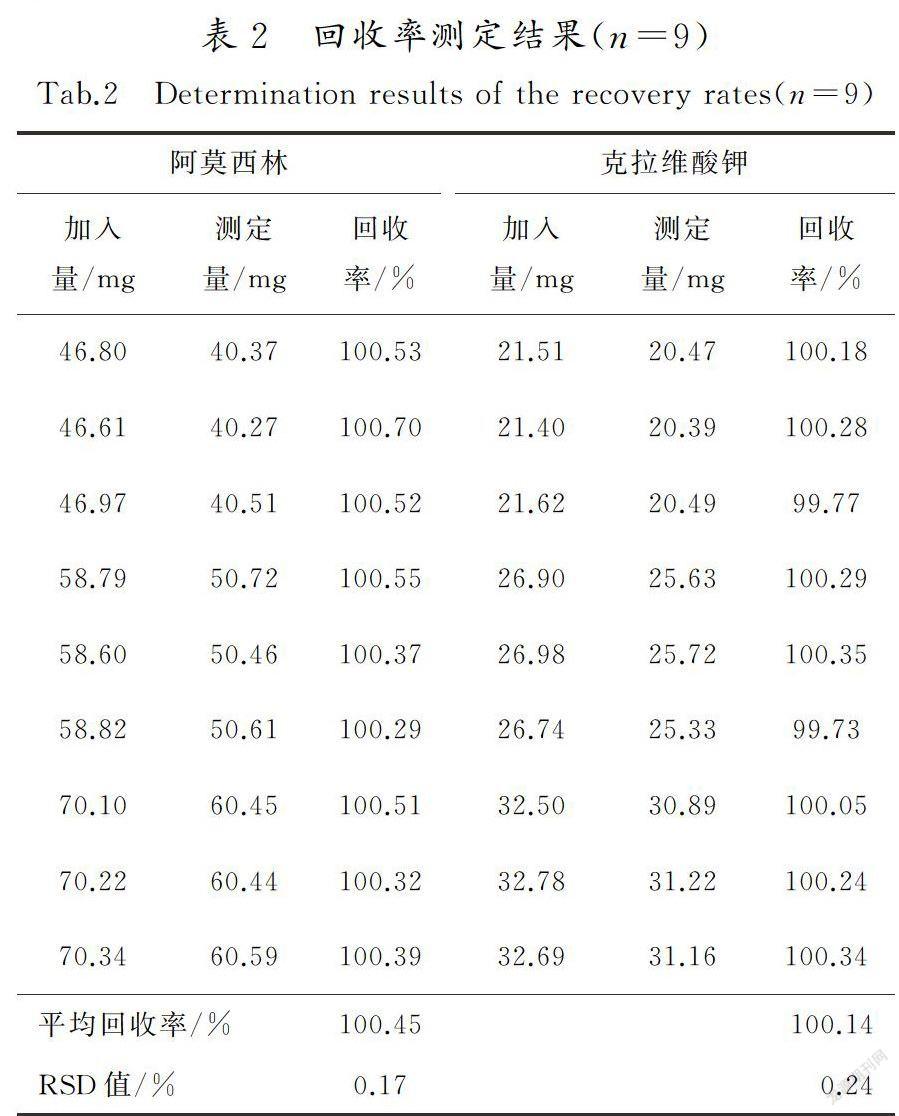
2.5回收率試驗
按處方比例稱取輔料和阿莫西林原料制成的無克拉維酸鉀的空白輔料,分成9等份,3 份為一組,分別精密加入一定量的克拉維酸鉀對照品,充分混
合均勻后置于100 mL 量瓶中,按“2.1”項所述方法進行分析,記錄色譜圖。按處方比例稱取輔料和克拉維酸鉀原料制成的無阿莫西林的空白輔料,分成9等份,3 份為一組,分別精密加入一定量的阿莫西林對照品,充分混合均勻后置于100 mL 量瓶中,按“2.1”項所述方法進行分析,記錄色譜圖。結果見表2。
2.6檢測限和定量限試驗
取阿莫西林對照品適量,加入超純水溶解,配制成質量濃度為0.101 1 mg/mL的溶液,然后逐步稀釋至原質量濃度的1/100 ,1/500 ,1/1 000,1/5 000 ,1/10 000,按上述色譜條件進樣測定,最小檢出限為10.11 ng/mL(S/N=3),最小定量限為20.22 ng/mL(S/N=10)。
取克拉維酸鉀對照品適量,加入超純水溶解,配制成質量濃度為0.100 4 mg/mL的溶液,然后逐步稀釋至原質量濃度的1/100 ,1/500 ,1/1 000,1/2 000,1/5 000,1/10 000,按上述色譜條件進樣測定,測得最小檢出限為10.04 ng/mL(S/N=3),最小定量限為50.20 ng/mL(S/N=10)。
2.7精密度試驗
精密吸取“2.2”項同一對照品溶液20 μL,連續重復進樣6次,以相應的色譜峰的面積計算RSD值,阿莫西林為0.15%、克拉維酸為0.07%(n=6),結果見表3。結果表明,儀器的精密度良好。
2.8重復性試驗
取阿莫西林克拉維酸鉀片樣品(規格為0.375 g,批號為170201),配制成供試樣品溶液6份,按“2.1”項所述色譜條件重復測定阿莫西林和克拉維酸鉀含量(質量分數,下同),結果見表4 。結果表明,該方法的重復性良好。
2.9穩定性試驗
取同批阿莫西林克拉維酸鉀片樣品(規格為 0375 g,批號為170201),按“2.2”項所述方法制備供試品溶液,室溫放置,按“2.1”項色譜條件分別于0,2,4,6和8 h進樣分析,記錄供試品溶液各色譜圖的峰面積,結果見表5。結果表明,供試品溶液在8 h內的穩定性良好。
3樣品測定
按外標法以峰面積計算克拉維酸鉀和阿莫西林的含量,分別用新方法和《藥典》方法對3批樣品的含量進行測定,測定結果如表6和表7所示。比較表6和表7中2種方法的測定結果發現,新方法中主峰與雜質峰達到基線分離,分離度大于1.5。
4結語
1)本文所述新方法采用Ultimate AQ-C18色譜柱、純緩沖鹽A相作為流動相進行等梯度洗脫,減少了有害溶劑的使用,將對人體的傷害降到最低,達到了綠色環保檢測的效果。
2)克拉維酸鉀尾部雜質被完全分離出,與相鄰雜質能夠實現完全基線分離,且克拉維酸鉀峰與其前鄰雜質峰的分離度達到3.8,與其后雜質峰的分離度達到5.0;阿莫西林主峰與其前峰的分離度達到23,與其后峰的分離度達到7.9,均優于《藥典》條件。
3)按外標法以峰面積計算克拉維酸鉀和阿莫西林的含量,新方法中主峰與雜質峰達到基線分離,分離度大于1.5,較好地解決了《藥典》方法峰型拖尾和分離度不好等問題。新方法的專屬性好,準確度高,操作簡便快捷,結果可靠,可作為質量控制方法。
4)本研究雖然相比《藥典》方法分離度好,使用的溶劑綠色環保,但尚存在不足之處,如分析時間較長,導致分析效率較低。未來需要在縮短分析時間方面加以深入研究,建議采用UPLC進行分析,因為在分離色譜峰時,UPLC的分離度高出HPLC 1倍,甚至更多,分析時間也縮短為HPLC的1/3,分辨率和靈敏度也能得到有效提高[21]。在條件允許的情況下,采用UPLC對該品種進行分析將是不錯的選擇。
參考文獻/References:
[1]CHONG X M, ZOU W B, YAO S C,et al. Rapid analysis of the quality of Amoxicillin and Clavulanate potassium tablets using diffuse reflectance near-infrared spectroscopy[J].AAPS Pharm Sci Tech, 2017,18(4):1312-1317.
[2]黃敏文,袁耀佐,張玫,等. 國產阿莫西林克拉維酸鉀片質量評價[J]. 藥物分析雜志,2012,32(3):520-526.
HUANG Minwen,YUAN Yaozuo,ZHANG Mei,et al.Quality evaluation of domestic Amoxicillin and Clavulanate potassium tablets [J].Chinese Journal of Pharmaceutical Analysis, 2012,32(3):520-526.
[3]關旭久,張旭,洪曉菲,等.阿莫西林克拉維酸鉀分散片含量測定方法的探討[J].中國處方藥,2015,13(1):16-17.
GUAN Xujiu,ZHANG Xu,HONG Xiaofei, et al. Determination of the content of Amoxicillin potassium Clavulanate dispersible tablets[J].Journal of China Preseription Drug,2015,13(1):16-17.
[4]蔡玲玲,鄒丹. 國產阿莫西林克拉維酸鉀片的質量評估[J]. 中國現代藥物應用,2015,9(16):272-273.
CAI Lingling,ZOU Dan. Quality evaluation of domestic Amoxicillin and Clavulanate potassium tablets[J].Chinese Journal of Modern Drug Application, 2015,9(16):272-273.
[5]郝瑞霞,王景欣. 自產阿莫西林克拉維酸鉀片與原研產品的體外溶出一致性分析[J].中國醫藥導刊,2016,18(8):854-857.
HAO Ruixia,WANG Jingxin.In vitro dissolution profile comparison on Amoxicillin and Clavulanate potassium tablets and innovator drug[J].Chinese Journal of Medicinal Guide, 2016,18(8):854-857.
[6]林蘭,牛劍釗,許明哲,等. 國外仿制藥一致性評價比較分析[J]. 中國新藥雜志,2013,22(21):2470-2474.
LIN Lan,NIU Jianzhao,XU Mingzhe,et al.Comparative analysis of consistency evaluation for generic drugs in foreign countries[J].Chinese Journal of New Drugs, 2013,22(21):2470-2474.
[7]劉昌孝. 藥品安全戰略與仿制藥一致性評價策略[J]. 中國臨床藥理學與治療學,2016,21(10):1081-1087.
LIU Changxiao.Strategy for drug safety and consistency evaluation of generic drugs[J]. Chinese Journal of Clinical Pharmacology Therapeutics,2016,21(10):1081-1087.
[8]許明哲,牛劍釗,陳華,等. 淺談仿制藥質量一致性評價過程管理的原則及政策依托[J]. 中國新藥雜志,2013,22(21):2475-2477.
XU Mingzhe, NIU Jianzhao,CHEN Hua,et al. Principle and policy for process management of consistency evaluation for generic drugs[J].Chinese Journal of New Drugs, 2013,22(21): 2475-2477.
[9]陳震,楊建紅,張彥彥,等.影響我國化學藥品仿制藥質量的潛在因素分析[J]. 中國新藥雜志,2017,26(12):1345-1350.
CHEN Zhen,YANG Jianhong,ZHANG Yanyan,et al. Analysis of the potential factors affecting the quality of chemical generic drugs in China[J]. Chinese Journal of New Drugs,2017,26(12):1345-1350.
[10]國家藥典委員會. 中華人民共和國藥典(二部)[M]. 北京: 中國醫藥科技出版社, 2015: 435.
[11]勞喬蓮,邱文濤,勞秋立. 阿莫西林-克拉維酸鉀干混懸劑(8∶1)的質量標準控制[J]. 中國處方藥,2017,15(8):29-31.
LAO Qiaolian,QIU Wentao,LAO Qiuli. The study of quality standards on Amoxicillin and Clavulanate potassium for suspension(8∶1)[J]. Journal of China Prescription Drug, 2017,15(8):29-31.
[12]張珂. HPLC法測定阿莫西林克拉維酸鉀顆粒的含量[J]. 藥學進展,2007,31(5):221-224.
ZHANG Ke. Determinationof Amoxicillin and Clavulanate potassium granules by HPLC[J]. Progressin Pharmaceutical Sciences, 2007,31(5):221-224.
[13]張亞洲,樊蘭蘭,屈嘯聲,等. RP-HPLC法測定阿莫西林克拉維酸鉀干混懸劑(14∶1) 中阿莫西林克拉維酸的含量[J].安徽醫藥,2013,17(2):207-210.
ZHANG Yazhou,FAN Lanlan,QU Xiaosheng,et al.Determinnation of Amoxicillin and Clavulanate potassium suspension (14∶1) by RP-HPLC[J].Anhui Medical and Pharmaceutical Journal, 2013,17(2):207-210.
[14]黃敏文,袁耀佐,錢文,等.UPLC-UV法同時測定阿莫西林克拉維酸鉀片中阿莫西林和克拉維酸的含量及其在國產片劑溶出曲線測定中的應用[J]. 藥物分析雜志,2013,33(12):2171-2175.
HUANG Minwen,YUAN Yaozuo,QIAN Wen,et al.Simultaneous determination of Amoxicillin and Clavulanate in amoxicillin and clavulanate potassium tablets by UPLC-UV and its application in the dissolution profile study in domestic tablets[J].Chinese Journal of Pharmaceutical Analysis,2013,33(12):2171-2175.
[15]沈丹丹,吳群,胡幸,等. 阿莫西林/克拉維酸鉀干混懸劑有關物質測定方法的比較研究[J]. 中國抗生素雜志,2016,41(11):848-852.
SHEN Dandan, WU Qun, HU Xing,et al. Comparative study on determination methods of Amoxicillin and Clavulanate potassium for suspension[J]. Chinese Journal of Antibiotics,2016,41(11):848-852.
[16] 王德剛,程玉寶,馬萍,等. 阿莫西林克拉維酸鉀緩釋片含量測定及釋放度測定方法研究[J]. 今日藥學,2010,20(10):19-22.
WANG Degang,CHENG Yubao,MA Ping,et al.Study on determination of content and release of Amoxicillin and Clavulanate potassium sustained-release tables[J].Pharmacy Today,2010,20(10):19-22.
[17]崇小萌,李進,王琰, 等. 阿莫西林克拉維酸鉀片劑的關鍵質量屬性與控制[J].藥學學報, 2016,51(7): 1121-1124.
CHONG Xiaomeng,LI Jin,WANG Yan,et al. The control of the critical quality attributes of Amoxicillin and Clavulanate potassium tablet[J]. Acta Pharmaceutica Sinica, 2016,51(7): 1121-1124.
[18] 左登平. 利用NIR技術建立阿莫西林克拉維酸鉀顆粒一致性比對模型的研究[J]. 黑龍江醫藥,2014,7(5):1044-1046.
ZUO Dengping.Study on conformity test of Amoxicillin and Clavulanate potassium granules by near infrared spectroscopy[J].Heilongjiang Medicine Journal,2014,7(5):1044-1046.
[19]薛晶,朱克旭,崇小萌,等. 水分對阿莫西林克拉維酸鉀顆粒穩定性的影響[J]. 中國藥學雜志,2016,51(3):224-229.
XUE Jing,ZHU Kexu,CHONG Xiaomeng,et al.Influence of moisture on stability of Amoxicillin and potassium Clavulanate granules[J].Chinese Pharmaceutical Journal, 2016,51 (3):224-229.
[20]周文杰,張麗英. 校正因子在阿莫西林/克拉維酸鉀片含量測定中的應用探討[J]. 中國抗生素雜志,2009,34(10):637-640.
ZHOU Wenjie,ZHANG Liying. Research of the application of correction factorin the determination of Amoxicillin and potassium Clavulanate tablets[J]. Chinese Journal of Antibiotics, 2009,34(10):637-640.
[21]鄭勤琴,項勛,段綱,等.高效液相色譜和超高效液相色譜在藥物分析中的應用研究[J].上海畜牧獸醫通訊,2017(2):57-59.
ZHENG Qinqin,XIANG Xun,DUAN Gang,et al.Applications of HPLC and UPLC in pharmaceutical analysis[J].Shanghai Journal of Animal Husbandry and Veterinary Medicine, 2017(2):57-59.

