恩替卡韋聯合雙歧桿菌乳桿菌三聯活菌片治療失代償期乙型肝炎肝硬化臨床療效觀察
李波,鄧存良
大約有四分之一的慢性乙型肝炎患者可能會發展成為肝硬化[1]。在疾病的早期,由于肝臟代償功能較強可無明顯癥狀。隨著病變進展,患者會進入失代償期肝硬化,從而出現較為嚴重的臨床癥狀和各種并發癥,預后極差。研究表明,未經過治療的失代償期肝硬化患者5 a病死率高達84%[2]。目前,治療失代償期乙型肝炎肝硬化的主要方法是口服抗病毒藥物,以抑制乙型肝炎病毒(hepatitis B virus,HBV)復制。恩替卡韋是一種強效的口服核苷酸類似物,已在多項臨床研究中顯示對乙型肝炎肝硬化患者具有良好的抗病毒療效[3]。近年來,越來越多的研究表明腸道菌群紊亂與慢性肝臟疾病關系密切,菌群失調的嚴重程度與肝臟疾病的嚴重程度相關[4]。本研究應用恩替卡韋聯合雙歧桿菌乳桿菌三聯活菌治療失代償期乙型肝炎肝硬化患者,現將結果報道如下。
1 對象與方法
1.1 病例選擇 2015年3月~2017年8月我院收治的失代償期乙型肝炎肝硬化患者120例,男性86例,女性34例;平均年齡(51.2±6.2)歲。符合《慢性乙型肝炎防治指南》的診斷標準[5],排除以下患者:1)感染人類免疫缺陷病毒或其他肝炎病毒;2)合并酒精性、自身免疫性或膽汁淤積性肝病;3)伴有惡性腫瘤、嚴重心臟病、糖尿病,腎功能損害;4)孕婦或哺乳期婦女。該研究經過本院醫學倫理委員會批準,全部入組患者簽署知情同意書。
1.2 治療方法 將患者隨機分為對照組60例和觀察組60例,兩組在性別、年齡、病程和肝功能Child-Pugh分級等一般資料方面比較無統計學差異(P>0.05),具有可比性。給予對照組患者恩替卡韋分散片(江蘇正大天晴藥業股份有限公司,國藥準字H20100019)0.5 mg口服,1次/d;觀察組在對照組治療基礎上加用雙歧桿菌乳桿菌三聯活菌片(內蒙古雙奇藥業股份有限公司,國藥準字S19980004)2 g口服,3次 /d。
1.3 指標檢測 使用西門子ADVIA2400全自動生化分析儀檢測血生化指標;采用Snibe MAGLUMI 4000全自動化學發光免疫分析儀檢測血清透明質酸(HA)、層粘連蛋白(LN)、三型前膠原N 端肽(PIIIP)和Ⅳ型膠原(C-IV,深圳市新產業生物醫學工程股份有限公司);使用羅氏 LightCycler 480熒光PCR分析儀檢測血清HBV DNA【羅氏診斷產品(上海)有限公司】;使用法國 Stago-evolution全自動血凝儀檢測凝血酶原時間(PT,法國Stago公司)。
1.4 統計分析 應用SPSS 19.0軟件進行統計分析。計量資料以(±s)表示,組間比較采用配對樣本的t檢驗,計數資料以%表示,組間比較采用x2檢驗。P<0.05被認為差異具有統計學意義。
表1 兩組肝功能指標(±s)變化比較
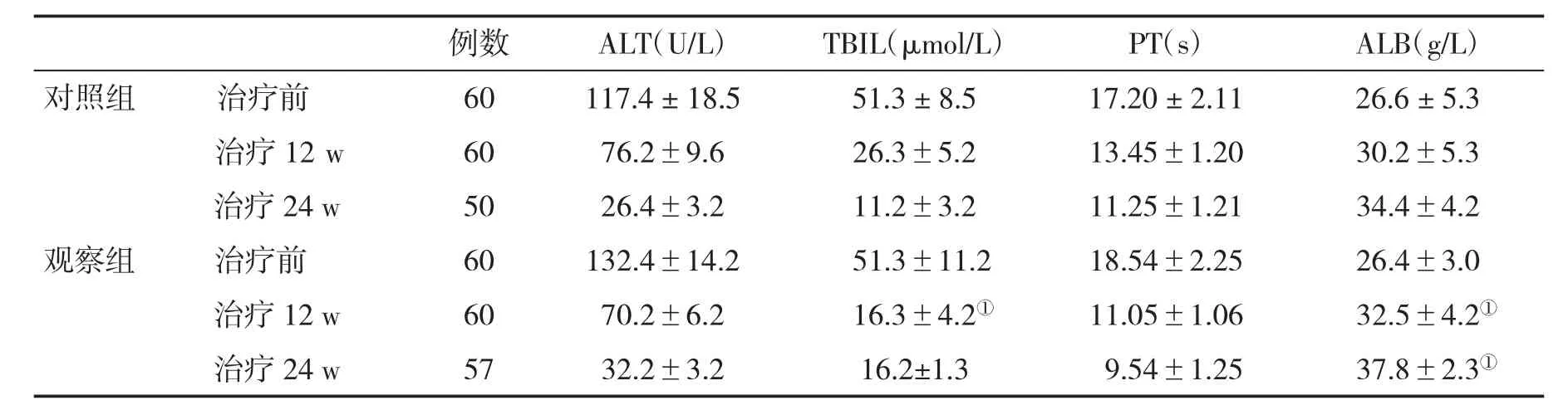
表1 兩組肝功能指標(±s)變化比較
與對照組比,①P<0.05
ALB(g/L)26.6±5.3 30.2±5.3 34.4±4.2 26.4±3.0 32.5±4.2①治療 24 w 57 32.2±3.2 16.2±1.3 9.54±1.25 37.8±2.3①
2 結果
2.1 兩組肝功能指標變化比較 治療前,兩組各項肝功能指標水平比較無顯著性差異(P>0.05);在治療12 w和24 w,觀察組血清ALB水平顯著高于對照組(P<0.05,表1)。
2.2 兩組血清肝纖維化指標變化比較 治療前,兩組各項血清肝纖維化指標比較無顯著性差異(P>0.05);在治療12 w和24 w,觀察組血清HA、PIIIP、LN和C-IV水平顯著低于對照組(P<0.05,表2)。
表2 兩組血清肝纖維化指標(±s)變化比較
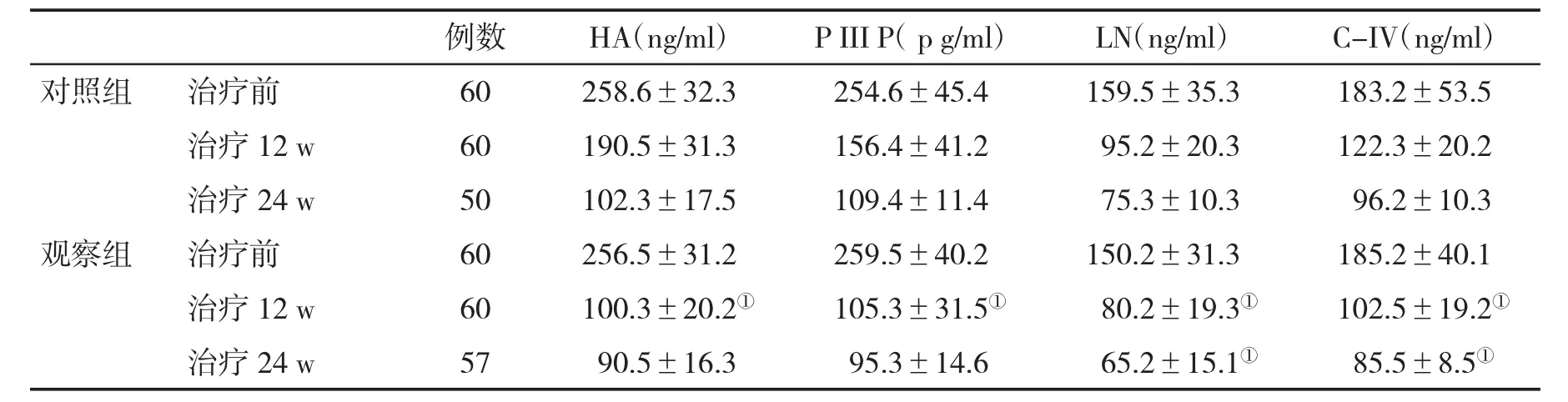
表2 兩組血清肝纖維化指標(±s)變化比較
與對照組比,①P<0.05
例數 HA(ng/ml) P III P(pg/ml) LN(ng/ml) C-IV(ng/ml)對照組 治療前 60 258.6±32.3 254.6±45.4 159.5±35.3 183.2±53.5治療 12 w 60 190.5±31.3 156.4±41.2 95.2±20.3 122.3±20.2治療 24 w 50 102.3±17.5 109.4±11.4 75.3±10.3 96.2±10.3觀察組 治療前 60 256.5±31.2 259.5±40.2 150.2±31.3 185.2±40.1治療12 w 60 100.3±20.2① 105.3±31.5① 80.2±19.3① 102.5±19.2①治療 24 w 57 90.5±16.3 95.3±14.6 65.2±15.1① 85.5±8.5①
2.3 兩組血清HBV DNA陰轉率比較 治療前,兩組血清HBV DNA水平比較無顯著性差異(P>0.05)。治療后,兩組血清HBV DNA陰轉率無顯著性差異(P>0.05,表3)。
表3 兩組血清HBV DNA水平(±s)和轉陰率(%)比較
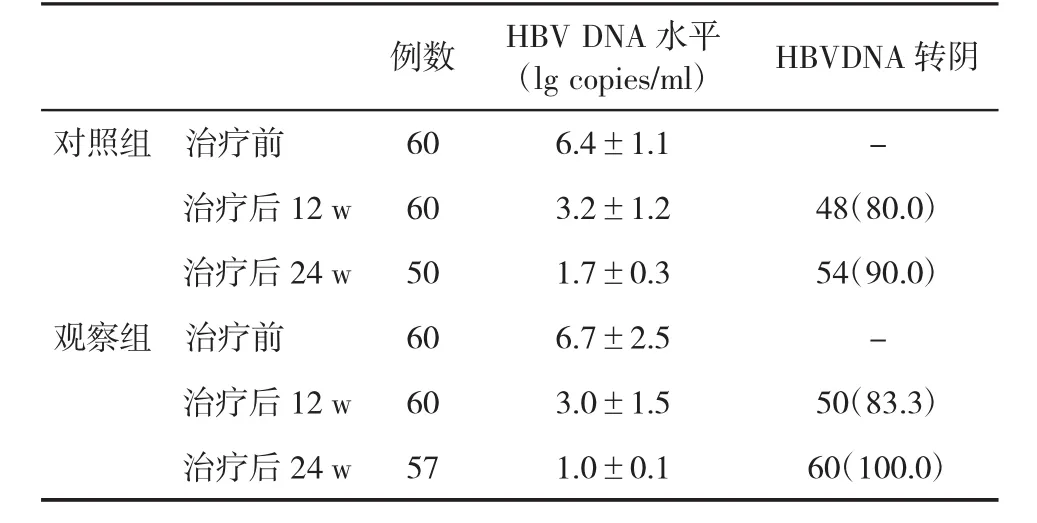
表3 兩組血清HBV DNA水平(±s)和轉陰率(%)比較
例數 HBV DNA水平(lg copies/ml) HBVDNA轉陰對照組 治療前 60 6.4±1.1 -治療后 12 w 60 3.2±1.2 48(80.0)治療后 24 w 50 1.7±0.3 54(90.0)觀察組 治療前 60 6.7±2.5 -治療后 12 w 60 3.0±1.5 50(83.3)治療后 24 w 57 1.0±0.1 60(100.0)
2.4 兩組并發癥和生存率比較 在治療12 w和24 w,觀察組發生自發性細菌性腹膜炎(SBP)5例(8.3%)和2例(3.3%),顯著低于對照組的10例(16.7%)和8例(13.3%,P<0.05);在治療24 w末,觀察組死亡3例(5%),而對照組死亡10例(16.7%,P<0.05)。
3 討論
乙型肝炎肝硬化是HBV感染導致的嚴重疾病,可以分為代償期和失代償期。當肝硬化發展到失代償期時,主要表現為肝功能受損和門靜脈高壓癥,可出現消化道出血、肝性腦病、感染以及頑固性腹水等并發癥[7],嚴重時患者會發生進行性肝功能衰竭而導致死亡[8]。乙型肝炎肝硬化的發病機制較為復雜,目前普遍認為HBV不斷復制導致活動性肝炎反復發作是疾病發生的最主要原因。因此,在臨床上給予患者抗病毒藥物已經成為治療的主要方法[9]。恩替卡韋是一種選擇性抑制HBV復制的脫氧鳥嘌呤核苷類似物,具有極強的抑制HBV復制、降低血清HBV DNA水平的作用[10],且未見明顯的不良反應和線粒體毒性,是一種安全性較高的治療乙型肝炎的有效藥物,在臨床上應用較廣泛[11]。近年來,隨著研究的深入,有關腸道微生物菌群在病毒性肝炎發生發展中所發揮的作用逐漸引起了學者們的重視[12,13]。有報道指出CHB和慢性丙型肝炎患者血液脂多糖(LPS)、腸型脂肪酸結合蛋白(I-FABP)、炎性因子可溶性 CD14(sCD14)和白細胞介素16(IL-16)水平均增高[14]。有理論認為腸道與肝臟的相關性不僅表現在解剖結構的緊密相連,而且兩者在生理功能方面構成了“腸肝軸”。腸道共生菌群的改變,例如菌群豐度或菌群組成的改變,都會影響腸道中的免疫微環境[15,16],進而引發劇烈的免疫反應,影響乙型肝炎的發生和發展。有學者也將這種腸道與肝臟系統功能上相互關聯的影響稱為“肝腸對話”[17]。
基于腸道微生物菌群對病毒性肝炎的影響,可利用益生菌改善腸道微環境輔助治療慢性乙型肝炎患者。何偉鋒等人[18]評價了恩替卡韋聯合益生菌治療失代償期乙型肝炎肝硬化患者的療效,發現同時給予恩替卡韋和益生菌的觀察組患者在1年的治療后,肝功能生化指標、血清內毒素水平和自發性細菌性腹膜炎發生率均明顯優于或低于僅接受恩替卡韋治療的對照組,提示兩者聯合用藥在治療失代償期乙型肝炎肝硬化方面具有較好的療效。王寶根[19]等人觀察了利用雙腸溶歧三聯活菌膠囊治療失代償期乙型肝炎肝硬化患者的效果,發現肝臟功能和腹水等觀察指標在治療前后比較均有明顯的改善,與對照組比,加用了益生菌的觀察組治療后血清ALT、AST和TBIL水平顯著降低。在本研究中,我們探討了雙歧桿菌乳桿菌三聯活菌片聯合恩替卡韋治療失代償期乙型肝炎肝硬化患者的臨床療效。所得到的結果顯示在給藥后12周和24周觀察組患者的臨床療效均顯著優于同一時點的對照組,各項指標的比較結果也顯示兩組患者的肝功能指標、肝纖維化指標和血清HBV DNA水平較治療前均顯著改善,而且觀察組患者的上述指標的改善程度均顯著優于對照組;在治療后24周,觀察組患者自發性細菌性腹膜炎發生率、并發癥和遠期病死率均顯著低于同一時間點的對照組。本研究所得到的研究結果與之前學者報道一致,提示益生菌類藥物聯合抗病毒藥物能夠有效地治療失代償期乙型肝炎肝硬化患者。
除此之外,越來越多的證據表明腸道菌群不僅可以影響肝臟疾病的發生,甚至有人認為腸道菌群是人體的“第二大腦”,腸道菌群可以與大腦之間通過形成“腦-腸軸”改變腦功能,影響神經性疾病的發生與發展[20]。這種相關性依賴于腸道菌群與大腦之間互通的復雜的信號網絡,這一觀點也為治療失代償期乙型肝炎肝硬化患者并發肝性腦病等神經系統并發癥提供了新的治療思路。目前,在臨床上已經有文獻開始探討應用益生菌聯合常規治療方法治療肝性腦病患者,得到的結果也提示了益生菌的有效治療作用[21-25]。

