Zeolites模板法制備氮摻雜多孔碳材料及其CO2吸附性能
劉康愷, 韓云龍, 孟龍月,, 樸英愛
(延邊大學 a.理學院 化學系;b.工學院 化學工程系;c.實驗室與設備管理處,吉林 延吉 133002)
0 引 言
溫室效應的不斷增強引起了全球氣候變暖、海平面上升等環境問題,CO2作為溫室氣體中最主要的成分,是溫室效應的主要貢獻者。為了有效地捕集并儲存CO2,目前常用的方法有固體吸附法、溶液吸收法、膜分離法、生物分離法和深冷分離法。固體吸附法具有操作簡單、能耗低、自動化程度高和對設備腐蝕程度低等優點,得到了廣泛的應用。常用的固體吸附材料有分子篩、活性氧化鋁、金屬有機框架和多孔碳材料等[1]。氮摻雜多孔碳材料(NPCs)是多孔碳材料吸附劑一類中的新型材料,相較于直接碳化制得的多孔碳材料,NPCs通過引入含雜原子N的堿性官能團,而提高其對酸性氣體CO2發生界面吸附時的結合力,從而大大提高了吸附劑對CO2的吸附性和選擇性,因此受到學者們的廣泛關注[2]。
用于CO2吸附的NPCs通常應滿足:①表面官能團含有吡啶型或吡咯型氮;②材料形貌以及孔隙結構尺寸。制備NPCs的主要方法有后處理法和原位摻雜法。后處理法是通入含氮氣體在高溫條件下對已經初步合成的多孔碳材料進行表面改性,或者將含氮有機基團嫁接到材料表面進行修飾,包括氨氣后處理法、化學活化法等。原位摻雜法則是在碳材料進行合成的同時引入氮源,或者是碳前驅體本身含有氮元素,在碳前驅體進行活化的過程中,氮原子摻雜內嵌在多孔碳材料的內部,使制備過程簡單,可有效控制其摻雜的氮的含量[3]。原位摻雜法制備NPCs的方法主要有模板法、化學氣相沉積法和水熱法。模板法常用多孔氧化硅、多孔陽極氧化鋁等多孔材料作為模板劑來制備氮摻雜多孔碳材料,其優點是可以根據不同孔道結構的模板劑控制所制備材料的形貌、比表面、孔隙結構等。聚吡咯作為既含碳元素,又含氮元素的碳前驅體,具有生物相容性好、環境穩定性強、價格便宜、制備簡單等優點,近年來廣泛應用于制備氮摻雜多孔碳材料[4]。聚吡咯的制備方式通常分為電化學聚合法和化學氧化聚合法兩大類,化學氧化聚合法制備過程簡單,且可以單次大量制備,包括溶液聚合、界面聚合及氣相聚合等,氣相聚合法是將單體以氣態的形式進行聚合。本研究采用氣相聚合法,使吡咯單體以氣相進入模板劑,并在模板劑中催化劑的作用下發生聚合反應,相較于其他聚合方式,此方法制備簡單,節省原料,不僅可以實現定向聚合,使吡咯單體均勻地聚合生長在模板劑的各級孔隙結構中,而且可以通過調節催化劑的量對反應程度進行方便有效地控制,這樣既可以得到分布均勻的材料,又可以防止其他聚合方法中常見的孔道堵塞及表面團聚現象[5]。
本文采用模板法,以吡咯單體為原料,分子篩為模板劑,FeCl3為催化劑,根據不同碳源與模板劑的比例,通過氣相聚合法及模板法制得前驅體聚吡咯,再將其高溫碳化,最終制得氮摻雜多孔碳材料。
1 實 驗
1.1 樣品的制備
取1 g吡咯置于燒杯中,將1 mol/L的FeCl3與不同質量的分子篩(質量比為1∶0.5、1∶1、1∶3)在乙醇溶液中混合,另做一組不加FeCl3的對照組實驗,分別命名為Zeolites,ZPC-0.5,ZPC-1,ZPC-3。干燥后裝進漏斗,并將漏斗置于燒杯上,用保鮮膜將其封閉。將燒杯加熱至120 ℃,吡咯單體蒸氣蒸發于分子篩中生成碳前驅體。將碳前驅體在850 ℃條件下進行活化(升/降溫速度為5 ℃/min),然后經酸洗、醇洗后干燥12 h,并獲得最終樣品。
1.2 樣品的表征
采用掃描電鏡(S-3500型,日本日立公司)、透射電鏡(JEM2100F型,日本JEOL公司)和表面積及孔徑分析儀(3H-2000PS2型,北京貝士德儀器科技有限公司)表征NPCs的形貌、比表面積、孔徑分布以及N2吸附脫附等溫線,測定了CO2吸附脫附等溫線(298 K,0~0.1 MPa),通過X射線光電子能譜法(ESCALAB220i-XL,英國VG Scientific公司)測量了NPCs的氮含量。
2 結果與討論
2.1 形貌結構分析
從圖1可以觀察到,Zeolites呈顆粒狀,且形貌規則,而ZPC-0.5表面形貌呈集聚塊狀結構,且其塊狀結構表面具有大量內向凹陷的孔道結構,增大了其比表面積。圖1(c)中材料內部呈現出明顯的絮狀結構,黑色區域顆粒尺寸較大,圖1(d)中明暗相間,亮色區域是內部的孔隙,分布較均勻,暗色區域是碳壁,孔尺寸約為2 nm。


圖1 Zeolites和ZPC-0.5的SEM圖(a,b)及ZPC-0.5的TEM圖(c,d)
2.2 孔隙結構分析
為了研究材料的結構特征,探究其內部孔隙結構,將材料在77 K進行N2吸附脫附測試,材料的吸附等溫線如圖2所示,材料呈現出典型的第Ⅰ型吸附等溫線和第Ⅳ型吸附等溫線。相對壓力小于0.1時,吸附量迅速上升;相對壓力為0.1~0.5時,吸附等溫線出現平臺,證明所制備材料中有微孔存在;相對壓力在0.3~1.0時,發生毛細凝聚現象,吸附等溫線中出現滯后回環,表明材料存在一定量的介孔,在此吸附過程中存在多層吸附。可以得出,當碳源與模板劑的質量比增大時,對N2吸附性能增強,而其質量比過大時,吸附性能減弱,甚至不及分子篩本身的吸附性能[6-7]。
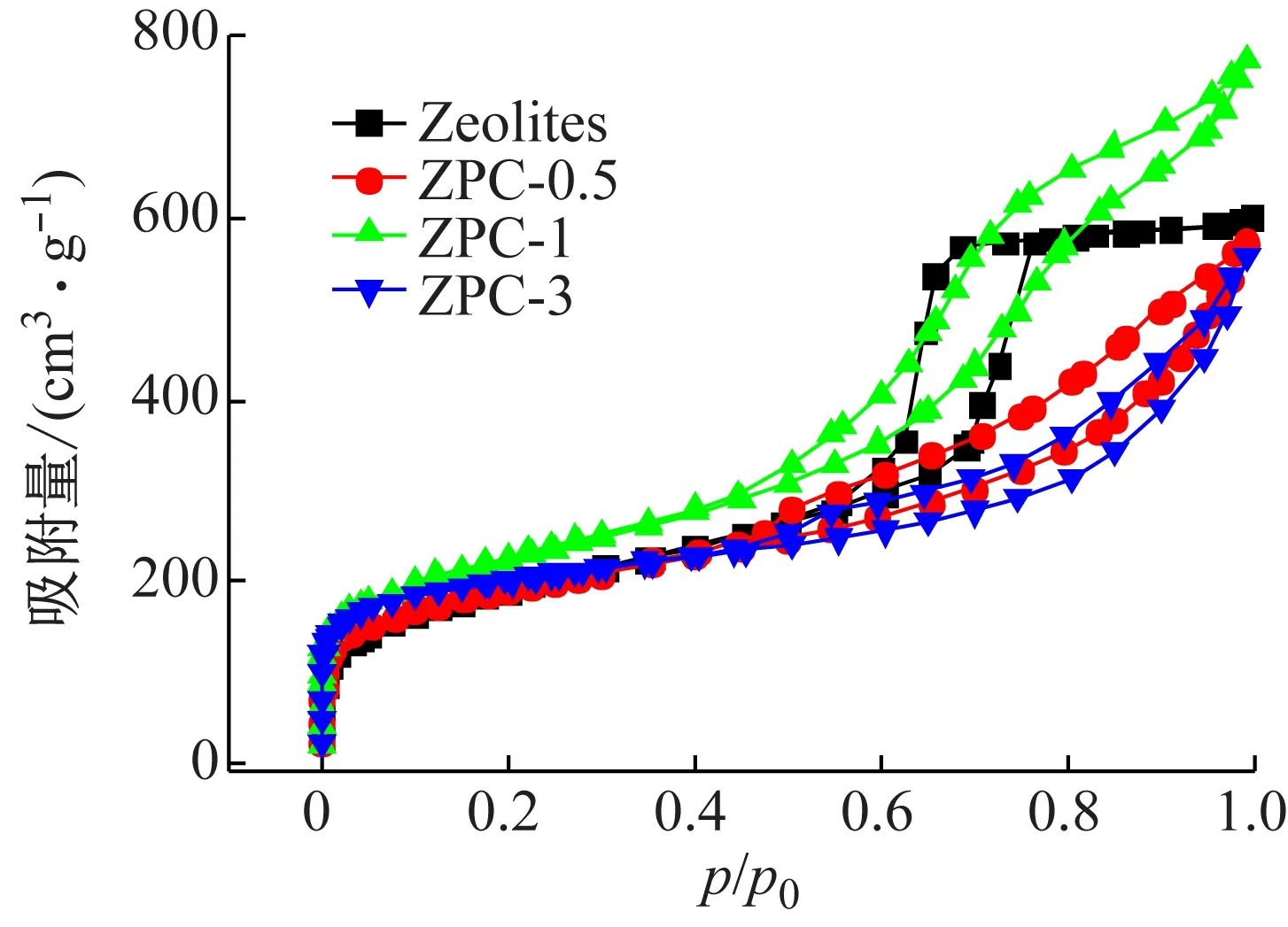
圖2 Zeolites和NPCs的N2吸附脫附等溫線
氮摻雜多孔碳材料的孔隙結構參數如表1所示。由表1可知,介孔孔容和總孔容在碳源與模板劑質量比為1∶1時分別達到最大值1.081 cm3/g和1.186 cm3/g,且介孔百分比也達到最大值91.1%,平均孔徑可達60.5 nm,材料擁有比模板劑更大的孔隙空間。相比于其他參數,微孔孔容隨碳源與模板劑質量比的逐漸增大呈現出不同的波動趨勢,即先減后增,并于ZPC-3達到最大值,說明催化劑的量有效控制了參與反應的碳前驅體的量[8]。
采用HK(Horvath Kawazoe)法和BJH(Barrett Joyner Halenda)法計算材料的微孔和介孔孔徑分布,如圖3所示。從圖中可以看出,材料的微孔孔徑分布主要是集中在0.5~0.7 nm之間的極微孔和小于1.3 nm的超微孔,孔徑大于0.8 nm時,材料的微孔分布含量均低于分子篩模板劑。如圖4所示,材料的介孔孔徑分布表明,模板劑的介孔集中在5.0~10 nm之間,ZPC-1的介孔主要分布于0.4~1.4 nm,ZPC-0.5和ZPC-3的分布趨勢相同[9-10]。
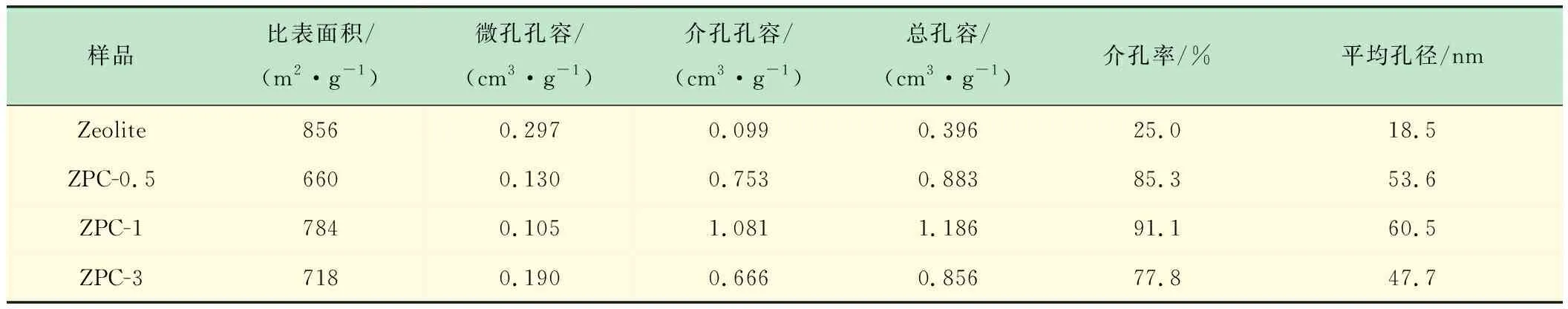
表1 Zeolites和NPCs的孔隙結構參數
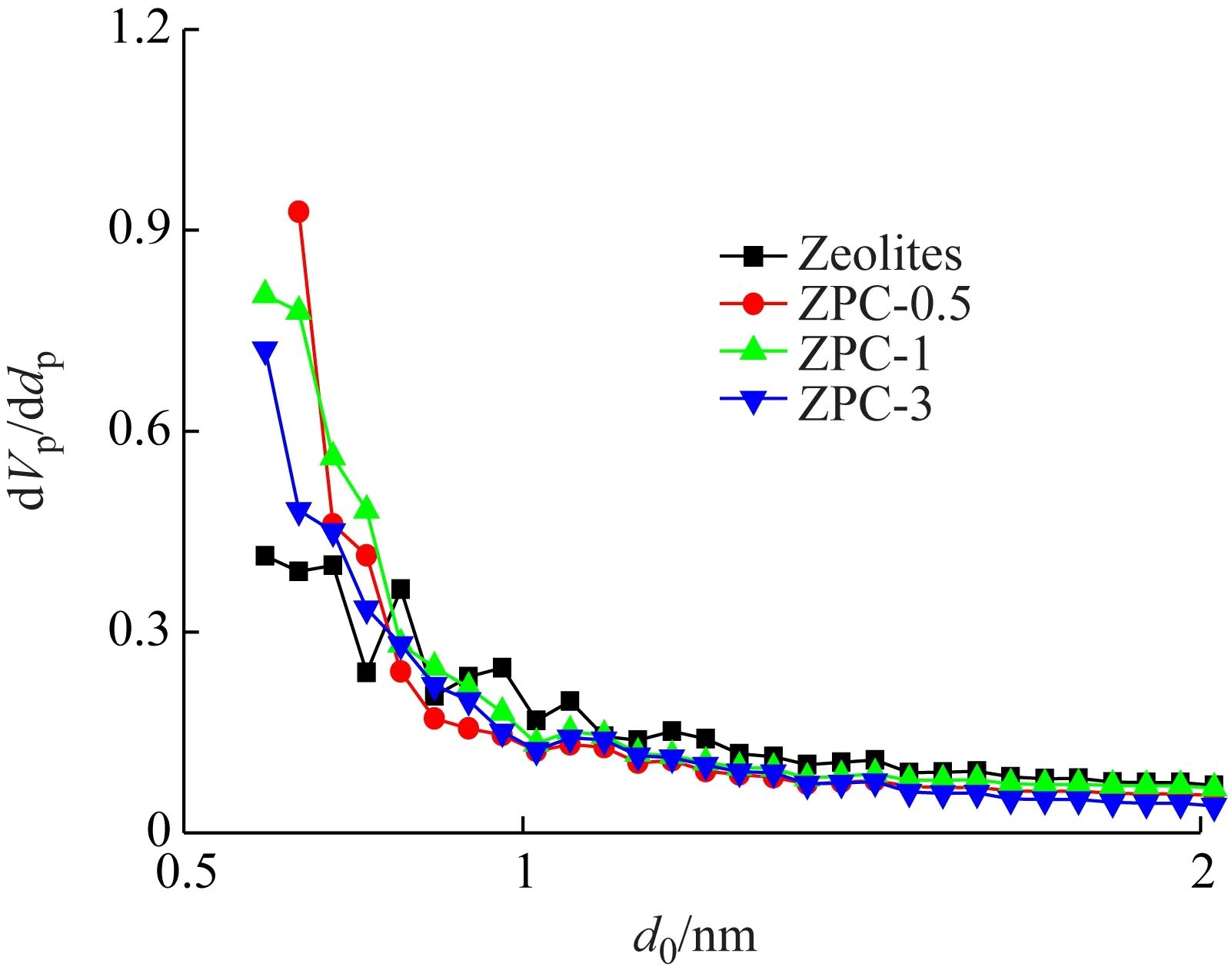
圖3 Zeolites和NPCs的微孔孔徑分布
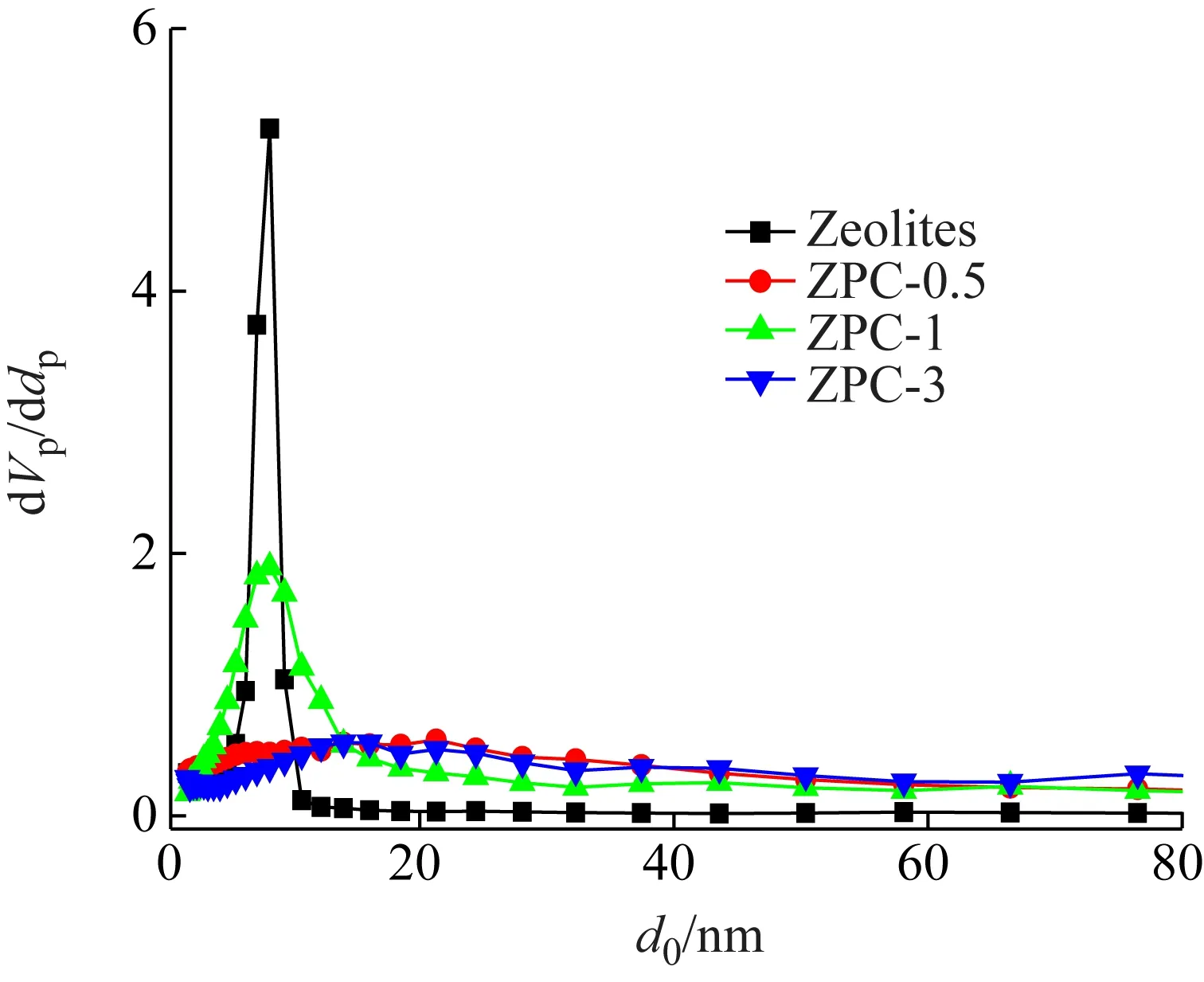
圖4 Zeolites和NPCs的介孔孔徑分布
2.3 CO2吸附性能表征
在298 K采用靜態吸附法進行CO2吸附脫附測試,如圖5所示。由圖5可見,所制備材料的吸附量隨著碳源與模板劑質量比的增大而減小,表明材料對CO2的吸附性能與兩者的用量比例呈線性關系,ZPC-0.5的CO2吸附量最高,吸附性能最好。ZPC-1的吸附量在吸附壓力小于70 kPa時高于Zeolites,ZPC-3的吸附量在吸附壓力小于20 kPa時高于Zeolites,這可能是由于所制備材料中的含氮堿基團與CO2有更強的相互作用力,導致其在低壓下的CO2吸附效果較好,而Zeolites在高壓下的較高吸附量說明超微孔與介孔的比例對CO2吸附性能有重要影響[11-12]。
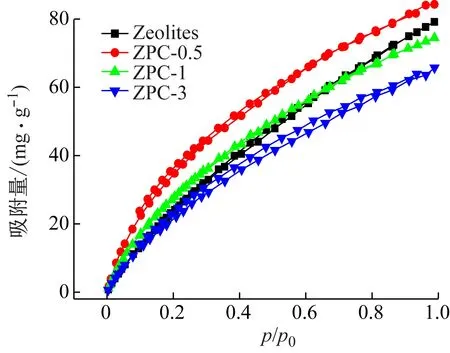
圖5 Zeolites和NPCs的CO2吸附脫附等溫線
2.4 XPS表征
圖6為NPCs(ZPC-0.5)的XPS N1s分峰結果。由圖可知,所制備的NPCs有4個N1s分峰,分別是398.15 eV處的吡啶型氮,400.55 eV處的吡咯型氮,401.69 eV處的石墨化氮以及403.40 eV處的氮氧化物,呈現出典型的吡咯基材料性質[13]。吡啶型氮以六元環的結構存在于NPCs表面,可提供一對未成鍵的孤對電子,使材料具有一定的堿性,吡咯型氮以五元環結構存在于NPCs表面,可為π系統提供p電子,對于小分子有一定的界面吸附力,但是相對吡啶型氮較弱[14]。吡啶型氮和吡咯型氮峰較高,使NPCs對CO2有較強的吸附選擇性。通過XPS測試和擬合計算,所制備樣品中的表面元素含量如表2所示。由表2可知,隨著分子篩與催化劑用量比的增大,碳含量下降,氮含量升高,說明催化劑用量的相對增多,對樣品的表面元素組成有很大影響。兩者質量比為0.5時,碳含量最多,NPCs石墨化程度較高,此時CO2吸附量也最多[15]。
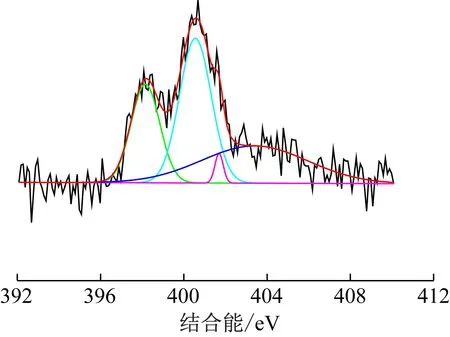
圖6 NPCs的N1s分峰
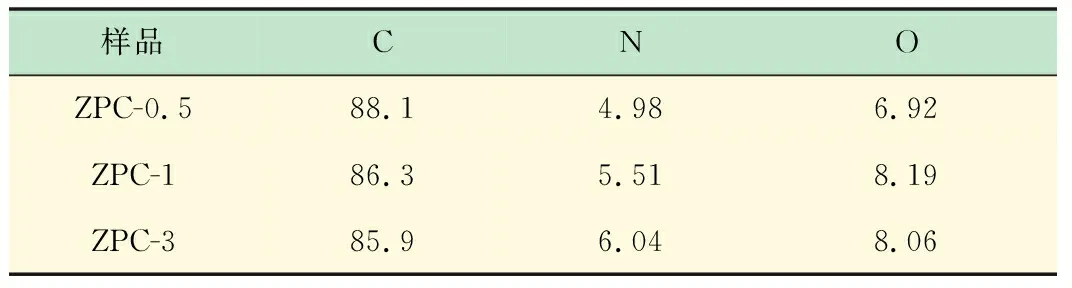
樣品CNOZPC-0.588.14.986.92ZPC-186.35.518.19ZPC-385.96.048.06
3 結 語
以吡咯為原料,分子篩為模板劑,FeCl3為催化劑,按照不同的碳源與模板劑質量比,通過模板法制得氮摻雜多孔碳材料,并對其CO2吸附性能進行了測試,分析討論不同的分子篩與聚吡咯的比例對材料的孔隙結構、孔徑分布、元素組成和CO2吸附量的關系。結果表明: 碳源與模板劑質量比對材料的比表面積、孔容、孔徑分布及對CO2的吸附能力等具有明顯的調節作用。當分子篩與聚吡咯的質量比為0.5時,所制備NPCs的比表面積為660 m2/g,平均孔徑為536 nm,總孔容為0.883 cm3/g,微孔孔容達0.130 cm3/g,材料的微孔中超微孔所占比例較大,對CO2的吸附能力最強。隨著碳源與模板劑質量比的減小,多孔碳的比表面積減小,超微孔的數目更多,對CO2的吸附性能較為優異。本研究所制備的NPCs,對于CO2捕集有著廣闊的應用前景。

