睪丸漿細胞瘤1例
李雙杰,黃后寶
(皖南醫學院弋磯山醫院泌尿外科,安徽 蕪湖 241001)
患者男,48歲,因“右側陰囊進行性增大2月余“于2016年10月10日入院。2013年7月患者因多發性骨髓瘤(D-SⅢ期B組,ISSⅡ期IgA-κ型)于我院行造血干細胞移植術,術后一般情況良好,口服地塞米松、沙利度胺維持治療。每3個月血液內科門診隨訪評估病情,疾病維持嚴格意義完全緩解(sCR)。2016年7月因右側睪丸鞘膜積液于外院行睪丸鞘膜翻轉術。入院前門診檢查:睪丸彩超:右側睪丸、附睪體積增大,回聲異常,提示多個鈣轉移灶形成。盆腔CT:(1)右側睪丸占位病灶,考慮為惡性腫瘤可能性大;(2)所及椎體、骨盆多發骨質異常,轉移瘤或骨髓瘤可能,見圖1。遂就診于我院泌尿外科。入院體格檢查:右側睪丸明顯增大,大小約6 cm×6 cm×4 cm,質硬,活動欠佳,與陰囊皮膚粘連,局部皮膚無紅腫,皮溫不高。左側睪丸未捫及異常,雙側附睪及精索未捫及明顯異常。尿常規:尿潛血(+)。血常規:紅細胞 3.91×1012/L,紅細胞壓積0.397,平均紅細胞體積101.7 fL,血紅蛋白133 g/L,白蛋白37.2 g/L。腹部B超:(1)肝臟輕度脂肪浸潤、肝臟右葉囊腫;(2)慢性膽囊炎;(3)脾臟多發性鈣化;(4)雙腎中盞結石。
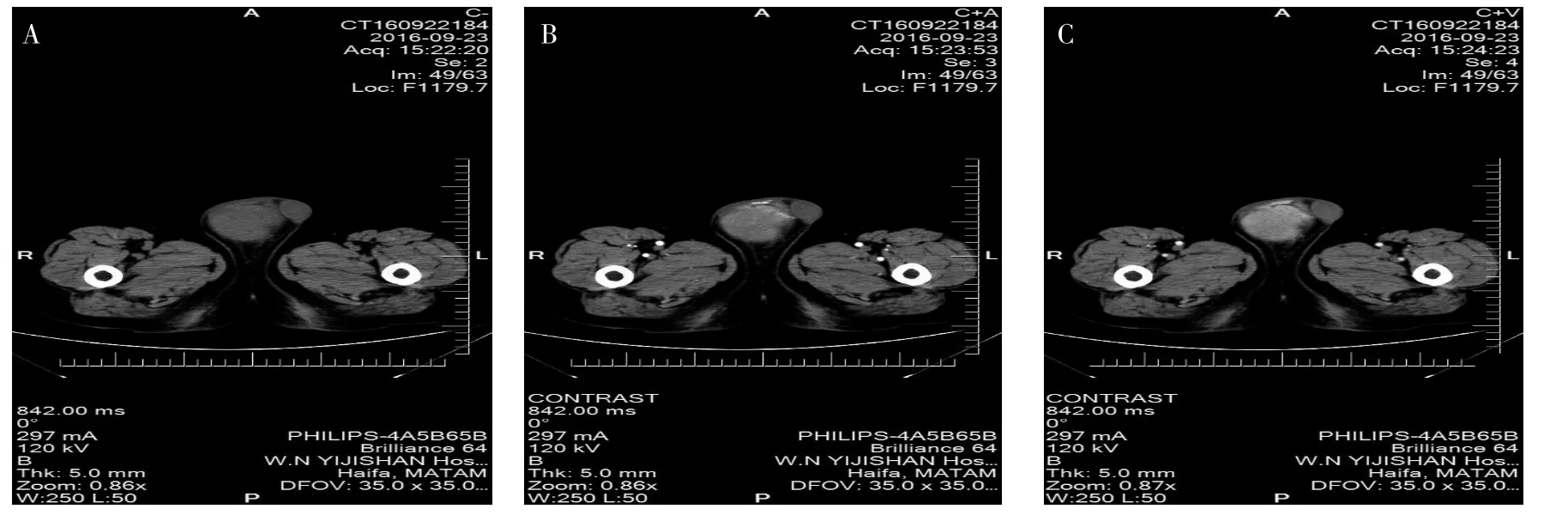
圖1 右側陰囊進行性增大患者的CT掃描結果
患者診斷為右側睪丸腫瘤,暫無明顯手術禁忌證。于2016年10月18日在腰麻下行右側睪丸腫瘤根治術。取右側腹股溝切口,術中見睪丸及鞘膜與周圍組織粘連明顯,部分與陰囊皮膚粘連,睪丸腫大,于鞘膜外游離,在睪丸底部切斷睪丸引帶,將粘連的部分陰囊皮膚切除后,并將右側陰囊內容物提出切口外。仔細止血后,陰囊底部放置引流皮片一條,逐層縫合切口及陰囊切口。手術順利,麻醉滿意,術后予以抗感染及對癥治療。標本行病理組織學檢查,結果顯示(右側睪丸)漿細胞瘤,請臨床結合病史,見圖2。免疫組化染色結果:瘤細胞 AE1/AE3(-)、EMA(-)、PLAP(-)、CD20(-)、CD79a(+)、Pax-5(-)、CD3(-)、CD43(-)、CD138(+)、CD38(+)、Mum-1(+)、bcl-2(+)、CD10(-)、bcl-6(-)、κ∶λ=3∶1、Ki-67(+):40%。復查骨髓象、免疫學等相關檢查發現異常漿細胞,CD138(+)、CD38(+)、CD56(+),提示多發性骨髓瘤復發。患者診斷為多發性骨髓瘤復發伴睪丸漿細胞瘤,術后定期于血液內科予以VAD(長春新堿、阿霉素、地塞米松)方案化療。在第二療程化療過程中,患者并發肺部重癥感染死亡。
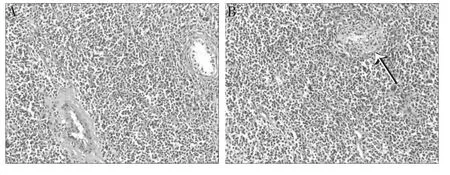
圖2 右側陰囊進行性增大患者手術切除組織HE染色(×100)
討論 漿細胞瘤是一種異常的漿細胞增殖,產生單克隆免疫球蛋白的血液病[1]。睪丸漿細胞瘤可為多發性骨髓瘤侵至睪丸或髓外漿細胞瘤原發于睪丸,亦有漿細胞白血病進展為睪丸漿細胞瘤的報道[2]。漿細胞瘤包括孤立性漿細胞瘤、髓外漿細胞瘤、多發性骨髓瘤、漿細胞性白血病 4類[3]。
多發性骨髓瘤是一種由單克隆漿細胞異常增生形成的惡性間葉組織腫瘤。原發病變主要在骨髓,瘤細胞也可廣泛浸潤其他組織器官,但睪丸受侵罕見。多發性骨髓瘤累及睪丸患者可有多發性骨髓瘤的典型臨床表現,如骨痛、貧血及出血傾向、感染、腎臟損害等[4]。多數睪丸漿細胞瘤以無痛性睪丸腫塊為首發表現[5],發生于睪丸的漿細胞瘤主要表現為陰囊的逐漸增大,睪丸內可觸及與睪丸相粘連的無痛性實性硬結[6]。本例患者即發現隨著時間的延長右側陰囊逐漸增大遂來就診。鑒于漿細胞瘤的臨床表現多樣性及不典型性,睪丸漿細胞瘤術前診斷較困難。詢問既往史尤為重要,對于有淋巴瘤、多發性骨髓瘤病史患者,發現睪丸腫塊,應考慮到睪丸漿細胞瘤的可能,本例患者有多發性骨髓瘤病史。
睪丸漿細胞瘤實驗室檢查結果通常無明顯異常,影像學檢查有特殊的價值。MRI具有較高的軟組織分辨率,可明確顯示病變范圍,充分了解病變與周圍組織關系,相對CT而言,更具優勢[7]。Salaun 等[8]研究發現相對于 MRI,PET-CT具有更高的靈敏性和特異性。任何睪丸漿細胞瘤,治療上首先行患側睪丸根治性切除術。睪丸漿細胞瘤主要依賴于術后病理組織學檢查,免疫組化染色結果常表達CD138(+)、CD38(+)。本例患者術前診斷為睪丸腫瘤,但術后病理提示睪丸漿細胞瘤。多發性骨髓瘤與髓外漿細胞瘤的鑒別診斷可以通過血常規、骨骼的檢查、血清蛋白電泳實驗、尿本周蛋白測定、骨髓穿刺等[3]。本例患者術前已明確診斷為多發性骨髓瘤并已行造血干細胞移植術,且睪丸切除術后復查相關指標提示多發性骨髓瘤臨床復發,可排除髓外漿細胞瘤的診斷。漿細胞瘤累及睪丸者術后需行化療,常用美法侖加潑尼松的MP方案。患者由于經濟原因,未采用MP方案,經血液內科調整,使用VAD方案。隨著聯合化療的應用,多發性骨髓瘤的存活時間已延長至平均3年以上。預后與臨床分期密切相關。在免疫分型中,IgG及IgA型預后較好,IgD型、輕鏈型預后差,平均生存期約1年[4]。此外,這些腫瘤對放射線高度敏感,放療可以達到很好的局部控制,可行手術與放療聯合治療。睪丸漿細胞瘤患者的總體預后差,因此長期密切隨訪觀察很有必要。

