亨氏馬尾藻醇提取物體內降血脂及抗氧化作用
,,,,,,,,,,*,
(1.廣州工商學院物流系,廣東廣州 510000; 2.廣東海洋大學食品科技學院,廣東湛江 524088; 3.廣東省水產品加工與安全重點實驗室,廣東湛江 524088; 4.廣東普通高等學校水產品深加工重點實驗室,廣東湛江 524088; 5.泉州師范學院福建省海洋藻類活性物質制備與功能開發重點實驗室,福建泉州 362000)
近年來,隨著人們生活模式的改變,飲食精細、運動少、生活及工作的壓力等因素導致高血脂癥患者急劇上升。大量研究[1-2]表明高血脂癥會導致動脈粥樣硬化,從而促發高血壓、冠心病、腦血栓、糖尿病等多種疾病,是心血管疾病的主要誘因。高血脂癥主要表現為血漿或血清中總膽固醇(TC)和低密度脂蛋白含量(LDL-C)升高和(或)甘油三酯(TG)含量增高,高密度脂蛋白含量(HDL-C)下降。目前,一些藥物可以有效調節血脂代謝,降低血脂水平,但存在不同程度的毒副作用,不適合長期服用。因此,尋找無毒高效的降血脂天然成分極為必要。
研究表明很多海藻如海帶、龍須菜等均有降血脂的功效[3-6]。隨著對南海海洋資源的開發,資源極為豐富的馬尾藻受到極大的關注。亨氏馬尾藻(SargassumhenslowianumC.Agardh)作為一種生長在南海海域的大型經濟褐藻,化學成分豐富且擁有多種生物活性。研究發現馬尾藻中多種成分具有降血脂、抗氧化、抗菌等作用[7-10],如諶素華等[11]的研究表明亨氏馬尾巖藻聚糖硫酸酯具有顯著的降血脂功能。由于馬尾藻中含有豐富的有效成分如多糖、多不飽和脂肪酸、多酚、甾醇、類胡蘿卜素等等,不同的成分結構和活性特點不同,可能存在協同或互補作用。亨氏馬尾藻除了含有多糖外,還含有豐富的其他次生產物,目前已有研究對這些次生產物進行了分離和純化及結構表征,但對這些成分的活性尚未展開較為系統的研究。
Triton WR-1339作為一種表面活化劑,注射一定劑量后能夠使小鼠血清TC、TG及LDL-C明顯上升,誘發急性高血脂癥,該模型具有操作簡便、藥效明顯快速的特點,因此被廣泛應用于篩選天然或者合成的降血脂藥物[12-16]。
本研究利用Triton WR-1339誘導建立急性高血脂小鼠模型研究亨氏馬尾藻醇提取物對動物血清及肝臟脂質水平的影響,評價其體內抗氧化作用,探討其降血脂、抗氧化作用和動脈粥樣硬化之間的關系,為亨氏馬尾藻的活性成分研究和開發提供理論基礎。
1 材料與方法
1.1 材料與儀器
亨氏馬尾藻 2016年5月采自廣東湛江硇洲島,洗凈風干,粉碎過60目篩,-20 ℃儲藏備用;SPF級昆明雄性小鼠,48只,體重(20±2) g,南方醫科大學大學動物實驗中心,許可證編號:SCXK(粵)2013-0034;動物飼料 廣東醫學院動物實驗中心;Triton WR-1339 廣州小木蟲生物科技有限公司;BCA蛋白測定試劑盒、總膽固醇檢測試劑盒、甘油三酯檢測試劑盒、高密度脂蛋白膽固醇測試盒、低密度脂蛋白膽固醇測試盒、總脂酶(LPL)測試盒、超氧化物歧化酶(SOD)測試盒、丙二醛(MDA)測試盒、過氧化氫酶(CAT)測試盒、總抗氧化能力(T-AOC)測試盒 南京建成生物工程研究所。
RT-34粉碎機 榮聰精密科技有限公司;N-1000V-W旋轉蒸發儀 日本EYELA公司;UV2550紫外分光光度計 日本島津公司;Varioskan Flash全自動酶標儀、微量移液器 均為美國Themo公司;CR22G高速冷凍離心機 日本Hitachi公司;Alphal-4真空冷凍干燥機 德國Christ公司;7000全自動生化分析儀 日本日立。
1.2 實驗方法
1.2.1 亨氏馬尾藻粗提物的制備 亨氏馬尾藻粉用95%乙醇按料液比1∶10進行室溫浸泡,室溫振蕩提取3次,提取時間依次為12、24、48 h,減壓抽濾,棄去濾渣,合并濾液,減壓濃縮(濃縮溫度42 ℃,濃縮壓力0 MPa),-52 ℃真空冷凍干燥24 h,得到亨氏馬尾藻提取物,用超純水配制稀釋至所需濃度樣品,進行給藥[17]。
1.2.2 動物分組及處理 基礎性飼料喂養,室溫(23±2) ℃,濕度40%~70%,12 h光照/黑暗交替。試驗前,飼養5 d以適應環境,自由采食,飲水。隨后隨機[18]分成4組:分別編號為正常組,高脂模型組,亨氏馬尾藻提取物低、高劑量組,每組12只。按參考文獻[14-15]方法,每天晚上7點進行灌胃,亨氏馬尾藻提取物低、高劑量組每天按照250、500 mg/kg分別灌胃亨氏馬尾藻提取物,正常組和高脂模型組給予等體積蒸餾水,灌胃體積均為10 mL/kg,試驗期間,各組小鼠自由采食,飲水。連續給藥12 d,末次給藥前18 h,除正常組尾靜脈注射等體積生理鹽水外,其余各組均以350 mg/kg的劑量尾靜脈注射Triton WR-1339,禁食不禁水。末次給藥1 h后,眼球取血,室溫靜置2 h,3000 r/min離心15 min分離血清,血清放于4 ℃保存,同時摘取肝臟用生理鹽水洗凈,濾干,稱重,于-80 ℃保存,備用。
1.2.3 檢測指標和方法
1.2.3.1 體重和肝臟指數 每隔6 d同一時間稱重一次,記錄小鼠體重的變化。肝臟指數按照肝臟指數=肝臟重量/體重×100進行計算。初重:連續給藥的第1 d小鼠重量。
1.2.3.2 血清血脂的測定 取血清測定TC、TG、LDL-C、HDL-C。所有測定均按照相應試劑盒測試說明在全自動生化分析儀上完成。按公式AI1=(TC-HDL-C)/HDL-C和AI2=LDL-C/HDL-C計算動脈粥樣硬化指數[19]。
1.2.3.3 肝組織勻漿液的制備及其蛋白的測定 稱取肝臟組織,按重量(g)∶體積(mL)=1∶9的比例,加入9倍體積的生理鹽水,冰水浴條件下勻漿,2500 r/min離心15 min,棄去沉淀得上清液即得到10%肝組織勻漿液,分裝,-80 ℃保存備用。
肝組織勻漿蛋白含量按照BCA法蛋白測定試劑盒進行測定。
1.2.3.4 肝勻漿脂質的測定 取10%肝組織勻漿液測定TC、TG、LDL-C、HDL-C。所有測定均按照相應試劑盒測試說明在全自動生化分析儀上完成。
1.2.3.5 肝勻漿脂蛋白脂酶(LPL)的測定 按照試劑盒說明以比色法進行測定。定義每毫克組織蛋白每小時在反應系統中所產生的1 μmol的游離脂肪酸為一個酶活性單位(FFAμmol/mg prot·h)。
1.2.3.6 肝勻漿抗氧化指標的測定 抗氧化能力(T-AOC)按照試劑盒說明以比色法進行測定。按照試劑盒說明進行測定。定義為在37 ℃時,每分鐘每毫克組織蛋白使反應體系的吸光度值升高,每增加0.01時,為一個總抗氧化能力單位。
過氧化氫酶(CAT)按照試劑盒說明以比色法進行測定。定義每毫克組織蛋白每秒鐘分解1 μmol 的H2O的量為一個活力單位。
超氧化物歧化酶(SOD)按照試劑盒說明進行測定。定義每毫克組織蛋白SOD抑制率達到50%時所對應的酶量為一個SOD活力單位(U)。
丙二醛按照試劑盒說明以TBA法進行測定。
其中,測定中所需要的肝組織勻漿液組織蛋白含量按照1.2.3.3測定的結果。
1.3 數據處理
采用JMP10.0軟件進行統計分析,采用t檢驗進行組間差異性分析,結果表示為平均值±標準差,p<0.05表示存在顯著差異性。
2 結果與分析
2.1 小鼠體重變化及肝臟指數
在實驗期間,各組別小鼠的體重均呈增長的趨勢,但是各組間小鼠體重無顯著性差異(表1),說明亨氏馬尾藻提取物沒有明顯影響小鼠的正常生理代謝和生長。高脂模型與正常對照組相比,肝臟指數有顯著差異性,而亨氏馬尾藻提取物低劑量組和高劑量組與正常對照組相比肝臟指數均無顯著差異性(表1),因此,亨氏馬尾藻提取物對小鼠肝臟的正常代謝影響不顯著,也表明實驗小鼠能夠適應此兩種劑量的亨氏馬尾藻提取物給藥處理。

表1 不同組別小鼠試驗期間體重的變化以及肝臟指數Table 1 Effect of S.henslowianum extract on body weight and liver index of mice with hyperlipidemia
2.2 亨氏馬尾藻提取物對小鼠血清脂質水平和動脈粥樣硬化指數的影響
與正常對照組相比,高脂模型組血清中TC、LDL-C含量均顯著升高,HDL-C顯著降低,TG含量雖有一定的升高,但并無顯著性差異,依然可以認為Triton WR-1339誘發的小鼠急性高脂血癥模型成功(表2)。與高脂模型組相比,亨氏馬尾藻提取物低劑量組小鼠血清TC含量顯著下降。低、高劑量組TG分別下降12.61%和7.14%,低劑量組TG接近正常水平,各組間無顯著差異。低、高劑量組的HDL-C均高于模型組,但僅高劑量組有顯著差異。低、高劑量組LDL-C水平明顯下降,均顯著低于模型組。
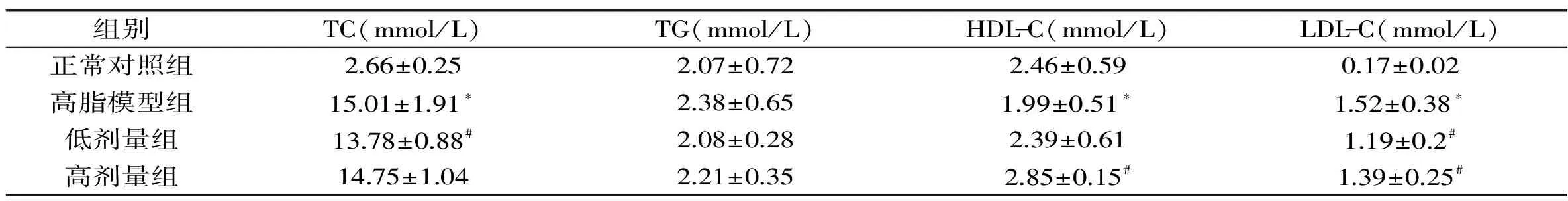
表2 亨氏馬尾藻提取物對試驗小鼠血清脂質水平的影響Table 2 Effect of S.henslowianum extract on serum lipid of mice with hyperlipidemia
醫學上常用動脈粥樣硬化指數AI1和AI2反應動脈硬化的嚴重程度。與正常對照組相比,高脂模型組的動脈粥樣硬化指數AI1和AI2顯著升高(表3)。亨氏馬尾藻提取物低劑量和高劑量處理組中,與高脂模型組相比AI1和AI2均呈顯著下降趨勢,其中,AI1分別下降了27.01%和33.02%,AI2分別下降了37.18%和42.31%。因此,亨氏馬尾藻提取物可能具有潛在降低動脈粥樣硬化的功效。
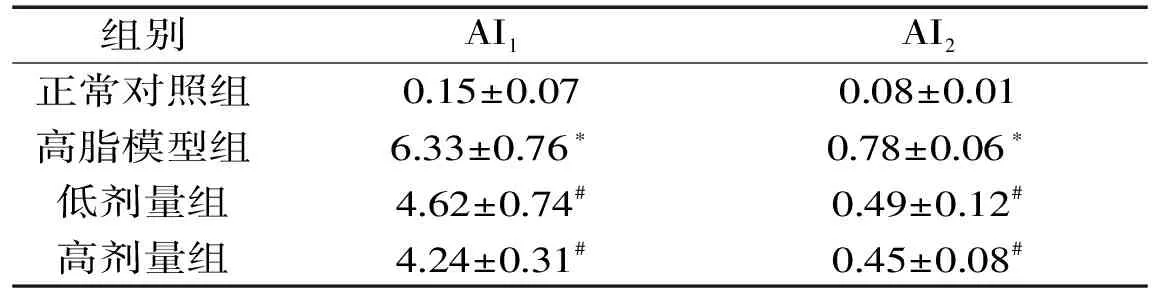
表3 亨氏馬尾藻提取物對試驗小鼠動脈粥樣硬化指數的影響Table 3 Effect of S.henslowianum extract on atherosclerosis index of mice with hyperlipidemia
2.3 亨氏馬尾藻提取物對小鼠肝臟脂質水平及脂蛋白脂酶活性的影響
為了進一步考查實驗動物體內的脂肪代謝情況,對小鼠肝臟中的脂質水平進行了檢測,結果表明(表4),各組小鼠的TC雖無明顯變化,但與模型組相比,亨氏馬尾藻提取物低劑量處理組的TG、LDL-C及高劑量處理組的TG含量顯著下降(p<0.05),高劑量處理組的LDL-C有所下降,但并不顯著,其中TG分別下降了19.53%和15.81%,LDL-C分別下降了17.39%和8.70%。

表4 亨氏馬尾藻提取物對試驗小鼠肝臟脂質水平以及脂蛋白脂酶活性的影響Table 4 Effect of S.henslowianum extract on hepatic lipid and LPL activity of mice with hyperlipidemia

表5 亨氏馬尾藻提取物對小鼠肝臟的抗氧化作用Table 5 Effect of S.henslowianum extract on hepatic antioxidant status of mice with hyperlipidemia
LPL主要是催化TG水解,在乳糜微粒(CM)和極低密度脂蛋白(VLDL)的降解中發揮重要作用。瞿羽佳等[12]通過研究指出Triton WR-1339誘發的急性高血脂模型可能與LPL活力有關系。本研究結果顯示,低劑量組和高劑量組的LPL活力均高于模型組,其中低劑量組變化尤其顯著,推測亨氏馬尾藻提取物的降脂活性可能與增強LPL活性有關。
2.4 亨氏馬尾藻提取物對高血脂癥小鼠肝臟的抗氧化作用
與正常對照組相比,高脂誘導后小鼠肝臟中的T-AOC、CAT活力顯著降低,MDA含量顯著上升,SOD也有一定程度的下降,但不顯著,說明Triton WR-1339誘導的急性高血脂會并發體內氧化-還原系統失衡。與高脂模型組相比,低劑量組和高劑量組的T-AOC均增加,其中低劑量組可達到正常對照組水平相當;低劑量和高劑量組的CAT活力顯著高于模型組,同時MDA含量也顯著低于模型組,分別減少34.74%和28.82%,SOD活力高于正常組和模型組,但無顯著差異性。這些指標水平顯示出與劑量存一定的相關性,即低劑量組對肝臟氧化還原系統的作用優于高劑量組。
血脂含量的高低與人體健康密切相關,高血脂癥是血脂代謝異常所導致,主要表現為血漿中TC、TG和LDL-C水平過高或HDL-C過低。HDL-C將其它器官中積累過多的膽固醇運送到肝臟進行分解,而LDL-C則將肝臟合成的膽固醇轉運至全身其它器官和組織,LDL-C過高,將會引起膽固醇在血管壁上的沉積[20-21]。有研究報道,張氏馬尾藻、鼠尾藻、羊棲菜等馬尾藻提取物[22-25]具有顯著的降血脂作用。其中,與高脂模型組對比,羊棲菜治療組的高脂大鼠血清中LDL-C降低23.14%,HDL-C上升43.33%,肝臟組織勻漿LPL酶活力增強46.08%[24],海帶治療組中TG、TC分別下降46.99%、25.91%[4]。本研究結果中與高脂模型組對比,灌胃亨氏馬尾藻提取物后的高脂小鼠血清LDL-C降低21.71%,HDL-C上升30.18%,TG、TC分別下降12.61%、8.19%,肝臟組織勻漿LPL酶活力增強21.82%。雖然亨氏馬尾藻的降血脂效果低于羊棲菜和海帶,但是和灌胃方式及提取方法的不同可能存在一定的關系。文中研究結果表明亨氏馬尾藻醇提取物仍能有效緩解脂質代謝紊亂造成脂質在體內的沉積。
盡管尚未確切清楚高血脂癥與脂質過氧化之間的機制,但是研究表明兩者間關系密切,高血脂癥引發機體體內氧化-還原系統失衡。近年來,大量的體內外實驗和臨床醫學研究證明抗氧化劑對防治高血脂癥引起的動脈粥樣硬化有確切作用[2,25]。抗氧化體系可分為酶促與非酶促體系,酶類抗氧化體系主要由SOD、CAT等內源性抗氧化酶組成,非酶抗氧化劑主要為VE、天然化合物(酚類等)等。內源性抗氧化酶可以抑制脂質發生過氧化作用,從而抑制多余脂質蓄積在血管內,有效防止動脈硬化。MDA是脂質過氧化產物,能引起細胞損傷,測定其含量可以反映機體內脂質過氧化以及細胞受損程度。本研究結果表明,高血脂癥模型SOD、CAT活力以及總抗氧化能力降低,可能是由于注射Triton WR-1339導致機體血脂升高并發生自氧化,產生過量自由基,破壞機體自由基產生和清除的平衡系統,引起機體氧化應激反應,從而降低酶活力。灌胃亨氏馬尾藻提取物后,CAT、SOD酶活力升高,總抗氧化能力增強,同時MDA含量顯著下降,有效防治高血脂引起的脂質過氧化,促進機體內系統平衡,而且低劑量組對肝臟氧化還原系統的作用優于高劑量組。
3 結論
本研究結果表明亨氏馬尾藻醇提取物能夠顯著降低高脂血癥小鼠體內TC、TG、LDL-C,而使HDL-C以及LPL活力顯著增加,顯著改善小鼠動脈粥樣硬化指數AI1和AI2;同時,增強小鼠肝臟T-AOC和CAT活力,而使MDA水平顯著降低,說明亨氏馬尾藻醇提取物能有效降低高血脂水平,增強抗氧化能力,為亨氏馬尾藻在降血脂和抗氧化性能方面的開發應用提供理論依據。

