糖尿病腎病患者血清25羥維生素D3水平變化及與TNF-α、IL-6關系分析
左湘川,胡淑芳,榮太梓
(1. 江漢大學文理學院,湖北 武漢 430000;2. 湖北省武漢市漢口醫院,湖北 武漢 430000)
糖尿病腎病為糖尿病患者微血管并發癥之一,是造成終末期腎臟病的主要原因。糖尿病腎病初始臨床特征為腎小管上皮細胞及腎小球肥大,腎小管基底膜一定程度增厚,隨病情進展可出現高濾過以及微量白蛋白尿,進而出現蛋白尿、腎小管間質纖維化以及腎小球硬化等,最終造成終末期腎臟病[1-2]。糖尿病腎病發病機制尚未完全明確,與氧化應激、炎癥反應、細胞因子、血流動力學異常改變以及遺傳易感性有關[3]。近年來的相關研究指出,對于胰島細胞,維生素D具有一定保護作用,維生素D濃度降低可能是造成機體糖耐量異常以及糖尿病及其并發癥發生發展的重要原因[4]。25羥維生素D3[25-(OH)D3]反映了體內活性維生素D的含量,通過測定25-(OH)D3值可以了解機體維生素D水平[5]。本研究分析了糖尿病腎病患者血清25-(OH)D3水平變化情況及其與腫瘤壞死因子-α(TNF-α)、白細胞介素-6(IL-6)、腎功能的關系,旨在為2型糖尿病腎病早期監控及嚴重程度評估提供參考依據,現報道如下。
1 臨床資料
1.1一般資料 收集2015年1月—2017年8月武漢市漢口醫院收治的2型糖尿病患者106例(病例組),均符合《中國2型糖尿病防治指南(2010年版)》[6]中的診斷標準。入選標準:①患者血壓正常,即<140/90 mmHg(1 mmHg=0.133 kPa);②無腎動脈狹窄;③入組前1個月內未使用過明顯影響腎功能的藥物或者腎毒性藥物;④均為原發性2型糖尿病。排除標準:①存在高鉀血癥、原發性腎小球腎炎、糖尿病酮癥及尿路梗阻者或者其他原發、繼發腎臟疾病者;②心、肝功能異常者;③合并感染、過敏、白血病或惡性腫瘤者;④其他原因導致的腎臟疾病者。根據106例患者的尿蛋白排泄率(UAER)分為單純糖尿病組(UAER<20 μg/min)、早期糖尿病腎病組(UAER 20~200 μg/min)、臨床期糖尿病腎病組(UAER>200 μg/min)。糖尿病組34例,男19例,女15例;年齡39~78(52.86±9.61)歲。早期糖尿病腎病組37例,男23例,女14例;年齡37~76(53.04±9.78)歲。臨床期糖尿病腎病組35例,男19例,女16例;年齡36~78(52.49±9.83)歲。另選取健康體檢者35例作為對照組,血糖、血壓、血脂、心肝腎功能、血常規等均正常,其中男20例,女15例;年齡35~79(53.29±10.16)歲。4組受試者年齡、性別比較差異均無統計學意義(P均>0.05)。
1.2方法 于入院第2天清晨抽取空腹靜脈血5mL,對照組于體檢之前采血,行EDTA抗凝,以3 500 r/min離心,離心5 min后提取血清,放置于-20 ℃冰箱中保存待檢;通過日立7170A型全自動生化分析儀檢測血尿素氮(BUN)、血肌酐(SCr);通過酶聯免疫吸附法檢測TNF-α、IL-6水平,通過放射免疫法檢測UAER,檢測試劑盒由北京北大維信生物科技有限公司生產,嚴格按照說明書進行檢測;通過電化學發光免疫法測定25-(OH)D3值,瑞士羅氏公司生產的Cobas8000E602型全自動電化學發光免疫分析儀,配套試劑購自羅氏公司,嚴格按照試劑盒說明書進行操作。
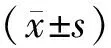
2 結 果
2.1病例組與對照組血清25-(OH)D3、TNF-α、IL-6及腎功能指標比較 病例組血清TNF-α、IL-6、SCr、BUN及UAER均明顯高于對照組(P均<0.05),血清25-(OH)D3明顯低于對照組(P<0.05)。見表1。
2.2患者組間血清25-(OH)D3、TNF-α、IL-6及腎功能指標比較 早期糖尿病腎病組、臨床期糖尿病腎病組血清TNF-α、IL-6、SCr、BUN均明顯高于單純糖尿病組(P均<0.05),血清25-(OH)D3均明顯低于單純糖尿病組(P均<0.05);臨床期糖尿病腎病組血清TNF-α、IL-6、SCr、BUN均明顯高于早期糖尿病腎病組(P均<0.05),血清25-(OH)D3明顯低于早期糖尿病腎病組(P<0.05)。見表2。

表1 病例組與對照組血清25-(OH)D3、TNF-α、IL-6及腎功能指標比較
2.325-(OH)D3與TNF-α、IL-6及腎功能指標相關性分析 Pearson相關分析結果顯示,25-(OH)D3與TNF-α、IL-6及腎功能指標均呈顯著負相關性(r<0,P均<0.05)。見表3。
2.42型糖尿病腎病多因素Logistic回歸分析 將2型糖尿病腎病作為因變量,將TNF-α、IL-6、25-(OH)D3作為自變量,進行多因素Logistic回歸分析,結果顯示,TNF-α、IL-6、25-(OH)D3為2型糖尿病腎病發生的影響因素(P均<0.05)。見表4。
3 討 論
臨床研究顯示,大約35%的2型糖尿病患者會發生糖尿病腎病,且隨病程延長呈進行性發展,約有70%的2型糖尿病腎病患者會在15~20年內發展為終末期腎病[7]。目前,UAER值為糖尿病腎病患者病情分期的主要標準,不過近年來亦有學者通過尿白蛋白/尿肌酐的比值對2型糖尿病早期腎臟損傷進行評估,具有一定臨床價值。2型糖尿病腎病發病機制比較復雜,目前對于該病發病機制臨床尚不夠明確。
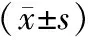
表2 不同病情糖尿病患者血清25-(OH)D3、TNF-α、IL-6及腎功能指標比較
注:①與單純糖尿病組比較,P<0.05;②與早期糖尿病腎病組比較,P<0.05。

表3 25-(OH)D3與TNF-α、IL-6及腎功能指標相關性分析
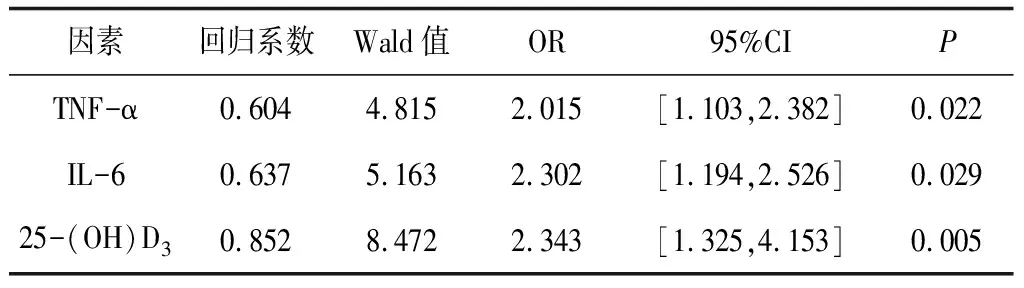
表4 2型糖尿病腎病多因素Logistic回歸分析
臨床研究指出,凝血功能障礙、炎癥反應、免疫功能紊亂等在糖尿病腎病的發生及病理損害過程中起到了重要作用[8]。免疫功能紊亂會造成腎臟內炎癥細胞的浸潤,增加了多種炎癥因子的分泌,促使腎臟固有的細胞尤其系膜細胞增生的發生,使得腎內微血管和固有細胞受到損害,造成凝血障礙,進而引起細胞外基質聚積,最終造成腎間質纖維化和腎小球硬化。人體內部有許多種細胞能夠分泌TNF-α,腎臟的固有細胞也可以分泌TNF-α,而TNF-α能夠對腎小管的內皮細胞造成損害,導致細胞外基質的分泌增多和沉積,并減少細胞外基質的降解,導致腎間質纖維化[9]。IL-6為有多種生物活性的炎癥細胞因子,高水平的IL-6可促進腎小球系膜細胞增殖,從而導致細胞外基質合成增加和聚積[10]。因此,減輕2型糖尿病腎病患者體內炎癥反應,促進細胞外基質的降解,并抑制其聚積,對改善患者腎臟病理損害具有重要意義。
維生素D對促進人體的骨骼生長發育具有重要作用,維生素D不足或者缺乏會導致骨骼生長發育緩慢或者異常;還可能導致慢性肝病、慢性腎病、慢性阻塞性肺疾病等慢性疾病的發生[11-12]。近年來的研究指出,慢性炎癥反應以及維生素D缺乏共同參與了2型糖尿病以及2型糖尿病腎病發生過程[13]。25-(OH)D3為維生素D代謝中間產物,血中穩定性好,半衰期長,為評估維生素D的有效指標。本研究中,2型糖尿病患者血清25-(OH)D3水平明顯低于健康人群;而且不同病情程度患者之間血清25-(OH)D3水平存在明顯差異,臨床期糖尿病腎病患者血清25-(OH)D3均明顯低于早期糖尿病腎病和單純糖尿病患者,提示25-(OH)D3在2型糖尿病腎病發生及發展過程中起到了重要促進作用。
本研究中,通過對IL-6和TNF-α的研究發現,2型糖尿病患者血清IL-6和TNF-α水平均明顯高于健康人群,而且臨床期糖尿病腎病患者血清IL-6和TNF-α水平均明顯高于早期糖尿病腎病患者和單純糖尿病患者;通過相關性分析發現,IL-6和TNF-α均與25-(OH)D3呈顯著負相關;多因素Logistic回歸分析結果顯示,TNF-α、IL-6、25-(OH)D3為2型糖尿病腎病發生的影響因素。研究結果提示,維生素D缺乏通過對IL-6和TNF-α等相關炎性因子的影響作用于2型糖尿病患者的腎臟,進而影響患者腎臟出現病理改變,最終導致腎臟損害的發生。近年來研究顯示,在2型糖尿病腎病患者治療中加用維生素D具有一定療效,通過補充維生素D,可降低24 h尿蛋白定量以及超敏C反應蛋白、高密度脂蛋白水平[14-16]。亦有研究指出,1,25二羥維生素D3可抑制TNF-α、IL-1等炎性因子分泌,減輕腎小球損害,進而保護患者腎功能[17-18]。因此,監測血清25-(OH)D3水平對于2型糖尿病腎病患者防治具有重要意義。
綜上所述,2型糖尿病腎病患者血清炎性因子水平明顯升高,血清25-(OH)D3明顯降低,且與炎癥反應及腎功能密切相關,可作為2型糖尿病患者腎臟損害早期檢查以及病情嚴重程度評估的重要指標。在隨后的研究中,應積極開展大樣本多中心研究,進一步研究證實。

