pOsHistone3啟動子在煙草中的表達特性分析
胡明瑜 白文欽 潘曉雪 吳紅 雷開榮
摘 ? 要 ? 啟動子在基因表達調控中發揮重要作用,分析啟動子表達特性對于基因功能研究和啟動子的開發利用有重要意義。本研究克隆了水稻組蛋白基因OsHistone3的啟動子pOsHistone3,在PlantCARE中分析顯示包含脫落酸、茉莉酸甲酯等生長調節劑信號應答元件和胚乳、莖尖、分生組織等部位特異表達元件。進一步構建啟動子分析載體并對煙草作遺傳轉化,GUS染色分析顯示,pOsHistone3在轉基因煙草幼嫩組織如莖尖、嫩葉中GUS活性較高,而在成熟組織中僅在維管組織周圍檢測到GUS活性,說明pOsHistone3具有組織表達特異性。這些結果初步表明OsHistone3基因作為表觀遺傳調控的一個重要基因,可能在轉錄水平參與了植物生長調節劑信號和植株發育調控的過程。
關鍵詞 ? 水稻;煙草;組蛋白;OsHistone3;植物生長調節劑;表達特性
中圖分類號:S572;Q78 ? ?文獻標志碼:A ? ?DOI:10.19415/j.cnki.1673-890x.2019.34.003
表觀遺傳調控在植物生長發育和適應環境的過程中發揮重要作用[1]。組蛋白修飾如組蛋白乙酰化、甲基化和泛素化等是表觀遺傳調控的方式之一。已有研究表明,組蛋白Histone3具有多種修飾酶和修飾位點,如甲基化酶ATX1、SDG8、SDG25和H3K4、H3K9、H3K27等,憑借對Histone3的不同修飾參與調控植物生長發育和環境應答反應[2]。在擬南芥中,ATX1激活WRKY70基因表達拮抗水楊酸和茉莉酸甲酯信號,PR1、THI2.1等水楊酸或茉莉酸甲酯信號應答基因的核小體也是ATX1蛋白的作用靶點[3]。SDG8能通過調控茉莉酸甲酯和乙烯信號相關基因,來防御蕓薹生鏈格孢菌(Alternaria brassicicola)和灰葡萄孢菌石竹變種(Botrytis cinerea)等病原菌侵染[4]。
雖然Histone3是植物進行表觀遺傳調控的重要靶蛋白,在植物生長發育調控和適應環境等方面具有重要作用,但對Histone3基因自身的表達特性還研究較少。為此,我們克隆了水稻OsHistone3基因(LOC_Os11g05730)的啟動子pOsHistone3,分析顯示其含有多個植物生長調節劑應答元件和組織特異表達元件。在轉基因煙草中的分析表明,pOsHistone3在幼嫩組織中高表達,而在成熟組織中僅在維管組織周圍表達,說明水稻OsHistone3基因可能參與了植物幼嫩組織到成熟組織發育過程的調控。這些結果為進一步探索Histone3基因在調控植物生長發育和生長調節劑信號反應中的功能提供了參考。
1 材料與方法
1.1 ? 實驗材料
水稻“秀水03”(Oryza sativa L. “Xiushui 03”)和煙草(Nicotiana tabacum L.),是逆境農業研究重慶市重點實驗室保存的試驗材料。
1.2 實驗方法
1.2.1 水稻和煙草基因組DNA提取
參照Luo等[5]的方法,取水稻或煙草嫩葉,用CTAB法提取基因組DNA。
1.2.2 啟動子的克隆
根據LOC_Os11g05730的上游調控序列設計引物(上游引物:5- ATTGAGGAATGTGATTTAATC-3,下游引物:5- CGCGGAGGAGGGAGGAGGAGG-3),以“秀水03”基因組DNA為模板,擴增LOC_Os11g05730的啟動子片段。PCR反應體系為:1×PCR Buffer、2.5 mmol·L-1 MgCl2、0.15 mmol·L-1 dNTPs、0.25 μmol·L-1引物、1U DNA聚合酶和約50 ng模板DNA。PCR反應程序為:94 ℃預變性5 min,1個循環;94 ℃變性30 s,56 ℃退火35 s,72 ℃延伸1 min,共32個循環;72 ℃延伸5 min,4 ℃保存。擴增產物于1%瓊脂糖凝膠中電泳,切取特異性強的DNA條帶,回收后,作TA克隆測序。
1.2.3 植物表達載體構建
測序鑒定的pOsHistone3啟動子片段,用Hind III和Xba I雙酶切,連入用相同酶切的pBI121載體,重組質粒即為啟動子分析植物表達載體。
1.2.4 煙草遺傳轉化
采用葉盤轉化法對煙草進行遺傳轉化。無菌苗葉片切成約0.5 cm×0.5 cm大小,用農桿菌菌液侵染10 min,外植體移入共培養基,24 ℃暗培養2~3 d;共培養后,外植體接入篩選培養基誘導分化,每2~3周繼代1次;出現不定芽后,切下,轉入生根培養基中生根。抗卡那霉素的陽性植株,提取DNA,用克隆pOsHistone3啟動子的引物進行PCR鑒定。
1.2.5 煙草GUS染色分析
萌發約10 d的轉基因煙草幼苗,浸入GUS染液,37 ℃孵育4 h,用75%乙醇脫色。四葉期幼苗和10~15片完全葉的煙草植株,用解剖刀徒手切取植物組織器官,浸入GUS染液,37 ℃孵育4 h,用75%乙醇脫色。
2 結果與分析
2.1 水稻OsHistone3基因啟動子的克隆和調控元件分析
在國家水稻數據中心(http://www.ricedata.cn/index.htm)查找OsHistone3基因(LOC_Os11g05730)的上游調控序列,設計特異性引物,從“秀水03”基因組中擴增得到約1 000 bp的DNA片段。測序結果表明,克隆的DNA片段長度為963 bp,與數據庫中登錄的序列完全相同,命名為pOsHistone3。
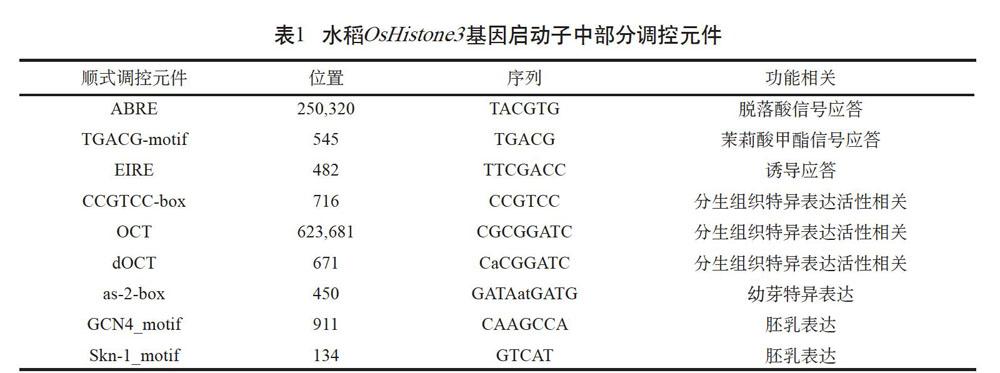
為了解pOsHistone3中的調控元件,在PlantCARE(http://bioinformatics.psb.ugent.be/ webtools/plantcare/html/)對順式調控元件作了分析(見表1)。結果表明,pOsHistone3中不僅有脫落酸、茉莉酸甲酯等植物生長調節劑的信號調控元件,還有胚乳、莖尖、分生組織等部位特異表達元件;同時,還有大量環境信號應答元件,包括光反應、低溫、干旱、缺氧反應和誘導子應答元件等。這些結果表明水稻OsHistone3同源基因的表達可能受到多種因素的調控。
2.2 pOsHistone3::GUS煙草的遺傳轉化
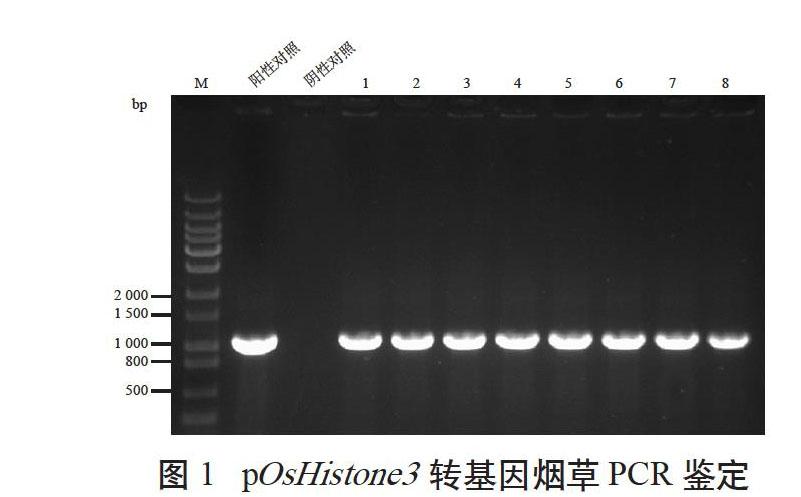
構建pOsHistone3控制GUS基因表達的植物表達載體,并導入農桿菌LBA4404。采用葉盤轉化法對煙草作遺傳轉化,通過GUS組織化學染色,分析pOsHistone3在煙草中的表達特性。通過遺傳轉化,獲得12株煙草再生植株,經鑒定獲得8株轉基因陽性植株(見圖1)。
2.3 pOsHistone3在煙草中的表達特性分析
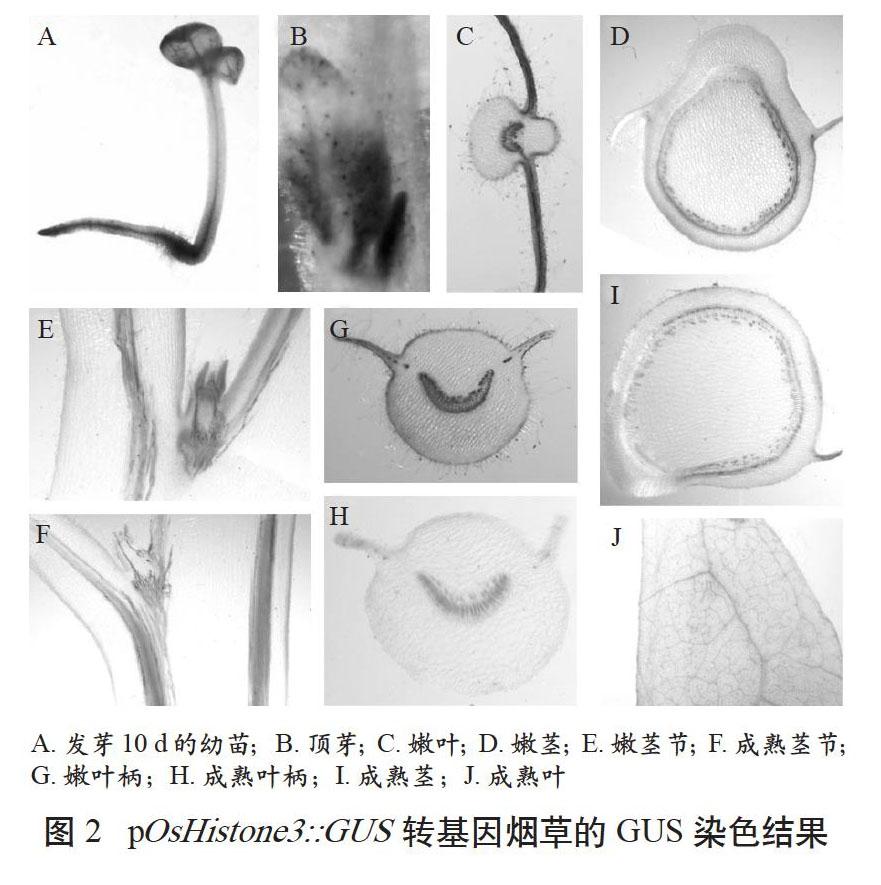
GUS染色結果表明,pOsHistone3在子葉和幼根中高表達(見圖2A),在下胚軸中表達相對較低。在四葉期幼苗中,GUS在頂芽高表達(見圖2B)。當植株生長出10~15片完全葉時,分別取幼嫩和成熟的莖葉作GUS染色,發現幼嫩葉、葉柄和莖中GUS活性相對較高(見圖2CDG),在成熟莖的維管組織周圍能檢測到GUS活性(見圖2I),而在成熟葉片和葉柄中不能檢測到GUS活性(見圖2HJ)。分別取成熟和幼嫩部位的腋芽作GUS染色,發現幼嫩部位的腋芽GUS活性較高(見圖2E),而成熟部位的腋芽僅在維管組織周圍檢測到GUS活性(見圖2F)。這些結果表明,pOsHistone3在煙草中具有組織表達特異性,在幼嫩組織中表達水平相對較高,在成熟組織中表達量較低甚至不表達。
3 小結
組蛋白Histone3是表觀遺傳調控的一個重要靶蛋白,通過對不同位點的修飾,來激發或抑制特定基因或功能元件的活性。如在水稻中,JMJ703是H3K4位點特異性去甲基酶,能特異地降低H3K4的甲基化水平,調控轉座子的活性[6]。Histone3除了通過在蛋白質不同位點修飾的方式來參與表觀遺傳調控外,也有可能在基因表達水平參與植物生長發育調控,但這方面報道相對較少。
在前期研究中,發現水稻有多個OsHistone3同源基因,這些基因編碼的蛋白質雖然高度保守,但在可修飾區段存在氨基酸位點差異(數據未發表),這些位點差異是否會影響OsHistone3蛋白的表觀遺傳調控尚未可知。本研究克隆了其中一個水稻OsHistone3同源基因的啟動子,試圖通過對該啟動子調控元件和表達特性的分析,了解水稻不同的OsHistone3基因是否在表達水平參與植物生長發育的調控。
研究結果顯示,克隆的pOsHistone3啟動子包含植物生長調節劑信號調控元件和大量的環境信號響應元件,說明OsHistone3基因可能在轉錄水平受到多種信號途徑的調控。進一步在煙草中分析pOsHistone3啟動子的表達特性,發現該啟動子主要在幼嫩組織中表達,在成熟組織中表達量很低甚至不表達。這些結果初步說明,組蛋白OsHistone3可能不僅在蛋白質修飾水平上參與表觀遺傳調控,而且在轉錄水平上對植物的生長發育可能也有重要的調控作用,這對于進一步揭示組蛋白Histone3的生物學功能有一定的參考價值。
參考文獻:
[1] Juan S R, Aala A A, Naganand R, et al. Plant immunity: from signaling to epigenetic control of defense [J]. Trends in Plant Science, Published online: July 02, 2018.
[2] Zhou C, Zhao Y, Zhou S L, et al. Progresses and perspectives of crop epigenome research (in Chinese) [J]. Chinese Bulletin of Life Sciences (生命科學) , 2016, 28(10):1138-1145.
[3] Alvarez-Venegas R and Avramova Z. Methylation patterns of histone H3 Lys 4, Lys 9 and Lys 27 in transcriptionally active and inactive Arabidopsis genes and in atx1 mutants [J]. Nucleic Acids Research, 2005, 33(16): 5199-5207.
[4] Alexandre B, Emily J M, Abdelmalek A, et al. Arabidopsis histone methyltransferase SET DOMAIN GROUP8 mediates induction of the jasmonate/ethylene pathway genes in plant defense response to necrotrophic fungi [J]. Plant physiology, 2010, 154(3): 1403-1414.
[5] Luo M, Xiao Y H, Hou L, et al. Cloning and expression analysis of a LIM1 domain protein gene from cotton (Gossypium hirsuturm L.) (in Chinese) [J]. Acta Genetica Sinica (遺傳學報), 2003, 30(2):175-182.
[6] Xiekui Cui, Ping Jin, Xia Cui, et al. Control of transposon activity by a histone H3K4 demethylase in rice [J]. Proceedings of the National Academy of Sciences, 2013, 110(5): 1953-1958.
(責任編輯:丁志祥)

