金屬納米材料對不同微生物聚集體的毒性研究進展
苗令占,王沛芳,侯 俊,王 超,姚 羽
(1.河海大學淺水湖泊綜合治理與資源開發教育部重點實驗室,江蘇南京 210098;2.河海大學環境學院,江蘇南京 210098)
人工納米材料(engineered nanomaterials,ENMs)是指在三維空間中至少有一維處于納米級尺度(1~100nm)內,或由納米尺度作為基本單元構成的材料。納米材料的發展已引起全球范圍內生物、物理、化學等領域以及工農業方面的重大變革,并將對人類社會產生深遠的影響[1-3]。納米材料具有獨特的理化特性,廣泛應用于人類生產與生活各個領域。其中,金屬類納米材料(metallic nanomaterials,MNMs)相關產品是目前使用最為廣泛的納米產品,包括納米 Ag、TiO2、SiO2、ZnO,CeO2、CuO 等[4-5]。 截至2015年,現有的納米材料應用產品種類已達1900多種。然而,人工納米材料可通過生產-運輸-使用-處理處置、污水處理尾水排放、地表徑流等途徑直接或間接地釋放到水環境中,經分散-團聚-沉降、生物攝取-累積放大等一系列的變化,最終對水生生物和生態系統產生毒性脅迫[6-9]。
微生物在水生態系統物質循環和能量流動中發揮著重要作用[10]。雖然目前已有研究證明部分納米材料對微生物存在毒性效應,但這些研究主要以特定(單一)菌種或浮游生物為研究對象,而有關納米材料對環境中復雜的微生物群落的潛在影響尚缺乏全面而系統的研究。水環境中,絕大部分的微生物都是以聚集體的形式存在(如活性污泥、生物膜、表層沉積物微生物群落等),并在污水生物處理、水生態系統平衡和水環境演變中扮演著非常重要的角色,對水體水質改善和生態修復具有重要作用[11]。然而,越來越多的納米材料被釋放到環境中,可能與微生物聚集體相互作用,影響聚集體的代謝活性和功能特性,進而對生態系統產生潛在威脅。
1 金屬納米材料在水環境中的傳輸
隨著對納米材料的需求和含納米材料產品的不斷增加,納米材料在生產、消耗、處理過程中不可避免地釋放到環境中。環境中人工納米材料主要種類和來源見圖1[12]。環境中納米材料的種類主要為金屬納米材料及金屬氧化物納米材料,如納米Ag、納米TiO2等,主要來源于電子工業與光學產業、涂料及顏料和個人護理產品等。
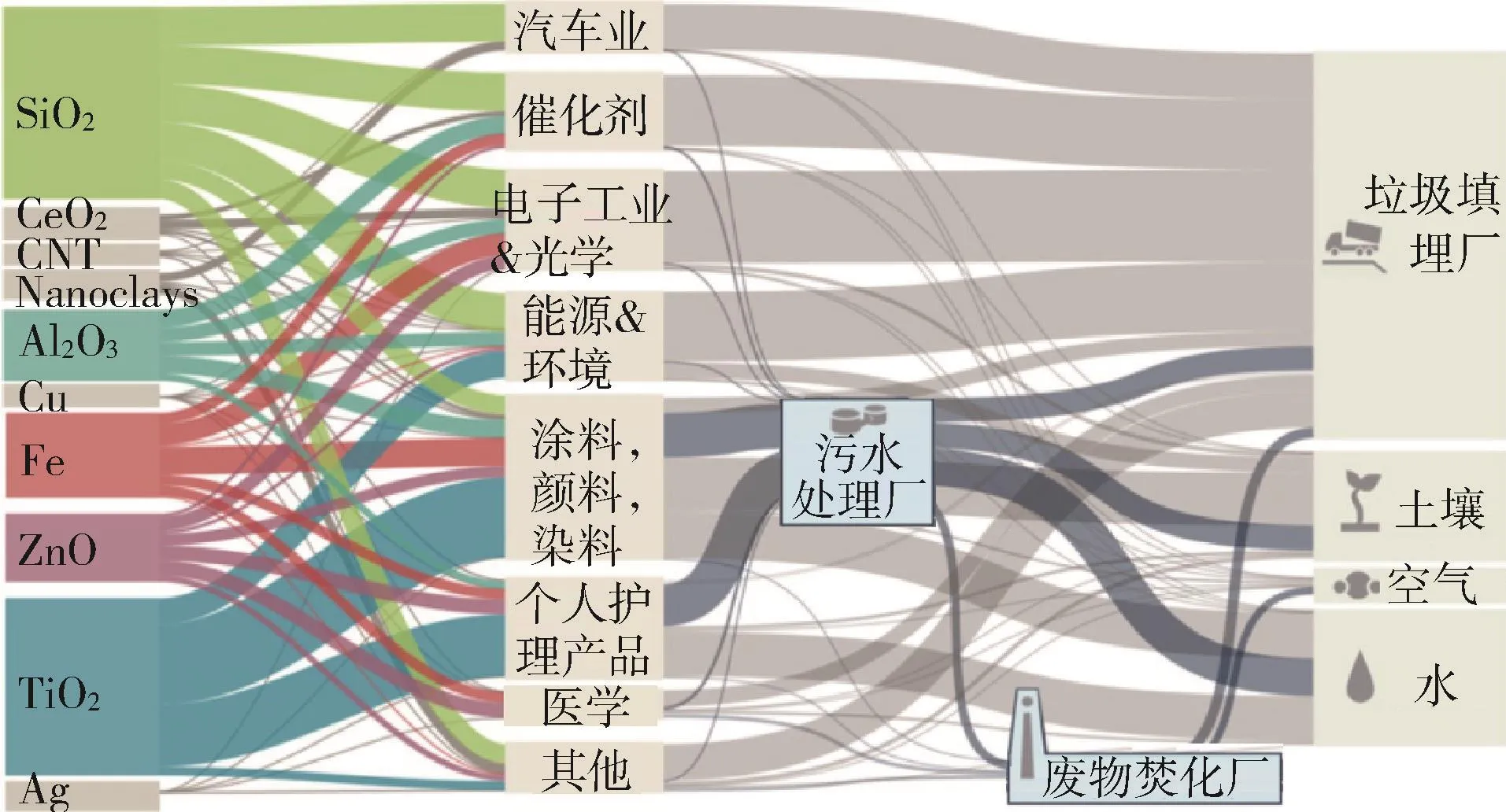
圖1 環境中人工納米材料種類和主要來源
一般而言,金屬納米材料污染物先由市政管網系統傳輸到污水處理廠,而后通過污水處理廠尾水排放、地表徑流侵蝕輸送或以大氣傳輸沉降等方式進入自然水生態系統[13]。根據 Musee等[14]的計算結果,洗漱用品中95%的納米材料最終會通過污水排放、垃圾滲漏等多種途徑進入廢水處理系統。Peijnenburg等[15]也確定了日常生活中若是清洗含有人工納米材料的衣物或紡織品,會有一定量的納米銀隨廢水排入污水處理系統或是直接進入水環境。目前環境中賦存的人工納米材料濃度比較低,對水生生物不會產生明顯的毒性影響。但多數的納米材料不能被生物降解,水生生物可通過直接接觸、吞食和攝取等途徑吸收水體中的人工納米材料。由于生物體清除納米材料速率慢,納米材料具有親脂性和小尺寸效應等,納米材料在生物體內長期累積,并可通過食物鏈或食物網進行傳遞或生物放大,導致高營養級生物的毒性效應,最終對整個水生態系統和人類造成嚴重影響[6-20]。同時,水中的理化條件(如離子強度、pH值及天然有機質等)也會影響納米材料在水環境的團聚、沉降和溶解等,納米顆粒會與其他污染物相互作用導致協同污染,最終對飲用水源帶來威脅[21-23]。
2 金屬納米材料在水環境中的濃度分布
2.1 在污水處理系統中的濃度分布
城市污水處理廠是污染物重要的集中處理地,也是納米材料最有可能發生累積的場所[24-25]。金屬納米材料進入污水處理廠的潛在途徑及污染途徑見圖2[26]。最近一份調查顯示,在亞洲、歐洲以及北美分別大約有10% ~30%,3% ~17%和4% ~19%的納米材料被釋放到水體中,污水處理廠污水中納米材料的質量濃度達到 mg/L級別[27]。Westerhoff等[28]對10座具有代表性的污水處理廠進水和出水中的納米材料質量濃度和種類進行了跟蹤監測,結果顯示,以納米TiO2為例,其在污水處理廠入水中的質量濃度范圍是181~1233 μg/L(平均質量濃度為321 μg/L),經污水處理廠處理后出水中質量濃度小于25 μg/L。污水生物處理系統對納米TiO2的去除率達到98%,其中絕大部分納米材料被截留在污泥中。對于多數種類的納米顆粒(如Ag,TiO,Cu等),污水處理廠對它們的去除率能達到90% 以上,主要去除機制有污泥絮體的吸附、生物攝取以及物理沉降等[28]。污水處理廠尾水中的納米材料質量濃度一般都低于μg/L的量級[24,27],污水處理廠成為納米材料主要積累的場所。因此,關于納米材料對污水處理效率的潛在影響及其對功能微生物毒性作用的研究顯得尤為迫切。
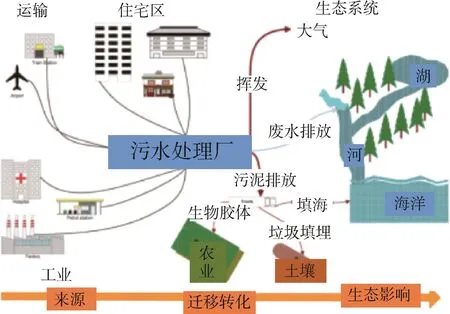
圖2 金屬納米材料進入污水處理廠的可能途徑及污染途徑
2.2 在自然水生態系統中的濃度分布
納米材料一旦排入水環境中,會有分散-團聚、沉降及遷移等過程,也可通過食物鏈在水生生物體內累積,或隨水流運動而遷移擴散[29-30]。此外,納米材料的高比表面積可作為水中其他污染物的吸附載體,促進污染物在地下水等環境中的長距離運輸,造成污染帶的大幅擴散[31-32]。近期,國內外學者紛紛嘗試通過數學模擬來預測環境中的納米材料濃度,但由于研究區域的差異以及模擬的精確度等問題,納米材料的環境濃度還沒有一個明確的數量級范圍。而在實際生活中,可能會發生納米泄漏事件而導致局部納米材料濃度過高,從而增加生物暴露風險。Liu等[33]以納米TiO2為例,利用年平均納米產品的使用量預測納米材料在不同環境介質中的濃度分布,發現釋放到水環境中的納米材料主要分布在自然水體和沉積物中,自然水體中的納米材料質量濃度值已達到100 ng/L,如此高濃度的納米材料將對水生生物構成潛在的威脅。但關于金屬納米材料在自然水體中的實際濃度仍需進一步研究。
3 金屬納米材料對微生物聚集體的毒性
3.1 對污水處理系統中活性污泥和生物膜的毒性作用
目前,有關納米材料對污水處理系統中活性污泥毒性影響的研究已取得不少進展。這些研究主要關注納米材料對活性污泥污水中N和P等的處理效率的影響、對微生物生長活性的抑制以及對微生物群落結構的改變等[34-37]。表1~2列出幾種常見的納米材料對污水處理廠營養物質去除及微生物群落結構的影響和因素表征。從表1~2可知,納米材料的種類、暴露濃度和作用時間均是對污水N、P去除和微生物群落結構變化至關重要的因素,影響作用主要表現在納米材料對活性污泥絮體中微生物細胞胞體產生破壞、對功能菌群的毒性作用以及對N、P去除過程相關酶活性的抑制作用。
大多數金屬或金屬氧化物納米顆粒對活性污泥工藝的脫氮效果都存在不同程度的抑制作用。低濃度的納米SiO2(1mg/L)無論是短期(1d)暴露還是長期(70d)暴露,對活性污泥生存能力和生物脫氮除磷效果并沒有產生明顯的影響。然而,當污泥長期暴露于高濃度(50mg/L)的納米SiO2后,出水硝酸鹽濃度增大,TN的去除率從79.6%下降到51.6%,但廢水中TP的去除率并沒有明顯變化[38]。Zheng等[39]研究表明,在厭氧-缺氧系統中,經過 10 mg/L和50 mg/L ZnO納米粒子短期暴露0.33 d后,TN去除率由初始的81.5%分別降到75.6%和70.8%。進一步的毒性機理研究表明TN去除率降低主要是由于ZnO納米粒子釋放出的Zn2+和產生的過量的活性氧自由基(ROS)抑制了硝酸還原酶的活性。此外,Chen等[40]研究了Cu納米粒子對活性污泥脫氮處理效果及N2O產生量的影響,表明質量濃度為0.1~10 mg/L的Cu納米粒子不僅可提高TN的去除率,而且會降低反硝化過程中N2O的產生量,主要原因是Cu納米粒子溶解釋放的Cu2+增加了反硝化菌的豐度,降低了亞硝酸鹽的含量。Ag納米粒子會降低微生物群落中變形菌門和擬桿菌門的豐度,而這兩種菌門中含有許多與污泥絮體形成及有機物降解有關的細菌[41]。加入10 mg/L ZnO納米粒子提高了活性污泥對COD的降解效率,而20、50和100 mg/L ZnO納米粒子則分別使COD降解效率降低了 8.05%、19.46%和 27.74%[42]。

表1 不同類型的納米材料對污水N/P營養物質去除的影響

表2 不同類型的納米材料對微生物群落的影響
除活性污泥法之外,好氧生物膜法也是污水處理常用的工藝。相比于傳統的活性污泥,好氧生物膜具有致密、穩定的結構,對沖擊負荷和有毒有害物質具有較高的耐受能力[50-51]。由生物膜內微生物分泌的胞外聚合物通過架橋作用將膜內微生物群體連接形成三維微生物聚合體結構,因此與懸浮的活性污泥絮體相比,生物膜這種穩定的三維結構可能會導致其在應對外界污染物時的響應機制與活性污泥絮體不同[51]。然而,目前關于納米材料對生物膜毒性作用的研究還不多見,Sheng等[52]研究發現,納米銀對污水生物膜的微生物群落有著短期的毒性影響,可抑制異樣微生物的生長代謝,并對生物膜整體結構也存在負面影響。Hou等[53]利用溶解氧微電極系統研究發現高濃度(50 mg/L)的納米氧化鋅會抑制生物膜表層微生物的氧呼吸活性,通過監測納米氧化鋅在污水中的溶解情況,并結合二價鋅離子對照試驗,得出納米氧化鋅對生物膜的毒性作用主要是由其溶解釋放的鋅離子而產生的結論。Miao等[54]研究發現暴露于納米氧化銅的生物膜會分泌更多的胞外聚合物,從而抑制納米顆粒的毒性。Miao等[54]還分析了納米氧化銅對生物膜微生物群落結構和組成的影響。但是,由于生物膜復雜的群落組成和結構特性復雜,對生物膜的毒性作用及相關機制仍需進一步研究。
3.2 對自然水生態系統中生物膜的毒性作用
自然水體生物膜是一種普遍存在于自然水生態系統中的微生物聚集體,多生在江河湖海水體中各種載體如石塊、水生植物莖葉、表層沉積物等[55]的表面上。生物膜是一種復雜的微生態系統,主要包括藻類、細菌、真菌、原生動物及后生動物等。由微生物分泌的胞外聚合物所包裹,構成了穩定的三維結構和復雜的微生物群落組成[56]。自然生物膜對驅動水體多種重要生源要素的生物地球化學循環至關重要,它們幾乎能參與水-沉積物界面中所有的生物化學反應,包括生態系統物質循環過程中不可或缺的碳循環、氮循環、磷循環等。生物膜這些生態功能特性及強弱很大程度上取決于微生物的群落結構,同時,微生物群落結構變化在指示水體環境變化上有重大作用[55]。
目前關于金屬納米材料對自然水體生物膜的毒性研究極少。Gil-Allue等[57]通過試驗證明,河流固著生物的呼吸作用、光合作用以及β-葡萄糖苷酶、亮氨酸氨肽酶會對納米銀產生毒性響應而受到不同程度的抑制,但其堿性磷酸酶的活性在不同程度納米銀暴露下不受抑制或刺激;Liu等[58]通過室內暴露試驗發現,當暴露于TiO2納米顆粒(5mg/L)中5d后,生物膜中微生物群落結構發現了明顯的變化,但生物膜的光合作用和代謝功能仍保持穩定。Tang等[59]研究發現5mg/L的Fe2O3納米顆粒能夠引起生物膜內葉綠素含量的升高,抑制了膜內總的抗氧化酶活性,同時改變了生物膜微生物的群落結構。納米材料對自然水體微生物聚集體表毒性的研究才剛剛開始。鑒于微生物聚集體對水生態系統的重要作用,在人工納米材料歸于水生態系統后,關于人工納米材料和生物膜群落結構之間相互作用的研究是必不可少的。
4 研究展望
截至目前,雖然金屬納米材料對污水處理系統中微生物聚集體的毒性研究已經取得了一定進展,但關于金屬納米材料對活性污泥和生物膜的毒性作用機制及其對水處理系統的影響研究還不夠全面。納米材料經污水處理廠尾水排放到水環境中后在自然水體中的遷移轉化和對微生物影響的有關研究才剛剛起步,尤其關于納米材料對自然水生態系統中的微生物聚集體影響的研究十分缺乏。同時,大多數研究采用的是室內短期暴露試驗,且納米材料的濃度遠高于環境中的實際濃度,缺乏野外現場的長期監測試驗研究,因而不能夠準確地反映納米材料對水生態系統的負面影響。
未來的研究方向可以包括以下幾個方面:
a.污水處理系統中生物膜的結構比活性污泥更加復雜,其對金屬納米材料的毒性響應可能與活性污泥不同,因此,可研究金屬納米材料對生物膜的生物活性和微生物群落結構的影響,解析其中的毒性作用機制,進一步明確納米材料對水處理系統的潛在影響。
b.自然水體生物膜作為一種常見的環境介質,富集水體中眾多的污染物質,因此,亟須開展金屬納米材料與自然水體生物膜的相互作用研究,并通過長期的連續監測,解析其對自然生物膜群落結構的影響。
c.自然生物膜廣泛參與水生態系統的物質循環和能量流動,金屬納米材料可能會對生物膜中的微生物群落產生毒性作用,進而影響其生態功能,因此,關于金屬納米材料對自然生物膜水體凈化功能,尤其是對特定物質循環(碳、氮、磷循環)所涉及的遷移轉化及其功能菌群的研究將是未來的研究重點,這對探明納米材料的環境效應與生態安全具有重要的理論和現實意義。

