腸內結合腸外營養對腹腔鏡下巨大消化性潰瘍穿孔修補術后患者營養狀況的影響
史麗
(天津市第五中心醫院,天津 300450)
巨大消化性潰瘍是急性上消化道出血的重要原因,腹腔鏡下穿孔修補術及造瘺術對患者腸道功能干擾少,腹腔沖洗徹底,術后較少發生腸道內營養不耐受,從而保證術后早期順利行腸內營養支持治療[1]。因局部水腫和瘢痕組織形成導致術后胃瘺并發癥發生率較高,臨床多采用禁食和完全腸外營養進行治療,缺點是延長康復時間、費用高、并發癥多[2]。多項研究證實[3],腸內營養的安全性更高。通過術中空腸造瘺術,術后早期即可通過空腸造瘺管行腸內營養,從而避免了早期進食導致胃潴留、胃穿孔等并發癥的發生。基于此,該研究旨在評價以腸內營養為主,結合腸外營養的營養方式在腹腔鏡下巨大消化性潰瘍穿孔修補術中的臨床應用價值。
1 對象與方法
1.1 對象 選擇2016年1月至2017年5月巨大消化性潰瘍(潰瘍穿孔直徑>2.5 cm)穿孔患者共80例,納入標準:①經內鏡檢查確診,病理排除惡性腫瘤;②無嚴重腹腔感染,經抗生素治療可控制病情;③出血量小于1 000 mL,無出血性休克;④能根據分組要求完成研究,臨床資料完善,取得知情同意權。排除標準:①合并其他胃腸道疾病,如結直腸癌、炎癥性腸病等;②出血障礙性疾病,嚴重心、肝、肺、腎、腦等臟器功能障礙;③原發營養障礙性疾病等。
采用隨機數字法將其分為對照組和觀察組各40例,其中對照組男26例,女14例;年齡38~77歲,平均(55.6±12.4)歲;發病時間 3~20 h,平均(8.9±3.6)h;胃潰瘍28例,十二指腸潰瘍12例;潰瘍最大直徑2.8~4.6 cm,平均(3.5±0.8) cm;出血量 500~900 mL,平均(750±120)mL。 觀察組男25例,女15例;年齡35~76 歲,平均(54.7±13.5)歲;發病時間 4~18.5 h,平均(8.5±3.3)h;胃潰瘍26例,十二指腸潰瘍14例;潰瘍最大直徑 2.6~4.5 cm,平均(3.4±0.7) cm;出血量550~950 ml,平均(745±116) mL。 兩組患者在性別(χ2=0.054,P=0.816)、年齡(t=0.311,P=0.757)、病變部位(χ2=0.228,P=0.633)、發病時間(t=0.518,P=0.606)、潰瘍最大直徑(t=0.595,P=0.554)及出血量(t=0.189,P=0.851)方面差異無統計學意義(P>0.05),均衡可比。
1.2 研究方法 對照組于術后第1~8 d采用完全腸外營養,營養液為復方氨基酸注射液,糖脂比1:1,熱氮比100:1,脂肪供給采用20%中長鏈脂肪乳注射液,維生素、電解質和微量元素采用均衡配方,胰島素常規1:5由微量泵泵入;3 000 mL腸外營養液經鎖骨下靜脈輸入。
觀察組采用腸內結合腸外營養方式,術后第1~8 d給予靜脈高營養(3 000 mL)并逐漸減少,同時第1d由空腸營養管內滴入5%葡萄糖鹽水500 mL,滴速100~150 mL/h,氨基酸型腸內制劑300 mL(維沃1袋),溫度保持在37~41℃;第2 d給予氨基酸型+短肽型腸內制劑(1/2全量),第3~4 d逐漸加至全量,過渡到整蛋白型(瑞素);起始能量為18~20 kcal/kg·d,維持能量為 25~30 kcal/kg·d;每 6~8 h 增加 20~40 mL,最快為100~120 mL/h;逐漸增加至正常量,停止腸外營養,24 h內微量泵勻速滴注整蛋白型腸內制劑(瑞素),剩余生理需要量由空腸營養管滴入,滴速200~300 mL/h;6 d后開始經口進流食,逐步減少腸內營養,經口進食能滿足機體需要時完全停止腸內營養。
1.3 觀察指標
1.3.1 對比兩組患者術后3 d、5 d和7 d營養學指標,包括血清白蛋白、前蛋白和轉鐵蛋白水平。營養學指標采用免疫比濁法檢測,白蛋白參考范圍35~55 g/L,前蛋白參考范圍100~400 mg/L,轉鐵蛋白參考范圍12~200 μg/L。
1.3.2 免疫學指標,包括IgG定量、CD3+、CD4+和CD4+/CD8+。免疫學指標采用流式細胞儀檢測,IgG定量參考范圍 6~16 mg/mL,CD3+T細胞參考范圍61.1%~77.02%,CD4+T細胞參考范圍 33.19%~47.85%,CD4+/CD8+T細胞參考范圍1.4~2.5。
1.3.3 炎性指標,包括血清白細胞計數、IL-6、C反應蛋白(CRP)、降鈣素原(PCT)水平。炎性指標采用酶聯免疫吸附(ELISA)法檢測,白細胞計數參考范圍(4~10)×109/L,IL-6 參 考 范 圍 67.37~150.33 ng/L,CRP≤10 mg/L,PCT<0.05 ng/mL。
1.3.4 臨床指標,包括首次排氣時間、大便潛血和切口感染陽性率。其中診斷切口感染標準:根據衛生部頒發的《醫院感染診斷標準(試行)》規定的標準,對手術切口感染病例作出診斷[4]。
1.4 統計學分析 采用SPSS20.0軟件進行統計分析,計量資料以均數±標準差表示,組間比較采用獨立樣本t檢驗,不同時間點數據比較采用重復測量方差分析;計數資料以例數或(%)表示,組間比較用χ2檢驗;P<0.05認為差異有統計學意義。
2 結果
2.1 營養學指標的比較 見表1。
2.2 免疫學指標的比較 見表2。
2.3 炎性指標的比較 見表3。
2.4 臨床指標的比較 觀察組首次排氣時間明顯縮短,大便潛血和切口感染陽性率明顯降低,差異有統計學意義(P<0.05)。 見表 4。
3 討論
3.1 腸內結合腸外營養支持可改善術后患者營養不良狀況 巨大消化性潰瘍患者往往整體營養狀況較差,急性穿孔時大量胃腸液流入腹腔,繼之高代謝、高分解和低蛋白綜合征,增加了敗血癥等發生風險[5];同時急性蛋白營養失調導致體液和細胞免疫功能低下,增加細菌感染和延長術后康復時間[6]。潰瘍穿孔和手術創傷增加了機體炎癥反應,也是影響手術效果的不利因素[7]。既往多數研究認為,腸內營養需在腸功能恢復后進行,早期多支持全腸外營養。但是臨床發現[8],全腸外營養多不能較好滿足術后患者的營養需求,同時增加了靜脈并發癥,患者耐受性較差。研究表明[9],術后胃腸道麻痹僅限于胃和結腸,在術后幾小時內小腸的蠕動和吸收功能即可恢復,而大量營養素的吸收均在小腸內完成,說明巨大消化性潰瘍穿孔修補術后早期實施腸內營養是可行的。消化性潰瘍患者多伴有營養不良,術前蛋白質即已缺乏,而營養支持的較敏感指標蛋白質可反映營養狀態。本研究結果顯示觀察組術后3 d、5 d和7 d血清白蛋白、前蛋白和轉鐵蛋白水平隨著時間的變化逐漸改善,這說明混合營養支持方式在一定程度上可糾正機體蛋白缺乏,改善患者營養不良狀況。
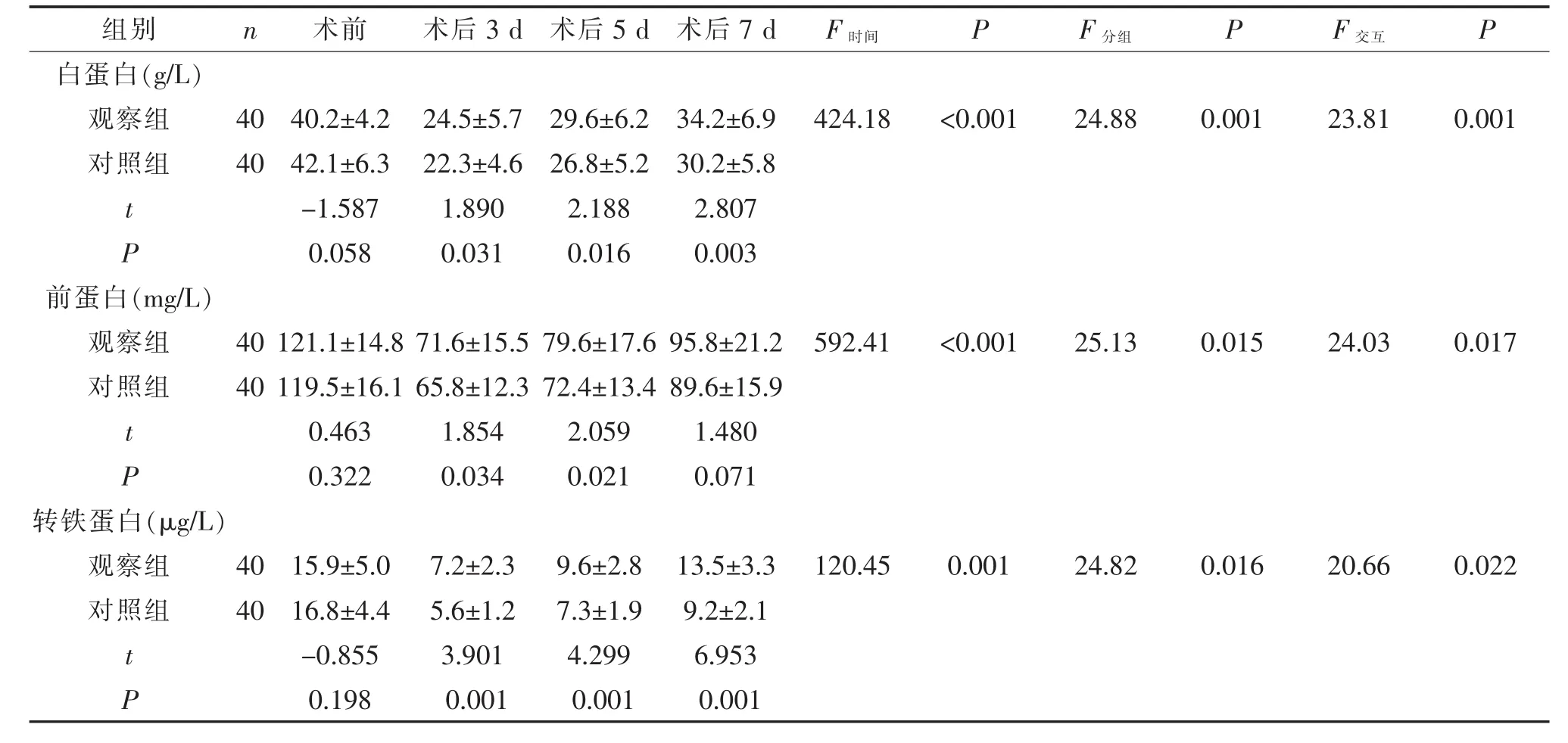
表1 兩組營養學指標的比較及不同時間點上的重復測量方差分析
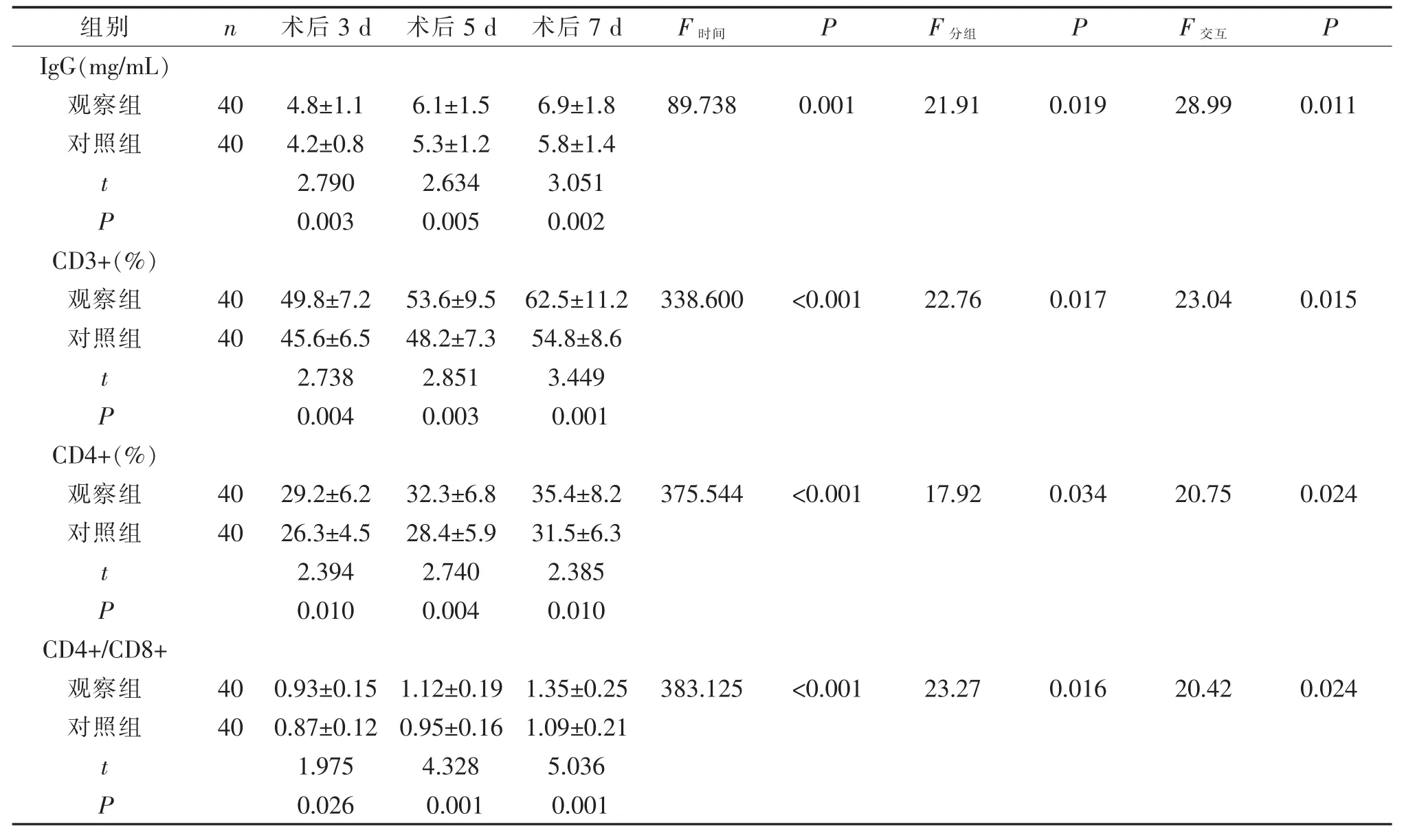
表2 兩組免疫學指標的比較及不同時間點上的重復測量方差分析

表3 兩組炎性指標的比較及不同時間點上的重復測量方差分析
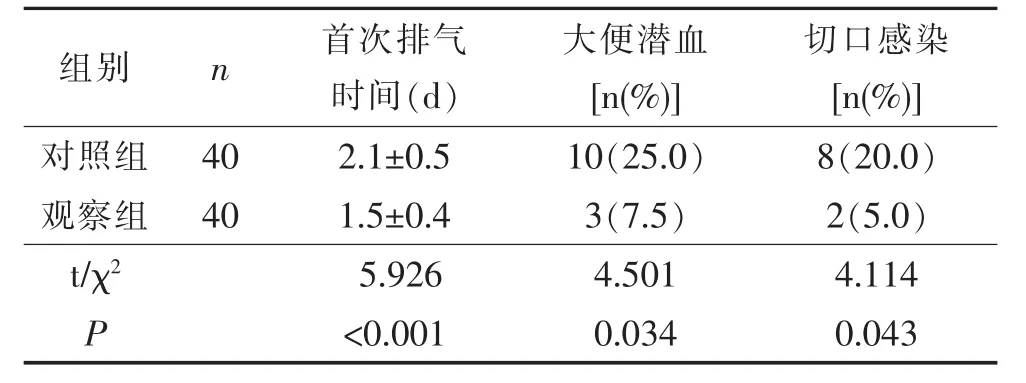
表4 臨床指標的比較
3.2 腸內結合腸外營養支持可調整患者免疫功能,促進康復 研究表明[10],術后早期營養支持可降低手術創傷所致的高代謝率、調節機體免疫功能、減少感染性并發癥,達到促進傷口愈合方面的作用。本研究結果顯示,觀察組血清IgG定量、CD3+、CD4+和CD4+/CD8+均明顯高于對照組,且隨時間變化而升高;觀察組血清白細胞計數、IL-6、CRP、PCT水平均明顯低于對照組,隨時間變化而降低,排氣時間明顯縮短,大便潛血和切口感染陽性率明顯降低,差異均有統計學意義(P<0.05)。因此,可認為以腸內營養為主,結合腸外營養的方式可改善腹腔鏡下巨大消化性潰瘍穿孔修補術后營養和免疫狀況,減輕炎性水平,提高了臨床和護理質量。與李守付[11]的研究結果相似,胃十二指腸潰瘍穿孔修補術后患者進行早期腸內營養效果較好,且較安全。張宗凱等[12]研究證實,早期腸內和腸外營養混合應用可顯著改善胃十二指腸潰瘍穿孔術后患者的營養狀況,促進腸道功能快速恢復。Osland等[13]研究指出,術后小腸的蠕動功能和吸收能力仍然保存是進行早期腸內營養的重要基礎。腸內營養對腸黏膜的新陳代謝和保持完整性具有非常重要的意義。經鼻空腸管進行腸內營養,多數患者有較好耐受管道和腸道的刺激能力。腸內營養可顯著減少蛋白質作為能量進行分解可能是其改善術后營養和免疫狀況,減輕炎性水平的重要機制[14]。
4 小結
腹腔鏡下巨大消化性潰瘍穿孔修補術后早期營養方式的管理是臨床和護理的重要內容,對提高手術效果,減少并發癥,促進患者快速康復均有十分重要的意義。該研究為腸內營養的應用提供了重要參考依據。不足是樣本量較小,隨訪時間較短,還需要進一步驗證。

