液質聯用技術在新藥研發中的應用
許曉輝,邱國玉,景武堂,馬友振,王小喬,賈汝玲,杜 清
(1蘭州市食品藥品檢驗所,甘肅 蘭州730050;2甘肅省人民醫院外科,甘肅 蘭州 730000;3江蘇萬邦生化醫藥集團有限責任公司,江蘇徐州,221004;4青海民族大學藥學院,青海省青藏高原植物化學重點實驗室,青海西寧810007)
0 引言
新藥研發是尋找替代目前臨床上使用有缺陷的藥物或者尋找能夠治療特定疾病的高效低毒藥物,它是從化合物庫中,通過體內體外活性篩選出候選藥物,再經過臨床試驗驗證,才上市應用到患者身上。因此,新藥研發是一項復雜、艱巨的工作,一個新藥的問世周期是12~15年(圖1)[1]。在新藥研發中應用的分析技術有色譜、質譜、核磁共振,而對復雜組分定性定量應用比較廣泛的是液質聯用(liquid chromatography-mass spectrometry,LC-MS)。目前,液質聯用技術已經成為新藥研發的重要技術手段,它具有高靈敏度、高通量、快速等優點,被廣泛的應用到新藥結構發現,新藥的吸收、分布、代謝、排泄檢測,新藥藥理活性的研究等方面。本文從與藥物相關化合物結構的鑒定、新藥體外活性研究、新藥體內藥代動力學及與新藥作用相關的藥效標志物等方面探討了液質聯用技術在新藥研究中的應用。

圖1 基于化合物生物活性篩選的新藥發現過程示意圖
1 LC-MS概述
LC-MS系統元件包括進樣器、HPLC系統(或UPLC系統)、電離源、質量分析器和檢測器。理想情況下,這些元素都在一個計算機系統的控制之下。典型的反相高效液相色譜系統連接到MS將使用一些水或甲醇或乙腈的組合作為流動相。同時還要添加離子化試劑,典型的離子化試劑主要包括乙酸銨、甲酸銨、乙酸和甲酸等。超高效液相色譜質譜聯用是目前使用比較廣泛的儀器,其有多種電離源。最常見的兩種源是電噴霧電離(electrospray ionization,ESI)和大氣壓化學電離(atmospheric pressure chemical ionization,APCI);這兩種類型源現在都是用于LC-MS應用的質譜儀標準配置。在ESI系統中,高壓場(3-5kv)向柱狀噴射,導致帶電荷的液滴聚焦于質量分析裂解器,這些液滴在接近質譜儀入口時變得越來越小,當液滴變得越來越小時,單個離子就會在一個被稱為“離子-蒸發”的過程中出現,這些離子就會被MS系統分離出來。在APCI中,加熱蒸發柱洗脫液,然后電暈放電電離溶劑分子,然后通過化學電離機制產生分析物離子。圖2列示了目前比較常見的幾種液質聯用儀,主要有單四極質譜儀、飛行時間質譜儀、三重四級桿質譜儀和離子阱質譜儀。其中,飛行時間(TOF)質譜計,它具有額外的能力提供更高質量分辨率光譜;三重四極質譜儀,它最常用于生物分析,但也可用于代謝物鑒定;離子阱質譜儀,其具有獨特的產生MSn數據的能力,這些數據可以進行化合物結構解析。除了這四種類型的質譜計之外,還有一種混合質譜儀,它將兩種基本的質譜儀結合在一起,構成了一個混合系統,該混合系統囊括了“Q-TOF”MS-MS系統[2]。總的來說,四級桿液質聯用的強項在定量,飛行時間或離子阱液質聯用的強項在定性。液質聯用強大的分析能力,分析級別能夠達到ng級別水平,能夠提供相對分子量和豐富的結構信息,與譜庫檢索聯合應用,能夠快速對化合物進行擬合匹配,定性化合物,尤其適合微量復雜組分體系的分析、不易分離或缺乏特征紫外吸收的化合物,對已知、未知物的定性定量、在以藥物生物活性為指導的目標化合物篩選,靶標分析,藥物及其代謝物血漿、膽汁、尿液中的檢測等。新藥研發經歷不同階段,從化學設計合成目標化合物到候選藥物的藥理篩選,LC-MS已被用于所有這些階段,并在許多情況下成為首選的分析工具。
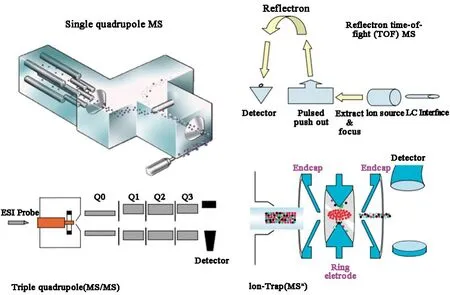
圖2 不同類型的質譜儀
2 液質聯用技術在新藥研發中的應用
在新藥研發過程中,對潛在的新藥先導化合物進行鑒定是新藥高通量篩選的關鍵。而液質聯用的高分離能力和高靈敏度選擇性于一體,能夠同時分析多個化合物,可對生物基質內的微量藥物進行可靠的定性驗證與定量檢測。目前液質聯用技術在新藥研發中的應用主要集中在與藥物相關化合物結構的確證、藥物體外生物活性篩選、體內藥物代謝和藥代動力學等方面。
2.1 與藥物相關化合物結構的確證在新藥研發的初級階段,目標化合物設計合成后,得到一系列潛在的可能成為候選藥物的目標化合物,應用LC-MS對這些潛在的可能成為候選藥物的化合物進行結構確證和純度分析,這是作為構建化合物庫的第一步。一個通用的系統是運用紫外檢測器對所得化合物進行純度評估,用液質聯用儀的MS系統對化合物結構進行確證,MS系統是單四級桿或飛行時間質譜或離子阱,這些系統通常高度自動化。目前,LC-MS工作中都具備高度的自動化和便捷化,能夠同時分析化合物的純度和給出化合物結構方面的質譜信息。這個過程是基于LC-MS硬件系統和軟件系統相組合的信號同時檢測,這些信號是根據所觀察到或預期的化合物的m/z響應觸發的。在新藥未知物結構鑒定方面,應用多的是飛行時間質譜或離子阱質譜,具體操作應該是:首先用Q-TOF獲得高分辨數據,得到分子構成,其次分析每一個碎片,得出結構,最后用標準品在相同的條件下做Q-TOF,如果得到的結果與分析出的結果是完全一致,則該未知物就被鑒定出來,如果需要進一步鑒定該未知物,則需要分離出該未知物,與1H-NMR、13C-NMR、IR相配合,確證結構。在已知藥物結構鑒定方面,用LC-MS/MS同時分析已知物與已知物的標準品,兩者結果相比較,如果完全一樣,一般情況就可確定已知物結構。與新藥作用相關的藥效標志物尋找是新藥體內體外篩選的主要依據,藥物活性標記物的識別與檢測對于研究藥物活性與作用機理非常重要,可以準確的預測藥物藥理活性,同時也可減少藥物研發和臨床試驗的時間和成本。目前,大多數藥物的研發模式都是基于活性標記物的藥理活性研究為目標,以藥物對該相關疾病模型的標志物的影響作用與大小為依據,通過檢測藥物作用于模型后,活性標志物上調或者下降用來預測被研究藥物藥理作用,同時,藥物活性標記物的變化可以預測或發現與候選藥物相關的安全問題,揭示藥理活性或表明臨床療效,在新藥研發方面,使用液質聯用去發現或鑒定藥物藥理活性標志物,藥理活性標記物的發現與確證將加速將加速藥物的研發速度[3-7]。吳光昊[8]基于液質聯用技術開展了抗體偶聯藥物(ADC)結構研究及鑒定,借助質譜技術,以ADC藥物的載藥分布與偶聯位點的質量特性為切入點對抗體偶聯藥物結構進行表征分析,為ADC藥物質量異質性研究打下扎實基礎。
2.2 藥物體外生物活性篩選藥物體外活性篩選主要包括以下幾個層次的篩選:計算機模擬藥物篩選、分子水平的藥物篩選模型、細胞水平的藥物篩選模型。候選藥物的體外活性篩選要經過一系列生物活性實驗來確證,主要有藥物作用于培養的人體細胞后細胞組織形態、DNA、RNA、酶、細胞周期等發生的變化,藥物與能夠體現藥物活性的藥物標志物的作用效果,比如藥物與拓撲異構酶的作用,藥物與細胞周期調控因子p53的作用,評估候選藥物抑制一種或多種人細胞調控因子的潛力,而LC-MS/MS被用于這個步驟主要是去研究藥物與靶點結合的識別或者通過高通量篩選去識別活性化合物。目前,已有大量應用液質聯用去篩選藥物體外生物的研究成果被報道。例如,活性乙酰水解酶(PAF-AH)是一種血小板活化因子,是血管系統及炎癥系統中的細胞間調節分子,劉維等[9]建立一種簡單、快速、特異、穩定地LC-MS/MS法檢測新型藥物過敏反應介質血小板活化因子C-18(PAF C-18)及其乙酰水解酶(PAF-AH)活性的方法,該方法可以通過外源性添加PAF C-18在一定時間內的下降程度,間接反映PAF-AH活性,為開展相關藥物過敏的臨床藥效學研究提供了指導。也有液質聯用與其他生物活性篩選方法相結合來篩選藥物藥理活性,如樸香蘭等[10]應用酪氨酸酶抑制實驗-液質聯用方法快速尋找到苦參中具有較強酪氨酸酶抑制成分槐屬二氫黃酮G和苦參酮,這兩個化合物的酪氨酸酶抑制活性強于已知的酪氨酸酶曲酸的活性。劉侗等[11]以體外培養的人臍靜脈內皮細胞(ECV-304)為研究材料,建立以H2O2誘導內皮細胞的氧化損傷模型,以內皮細胞的存活率為指標,研究通頂散各萃取部位對ECV-304的保護作用,結果表明藜蘆生物堿、人參皂苷和甘草皂苷是通頂散抗過氧化氫損傷活性物質。近年來,蛋白質組學和代謝組學研究是新藥開發的一種重要高通量篩選技術,新藥靶標的發現鑒定、藥物的作用模式、藥物與蛋白質作用機理是藥物篩選蛋白質組學研究的主要內容[12],而液質聯用是蛋白質組學和代謝組學研究分析的主要工具,基于液質聯用分析技術的高通量蛋白質組學藥物活性篩選有利于加速新藥研發的速度。ZHU等[13]基于代謝組學,開發了一種快速、靈敏、高通量的腫瘤細胞中20種內源性核苷和核苷酸的液質聯用分析方法,而內源性核苷和核苷酸是代謝組學研究中最具差異性的代謝物,這20種內源性核苷酸和核苷酸的定量分析方法符合具體擴增代謝組學研究的定量要求,具有較好的選擇性,當應用腫瘤細胞篩選抗腫瘤藥物,可以通過檢測施加藥物后的腫瘤細胞中內源性核苷和核苷酸而判斷藥物藥效。
2.3 體內藥物代謝和藥代動力學藥物體內活性篩選主要有以下兩個層次:動物個體水平的藥物篩選模型和人體臨床篩選模型。LC-MS在新藥發現中最常見的應用是藥物的吸收、分布、代謝、排泄(ADME)研究,它們占藥物代謝和藥代動力學(DMPK)研究的大部分工作。藥代學研究首先是體內ADME篩查、其次是各種體內臨床前ADME-PK篩查、代謝產物的鑒定、體內篩選還有一個重要指標是代謝穩定性試驗。圖3是動物體內藥代動力學篩選樣品制備策略圖,它使用96孔板進行樣品制備,蛋白質沉淀常常是樣品制備的首要步驟,這種制備方式有一定的便利性和高效性,而對于一些特殊的化合物,常常液-液萃取或者固相萃取方法進行前處理,藥代動力學研究應用比較多的是三重四級桿液質聯用[2]。早期藥代動力學評價是藥物發現過程的重要組成部分,能夠區分化合物的體內藥動學特性,從而使研究具有有針對性,加快研發進程。基于可供篩選的化合物數量、新靶點篩選技術,藥代動力學篩選速度成為新藥研發進展的關鍵。目前采用基于液相色譜質譜聯用技術篩選藥代動力學,有單一給藥,也有盒式給藥方法,所謂盒式給藥即幾種候選化合物混合后同時給單一動物進行快速樣品分析,在體內研究多選擇盒式給藥,這樣可提高化合物在體內的藥代動力學篩選通量,節省實驗資源和成本,缺點是可能會出現化合物相互作用,因此對所采用的分析方法進行評價和驗證是必要的[14]。 王蕊等[15]應用 HPLC-MS/MS 分析恒河猴全血中調血脂化合物IMM-H007(見圖3)的藥代動力學,結果表明,IMM-007在體內血藥濃度較低,主要以活性代謝產物M1和MP形式存在,MP的體內暴露量明顯高于M1,該研究為進一步為探明新型調血脂藥IMM-007后續藥理毒理研究提供參考數據。楊兵等[16]基于高效液相-電噴霧-四級桿-線性離子阱串聯質譜技術建立了一種高通量靶標磷脂組學分析方法,研究尿液中的磷脂輪廓并篩選出尿液樣本中潛在的磷脂標志物,該檢測分析方法在磷脂組學研究中具有簡單、穩定和敏感的特點,可應用于后續大樣本量的磷脂組學研究及潛在尿磷脂標志物的定量研究,為研究具有磷脂標記物的藥物的體內代謝、藥物動力學提供了指導。Hallur等[17]以 LC-ESI-MS/MS方法分析了FAK抑制劑Defactinib在小鼠體內的藥代動力學,該方法簡單、靈敏,具有良好的準確性和精密度,完全符合美國FDA的指導方針。恩曲替尼是一種有效的口腔間變性淋巴瘤激酶(ALK)抑制劑,Attwa等[18]建立了一種有效的LC-MS/MS方法,用于定量人血漿基質中的恩曲替尼,該方法具有快速、特異、靈敏等特點,被認為是人類血漿中恩曲替尼定量及其代謝降解評估的第一種方法。總之,應用液質聯用去分析藥物體內代謝物及藥物藥代動力學方面越來越受到研究者的關注[19-21],尤其在藥物早期發現中,代謝物研究能夠在實驗動物模型描繪出完整的代謝輪廓圖,發現不穩定的代謝途徑以及評估代謝物的安全性,反過來通過化學途徑修飾母體藥物以改善藥物的穩定性,尋找到代謝有利于藥物發揮最大藥效的結構[22]。然而,盡管LC-MS/MS作為藥物和代謝物定量主要分析技術,但是一些非常基本的問題還沒有得到充分的解決,如串聯質譜法對被分析物的選擇性,基質效應(離子抑制或增強)的潛在影響等[23]。
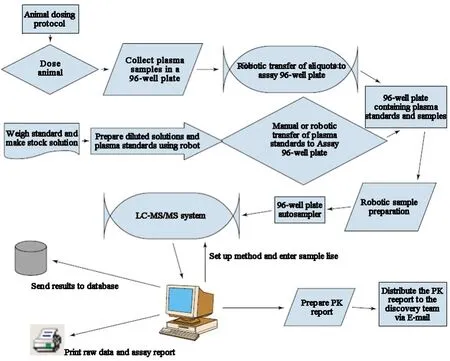
圖3動物體內藥代動力學樣品制備分析策略圖
3 總結
目前,液質聯用技術已經變成新藥研發中的重要分析技術之一,在新合成目標化合物或新發現能夠潛在成為候選藥物的化合物結構鑒定、高通量篩選,隨著新型質譜技術及離子化技術的不斷改進和發展,樣品前處理技術的不斷革新,鑒于現有儀器的潛力和可預見性,從分析能力和數據采集到化學計量學以及分析方法驗證的瓶頸正在被取代,從自動化分析過程到快速、高通量的分析結果,液質聯用將成為新藥發現過程不可或缺的分析技術,將越來越多的被應用到新藥研發中。

