基于巢氏病例對照研究丹參川芎嗪注射液疑似過敏反應的影響因素分析?
李 敏,謝雁鳴,章軼立,高 陽△,徐鴻燕
(1. 中國中醫科學院中醫臨床基礎醫學研究所,北京 100700; 2. 中國中醫科學院眼科醫院,北京 100040;3.中國人民大學統計學院,北京 100872)
丹參川芎嗪注射液(貴州拜特制藥有限公司,國藥準字H52020959)具有擴張動脈、抗血小板凝集和改善微循環等作用,主要用于心腦血管疾病的治療。丹參川芎嗪注射液雖然治療效果顯著,但發生過敏反應的情況也同樣不容忽視[1-3]。丹參川芎嗪注射液最新版說明書上記有“未發現明顯毒副作用,曾報道有過敏反應,可見皮疹、瘙癢、心悸、胸悶、寒戰、頭暈、頭疼、惡心、嘔吐、胃腸道不適、淺靜脈炎等,停藥后消失。曾有過敏性休克和喉頭水腫報道”的標注。為了解真實世界中丹參川芎嗪注射液發生過敏反應的影響因素,本研究收集全國24家三甲醫院信息系統(hospital information system,HIS)中使用丹參川芎嗪注射液住院患者的住院信息,采用巢氏病例對照(nested case-control study,NCCS)研究設計和Logistic回歸分析的統計方法,探索使用丹參川芎嗪注射液出現疑似過敏反應的人群中,可能引起過敏反應的相關因素,為丹參川芎嗪注射液的合理用藥提供科學依據。
1 材料與方法
1.1 數據來源
本數據來源于中國中醫科學院中醫臨床基礎醫學研究所構建的HIS數據倉庫,選取2006年10月至2015年12月全國24家大型三甲醫院HIS數據庫中使用丹參川芎嗪注射液的住院患者,包括基本信息表、西醫診斷信息表、醫囑信息表等數據。
1.2 數據規范化
本研究數據來源于多家醫院,各家醫院在同一項目中采納的標準不盡相同。為便于分析,需要對數據進行規范化。參照西醫《診斷學》第7版對西醫診斷信息進行規范化;將數據庫中記錄為商品名稱的化學藥物轉化為化學通用名稱并合并相同項。對合并用藥,采取合并同種化學成分的方式對化學藥物進行規范,將同類藥物成分但劑型不同的中成藥進行合并,其他中成藥保留原始名稱,對合并用藥的分析均基于標準化后的數據。
1.3 研究對象及數據界定
本研究的研究對象為使用丹參川芎嗪注射液后出現疑似過敏反應的人群。疑似過敏反應人群的界定:使用丹參川芎嗪注射液后立即停藥,并且在24 h以內使用抗過敏藥物(苯海拉明、異丙嗪、撲爾敏、賽庚啶、息斯敏、特非拉丁、地塞米松、氯雷他定、地氯雷他定、西替利嗪、咪唑斯汀、依巴斯汀、非索非那定、左西替利嗪、葡萄糖酸鈣等)。
1.4 研究設計
根據數據的界定標準,在數據庫中使用丹參川芎嗪注射液共有37548例住院患者,其中發生疑似過敏反應的病歷124例(0.33%),未發生過敏反應的病歷37424例。采用回顧性NCCS的設計方法,以性別相同、年齡±3歲作為配比條件,按照1∶4的方法進行匹配,最終納入620個數據。將研究對象分為過敏組和對照組,病例組開始使用丹參川芎嗪至停止使用的時間范圍在0~24 h,期間僅使用1次,停止使用后的24 h內使用抗過敏藥物,且使用丹參川芎嗪注射液前與使用中均未使用抗過敏藥物者。對照組開始至停止使用丹參川芎嗪注射液時間>7 d,且用藥時未使用地塞米松注射液、異丙嗪、氯雷他定、維生素C注射液、葡萄糖酸鈣注射液等常用抗過敏藥物。
1.5 統計學方法
采用Logistic回歸分析統計方法,采用SAS.9.2軟件作為分析軟件。
2 結果
基于現有HIS數據庫信息,結合臨床實際情況,考慮最有可能成為過敏反應影響因素的有64個,分別為合并病(頻數前30位)、合并用藥(剔除苯海拉明、異丙嗪、撲爾敏、賽庚啶、息斯敏、特非拉丁、地塞米松、氯雷他定、地氯雷他定、西替利嗪、咪唑斯汀、依巴斯汀、非索非那定、左西替利嗪、葡萄糖酸鈣后的頻數前30位)、住院天數、療程、單次劑量、日劑量。運用條件logistic回歸進行數據建模分析,采用逐步選擇法篩選變量,對使用丹參川芎嗪注射液出現疑似過敏反應的影響因素進行分析判斷。
2.1 合并用藥對比分析
過敏組與對照組比較,合并用藥影響因素中呋塞米片和前列地爾注射液的P值分別為0.003、0.007,且回歸系數為正,說明丹參川芎嗪注射液在聯合使用呋塞米片或前列地爾注射液時,發生過敏反應的危險會大大增加。同時篩選聯合用藥中胸腺肽的P值為0.001,回歸系數為負數,說明胸腺肽是使用丹參川芎嗪注射液疑似發生過敏反應的保護因素。
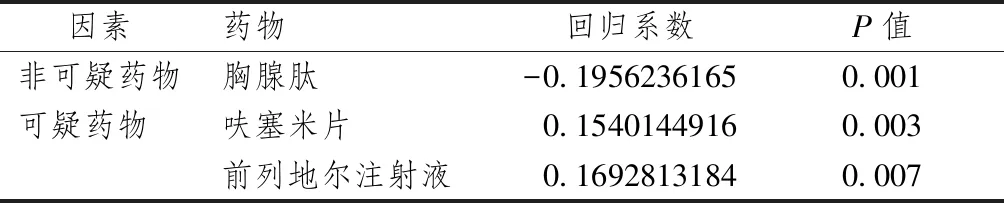
表1 合并用藥影響因素分析結果
2.2 合并疾病對比分析
過敏組與對照組比較,惡性腫瘤的P值為0.045,且回歸系數估計值為正,說明使用丹參川芎嗪注射液合并惡性腫瘤時發生疑似過敏反應的危險會大大增加;同時篩選合并疾病中慢性腎病的P值為0.022,回歸系數估計值為負數,說明慢性腎病是使用丹參川芎嗪注射液疑似發生過敏反應的保護因素。

表2 合并疾病影響因素分析結果
2.3 住院天數對比分析
過敏組與對照組比較,住院天數時間段為8~14、15~28、>28 d的P值分別為0.018、0.003和0.001,且其回歸系數均為負數,說明住院天數分段中8~14、15~28、>28 d是使用丹參川芎嗪注射液的保護因素。

表3 住院天數影響因素分析結果
2.4 用藥劑量對比分析
過敏組與對照組比較,丹參川芎嗪注射液單次用藥劑量、日劑量、療程分段P值均>0.05,說明單次用藥劑量、日劑量、療程分段并不是導致丹參川芎嗪發生過敏反應的影響因素。
3 討論
3.1 使用丹參川芎嗪注射液發生疑似過敏反應的影響因素
聯合用藥是藥物相互作用的基礎,藥物相互作用的結果是將單一藥物的療效變成多個藥物的綜合療效,而不良反應的出現是藥物相互作用不良效應的體現[4]。
丹參川芎嗪注射液與前列地爾注射液聯合用藥時發生過敏反應的可能性較大,其原因可能是前列地爾注射液可擴張血管,增加毛細血管通透性,促使炎癥滲出和黏液腺分泌增多,機體可出現過敏癥狀[5]。前列地爾注射液是以脂微球為藥物載體的靜脈注射用制劑,其將前列腺素E1封入直徑0.2 μm的脂微球中,增加其靶向性。但如果少量的前列腺素E滲透至脂微球載體外,即可引起一系列的不良反應[6]。丹參川芎嗪注射液與前列地爾注射液皆可擴張血管,改善微循環,兩種藥物的藥理作用疊加是導致不良反應的主要原因[7]。丹參川芎嗪為含有丹參提取物和鹽酸川芎嗪的化學藥物,其中丹參提取物以丹參素為代表成分在體內的吸收,但其在體內分布、代謝和排泄的機制并不是十分清楚,可能因化學成分、pH值等改變使微粒數增加,微粒進入血管引起局部血栓、血腫、損傷、壞死,產生微血管阻塞并發生不良反應。而前列地爾注射液是一種分子量較大,含有注射用大豆油、卵磷脂、甘油等油性成分的乳狀液體,對血管有一定的刺激作用,兩種藥物合用可能通過化學成分改變增加微粒數引起不良反應[8]。
丹參川芎嗪注射液與呋塞米片聯合用藥發生過敏反應的可能性較大,其原因在于呋塞米與丹參川芎嗪注射液存在配伍禁忌[9-11]。有學者提出丹參川芎嗪注射液與呋塞米注射液配伍后產生白色沉淀,因丹參川芎嗪注射液為酸性,呋塞米注射液為弱堿性,混合后pH值發生改變,因而使藥物析出[12]。這類文獻報道為本研究探討丹參川芎嗪注射液與呋塞米片聯用發生過敏反應的機制提供了相關線索。且呋塞米片屬于磺胺類非抗菌藥,其與磺胺類抗菌藥之間易發生交叉過敏反應。也有學者認為,本身過敏反應易感性增高的患者(如青霉素過敏史患者)在使用磺胺類非抗菌藥之后亦有較大可能出現過敏反應,因此臨床對于存在磺胺類抗過敏藥物和青霉素過敏的病人使用呋塞米片時要謹慎[13]。
丹參川芎嗪注射液與惡性腫瘤合并使用時發生過敏反應的情況往往較多。對于腫瘤患者而言,過敏產生的原因與腫瘤產生的組胺、癌胚蛋白等生物活性物質的釋放刺激感覺神經有關。另一方面腫瘤致病因子和腫瘤細胞作為一種異體抗原或致敏原,不斷刺激機體產生抗體如IgE抗體等,從而形成類過敏反應[14]。中藥抗癌要把握合適的時機,如患者已行根治手術或放化療術后,中醫藥治療應以“扶正”為主,此時若再以活血化瘀藥攻伐,稍有疏忽就會產生中藥的毒副作用。相關文獻報道,丹參類制劑不宜與抗癌藥環磷酰胺、環己亞硝胺等通用,其可能會促進惡性腫瘤的轉移,并對某些抗癌藥物具有增敏作用。這可能與其減少瘤組織內DNA含量有關[15-16]。 丹參川芎嗪注射液成分復雜,其主要致敏原因是由鞣質引起的,鞣質進入機體后,可作為半抗原與血漿蛋白的氨基締合成更大分子的復合物,引起機體的變態反應。抗癌靶向藥物中阿昔替尼、厄洛替尼、利妥昔單抗和曲妥珠單抗等均屬于大分子藥物,其引起的過敏反應在國內外均有文獻報道,推測可能與其影響皮膚濾泡和間質細胞表皮生長因子信號通路有關。由于丹參川芎嗪注射液和抗癌藥都有致變態反應特性,且兩藥物聯合使用時,丹參川芎嗪注射液中的某些成分可能與抗癌藥物締合成更大分子的復合物而加大過敏反應[17-19]。
3.2 本研究的不足
本研究的局限性在于HIS數據庫提供的是回顧性數據,且研究數據也是根據患者是否使用抗過敏藥物推測獲得,缺乏過敏反應的判斷。因此本研究得到的可疑過敏反應影響因素僅做參考,還需要進一步的臨床試驗進行驗證。

