撬拔復位空心螺釘術與切開復位術治療Sanders II、III型跟骨骨折臨床療效分析
姚 竣,張中發
(四川省合江縣人民醫院骨科,四川 合江 646200)
跟骨骨折的損傷機制較為復雜,多由高處墜落所致,其男性群體發病率高于女性,患者具有足弓塌陷、跟骨外側壁外膨等病理改變,跟骨骨折的治療方式多樣,但目前尚無明確標準[1,2]。撬撥復位空心螺釘術屬于閉合復位,具有微創優勢,患者術后恢復更快,而切開復位術復位準確性良好[3,4]。Sanders II、III型跟骨骨折患者跟骨關節面發生兩部分或三部分骨折,為對比撬撥復位空心螺釘術與切開復位術在Sanders II、III型跟骨骨折患者中的應用效果,本文開展如下研究。
1 資料與方法
1.1 一般資料2016年6月至2019年1月我院收治的82例Sanders II/III型跟骨骨折患者。納入標準:①術前行雙側足正側位、跟骨軸位、水平與管狀面CT掃描,確診為跟骨骨折;②根據跟骨冠狀位及軸位CT掃描結果對骨折進行Sanders分型,其中II型44足,表現為跟骨后關節面兩部分骨折,移位不小于2 mm,III型39足,表現為跟骨后關節面有兩條骨折線,為三部分移位骨折;③骨折至手術時間1~10 d;④致傷原因為高處墜落、車禍、砸傷等;⑤均為閉合性骨折。排除標準:①病理性骨折者;②不可耐受手術者;③足踝部神經損傷者。根據手術方式分為撬撥復位組(41例42足)與切開復位組(41例41足),兩組一般資料比較差異無統計學意義(P> 0.05),見表1。

表1 兩組一般資料比較
1.2 方法撬撥復位組采用撬撥復位空心螺釘術,患者取仰臥位,硬腰聯合麻醉,C形臂X射線透視下,從骨結節上緣少外側向骨前部方向打入一枚4.0 mm克氏針,接著由跟骨結節上方,與跟骨縱軸呈60°夾角方向置入一枚撬撥針,保證其針尖不超過骨折線。助手雙手握緊前足,將足部用力背伸,撬起塌陷骨折塊,維持Bohler角25°~40°,術者將克氏針向跖側按壓,恢復跟骨結節關節角及跟骨交叉角,若跟骨存在長度變短、內外翻、高度變低等問題,可向其內部打入一枚4.0 mm克氏針,調整以上問題,復位骨折塊,保持關節面平整,C形臂機透視復位滿意后,助手持續向跖側用力推壓前足及撬撥針尾,術者從骨結節下沿骨縱軸相平行方向打入1~4枚克氏針,經關節面骨塊、跟骨前部進入距骨、舟骨固定,撥出原來打入的撬撥針或將其打過骨線,拔除牽引針,將固定針剪短。
切開復位組采用切開復位術,麻醉方式與撬撥復位空心螺釘術相同,從跟腱外側緣向下至足背皮膚與足底皮膚相交處做一“L”形延長切口,并在水平向前第五跖骨基底附近,將皮膚及其皮下組織一并切開,掀起包含腓骨肌腱及腓腸肌神經的皮瓣。三根克氏針分別鉆入距骨、骰骨與腓骨,利用“不接觸”牽開術牽開軟組織,充分暴露距下、跟骰關節面及跟骨外側壁,使用一枚克氏針橫穿跟骨后結節牽引,將骨刀插入塌陷的距下關節面進行撬撥,同時使用手法從兩側相向擠壓跟骨,恢復關節面平整,使用數跟克氏針將已恢復的骨折塊進行臨時固定,此時骨體遺留較大的空隙,根據術中情況進行不植入或植入同種異體骨。C形臂機透視滿意后,將外側壁骨皮質蓋回原處,根據距下關節關節面受損情況選擇合適大小的鋼板,避開骨折線打入人螺釘,再次透視,透視滿意后拔除克氏針,切口兩端放置引流片,逐層縫合后適當加壓包扎。
術后處理:患者術后保持患肢抬高,24 h后開始被動活動足趾,2 d后自主進行趾和踝活動,患肢腫脹明顯者采用甘露醇消腫,術后2~4周拆線,4周后除去石膏板,6~8周后復查X射線,骨折線模糊后撥出克氏針,術后4周開始扶雙拐下地活動,每月復查X射線,了解骨折位置及愈合情況,內固定物一般于術后1年取出。
1.3 觀察指標①圍術期相關指標。②術后疼痛情況,分別于術后1、2、3、5 d,采用視覺模擬疼痛量表(VAS)[5]對患者術后疼痛情況進行評估。③術后并發癥。④治療前后跟骨結節關節角(Bohler角)、根骨交叉角(Gissane角)變化。⑤足踝功能:術后1年,采用美國足與踝關節協會(AOFAS)踝與后足評分標準[6]評價患者治療后踝與足功能,評估項目包括疼痛、功能與自主活動、最大步行距離、地面步行、反常態步、前后活動、后足活動、踝-后足穩定性及足部對角線,總分90~100分為優、75~89分為良、50~74分為可、50分以下為差。
1.4 統計學方法采用SPSS 19.0統計學軟件分析數據。計量資料比較采用t檢驗;計數資料比較采用χ2檢驗;重復測量數據比較采用方差分析及LSD-t檢驗。P< 0.05為差異有統計學意義。
2 結果
2.1 兩組圍術期相關指標比較撬撥復位組手術時間及術后住院時間均短于切開復位組(P< 0.05),見表2。
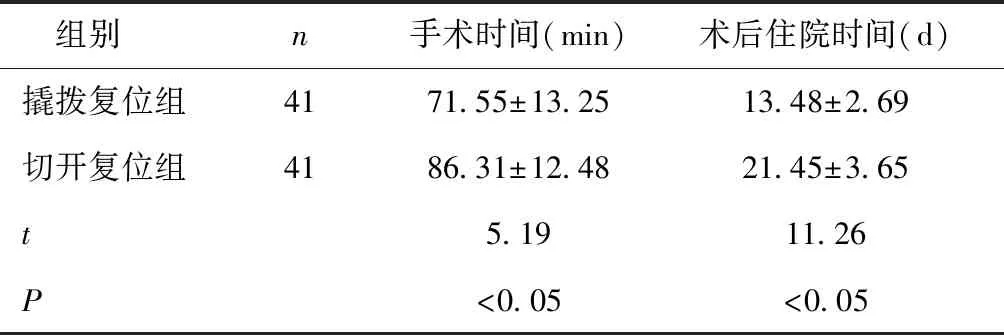
表2 兩組圍術期相關指標比較
2.2 兩組術后疼痛情況比較術后1、2、3、5 d,兩組患肢疼痛程度均呈下降趨勢,組內不同時間點比較差異有統計學意義(P< 0.05),撬撥復位組術后不同時間點疼痛程度均輕于切開復位組(P< 0.05),見表3。

表3 兩組術后疼痛情況比較 (分)
2.3 兩組Bohler角、Gissane角比較兩組治療后Bohler角及Gissane角均較治療前增大(P< 0.05),但組間比較差異無統計學意義(P> 0.05),見表4。
2.4 兩組術后并發癥比較撬撥復位組術后并發癥發生率低于切開復位組(χ2=4.99,P< 0.05),見表5。
2.5 兩組足踝功能評分比較術后1年,兩組患者足踝功能比較,差異無統計學意義(P> 0.05)。見表6。

表4 兩組Bohler角、Gissane角比較

表5 兩組術后并發癥比較 [n(%)]

表6 兩組足踝功能評分比較
3 討論
跟骨是足部最大的跗骨,是身體的負重骨,跟骨骨折是一種常見的復雜性骨折,其治療手段多樣,包括保守治療、手術治療、微創治療等,但其治療方法及評價標準依舊尚未形成同一標準[7~9]。本文對比撬撥復位空心螺釘術與切開復位術在Sanders II、III型跟骨骨折中的應用效果,發現兩術式在恢復跟骨解剖形態、改善足踝功能中的療效相似,切開復位后骨折位置好,關節面不易塌陷,利于術后關節功能的恢復,但切開復位術后并發癥多,而撬撥復位空心螺釘術術后并發癥少,手術時間短,具有微創優勢,但其適用范圍有限。
跟骨體呈不規則長方形,上方有與距骨關節相連接的三個關節面,前方有一關節面與骰骨相連,形成骰關節,與其他部位共同構成足縱弓[10~12]。跟骨大部分由松質骨構成,外周包圍一層極薄的骨皮質,僅在后關節面前下方及骨結節后下方骨皮質稍厚,跟骨骨小梁主要分為張力骨小梁與壓力骨小梁,由距骨向下呈輻射狀分布,分為前、中、后三束,跟骨三束骨小梁在跟骨溝下方形成一個尖端向上的三角形骨小梁分布稀少的空間,醫學上將其命名為“中和三角區”,是跟骨結構的薄弱部分,等跟骨承重或遭受暴力襲擊時,容易出現壓縮坍塌[13]。跟骨骨折的治療主要是恢復跟骨解剖結構,包括跟骨關節面、跟骨外形及其周圍結構,以使得后足生物力學特點得以恢復,患者能夠進行早期功能鍛煉與下地負重。
切開復位術中所用跟骨鋼板具有分叉角度大、厚度薄,易于塑型,中部結構堅強、組織相容性好等特點,鋼板分前、中、后三部分,前部有水平翼與垂直翼,水平翼可固定到骰骨外側,垂直翼可固定于跟骨前部,鋼板中部可用經鋼板螺釘固定載距突,鋼板后部由上、中、下三壁組成,上臂用于與骨丘部固定,中壁用于與骨舌形骨塊固定,下臂用于與骨外下粗隆骨折塊固定,前后、上下同時固定形成三維成型,是跟骨復位的關鍵。加上切開復位可在直視下準確進行骨折復位,鋼板固定后可與骨頭融為整體,關節面不易塌陷,利于早期功能鍛煉,可避免關節僵硬。本文切開復位組患者行手術治療后,Bohler角及Gissane角增大,術后1年足踝功能優良率達到82.93%,與Okuizumt等[14]研究結果一致。
但切開復位術術后并發癥較多,本文切開復位組中發生的并發癥包括皮緣壞死、感染、神經損傷、肌腱炎、延遲愈合。切開復位術后中不同的入路方式均易損傷正常神經,其中跟骨外側入路常損傷腓腸神經,內側入路可損傷脛后神經等內側血管神經束;跟骨外側軟組織較薄,移動性差,切口水平段位置偏上易損傷跟外側血管及皮神經,減少局部皮膚供血,造成傷口愈合延遲;術后皮瓣壞死常與術后暴露不巧當、操作粗魯、前拉力過大或牽拉時間過長等因素相關。
撬撥復位空心螺釘術屬于微創治療,其能有效減少術中軟組織損傷,避免切開復位術后高發的并發癥,本文撬撥復位組中僅有1例術后發生感染。撬撥復位后以克氏針內固定時穿入距骨后,有支撐點的作用,多枚克氏針固定較大骨塊后,起到支架作用,其形成的立體結構能有效固定骨結節骨折塊及舌狀骨折塊,對抗由于肌腱牽引引起的移位,并有效防止繼發性跟腱膜炎引起的疼痛。本文撬撥復位組患者術后疼痛程度顯著輕于切開復位組,提示撬撥復位的微創優勢。
撬撥復位空心螺釘術采用閉合復位方式,較傳統切開復位術創傷小,降低對骨折端神經肌肉組織、血管的損傷,有助于足踝功能恢復,但由于其缺乏有效的工具將外側壁復位,導致患者術后足踝功能未能恢復正常,故本文撬撥復位術患者與切開復位組的足踝功能恢復程度幾乎一致。
綜上所述,切開復位術與撬撥復位空心螺釘術均能有效恢復跟骨骨折患者解剖學結構,治療跟骨骨折,切開復位術骨折復位準確性好,鋼板固定后關節面不易塌陷,利于后期足踝關節功能的恢復,而撬撥復位空心螺釘術具有微創優勢,可減少術后并發癥,縮短手術及術后住院時間。

