兩種肌萎縮側索硬化基因表達譜差異性比較
林啟鵬,朱 茜,馬立偉
運動神經元病是指一類能快速進展的致死性神經變性疾病,能引起大腦皮質、腦干及脊髓運動神經元變性[1-3]。肌萎縮側索硬化是最常見的運動神經元病,能引起患者肌萎縮、肌無力、構音障礙和呼吸衰竭,通常不伴有感覺受累。大部分肌萎縮側索硬化患者在確診后2~5年死亡,在美國和歐洲肌萎縮側索硬化的發病率分別是5/10萬和2/10萬;其中約10%為家族性肌萎縮側索硬化,其余均為散發性肌萎縮側索硬化[1-3]。研究發現,利魯唑及依達拉奉能延緩肌萎縮側索硬化病進展,已被美國FDA批準用于治療該病。目前尚無其他治愈方法[1-3]。
SOD1基因突變是首個被證實與肌萎縮側索硬化疾病發生相關的基因突變位點[4]。隨著對肌萎縮側索硬化疾病的認識,越來越多的基因被發現與肌萎縮側索硬化相關,包括SOD1、C9orf72、CHMP2B、FUS及TDP-43等[4,5]。C9orf72 和 CHMP2B突變已被證實與額顳葉癡呆及肌萎縮側索硬化相關[6,7];Cox等[7]發現CHMP2B突變的肌萎縮側索硬化主要表現為下運動神經元綜合征;而C9orf72突變的肌萎縮側索硬化表現為上下運動神經元均受累[4-6]。本研究通過比較C9orf72 和 CHMP2B突變肌萎縮側索硬化的表達譜差異來尋找用于診斷及治療肌萎縮側索硬化的靶點。
1 材料及方法
1.1 差異基因的分析 在GEO數據庫中(http://www.ncbi.nlm.nih.gov/geo/)使用“amyotrophic lateral sclerosis”進行檢索,獲取2個數據集(GSE68605 and GSE19332),并從中挑選C9orf72突變及CHMP2B突變的樣本。從昂飛公司官網下載基因注釋文件,使用R軟件(3.5.0版本)對樣本進行分析[8,9]。
1.2 功能富集分析 對獲得的差異基因采用在線工具DAVID(https://david.ncifcrf.gov/)進行功能富集分析,獲取GO分析及KEGG通路分析結果[10]。
1.3 蛋白互作網絡及關鍵蛋白的篩選 使用在線功能STRING(http://string-db.org/)及Cytoscape 3.6.1軟件進行分析及可視化蛋白互作網絡[10];使用Cytoscape 3.6.1軟件中的插件cytoHubba進行關鍵蛋白的篩選[10,11]。
2 結 果
2.1 納入樣本信息 從GEO數據庫中獲得2個數據集(GSE68605 and GSE19332),從中我們獲得了11個獨立樣本,其中包含8個C9orf72突變型肌萎縮側索硬化和3個CHMP2B突變肌萎縮側索硬化。該樣本的組織均來源于死后患者頸段脊髓的運動神經元。
2.2 差異基因分析 經過分析,共發現13個差異基因,其中在C9orf72突變型肌萎縮側索硬化中表達水平上升的有CALM2、CALM1、CALM3、MT1X、RP11-480A16.1和RYR2;表達水平下降的有SLIT2、SEZ6L、SEC22B、WTAP、SAMD12、MALAT1和RAP1GDS1(圖1)。
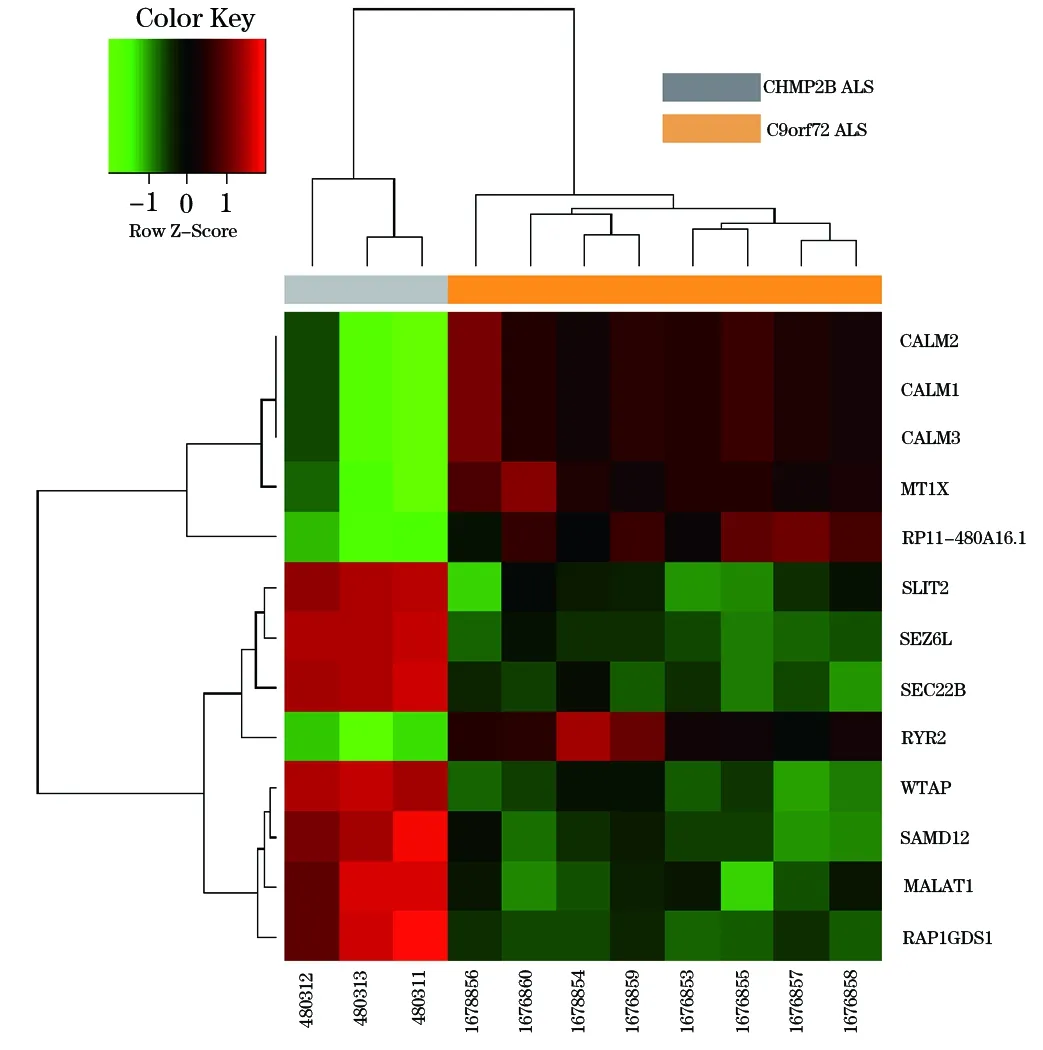
圖1 兩種肌萎縮側索硬化差異基因的熱點分析
2.3 差異基因功能分析 獲得的13種差異基因經DAVID分析后發現僅有CALM2、CALM1、CALM3 和 RYR2能夠被分類。而這些基因主要參與鈣離子檢測、通過調控靜息態鈣離子來調節心肌的收縮、調節心率、正向調節環核苷酸代謝過程及鈣調通路等生物學過程。同時參與了晝夜調節、心肌細胞中的腎上腺素通路、光傳導、催產素信號通路及鈣信號通路等生物學通路。GO分析及KEGG分析的前10結果,見表1、2。
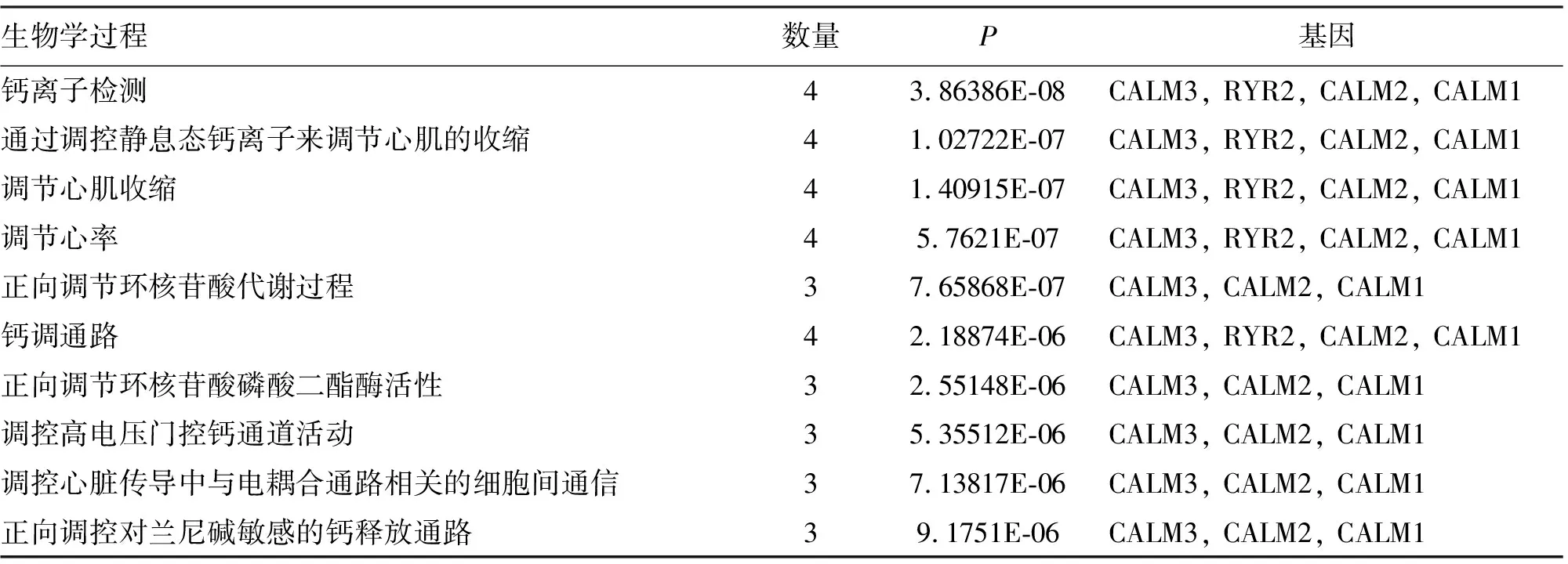
表1 兩種肌萎縮側索硬化差異基因的功能富集分析(GO分析)

表2 兩種肌萎縮側索硬化差異基因所涉及的生物學通路(KEGG分析)
使用STING及Cytoscape軟件分析蛋白互作網絡,并使用cytoHubba中的不同算法計算前10關鍵蛋白,結果發現在 MCC、Betweenness、BottleNeck、Closeness、Degree和EPC算法中,CALM1、CALM2和CALM3均位于前10的關鍵蛋白。圖2展示了不同算法中的前10關鍵蛋白。
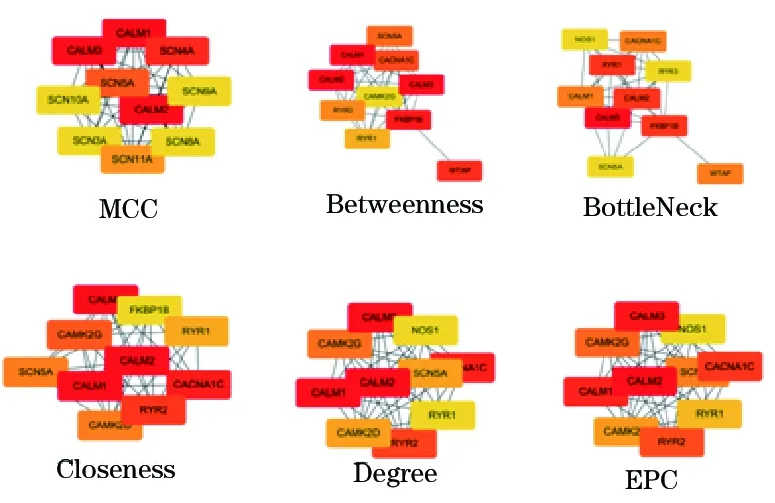
圖2 兩種肌萎縮側索硬化cytoHubba算法計算出的前10關鍵蛋白
3 討 論
本研究通過生物信息學分析C9orf72突變肌萎縮側索硬化及CHMP2B突變肌萎縮側索硬化的表達譜差異,從而尋找用于診斷及治療肌萎縮側索硬化的生物標志物及治療靶點。分析后發現在C9orf72突變肌萎縮側索硬化樣本中有6個表達水平升高的基因及7個表達水平下降的基因。對其功能進行分析發現主要影響鈣離子通路,并且CALM3、CALM2和CALM1是引起兩種疾病差異的關鍵蛋白。
CALM1、CALM2和CALM3基因能編碼鈣調蛋白;鈣調蛋白又被稱為delta磷酸化酶激酶,它在多種生物學過程中起著重要的作用,如神經生長、代謝、細胞凋亡、肌肉收縮、細胞內運動、短期和長期記憶、以及免疫反應等[12,13]。鈣調蛋白在腦及心臟中大量存在,而且在多種心臟及癌癥疾病中均發現CALM基因的突變[12,13]。在心臟疾病合并有兒茶酚胺型多形性室性心動過速、長QT綜合征或特發性心室顫動的患者常發現有CALM基因突變[13]。在中樞神經系統中,鈣調蛋白與突觸可塑性及細胞骨架重塑有關[12,14-17]。在以往報道中發現,與健康人相比,散發型肌萎縮側索硬化患者的鈣調蛋白表達水平下降,但在這些散發的患者中著重排除了SOD1、TARDBP、FUS、VCP、OPTN、UBQLN2或者C9orf72突變的患者[14]。我們發現,鈣調蛋白在C9orf72突變肌萎縮側索硬化患者中表達水平升高,其原因可能與肌萎縮側索硬化患者上運動神經元受損相關。
本研究采用生物信息學方法分析兩種類型肌萎縮側索硬化的表達譜差異,獲得可能的發病機制及治療的靶點。但納入樣本數少,未經過體內及體外實驗的驗證,可能會對結果造成影響,希望將來有更多的數據可用于分析。
總之,在C9orf72突變肌萎縮側索硬化患者中,CALM基因表達水平上調,這一關鍵蛋白可能是肌萎縮側索硬化發病的重要機制,也可能是治療該類疾病的重要靶點。

