桑葉提取物對大鼠體內細胞色素P450酶活性的影響
盛晨鳴,施曉艷,丁澤賢,陳云娜,彭代銀,陳衛東
(1.安徽中醫藥大學藥學院,安徽 合肥 230012;2.安徽省中醫藥科學院,安徽 合肥 230012)
桑葉為桑科植物桑(MorusalbaL.)的干燥葉,中醫又稱“鐵扇子”。《神農本草經》最早記載其“氣味苦甘寒,有小毒,主寒熱出汗”,具有疏散風熱的功效,可用于治療風熱感冒[1]。此外,《本草綱目》有明確記載:“桑葉乃手、足陽明之藥,治勞熱咳嗽,明目長發,止消渴。”現代研究表明,桑葉具有降血糖[2]、降血脂[3]等作用,是臨床常見的中藥之一。
隨著臨床上聯合用藥現象的普遍化,藥物間發生相互作用的頻率也越來越大。代謝性相互作用主要是由于藥物對代謝酶產生誘導或抑制作用所致,細胞色素P450酶(cytochrome P450,CYP450)起著重要作用[4]。藥物代謝酶被抑制或者誘導是引發藥物相互作用的關鍵機制。據統計有70%藥物相互作用是由于代謝酶被抑制所引起的,代謝酶被誘導的約占23%,其他約占7%[5]。
本研究參考相關文獻[6-9],采用“Cocktail”探針藥物法研究桑葉水提物(aqueous extract of mulberry leaves,AML)和桑葉醇提物(ethanol extract of mulberry leaves,EML)對大鼠體內CYP450同工酶活性的影響。通過使用安非他酮、非那西丁、雙氯酚酸鈉這3種探針底物初步探討桑葉提取物對大鼠體內CYP450酶活性的影響。
1 材料
1.1 儀器 超高液相色譜-質譜聯用儀:美國 Agilent 公司;API 4500 3Q/MS,美國AB SCIEX公司。TG16-WS 臺式高速離心機:長沙湘儀離心機儀器有限公司;KAB135-S型十萬分之一電子天平:德國METTLER TOLEDO公司;XW-80A 微型旋渦混合儀:上海滬西分析儀器廠有限公司;LC-4016 型低速離心機:安徽中科中佳科學儀器有限公司。
1.2 藥品與試劑 桑葉采摘于安徽省大別山地區,經安徽中醫藥大學俞年軍教授鑒定為桑科植物MorusalbaL.的干燥葉。非那西丁(純度≥98.0%,批號 100095-201502)、雙氯酚酸鈉(純度≥99.9%,批號 10033-200302)、安非他酮(純度≥99.9%,批號 100671-200301)標準品:中國食品藥品檢定研究院;格列本脲標準品(純度≥98.0%,批號 10238-21-8):上海源葉生物科技有限公司;氯化鈉注射液(批號 L216061408):安徽豐原藥業有限公司;甲酸:江蘇強盛功能化學股份有限公司;鹽酸:上海振企化學試劑有限公司;甲醇、乙腈(色譜純):德國Merck公司。
1.3 實驗動物 24只SD雄性大鼠,體質量為(200±20)g ,由安徽醫科大學試驗動物中心[生產許可證號為SCXK(皖)2011-002]提供。動物飼養環境:相對濕度(50±5)%,溫度(25±2)℃。
2 方法
2.1 色譜條件 色譜柱:ACQUITY UPLC BEH C18(2.1 mm×50 mm,1.7 μm);流動相:0.1%甲酸水溶液-乙腈;梯度洗脫程序:0.01~1 min,10%~80%乙腈;1~1.3 min,80%乙腈;1.3~2.0 min,80%~95%乙腈;2.0~3.0 min,95%~90%乙腈;3.0~3.5 min,90%乙腈,3.5~5.0 min,90%~10%乙腈。流速:0.2 mL/min;進樣體積:2 μL;柱溫:30 ℃。
2.2 質譜條件 離子化方式:電噴霧離子化(electron spray ionization,ESI),電多反應離子檢測(multiple reaction monitoring,MRM)。毛細管電壓:3.60 kV,離子源溫度:400 ℃,去溶劑化溫度:500 ℃。各成分質譜相關參數,見表1。
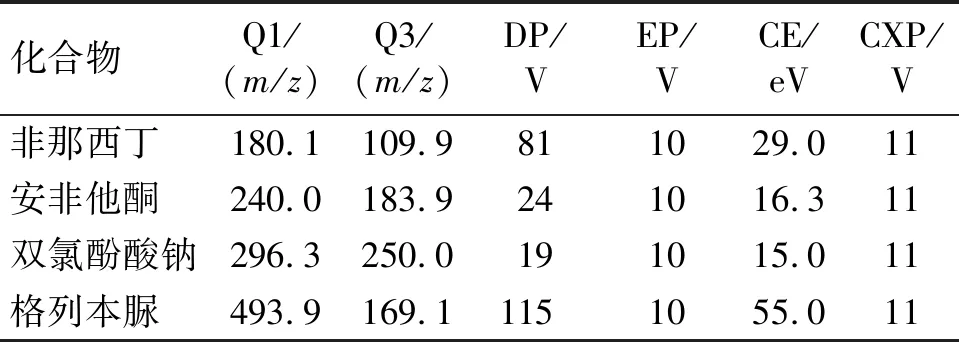
表1 探針藥物及內標格列本脲的質譜相關參數
2.3 溶液配制
2.3.1 桑葉提取物的制備 AML:取適量桑葉與鹽酸水溶液(pH=2)按料液比1∶25,在70 ℃條件下回流提取2次,每次2.5 h,合并濾液,旋轉蒸發后進行真空干燥;EML:取適量桑葉與95%乙醇按料液比1∶15,回流提取2次,提取溫度為85 ℃,每次1.5 h,合并兩次濾液,旋轉蒸發儀后真空干燥。臨用前AML組用9.0 g/L氯化鈉注射液(normal saline,NS),EML組用羧甲基纖維素鈉(carboxymethylcellulose sodium,CMC)配制成0.2 g/mL(以桑葉生藥量計)備用。
2.3.2 探針底物混合溶液的配制 在避光條件下分別精密稱取安非他酮、非那西丁、雙氯酚酸鈉標準品15.04、15.12、14.99 mg置于50 mL棕色容量瓶中,精密加入0.50 mL無水乙醇,滴加20 μL吐溫-80助溶,用生理鹽水定容至刻度后混勻,超聲,配制成質量濃度為0.3 mg/mL的“Cocktail”混合探針藥物溶液,實驗當天現配現用。
2.3.3 內標溶液配制 在避光條件下精密稱取格列本脲對照品5 mg置于10 mL棕色容量瓶中,用甲醇溶液先溶解后定容至刻度,混勻配制成500 μg/mL的格列本脲儲備液。吸取格列本脲溶液適量,用甲醇稀釋配制成500 ng/mL的格列本脲內標溶液。
2.4 分組給藥及樣品采集 將24只SD雄性大鼠隨機分為EML組、AML組、NS組、CMC組,每組6只。適應性飼養3 d后于每日早晨按照1 g/kg給藥量灌胃桑葉提取物溶液,NS組灌胃相同容積的NS,CMC組灌胃相同容積的0.5% CMC。連續給藥14 d,第14天給藥30 min后,4組大鼠均尾靜脈注射“Cocktail”探針底物混合溶液,給藥劑量為1 mg/kg。尾靜脈注射探針底物混合溶液后的0.05、0.08、0.17、0.25、0.5、1、2、4、6、8、12 h,眼底靜脈叢取血200 μL至已提前備好的肝素化離心管中,3 500 r/min離心15 min,取血漿上清液,放于-80 ℃冰箱保存。
2.5 血漿樣品處理方法 本實驗采用蛋白沉淀法處理血漿樣品,精密吸取90 μL血漿樣品置1.5 mL離心管中,精密加入10 μL已配制的格列本脲內標溶液,再加入300 μL甲醇溶液,1 500 r/min渦旋5 min,12 000 r/min高速離心10 min,取80 μL上清液置于進樣小瓶中進樣分析。
2.6 統計學方法 根據在不同時間點采血后得出的各組探針藥物的血藥濃度,使用Origin 8.0軟件對血藥濃度-時間曲線進行擬合,使用DAS 2.0軟件擬合相關藥物代謝動力學參數包括機體總清除率(clearance,CL)、藥時曲線下面積(area under the curve,AUC)、生物半衰期(biological half time,t1/2)等。用SPSS 21.0 軟件對各探針藥物的藥物代謝動力學參數進行統計學分析,采用獨立樣本t檢驗法對AML與NS組、EML與CMC組的藥物代謝動力學參數進行統計學分析。P<0.05表示差異有統計學意義。
3 方法學驗證
3.1 專屬性考察 取大鼠空白血漿混合液,大鼠空白血漿加混合探針藥物加內標混合液,以及尾靜脈注射混合探針藥物后大鼠血漿,按“2.5”項下方法處理,采用“2.1”項下方法分析。結果表明,大鼠血漿中內源性物質不干擾色譜分析。
3.2 線性范圍考察 精密吸取大鼠空白血漿90 μL,各加入一系列不同濃度的混合探針藥物溶液10 μL,制備成安非他酮、非那西丁、雙氯酚酸鈉的系列濃度血漿樣品,按“2.5”項下方法處理血漿樣品,按“2.1”項下方法進樣測定,記錄各個峰面積,橫坐標(x)為血漿樣品標準品濃度(ng/mL),縱坐標(y)為對照品峰面積與內標峰面積之比,繪制各探針底物的標準曲線,計算各線性回歸方程,結果見表2。

表2 大鼠血漿中3種探針藥物的回歸方程和回歸系數
3.3 精密度和準確度考察 取適量探針藥物混合溶液,配置5份混合探針藥物的高、中、低、定量下限4個濃度的質控樣品,按“2.5”項下方法處理,采用“2.1”項下方法分析依次進樣測定。分別于一日內測定多次及連續3 d內測定3次,記錄各個峰面積并計算各探針底物峰面積與內標峰面積的比值,代入“3.2”項下標準曲線中得出各探針底物的濃度,計算實際測得量與加入量的比值,從而計算準確度及日間、日內精密度。結果表明該方法測得探針底物血漿樣品的日內及日間精密度均良好,能夠滿足本實驗中生物樣品的分析要求。
3.4 穩定性試驗 按“2.5”項下方法操作,經血漿樣品處理后混合探針藥物的高、中、低、定量下限4個濃度的質控樣品,分別考察血漿樣品在室溫放置2 h以及反復凍融3次的短期穩定性,以及在-80 ℃條件下放置20 d情況下的長期穩定性,依次進樣測定。結果表明穩定性良好,滿足生物樣品分析要求。
3.5 基質效應考察 取來自不同大鼠的空白血漿90 μL,分別加入各個不同濃度的探針底物混合溶液10 μL,配制成含安非他酮、非那西丁、雙氯酚酸鈉的高、中、低標準添加SD大鼠的血漿樣本,每個濃度配制6份,然后按“2.5”項下方法處理血漿樣品,按“2.1”項下方法進樣測定,記錄安非他酮、非那西丁、雙氯酚酸鈉的峰面積均為A1。另外用90 μL水代替SD大鼠空白血漿,其他步驟同上,記錄安非他酮、非那西丁、雙氯酚酸鈉峰面積均為A2,則安非他酮、非那西丁、雙氯酚酸鈉的基質效應的計算公式均為(A1/A2)×100%。采用同樣的方法計算內標格列苯脲峰面積并計算其基質效應。由結果可知,探針底物及內標的基質效應均在(100±5)%之間,即離子強度對本試驗結果測定不產生干擾,能夠滿足底物定量分析的要求。
4 結果
4.1 探針藥物的濃度-時間曲線 4組大鼠尾靜脈探針藥物后,將不同的采血點所得的血漿樣品按“2.5”項下方法進行處理,使用Origin 8.0軟件對血藥濃度-時間曲線進行擬合,結果見圖1。
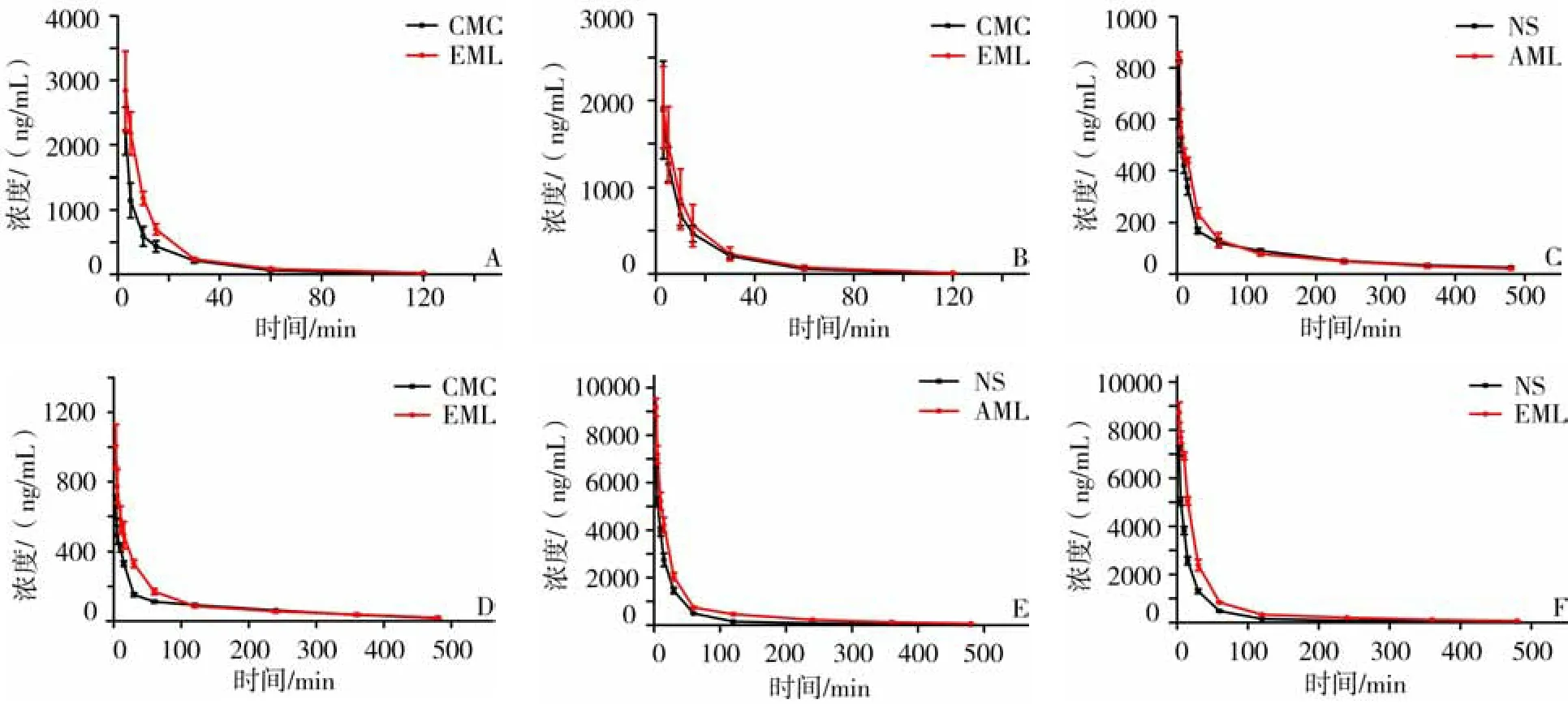
注:A. AML組非那西丁;B. EML組非那西丁;C. AML組安非他酮;D. EML組安非他酮;E. AML組雙氯酚酸鈉;F. EML組雙氯酚酸鈉
圖1探針底物在大鼠體內的濃度-時間曲線
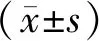
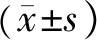
表3 桑葉提取物對非那西丁在大鼠體內藥物代謝動力學參數的影響
注:與NS組比較,*P<0.05
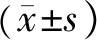
表4 桑葉提取物對安非他酮在大鼠體內藥物代謝動力學參數的影響
與CMC組比較,#P<0.05
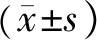
表5 桑葉提取物對雙氯酚酸鈉在大鼠體內藥物代謝動力學參數的影響
注:與NS組比較,*P<0.05;與CMC組比較,#P<0.05
5 討論
隨著中藥及中藥制劑在醫療救治中的廣泛使用,由中藥-中藥、中藥-西藥聯合用藥引起CYP450酶的誘導/抑制,產生的藥物相互作用和不良反應的事件明顯增加,受到臨床藥師和醫師的廣泛關注[10-16]。通過研究中藥對CYP450酶的調控作用可以預測中藥的某些臨床療效,揭示中藥之間及中西藥并用的相互作用,從而指導臨床合理用藥,避免藥物相互作用的發生,提高中藥使用的安全性和有效性[17-18]。因此,本研究希望通過初步探討桑葉不同提取物對大鼠體內CYP450酶活性的影響來為后期臨床聯合給藥提供一定的參考意見。
本實驗參考2015年版《中華人民共和國藥典》以確定桑葉不同提取物的給藥量[19],最終桑葉不同提取物的給藥量為1 g/kg。由于中藥多為口服,故本實驗給藥方式的選擇為灌胃給藥。本實驗參照課題組前期研究并進行驗證[20-22]。與NS組相比,CMC組中各探針底物的主要藥物代謝動力學參數無顯著差異,表明可以用0.5% CMC-Na溶液溶解難溶性藥物用于研究藥物對CYP450酶活性的影響。
CYP1A2是CYP家族中與藥物代謝關系最為密切的亞酶,其可以代謝8%~10%的上市藥物[23-24]。本實驗結果表明,連續灌胃給予桑葉不同提取物14 d后,與NS組相比,AML組中非那西丁在大鼠體內血藥濃度升高,代謝減慢,表明連續灌胃給藥AML對大鼠體內CYP1A2可能存在一定的抑制作用,而連續灌胃給藥EML對大鼠體內CYP2B1酶活性無顯著性影響。提示AML與其他通過CYP1A2酶代謝的藥物同時使用時可能需要調整劑量。另外,3種CYP1酶(CYP1A1、CYP1A2和CYP1B1)都參與各種致癌物的代謝活化,它們的誘導可能對人類健康構成嚴重危害[25]。因此,AML對其的抑制作用可能在癌癥預防中起重要作用。
CYP2B6在人體內參與某些前致癌物和毒素物質的激活而備受人們的關注。本實驗結果表明,連續灌胃給予AML對大鼠體內CYP2B6酶活性無顯著性影響,而EML中安非他酮在大鼠體內血藥濃度升高,代謝減慢,表明對大鼠體內CYP2B6可能存在一定的抑制作用。說明AML可減少機體對前致癌物和前毒性物質的代謝,對糖尿病狀態下的機體代謝可能起到一定的改善和保護作用。值得注意的是,與CMC相比,EML組中cmax增大了1.54倍,這意味著連續灌胃EML對大鼠CYP酶的活性產生了相當大的影響。因此,EML與其他通過CYP2B6酶代謝的藥物聯合使用時需謹慎,應及時調整給藥劑量并對其進行監測,避免藥物之間相互作用導致產生藥物不良反應。
CYP2C是CYP450家族中具有代表性的重要酶類,占總肝CYP含量的1/5,參與臨床藥物代謝的約有16%。在這個家族中,CYP2C9參與了多種降糖藥(如格列本脲、甲苯磺丁脲和二甲雙胍)的代謝[26]。本實驗結果顯示,連續灌胃給予桑葉不同提取物14 d后,AML和EML組中雙氯芬酸鈉在大鼠體內均存在血藥濃度升高,代謝減慢的現象,表明CYP2C6在給大鼠連續灌胃給藥AML和EML后存在一定的抑制作用。提示臨床上AML和EML與CYP2C9底物藥物聯用時,應注意及時調整劑量,避免在用藥過程中引發藥物濃度過高所引起的毒性及不良反應。
綜上所述,本研究探索藥物相互作用的方法和模型,適合初步篩選可能存在的藥物相互作用。當桑葉提取物與CYP1A2,CYP2B6,CYP2C9酶代謝的藥物聯用時,應密切關注臨床藥物-藥物的相互作用。

