不同菌種對中華稻蝗抗氧化酶活性的影響
王小莉,張雪娟,張 欣,劉慶華,張小民
(1.山西大學生命科學學院,山西太原030006;2.太原市食品藥品檢驗所,山西太原030006)
昆蟲不像哺乳動物那樣擁有完善的免疫系統,血淋巴是其參與免疫反應的主要執行者,在抵抗外源物的入侵過程中發揮重要的作用[1-2]。在生物體內,氧化應激是機體進行自我保護的一種方式,因為機體生命活動過程中會伴隨自由基的產生與消除,二者之間只有保持動態平衡,才能保證生命活動的正常進行。如果二者之間的平衡被打破,機體將會受到損傷或導致死亡。有研究表明,昆蟲體內存在超氧化物歧化酶(SOD)、過氧化物酶(POD)和過氧化氫酶(CAT)等保護酶[3-4]。生物體受到刺激后,將導致機體中抗氧化物酶系的動態平衡被打破,使得自由基的數量增加,從而引起機體的應激反應。SOD是一種以自由基為底物的抗氧化酶,與POD共同作用,清除體內產生的活性氧自由基,保護機體免受傷害[5-6]。張奎花等[5]研究表明,采用異小桿線蟲感染菜青蟲(Pieris rapae)后,體內SOD活性呈先升高后降低的變化趨勢,POD活性呈先降低后升高的變化趨勢;靳曉敏等[6]研究表明,采用2種菊酯類農藥感染鯉血清后,體內SOD活性呈下降趨勢,CAT活性呈先升高后降低的變化趨勢。可見,氧化應激在免疫防御過程中也發揮重要作用。
本研究通過給稻蝗(Oxya chinensis)注射枯草芽孢桿菌(Bacillus subtilis)和金黃色葡萄球菌(Staphylococcus aureus),并測定不同時間段稻蝗血淋巴中SOD和POD的活性,旨在為進一步研究稻蝗的免疫反應提供理論依據。
1 材料和方法
1.1 材料
供試昆蟲為中華稻蝗成蟲,于2017年9月11日采自山西省太原市晉源區(112°48′E,37°73′N)。
供試枯草芽孢桿菌菌種、金黃色葡萄球菌菌種由山西大學微生物實驗室提供;昆蟲超氧化物歧化酶酶聯免疫分析試劑盒、昆蟲過氧化物酶酶聯免疫分析試劑盒均購于上海酶聯生物科技有限公司。采用酶標儀進行測定。
1.2 方法
1.2.1 飼養方法 將從田間采回的稻蝗成蟲放置在90 cm×60 cm×60 cm的養蟲籠內,喂食新鮮的狗尾巴草,每天換草1~2次;飼養期間每隔4 h在籠外灑水以保持濕度,持續飼養7 d。
1.2.2 菌液的配制 取LB瓊脂斜面培養48 h的枯草芽孢桿菌一支和LB瓊脂斜面培養72 h的金黃色葡萄球菌一支,每種菌均用10 mL的無菌水分2次將斜面菌苔完全洗下,分別倒入含有玻璃珠的三角瓶中,做好標簽,充分振蕩,使菌落分散。吸取配好的菌液置于血球計數板計數,若濃度過高,則稀釋至菌液濃度大致為1×105個/mL。
1.2.3 供試蟲處理 試驗當天,7:00給飼養7 d的稻蝗成蟲分別注射1×105個/mL枯草芽孢桿菌菌液和金黃色葡萄球菌菌液,每只稻蝗注射20 μL,每種菌液注射100只,注射完依次放置在相應的30 cm×30 cm×30 cm的養蟲籠內,做好標簽;再取30只稻蝗放置在另一個籠中作為空白對照。在注射 4,8,12,24,48 h 時取血,將所取稻蝗的血淋巴放入PC管中,貼上標簽,放置在-80℃的冰箱中備用。
1.2.4 血淋巴中SOD和POD的酶活性測定 利用試劑盒測定血淋巴中SOD和POD的酶活性。
1.3 數據統計
試驗數據采用SPSS 22.0統計軟件進行差異顯著性分析。采用單因素方差分析法分析試驗組與空白對照組間的差異顯著性(*表示P<0.05,**表示P<0.01)。
2 結果與分析
2.1 感染菌后稻蝗血細胞中超氧化物歧化酶(SOD)活性的變化
由圖1可知,試驗組SOD活性整體高于對照組,SOD活性隨注射菌液后時間的延長呈先升高后降低的變化趨勢,其中,枯草芽孢桿菌組在12 h時活性達到最高,金黃色葡萄球菌組在8 h時活性達到最高。與空白對照組相比,枯草芽孢桿菌組在8,12,24 h 時表現出明顯的差異性(P<0.05),金黃色葡萄球菌組在8 h時表現出明顯的差異性(P<0.05),其他時間段試驗組的SOD活性均與對照組間無明顯的差異性(P>0.05)。

2.2 感染菌后稻蝗血細胞中過氧化物酶(POD)活性的變化
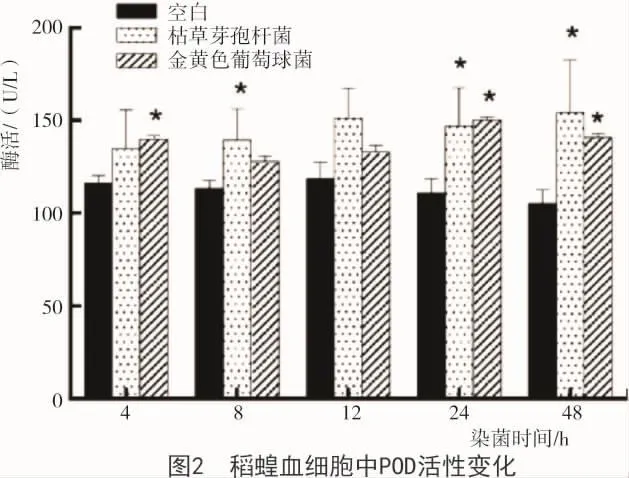
由圖2可知,試驗組POD活性均高于對照組,活性變化不穩定。與空白對照組相比,枯草芽孢桿菌組在8,24,48 h時POD活性表現出顯著性差異(P<0.05);金黃色葡萄球菌組POD活性在4,24,48 h時表現出顯著性差異(P<0.05),其余時間段與對照組相比均無明顯差異(P>0.05)。
3 結論與討論
超氧化物歧化酶、過氧化氫酶和過氧化物酶是氧化應激保護酶系統中重要的成分[9]。正常情況下,以上3種酶協調一致參與細胞內自由基的產生和消除,使生物體的自由基維持在一個相對穩定的狀態,保證生命活動的正常進行[10-11]。若自由基的清除功能出現異常,會使機體受到自由基的損傷[8]。受到異物刺激后,昆蟲體內自由基的清除將出現故障,自由基增多,使昆蟲生化反應和生理功能紊亂,機體出現病理性變化。因而,研究昆蟲的抗氧化酶系具有重要的意義。當機體中自由基數量增加時,SOD催化O2-轉化為H2O2,再由CAT或POD將H2O2分解成H2O和O2,這樣有毒性的自由基會轉化成無毒的H2O和O2,從而達到清除自由基的目的[12-17]。姬國紅等[18]研究線蟲感染菜青蟲(Pieris rapae)后體內SOD和POD活性呈現先升高后降低的趨勢。張玨鋒等[19]研究表明,綠僵菌感染褐飛虱后,褐飛虱體內的SOD活性和POD活性均顯著升高。李嘉豐等[20]研究表明,黑斑病侵染五味子后,導致五味子體內的SOD和POD酶活性顯著提高。
本研究中,稻蝗感染菌種后其血細胞中SOD活性呈現先增加后降低的趨勢,原因可能是由于菌種對稻蝗血細胞造成傷害,導致血細胞中自由基數量增加,從而使血細胞中SOD活性增加,用于清除菌種對稻蝗血細胞的氧化損傷;稻蝗感染菌種后POD活性變化不穩定,POD主要用于清除SOD作用過程中產生的H2O2,使自由基變成無毒害作用的H2O和O2。綜合2種酶活性可知,2種菌均可引起血細胞抗氧化酶活性的變化,其中,枯草芽孢桿菌對稻蝗血細胞抗氧化酶的活性影響較大。受到菌種感染后,稻蝗血細胞產生一系列的應激反應,其迅速啟動血細胞中SOD和POD清除自由基,消除自由基對機體的毒害,維持機體正常的生命活動。菌種感染稻蝗后,稻蝗血細胞中SOD和POD活性均高于對照組,可見,稻蝗血細胞可以通過提高酶活性來抵御菌種的毒害作用,這可為研究稻蝗的免疫反應提供試驗依據。

