皮質下缺血性血管病患者ApoE基因多態性及血清親環素A濃度對認知障礙的影響
王 瑤,倪明珠,劉文燦,宋莉莉,王兆平,王文靜
皮質下缺血性血管性認知障礙(subcortical ischemic vascular disease with cognitive impairment,SVCI)是血管性認知障礙的主要亞型之一,是引起老年性認知障礙的第二大原因[1],因其較高的發病率和較好的均質性[2],一直以來被研究者廣泛關注。目前SVCI發病的遺傳機制仍不清楚。載脂蛋白E(apolipoprotein E,ApoE)基因是熱門的癡呆備選基因之一,已有研究[3]證實,攜帶ApoE ε 4等位基因的皮質下缺血性血管病(subcortical ischemic vascular disease,SIVD)患者較未攜帶者出現認知障礙的風險增高,但具體機制仍不明確。而在Bell et al[4]構建的ApoE轉基因小鼠模型中顯示,親環素A(cyclophilin A,CypA)可能是ApoE ε 4等位基因引起腦血管功能異常及神經元退行性變的關鍵因子。該研究為進一步探索ApoE基因多態性及血清CypA濃度對SIVD患者認知障礙的影響,進行了下列研究。
1 材料與方法
1.1 病例資料
1.1.1SVCI組 選取2017年9月~2018年4月安徽省立醫院神經內科SIVD住院患者126例,其中SVCI組為82例。SIVD納入標準參照Galluzzi et al[5]提出的影像學標準并加以修改:① 年齡50~80歲; ② 受教育年限≥5年; ③ 頭顱磁共振(magnetic resonance imaging,MRI)檢查示腦室旁和(或)深部白質病變(white matter lesions,WML)及深部灰質多發性腔隙性梗死灶(lacunar infarcts,LI)。所有入選患者知情同意并簽署知情同意書。SVCI診斷標準為:① 符合SIVD納入標準;② 患者有明確的認知功能下降,蒙特利爾認知評估量表(montreal cognitive assessment,MoCA)量表評分<26分,記憶、視空間、語言、執行中≥1個認知領域受損;③ 保留獨立生活能力;④ 認知功能損傷與腦血管病間具有相關性:認知功能損害發生在卒中后3個月內;或無明顯腦血管病時間發生,但存在信息處理速度明顯減慢,且具有早期尿、便障礙、早期步態異常、人格和性格改變特征之一[6-7]。
1.1.2皮質下缺血性血管病無認知障礙組(SIVD withnon-cognitive impairment,SNCI)納入標準 選取同期年齡、性別相匹配,認知功能正常(MoCA量表評分≥26分)的SIVD患者44例作為SNCI組。
1.1.3排除標準 ① 有腦外傷、皮質梗死、腦出血、腦腫瘤史;② 有阿爾茲海默病、帕金森病、路易體癡呆等其他引起認知損害的疾病;③ 代謝、多發性硬化、免疫等非血管因素引起的腦白質病變;④ 有風濕結締組織及炎性疾病、傳染病史;⑤ 患有嚴重的軀體或精神疾病;⑥ 不能配合神經心理學評估者。
1.2 研究方法
1.2.1一般臨床資料的收集 收集所有入選者的年齡、性別、受教育程度、吸煙飲酒史、高血壓病史、糖尿病病史、癡呆及精神疾病家族史等一般資料,并記錄空腹血糖、血脂等指標。
1.2.2神經影像學評估 應用3.0 T MRI機(德國西門子公司)掃描,依據頭顱MRI T 2像、液體衰減反轉恢復序列成像,從皮質下LI數目及WML兩方面對所有受試者腦損傷程度進行評估。LI定義為皮質下直徑為3~15 mm、邊界清楚的缺血性病灶(皮質下和/或腦室旁)[8]。腦白質病變程度依據Fazekas et al[9]的分級方法分為3級:1級(輕度,斑點狀病變);2級(中度,病變開始融合);3級(重度,融合成彌漫性病變)。
1.2.3神經心理學評估 采用MoCA量表、日常生活活動能力量表(activity of dailyliving scale,ADL)進行整體認知功能及日常生活能力評估;應用哈金斯基缺血指數量表(hachinskiischemic score,HIS)鑒別SVCI和老年性認知障礙、漢密頓抑郁量表(hamilton depression scale,HAMD)評估抑郁狀態。
1.2.4血液標本的收集和檢測 采取受試者空腹外周靜脈血A、B兩管各4 ml,A管為聚丙烯EDTA抗凝真空采血管,4 ℃冰箱內保存,進行ApoE基因測序;B管未添加抗凝劑,采血后立即3 000 r/min離心10 min,分離血清并保存于-80 ℃冰箱中,檢測CypA濃度。
1.2.4.1ApoE基因檢測方法 采用snapshot檢測方法檢測所有受試者ApoE基因型,按試劑盒操作步驟對共ApoE共2個SNP位點擴增檢測。① 提取白細胞DNA;② PCR擴增:設計引物序列,反應條件:96 ℃、1 min,96 ℃、10 s,60 ℃、30 s,52 ℃、5 s共30個循環;③ DNA測序:取1 μl延伸產物,加10 μl高度去離子甲酰胺,95 ℃變性3 min,立即冰水浴,上測序儀(Snapshot試劑盒、3730 XL基因測序儀均購自美國ABI公司)。
1.2.4.2CypA含量測定 應用ELISA法測定血清CypA濃度。操作方法嚴格按照試劑盒(購自上海聯碩生物科技有限公司,批號:201804)說明書進行。
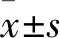
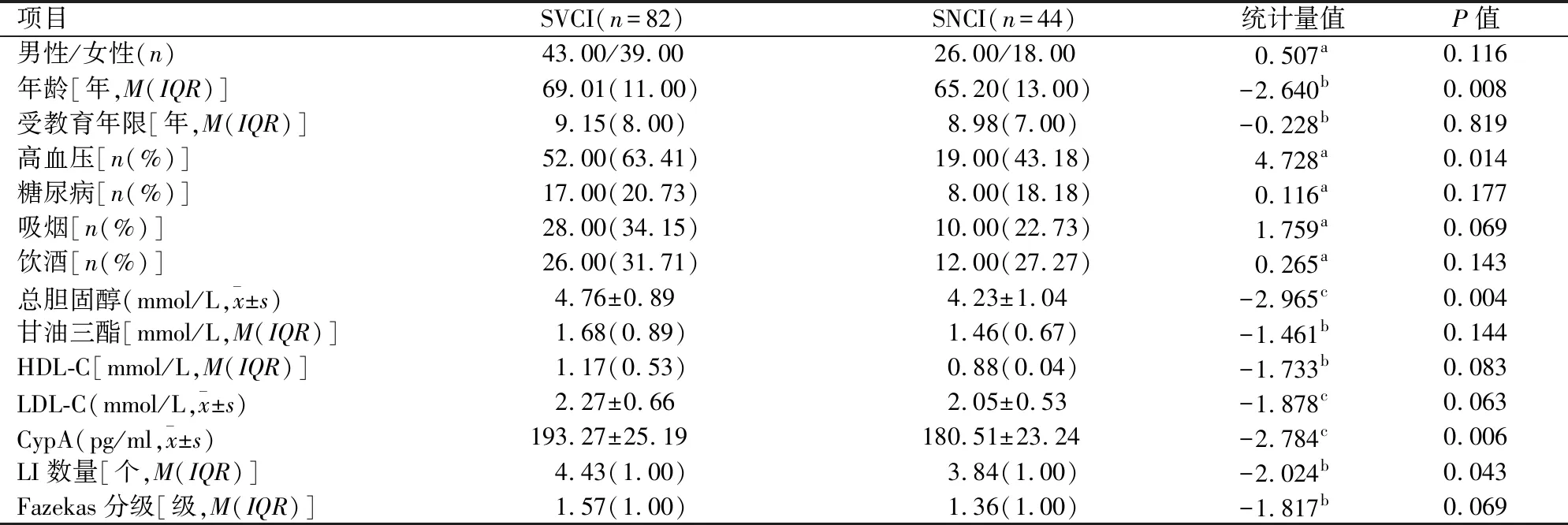
表1 SVCI和SNCI兩組一般臨床資料及血清CypA濃度比較
a采用χ2檢驗;b采用Mann-WhitneyU檢驗;c采用獨立樣本t檢驗;HDL-C:高密度脂蛋白膽固醇;LDL-C:低密度脂蛋白膽固醇
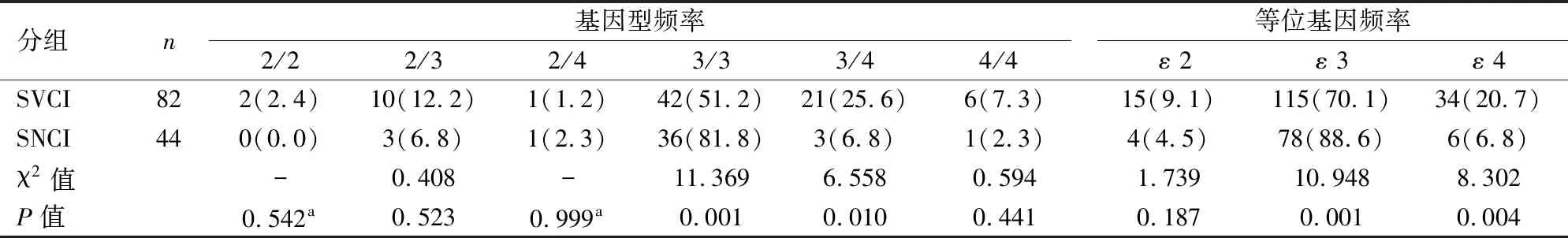
表2 SVCI和SNCI兩組ApoE基因型與等位基因頻率分布比較[n(%)]
a采用Fisher確切概率檢驗
2 結果
2.1 SVCI和SNCI兩組一般臨床資料及血清CypA濃度比較SVCI和SNCI兩組間在受教育年限、吸煙飲酒史、糖尿病比例、Fazekas分級等方面差異無統計學意義(P>0.05);與SNCI組比較,SVCI中的高血壓比例、年齡、總膽固醇水平及LI數量等方面較SNCI組高,差異有統計學意義(P<0.05)。SVCI組血清CypA濃度高于SNCI組(P<0.01)。見表1。
2.2 SVCI和SNCI兩組ApoE基因頻率的比較SVCI組中共檢出2/2、2/3、2/4、3/3、3/4、4/4 6種基因型以及ε 2、ε 3、ε 4 3種等位基因;SNCI組中共檢出2/3、2/4、3/3、3/4、4/4 5種基因型以及ε 2、ε 3、ε 4 3種等位基因。其中SVCI組中3/4基因型及ε 4等位基因頻率(25.6%/20.7%)顯著高于SNCI組(6.8%/6.8%),3/3基因型及ε 3等位基因頻率(51.2%/70.1%)明顯低于SNCI組(81.8%/88.6%),差異均有統計學意義(P<0.05)。見表2。
2.3 ε 4基因攜帶組和ε 4基因非攜帶組兩組間血清CypA濃度的比較ε 4基因攜帶組血清CypA濃度較ε 4基因非攜帶組高(ε 4等位基因攜帶組包括基因型為ApoE 2/4、ApoE 3/4、ApoE 4/4者,ε 4等位基因非攜帶組包括基因型為ApoE 2/2、ApoE 2/3、ApoE 3/3者),差異有統計學意義(P<0.01)。見表3。
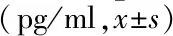
表3 兩組間血清CypA濃度的比較
2.4 SVCI組危險因素logistic回歸分析以有無SVCI作為因變量(SVCI=1,SNCI=0),將SVCI主要的危險因素進行logistic回歸分析(自變量賦值為如下:有高血壓=1,無高血壓=0;攜帶ε 4基因=1,未攜帶ε 4基因=0;其余變量均以連續性變量直接納入模型分析),結果顯示:高血壓、血清總膽固醇水平增加、血清CypA濃度的增加以及攜帶ε 4等位基因,均增加SVCI的發病風險(P<0.05)。見表4。
3 討論
ApoE基因位于19號染色體長臂上,具有ε 2、ε 3及ε 4 3種不同的等位基因,研究普遍認為在3種等位基因中,攜帶ε 4等位基因者體內LDL-C水平及出現動脈粥樣硬化的風險較高[10],且會加劇腦白質損傷、引起認知功能減退[11],與SVCI具有相關性[3]。目前為止,已有不少研究者[12-14]從顱內β淀粉蛋白沉積、動脈粥樣硬化及血腦屏障(blood-brain barrier,BBB)破壞等不同方面進行發病機制的探索,但ε 4等位基因和SVCI之間具體發病機制仍不明確。
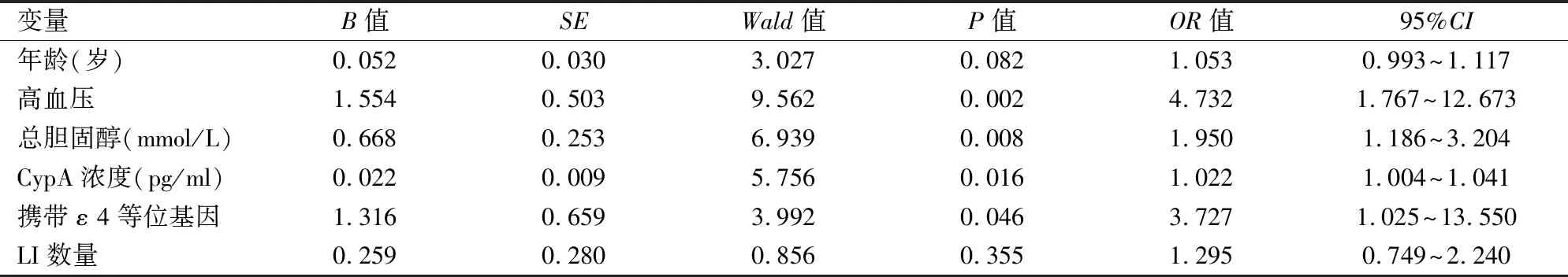
表4 SVCI影響因素多因素logistic回歸分析
CypA作為親環素家族中的一員,參與了蛋白質折疊、膽固醇的代謝、免疫功能的調節和機體炎性反應等許多生物學過程,與冠心病、系統性紅斑狼瘡等疾病關系密切[15],近年來也有研究[16]顯示CypA在腦血管病中發揮重要作用。
本研究檢測了SVCI組和SNCI組ApoE基因多態性及血清CypA濃度,旨在進一步探索SVCI與ApoE基因多態性及血清CypA濃度之間的關系。結果顯示,SVCI組患者的ε 4等位基因頻率及血清CypA濃度均高于SNCI組,提示ε 4等位基因和CypA在SVCI發病過程中可能發揮一定作用。為了進一步分析ε 4等位基因和CypA是否具有協同作用,本研究將入組患者根據是否攜帶ε 4等位基因重新分組,對兩組血清CypA濃度進行比較,結果顯示ε 4等位基因攜帶組血清CypA濃度較非攜帶者高。
通過對上述研究結果進行討論與總結,ε 4等位基因和CypA促進SVCI的發生、發展的機制可能如下:① ε 4等位基因和CypA均可引起小動脈硬化、脂質斑塊形成,導致血管管腔狹窄甚至閉塞、腦血流灌注不足,從而出現皮質下LI或白質缺血性改變,破壞額葉-皮質下環路或(和)丘腦皮質環路,表現出以執行功能受損為主的認知功能減退[6];② ε 4等位基因可通過激活CypA-MMP-9途徑,引起BBB的破壞。CypA是一種前炎癥因子,當機體在應激狀態下,由受損的血管內皮細胞或血管平滑肌細胞分泌,CypA可以促進血管平滑肌細胞中基質金屬蛋白酶(matrix metalloproteinase,MMPs),如MMP-2和MMP-9的活化[17],進而降解BBB的緊密連接蛋白、膠原蛋白IV和一些基膜蛋白,破壞BBB的完整性,從而造成神經元攝取多種血源性神經毒性物質,最終引起認知功能下降。但由于本研究樣本量有限,上述機制還需要大樣本、多中心的研究來進一步進行驗證。
同時本研究對SVCI影響因素進行了多因素分析,結果顯示除攜帶ε 4等位基因和血清CypA濃度增高外,高血壓及血清總膽固醇水平增高也會增加SVCI的發病風險,這與國內外相關研究[18-19]結果一致,故而控制上述因素對預防SVCI具有重要意義。

