每搏量變異在急性非等容血液稀釋中的應用
劉曉梅,董 蘭,靳 冰
外科大手術具有時間長、出血量大的特點,而目前血源緊張,圍術期如何實施最大限度的血液保護已成為麻醉科醫師面臨的重要問題。隨著圍術期血液保護理論與臨床研究的不斷深入,術前血液稀釋被認為是行之有效的血液保護措施[1,2]。目前,血液稀釋逐步應用于重大手術,已成為臨床中解決血源緊張和避免異體輸血的重要麻醉技術。有臨床研究指出,急性非等容血液稀釋能提高機體對失血的耐受程度,增加血液稀釋的安全性。急性非等容血液稀釋一般需要在監測中心靜脈壓(CVP)、平均動脈壓(MAP)、心率(HR)等傳統血流動力學指標下完成[3],也有研究認為,傳統的靜態指標對機體容量狀況的預測價值較低,而動態指標如每搏量變異(stroke volume variation,SVV)在預測容量反應方面有較高的靈敏性[4-6]。本研究采用SVV/MAP、HR作為監測指標,分析SVV對急性非等容血液稀釋的指導價值。
1 對象與方法
1.1 對象 選擇2017年3-12月擬在全麻下行擇期脊柱手術患者60例,其中男36例,女24例;年齡18~60歲;身高155~178 cm;體重44~82 kg;ASA分級Ⅰ~Ⅱ級;術中估計失血量≥500 ml;Hb≥100 g/L,Hct≥35%,PLT≥100×109/L,凝血功能正常。入選標準:(1)年齡18~60歲,身高155~178 cm;體重44~82 kg;(2)ASA分級Ⅰ~Ⅱ級;(3)術中估計失血量≥500 ml;(4)Hb≥100 g/L,Hct≥35%,PLT≥100×109/L,凝血功能正常;(5)患者或家屬均簽署知情同意書。排除標準:(1)高血壓、冠心病、心律失常、心內分流;(2)外周血管疾病、肝腎疾病等病史;(3)長期口服血管活性藥等藥物史。隨機分為觀察組和對照組,每組30例,兩組在性別、年齡、身高、體重等方面差異無統計學意義(P>0.05),具有可比性。本研究經醫院醫學倫理委員會批準,患者或家屬均簽署知情同意書。
1.2 方法
1.2.1 麻醉及監測 選擇全身靜脈麻醉。患者入室后常規開放外周靜脈,給予復方林格平衡液7 ml/kg輸注。采用InteHivueMP50監測儀(荷蘭Philips公司)常規監測心電圖、HR、袖帶血壓、脈搏氧飽和度及呼氣末二氧化碳分壓,并連接腦電雙頻指數(BIS)監測儀(AspectXP,美國Aspect公司)。局麻下行左或右橈動脈穿刺置管。對照組患者連接InteHivue MP50監測儀(荷蘭Philips公司)監測HR和有創MAP;觀察組患者連接FloTracTM傳感器,傳感器一端連接InteHivue MP50監測儀(荷蘭Philips公司)監測HR和有創MAP;另一端連接Vigelo/FloTrac監測儀(美國Edwards公司),連續監測CI、SV、SVI、SVV等各項指標。麻醉誘導給予咪達唑侖0.05~0.1 mg/kg,異丙酚1~2 mg/kg,舒芬太尼0.4 μg/kg,愛可松0.6 mg/kg, 靜脈快速誘導行氣管內插管,容量控制模式控制呼吸,呼吸參數:潮氣量8 ml/kg,呼吸頻率10次/min,維持呼氣末二氧化碳分壓35~40 mmHg,氧流量設定為1.0 L/min。全麻插管后微量輸注泵持續靜脈輸注異丙酚50~100 μg/(kg·min)+瑞芬太尼0.1~0.2 μg/(kg·min)維持麻醉,輸注速度根據BIS監測值進行調控,維持BIS值40~60。麻醉完畢經右頸內靜脈穿刺置管,以備血液稀釋時采血。
1.2.2 血液稀釋與采血 血液稀釋由麻醉科醫師和輸血科醫師共同實施。麻醉維持平穩后開始經頸內靜脈采血,預計采血量400 ml,采血時間15~20 min。入室后至采血前先經外周靜脈輸入復方氯化鈉溶液10 ml/kg,以補充部分禁食水所需的液體量。采血過程中,觀察組以SVV作為血流動力學監測指標,對照組以MAP和HR作為血流動力學監測指標。采血前,觀察組如SVV<10%,則開始經頸內靜脈采血,同時經外周靜脈輸入6%羥乙基淀粉(HES,200/0.5),輸注速度以維持SVV<10%為準;如SVV≥10%,則先經外周靜脈輸入HES,輸注速率為50 ml/min,待SVV<10%,再經頸內靜脈采血。采血過程中如SVV≥10%,則減慢采血速度或停止采血,同時加快HES輸注速率(50 ml/min),待SVV<10%時再繼續采血。對照組以采血前即刻的MAP為基礎值,采血速度以維持MAP波動范圍<±20%基礎值為準,如MAP波動范圍≥±20%基礎值則調整采血速度及HES輸注速度,待MAP恢復至正常范圍再繼續采血。無論采血量是否達預計值(400 ml),當觀察組SVV≥10%或對照組MAP<80%基礎值,且Hct≤25%或Hb≤90 g/L時終止采血。為避免體位對MAP和SVV的影響,采血過程中患者保持平臥位。采集的全血儲存于ACD采血袋內,4 ℃冰箱內編號保存備用,于4 h內回輸。
1.3 觀察指標 分別于采血前即刻(T0)、采血100 ml(T1)、采血200 ml(T2)、采血300 ml(T3)、采血結束(T4)5個時間點記錄兩組患者的MAP、HR或SVV、Hct和Hb數值,記錄兩組患者的采血時間、采血量、采血結束時HES用量及尿量。
2 結 果
2.1 采血相關指標比較 觀察組平均采血量明顯高于對照組,差異有統計學意義(P<0.05)。觀察組輸入HES量顯著高于對照組,差異有統計學意義(P<0.05,表1)。兩組采血時間、尿量比較,差異均無統計學意義。
表1 兩組手術患者HES入量、采血量、采血時間及尿量比較

表1 兩組手術患者HES入量、采血量、采血時間及尿量比較
組 別采血量(ml)HES用量(ml)采血時間(min)尿量(ml)觀察組396±91①476±101①15±638±4對照組357±86 399±87 14±736±5
注:與對照組比較, ①P<0.05
2.2 血流動力學指標對比 觀察組中,與T0相比,T1~T3SVV差異無統計學意義,T4時SVV為(9.8±1.2)%,顯著高于T0時的(5.5±1.3)%,差異有統計學意義(P<0.05)。對照組中,T1和T0時相比,MAP及HR差異無統計學意義;T2-T4時MAP顯著低于T0,HR顯著高于T0,差異有有統計學意義(P<0.05,表2)。
表2 兩組手術患者采血前后各時間點血流動力學指標比較

表2 兩組手術患者采血前后各時間點血流動力學指標比較
指標觀察組對照組MAP(mmHg) T079.2±12.280.6±12.1 T178.3±11.879.3±11.1 T277.5±11.471.8±11.2① T370.9±9.865.6±8.1① T468.4±5.760.0±5.3①HR(次/ min) T071.3±12.670.5±13.4 T172.4±11.872.8±11.5 T273.0±11.977.6±12.7① T378.1±12.385.2±11.3① T481.3±11.287.9±11.5①SVV(%) T05.5±1.3 T16.1±1.1 T26.9±1.0 T37.2±0.7 T49.8±1.2①
注:與T0比較,①P<0.05
2.3 采血前后各時點Hct及Hb比較 T0-T1時點兩組Hb及Hct比較,差異無統計學意義,T2-T4時點觀察組Hb及Hct均顯著低于對照組,差異有統計學意義(P<0.05,表3)。
表3 兩組手術患者采血前后各時點Hct及Hb比較
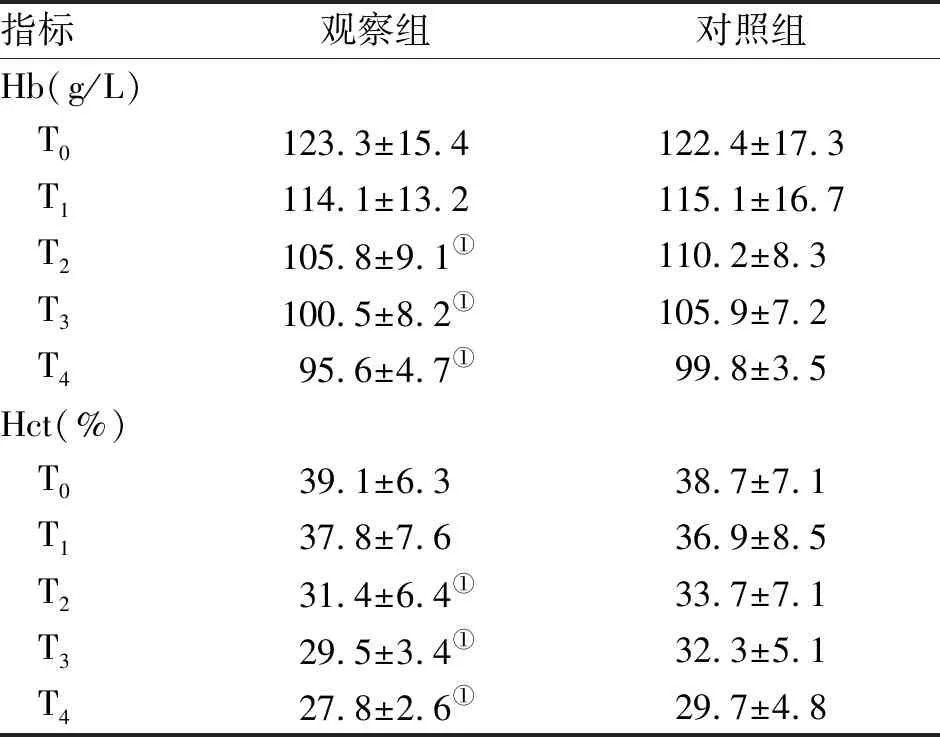
表3 兩組手術患者采血前后各時點Hct及Hb比較
指標觀察組對照組Hb(g/L) T0123.3±15.4122.4±17.3 T1114.1±13.2115.1±16.7 T2105.8±9.1①110.2±8.3 T3100.5±8.2①105.9±7.2 T495.6±4.7①99.8±3.5Hct(%) T039.1±6.338.7±7.1 T137.8±7.636.9±8.5 T231.4±6.4①33.7±7.1 T329.5±3.4①32.3±5.1 T427.8±2.6①29.7±4.8
注:與對照組比較,①P<0.05
3 討 論
近年來,隨著圍術期血液保護理論與臨床研究的不斷深入,血液稀釋已成為圍術期減少異體血用量、降低輸血危害、提高麻醉質量的重要麻醉技術[7,8]。圍術期血液稀釋主要有3種形式[9]:急性等容血液稀釋、急性高容血液稀釋和急性非等容血液稀釋。有研究指出,急性非等容血液稀釋能夠進行有效的急性血液稀釋,既可減少術中有效成分的丟失,又能提高循環的穩定性,還可增強抗出血的儲備能力[1]。Hobisch等[10]研究認為,血液稀釋后黏稠度降低,尤其是紅細胞聚集降低,靜脈血流增加,心排量增加和外周血管阻力降低,可改善組織氧供,使代償血液攜氧能力的降低,故可避免組織器官缺氧的發生。文獻[11]報道,采血400~600 ml循環血流未出現較大變化;但血液稀釋時血液黏稠度降低,使外周血管阻力降低,后負荷減少,靜脈回流增加,從而可使每搏量增加,心排量增加。但王清秀等[12]認為,雖然機體能通過攝氧率和心輸出量的升高進行代償以耐受一定程度的血液稀釋,但在極度血液稀釋時,心臟射血和心室功能不再繼續升高反而開始下降,心臟不再代償。因此,有效的血流動力學監測是血液稀釋中維持循環動力學穩定、保證組織氧供、避免組織器官缺氧發生的重要保證。
目前臨床血流動力學監測指標有多種,如血壓、HR、CVP等傳統指標,但這些指標對容量的評估具有一定的局限性[13,14],不能完全反映容量狀態,可能誤導臨床治療[15]。有研究認為,動態血流動力學指標如SVV能預測機械通氣患者血流動力學變化,且預測容量反應的能力優于靜態指標CVP等[16-19],以其作為液體治療目標可以預防潛在的容量不足或容量過量,使液體治療個體化,減少并發癥的發生[20],有研究機構將其推薦為大手術過程中標準治療策略的監測指標[21]。
本研究中,兩組患者的一般情況及采血時間無顯著差異,采血初始時T0-T1時點兩組Hb及Hct比較,差異無統計學意義,而觀察組和對照組平均采血量分別為(396±91)ml和(357±86)ml,觀察組采血量顯著高于對照組,T2-T4時點觀察組Hb及Hct顯著低于對照組,但均在安全范圍,這與李衛等[22]的研究結果相似。觀察組和對照組稀釋用HES平均每例輸入量分別為(476±101)ml和(399±87)ml,觀察組輸入HES量顯著高于對照組,說明在SVV的指導下,觀察組通過輸入更多的HES液,對血液進行了更充分的稀釋,從而采集到了更多的自體血。在血液稀釋過程中,觀察組T1-T3時點SVV與T0相比差異無統計學意義,僅T4時點SVV顯著高于T0時點,而對照組除T1時點外,T2-T4時點MAP顯著低于T0時點、HR顯著高于T0時點,表明血液稀釋過程中觀察組血流動力學比對照組穩定,說明觀察組在SVV的指導下及時有效地對血容量進行了補充。且HES液的輸注量觀察組比對照組大,對于穩定血流動力學起到了關鍵作用,說明急性非等容血液稀釋中應用SVV作為血流動力學監測指標,比MAP及HR能更好地預測血液稀釋過程中的容量不足,并能及時指導液體補充,維持血流動力學的穩定。另外,血液稀釋過程中,兩組采血量、膠體液輸入量及各時點Hb及Hct的顯著差異,表明SVV指導的急性非等容血液稀釋能有效優化液體輸入量及液體配比,在維持血流動力學穩定的同時,增加了采血量,避免了血源的浪費。
綜上所述,術中行急性非等容血液稀釋時,以SVV作為血流動力學監測指標,與MAP、HR相比,可更好地維持血流動力學穩定,在增加采血量的同時還能有效優化液體輸入量及液體配比,使患者容量狀況處于一種理想狀態,在急性非等容血液稀釋的安全實施中具有較好的指導作用,下一步我們將擴大樣本進行更深入地研究。

