系統性紅斑狼瘡早發動脈粥樣硬化模型小鼠的建立
郭曉玲,朱春紅
系統性紅斑狼瘡(systemic lupus erythematosus,SLE)是自身免疫介導的,以免疫性炎性反應為突出表現的彌漫性結締組織病,可造成皮膚、腎臟、血液等全身多系統受累。近年發現,SLE患者發生動脈粥樣硬化的風險顯著增加, 50%以上患者存在中到重度動脈粥樣硬化,已成為導致死亡的主要原因[1]。目前該病尚無根治辦法,而且常用治療藥物均不理想,不良反應較多,嚴重影響遠期預后和生存質量。造成這些問題的根本原因是該病發生機制復雜,人們對其發病規律及影響因素還缺乏全面認識。因此,揭示SLE早發動脈粥樣硬化的核心發病機制,對于發現藥物靶點和疾病治療具有重要意義。本研究通過小鼠模型的建立初步探討SLE早發動脈粥樣硬化。
1 材料與方法
1.1 試劑與儀器 降植烷購自Sigma公司;三酰甘油(triglyceride, TG)、總膽固醇(total cholesterol, TC)、低密度脂蛋白膽固醇(low density lipoprotein cholesterol ,LDL-C)、高密度脂蛋白膽固醇(high density lipoprotein cholesterol ,HDL-C)、尿素氮(blood urea nitrogen ,BUN)、肌酐(creatinine, CRE)定量試劑盒等購自南京建成公司;蘇木精-伊紅(HE)染色試劑盒購于beyotime公司。
1.2 方法 選擇10只ApoE-/-敲除小鼠(ApoE-/-,C57BL/6背景,12周齡,雌性)為實驗組,10只C57BL/6小鼠為對照組,體質量(22±2)g,均購自天津市奧臣實驗動物銷售有限公司(動物批號1601826)。適應性飼養2周后開始實驗,實驗過程中對動物的處置符合倫理學標準。實驗組ApoE-/-小鼠一次性腹腔注射降植烷0.5 ml/只,再高脂喂養8周建立模型,對照組C57BL/6小鼠腹腔注射等量生理鹽水,每組10只。實驗過程中觀察小鼠毛發、飲食、活動狀況等一般情況,繪制體重變化曲線。實驗結束后眼球取血,12 000 r/min離心,10 min,分離血清,凍存備用。同時,取各組小鼠腎臟組織,置中性甲醛固定24 h,石蠟包埋,切片, HE染色,80%、90%、95%、100%乙醇梯度脫水,二甲苯透明,中性樹膠封片,鏡下觀察各組小鼠腎臟組織形態變化。
1.3 觀察指標 取兩組小鼠外周血樣本,根據試劑盒說明書,采用分光光度計檢測血清TG、TC、LDL-C、HDL-C、CRE、BUN及腎功能指標。
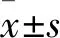
2 結 果
2.1 小鼠腎功能與血脂水平檢測結果 實驗組小鼠毛色暗淡甚至剝脫,活動減少,一般狀態較差。實驗組CRE、BUN腎功能指標明顯惡化,同時TC、TG及LDL-C水平均顯著升高,而HDL-C水平明顯降低,與對照組比較差異均有統計學意義(P<0.01,表1)。
2.2 組織形態學變化 HE染色結果顯示,實驗組腎小球細胞增多、腫大,可見大量炎性細胞浸潤,腎小管空泡變性,基底膜異常增厚,系膜增生(圖1)。
表1 兩組小鼠腎功能、血脂水平比較

表1 兩組小鼠腎功能、血脂水平比較
指標對照組實驗組CRE(μmol/L)3.48±1.0336.87±3.89①BUN(mmol/L)1.86±0.9512.72±3.09①TC(mmol/L)6.52±3.4017.53±2.32①TG(mmol/L)0.49±0.14 1.30±0.21①LDL-C(mmol/L)0.30±0.301.25±0.33①HDL-C(mmol/L)1.66±0.17 0.79±0.17①
注:與對照組比較,①P<0.01

圖1 兩組小鼠腎臟組織HE染色特點(HE,×400)
3 討 論
SLE是一種以產生自身抗體,免疫復合物沉積,巨噬細胞組織浸潤及組織損傷為特點的自身免疫性疾病,近年來,隨著醫學迅速發展,其預后顯著改善,生存期和總體預后均有所提高。但是,生存期延長易導致患者重要臟器,如心血管受累,使得動脈粥樣硬化性心血管疾病成為SLE疾病后期最重要的并發癥之一,亦成為SLE遠期死亡的主要原因[2]。進一步揭示,SLE本身引起的慢性血管炎性反應性改變和長期的免疫系統紊亂是導致SLE患者動脈粥樣硬化性疾病發病增加的一個主要原因,即使努力控制已知危險因素后, SLE 患者出現心血管事件的相對危險率仍高出健康人10倍。因此,SLE早發動脈粥樣硬化的研究日益受到關注,而理想的動物模型是對深入探討疾病機制及提出有效防治對策的重要物質基礎。本研究以ApoE突變小鼠作為研究對象,采用自發性動脈粥樣硬化小鼠模型,結果顯示實驗組血清CRE、BUN水平比正常對照小鼠顯著增加,同時實驗組腎臟組織形態明顯改變,腎小球細胞增多、基底膜異常增厚、系膜細胞增生,證實動脈粥樣硬化小鼠具有狼瘡樣臨床表現。
目前,國內外已建立多種SLE合并動脈粥樣硬化模型小鼠,但是成功率有限。文獻[3]發現,自發性模型MRL/lpr狼瘡鼠即使予以高脂喂養也幾乎不能出現動脈粥樣硬化病變。另外,有研究人員通過將同品系的Fas-/-小鼠,lpr(fas)或 gld(fasl)基因突變小鼠與ApoE-/-或 LDLr-/-小鼠交配繁殖;或通過誘發ApoE-/-或 LDLr-/-小鼠,均可成功建立SLE 伴動脈粥樣硬化模型[4-6]。但該方案繁殖純化周期較長,不確定因素較多。降植烷(Pristane)是可引起炎性反應和增強免疫反應的類異戊二烯烷烴,可被單核吞噬細胞吞噬,使T、B淋巴細胞增殖聚集,通過線粒體損傷途徑誘發細胞凋亡產生核抗原,由于T細胞高度活化、B細胞反應性增高,產生多種抗體,啟動自身免疫反應,常常能成功誘發狼瘡[7]。有研究報道,應用Pristane誘導小鼠建立動物模型所涉及的小鼠種類、周齡、Pristane劑量等均有差異,尚無統一標準[8,9]。因此,本研究采用ApoE-/-小鼠腹腔注射Pristane建立SLE伴發動脈粥樣硬化模型,以期為充實SLE早發動脈粥樣硬化動物模型的資料提供更多依據。結果顯示,12周齡實驗組小鼠注射Pristane后即可呈明顯的狼瘡表現,而一般自發性動脈粥樣硬化模型鼠出現SLE癥狀約需20周以上,可見Pristane刺激能大大縮短實驗周期。同時,實驗組小鼠腎炎性反應癥狀明顯,組織形態學顯示腎小球硬化和主動脈動脈粥樣硬化,血CRE和BUN等腎功能檢測指標顯著升高,血脂水平異常,具有和臨床相似的狼瘡表型及動脈粥樣硬化表現,表明成功構建SLE合并動脈粥樣硬化小鼠模型。
綜上所述,SLE是發病機制復雜的自身免疫性疾病,對其進行有效的干預治療已取得巨大進展,近年來,主要通過自發性和實驗性誘導動物模型進行更深入病因和發病機制的探索,因此建立便利、穩定的模型動物具有重要意義。本研究使用Pristane誘導自發性動脈粥樣硬化ApoE-/-小鼠建立SLE合并動脈粥樣硬化動物模型,制備方法簡便,一次注射即可。此外,與自發性動物模型病程較長不同,該造模方案實驗周期短,對實驗條件的要求相對較低,且實驗復制成功率高,能夠獲得與人類相似的發病情況。因此,本研究建立的動物模型可為進一步揭示疾病的發病機制及探索新的治療策略提供借鑒作用。

