急性早幼粒細胞白血病細胞分化的調控機制新進展①
于 麗 吳 靜 王 迪 肖 驍 張鳳民
(哈爾濱醫科大學微生物學教研室,黑龍江省感染與免疫重點實驗室,哈爾濱150081)
急性早幼粒細胞白血病(Acute promyelocytic leukemia,APL)是急性髓系白血病的一個常見亞型,占急性髓系白血病的10%~15%[1]。主要表現為未成熟的粒細胞在發育早期分化阻滯[2],臨床上以出血和血細胞減少為典型表現,嚴重者可發生彌漫性血管內凝血及顱內出血而致死[3]。誘導細胞分化是臨床治療APL的主要策略,目前存在多種誘導APL細胞分化的方法,常用的誘導分化劑包括全反式維甲酸、三氧化二砷、1,25-二羥維生素D3等[4]。而誘導APL細胞分化的機制也很復雜,深入研究影響誘導APL細胞分化的因素及機制將有助于闡明APL的發病機理,為其治療提供新的思路。本文主要對調控APL細胞分化的分子機制進行總結。
1 基因表達與APL細胞分化
在APL細胞中各種基因的異常表達都會直接或間接影響細胞分化。PML/RARA融合蛋白的形成是APL發生的最主要因素,降低PML/RARα融合蛋白的表達,可促進APL細胞分化[5];PML/RARA融合蛋白也可以調控其下游靶基因,如抑制CDKN2D、NEAT1、C/EBPβ等的表達從而抑制細胞分化[5-7]。更多基因表達與APL細胞分化的關系見表1、2。
2 自噬與APL細胞分化
自噬(Autophagy)在哺乳動物發育和分化過程中起著重要作用。與APL分化相關的物質主要有自噬相關基因、自噬體、自噬底物等。
表1 APL細胞分化后表達上調的基因
Tab.1 Up-regulated gene expression after APL cell differentiation

NameExpressionReferenceDEFA4,HP-1,ICAM1,K6HF,PRTN3,PDI2,PENK,MYBL2,CDW52,AAD27764,CYP26A1,CAPN4,CADPS, BM040,BC002447,PSME2,DUSP6,TCIRG1,HOXB7,ITGA2B,OAS1,SH3BGRL,XP03817,CREG,FYB,MAP4K2,ACAA1,HLA-G,IL5RA,KCNC1,IFI41,PRKAR1A,ITGAM,PHTF,IFI17,BPI,FADSD6,SAT,PT-PNS1,SCYA20,SCYA14,PRKCD,PTPN22,DBI,AK3,MAFG,ADD3,MYL4,ITPK1,ITPR2,PPIF F,SUPT3H,CD68,MTMR2,PTMA,CYCL,SCD,TCF2,NIPSNAP1,1-8D,BIK,PLSCR1↑[8]HHEX↑[9]
表2 APL細胞分化后表達下調的基因
Tab.2 Down-regulated gene expression after APL cell differentiation

NameExpressionReferenceNYP,CFL1,TPS1,CDH1,CEP3,GTF2H4,ASS,TP53TG3,P-B,PCYT1B,IGFBP2,MNDA,MAP3K1,EBBP,KI-AA0266,SEMG2,PTD010,CEBPA,RAD53,20D7-FC4,POLH,SECTM1,BAI1,GABRB3,BC10,SPS2,MSF,BCL2, MYO1E,KPNB1,UST,PCYT2,SOX10,FPGT,PCDH2,LY9,INPP4A,WSX-1,PTPN3,TF (F3),PLU-1,HFL-EDDG1,ACVR1↓[8]C-MYC↓[10]PAD4↓[11]CIP2A↓[12]
自噬相關基因是自噬的主要分子組成[13]。哺乳動物雷帕霉素靶點(mammalian target of rapamycin,mTOR)信號通路是調節自噬發生的中心通路[14],mTOR位于PI3K/Akt信號的下游,能夠激活哺乳動物自噬的關鍵調控蛋白ULK1,直接抑制自噬進程[15,16],從而誘導APL細胞分化;而自噬基因Atg7靶向敲除可減少微管相關蛋白1輕鏈的形成,從而抑制APL細胞分化[17]。
自噬體為雙層膜的細胞器。WD-重復蛋白的成員與磷酸肌醇家族相互作用,形成磷脂酰肌醇3磷酸(PI3P)效應,參與自噬體的形成[18],PI3P依賴磷酸肌醇介導的自噬誘導細胞分化[18]。而抑制mTOR信號通路,激活Atg1-PI3KC3-Atg5依賴性自噬通路,也可促進自噬體形成[19]。核糖核酸酶也與自噬相關,RNaseⅢ類成員DICER1為miRNA加工的關鍵酶,其高表達可激活自噬,誘導APL細胞向中性粒細胞分化[20]。
p62/SQSTM1為自噬底物,是支架蛋白。有文獻表明p62與PML-RARα融合蛋白結合調節PML-RARα融合蛋白降解和APL細胞分化[21]。
3 ROS與APL細胞分化
APL細胞的分化過程也可以通過活性氧(Reactive oxygen species,ROS)調控。過多的ROS生成或氧化的DNA損傷經常發生在造血系統惡性腫瘤中[22,23]。在ROS調控的APL分化過程中,過氧化物酶(Peroxiredoxin,PrdxI)發揮重要作用,PrdxI可作為新的靶點,通過PrdxI/ROS軸誘導APL細胞分化[2]。
ROS可以通過自噬調控細胞存活和死亡的信號分子。一方面,ROS可通過不同的機制包括Atg4過氧化氫酶的激活抑制mETC誘導自噬。另一方面,自噬可以增加腫瘤細胞的氧化應激。高遷移率族蛋白1(High-mobility group box 1,HMGB1)是一種與氧化應激相關的自噬傳感器,過氧化氫和HMGB1基因介導的氧化應激的損傷促進HMGB1的胞漿表達和APL細胞分化[21]。
谷胱甘肽(Glutathion,GSH)在ROS引起的細胞分化中也發揮重要作用。在細胞分化初期,ROS和GSH消耗快速增強,通過Nrf2/ARE通路提供GSH和其他抗氧化劑,緩沖ROS和其他親電分子,調節細胞內氧化還原平衡,從而促進細胞分化。細胞內ROS水平也可由MUC1異二聚體蛋白調控。MUC1含有N-末端胞亞基(muc1-n),具有黏蛋白的結構特點,可結合在復雜的C端跨膜亞基的細胞表面(muc1-c)。靶向 muc1-c,增加細胞內ROS,可誘導APL細胞分化[24]。
氧化還原敏感的轉錄因子的調控可改變ROS水平誘發白血病,如Nrf2、Bach1、NF-κB、AP-1和HIF1α[25,26]。激活此類轉錄因子增加細胞內ROS水平,可穩定RARα蛋白[27]。而RARα蛋白的穩定與表觀遺傳學關系密切[28]。
4 表觀遺傳學與APL細胞分化
表觀遺傳學主要包括甲基化、乙酰化、磷酸化、泛素化、類泛素化、去乙酰化等[29]。表觀遺傳異常是癌癥、遺傳性疾病、兒科綜合征、自身免疫性疾病和衰老的因素[30]。有研究表明,表觀遺傳學與APL細胞分化相關。表3對與APL細胞分化相關的表觀遺傳機制進行總結。
5 APL細胞分化相關的其他因素
5.1細胞因子與APL細胞分化 細胞因子是由免疫系統細胞產生的生物活性蛋白[38]。有研究表明,細胞因子與RA聯合應用時可誘導APL細胞的分化。表4對與APL細胞分化相關的細胞因子進行總結。
5.2Toll樣受體與APL細胞分化 Toll樣受體(Toll-like receptors,TLRs)是與炎癥相關的關鍵受體家族。有研究表明,在TLR8興奮劑存在的條件下,可通過TLR8/MyD88/p38依賴方式誘導APL細胞分化[43]。
5.3抗體誘導APL細胞分化 目前誘導APL細胞分化的藥物主要有全反式維甲酸、三氧化二砷等,雖然其治療效果甚好,但可引起嚴重并發癥。而基于抗體治療白血病的方法,主要是針對細胞表面因子,存在的抗體藥物基本都是抗體與化療藥物結合應用[44],且存在毒性,但抗體誘導APL細胞的分化作用至今仍未有研究。本課題組研究發現,全人源單克隆自身抗體因其自體性,能夠克服毒性及副作用等缺點,并可顯著誘導APL細胞分化,這為開發新的治療白血病的抗體藥物,并發現促進APL細胞分化的新機制提供科學依據。
表3 與APL細胞分化相關的表觀遺傳機制
Tab.3 Epigenetic mechanism associated with APL cell differentiation
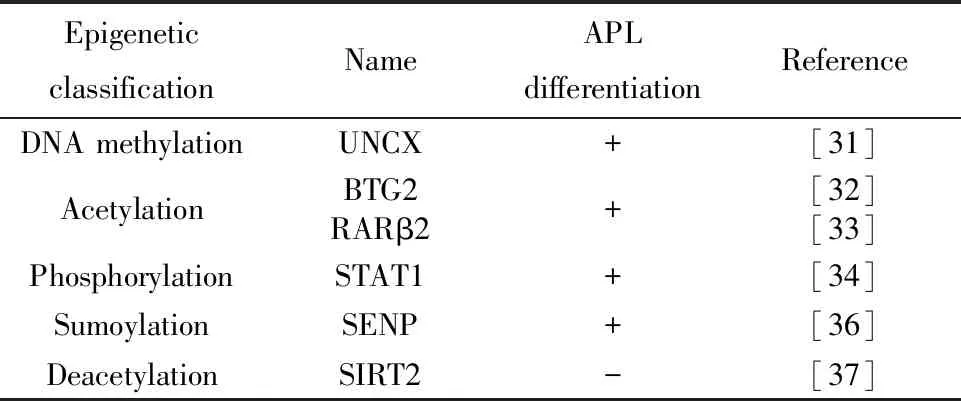
EpigeneticclassificationNameAPLdifferentiationReferenceDNA methylationUNCX+[31]AcetylationBTG2RARβ2+[32][33]PhosphorylationSTAT1+[34]SumoylationSENP+[36]DeacetylationSIRT2-[37]
Note:+.Promote cell differentiation;-.Inhibit cell differentiation.
表4 與APL細胞分化相關的細胞因子
Tab.4 Cytokine associated with APL cell differentiation
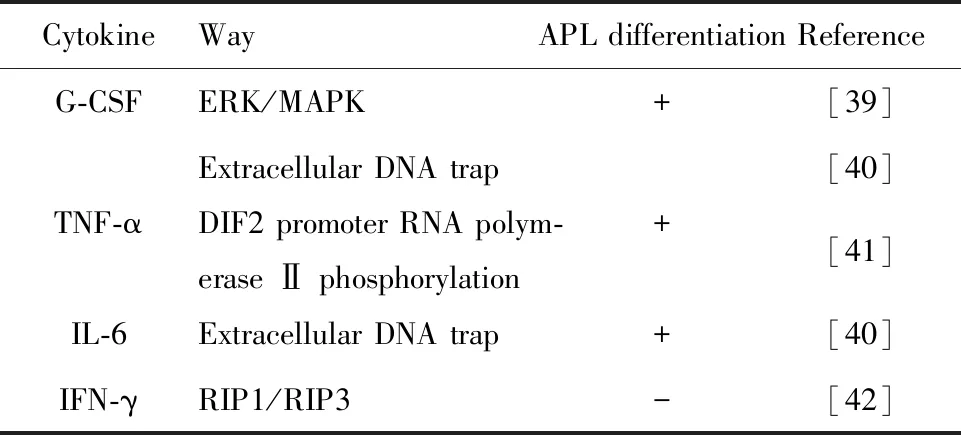
CytokineWayAPL differentiationReferenceG-CSFERK/MAPK+[39]Extracellular DNA trap[40]TNF-αDIF2 promoter RNA polym-erase Ⅱ phosphorylation+[41]IL-6Extracellular DNA trap+[40]IFN-γRIP1/RIP3-[42]
Note:+.Promote cell differentiation,-.Inhibit cell differentiation.
6 結語
急性早幼粒細胞白血病已從成人最致命的急性白血病轉變為可治愈的疾病,而誘導分化治療在白血病治療中具有重要意義。基因表達異常、自噬、氧化應激、表觀遺傳學等在調控APL細胞分化過程中發揮重要作用。除此之外,抗體在誘導白血病細胞分化過程中發揮的作用也不可忽視。因此,更深入了解調控APL細胞分化的不同方式及機制,有助于開發更安全、特異的治療方法。

