續斷切制工藝的優化
李 妍, 王建科?, 王新村, 王元鎂
(1. 貴陽中醫學院, 貴州 貴陽 550025; 2. 貴州同濟堂中藥材種植有限公司, 貴州 貴陽550009)
續斷是傳統常用中藥, 首載于 《神農本草經》, 被列為上品[1], 為川續斷科植物川續斷Dipsacus asper Wall. ex Henry 的干燥根, 在秋季采挖,除去蘆頭及須根, 清洗后用微火烘至半干, 堆積“發汗” 至內部變綠后再烘干[2], 它含有三萜皂苷、 木通皂苷、 馬錢子苷、 多糖、 β-谷甾醇等成分, 另外其揮發油主要組成有漪羅艾菊酮、 2, 4,6-三叔丁基苯酚等[1,3-6]。 藥理研究表明, 續斷對骨組織、 生殖系統、 免疫系統、 神經系統等均有一定影響, 具有抗炎、 抗衰老、 修復肝損傷等藥理作用[7-14]。 然而, 目前續斷切制工藝尚無具體的技術參數, 導致飲片質量參差不齊, 影響臨床療效發揮及相關產業發展, 故本研究采用正交試驗優化該藥材切制工藝, 為其進一步研究奠定基礎。
1 材料
1.1 儀器 UltiMate 3000 型高效液相色譜儀(美國賽默飛世爾科技公司); TU-1810 型紫外-可見分光光度儀(北京普析通用儀器有限責任公司);AUW220D 型全自動電子天平[島津儀器(蘇州)有限公司]; 中藥粉碎機(天津泰斯特儀器有限公司)。
1.2 試藥 川續斷皂苷Ⅵ(批號GZDD-0006) 對照品購于貴州迪大生物科技有限責任公司。 續斷采自貴州同濟堂中藥材種植有限公司續斷種植基地(威寧縣二塘鎮梅花村), 經貴陽中醫學院生藥教研室魏升華教授鑒定為續斷科植物川續斷Dipsacus asper Wall. ex Henry 的干燥根, 將其除去雜質, 洗凈, 潤透, 切薄片, 干燥, 篩去碎屑。 甲醇、 乙醇、 磷酸均為分析純; 甲醇、 乙腈均為色譜純; 水為純凈水,
2 方法與結果
2.1 川續斷皂苷Ⅵ含有量測定
2.1.1 色譜條件 Agilent Eclipse C18色譜柱(250 mm×4.6 mm, 5 μm); 流動相乙腈-0.20%磷酸(30 ∶ 70); 檢 測 波 長206 nm; 體 積 流 量1 mL/min; 柱溫30 ℃; 進樣量20 μL。 色譜圖見圖1。

圖1 川續斷皂苷ⅥHPLC 色譜圖Fig.1 HPLC chromatograms of asperosaponin Ⅵ
2.1.2 對照品溶液制備 取川續斷皂苷Ⅵ對照品適量, 甲醇稀釋成1.5 mg/mL, 精密量取1 mL 置于10 mL 量瓶中, 流動相稀釋至刻度, 搖勻,即得。
2.1.3 供試品溶液制備 精密稱取藥材細粉約0.5 g, 置于50 mL 具塞錐形瓶中, 精密加入15 mL 90%甲醇, 密塞, 稱定質量, 回流提取3 次, 每次30 min, 放冷, 90% 甲醇補足減失的質量, 搖勻,濾過, 合并濾液, 精密吸取1 mL, 置于10 mL 量瓶中, 流動相稀釋至刻度, 搖勻, 0.45 μm 微孔濾膜過濾, 即得。
2.1.4 線性關系考察 精密稱取川續斷皂苷Ⅵ對照品15.05 mg, 甲醇稀釋成1.505 mg/mL, 精密吸取0.05、 0.2、 0.8、 1.2、 1.8 mL 于2 mL 量瓶中,甲醇定容, 在“2.1.1” 項色譜條件下進樣20 μL測定。 以進樣量為橫坐標(X), 峰面積為縱坐標(Y) 進行回歸, 得方程為Y=4.616 6X +1.038 3(r=0.999 8), 在0.075 3~2.709 μg 范圍內線性關系良好。
2.2 續斷總皂苷含有量測定
2.2.1 對照品溶液制備 精密稱取川續斷皂苷Ⅵ對照品適量, 甲醇定容至25 mL, 即得(0.226 mg/mL)。
2.2.2 供試品溶液制備 精密稱取藥材粉末約0.3 g, 加入60 mL 70% 乙醇, 超聲 (500 W、40 kHz) 50 min, 濾過, 濾液置于100 mL 量瓶中,70%乙醇定容至刻度, 搖勻, 即得。
2.2.3 顯色條件 精密吸取供試品0.3 mL 于10 mL比色管中, 沸水浴揮干溶劑, 精密加入甲醇2 mL、 濃硫酸3 mL, 密塞, 搖勻, 95 ℃恒溫水浴中加熱20 min 后, 再放入冰水浴中冷卻5 min, 搖勻, 于528 nm 波長處測定吸光度。
2.2.4 線性關系考察 精密吸取對照品溶液0.3、0.4、 0.5、 0.6、 0.7、 0.8、 0.9 mL 于具塞試管中, 隨行試劑作為空白對照, 按“2.2.3” 項下方法操作, 于528 nm 波長處測定吸光度。 以吸光度為縱坐標(A), 進樣量為橫坐標(X) 進行回歸,得方程為A = 3.641X-0.022 6 (r = 0.999 6),在0.067 8~0.203 4 mg 范圍內線性關系良好。
2.3 水浸出物測定 參照2015 年版《中國藥典》四部水浸出物項下熱浸法測定。
2.4 醇浸出物測定 參照2015 年版《中國藥典》四部醇浸出物項下熱浸法測定, 以50%乙醇為溶劑。
2.5 切制工藝優化
2.5.1 單因素試驗 以川續斷皂苷Ⅵ、 總皂苷為評價指標, 對軟化用水量(A)、 軟化時間(B)、切制片型(C)、 干燥溫度(D) 進行考察, 發現在軟化用水量2 倍、 軟化時間4 h、 切制片型橫片、干燥溫度80 ℃條件下效果最佳。
2.5.2 正交試驗 在單因素試驗基礎上, 各因素選取3 個水平, 通過L9(34) 正交表安排試驗。 取9 份藥材, 每份1 kg, 按表1 參數設計, 加入不同用量水軟化一定時間后取出, 切制成不同片型, 于不同溫度下干燥, 得到9 份樣品, 粉碎, 過40 目篩, 測定各成分含有量, 再進行綜合評分。 根據所測成分在藥材中的重要性, 設定權重分別為川續斷皂苷Ⅵ40%、 總皂苷30%、 醇浸出物15%、 水浸出物15%, 計算公式為綜合評分=川續斷皂苷Ⅵ隸屬度×40% +總皂苷隸屬度×30% +醇浸出物隸屬度×15%+水浸出物隸屬度×15% [隸屬度= (指標值-指標最小值) /(指標最大值-指標最小值) ], 滿分1.00。 結果見表1, 方差分析見表2。

表1 試驗設計及結果Tab.1 Design and results of tests
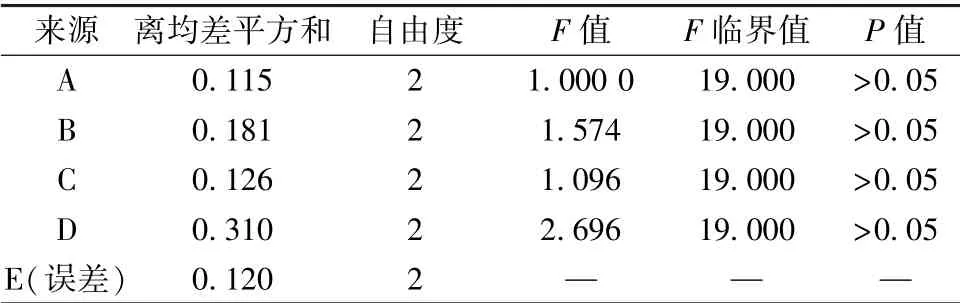
表2 方差分析Tab.2 Analysis of variance
由表1 可知, 各因素對綜合評分的影響程度依次為D>B>C>A, 即干燥溫度影響最大, 軟化用水量影響最小, 最優工藝為A2B3C1D2; 由表2 可知,各因素對實驗結果均無顯著性影響(P>0.05)。 綜合各因素考慮, 最終確定最優工藝為A2B3C2D2,即用4 倍量水軟化藥材, 軟化時間6 h, 切橫片,干燥溫度70 ℃。
2.6 切制工藝比較 取藥材3 份, 每份5 kg, 分別按“1.2” 項下傳統工藝和“2.5.2” 項下優化工藝切制, 測定川續斷皂苷Ⅵ、 續斷總皂苷、 水浸出物、 醇浸出物含有量, 結果見表3 ~4。 由表可知, 優化工藝穩定可行, 測得值高于傳統工藝。
3 討論與結論
本實驗所用續斷采自種植基地, 按照傳統工藝加工, 即將新鮮藥材剪掉須根及蘆頭, 清洗干凈,濾水, 60 ℃干燥箱中減重, 堆積“發汗” 以使藥材內部變綠后再烘干。 切制時, 先用水軟化續斷,發現切制后其外表皮呈灰褐色, 而切面皮部呈墨綠色, 并且在軟化過程中出現下色現象, 是否表明某些成分有損失或變化尚需進一步研究。
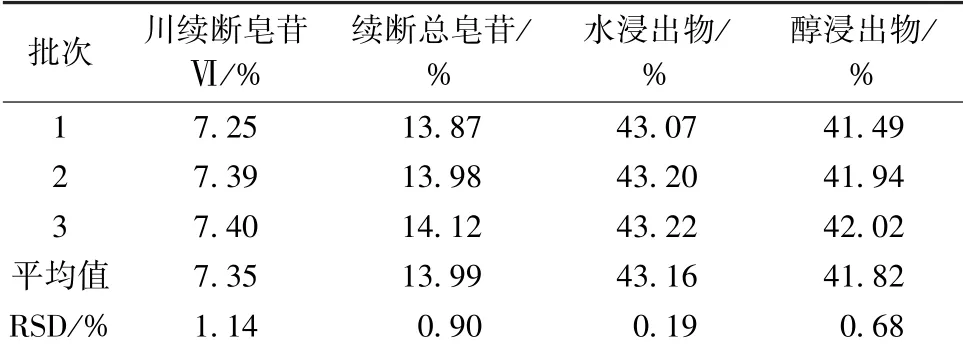
表3 傳統工藝下含有量測定結果(n=3)Tab.3 Results of content determination under traditional process (n=3)
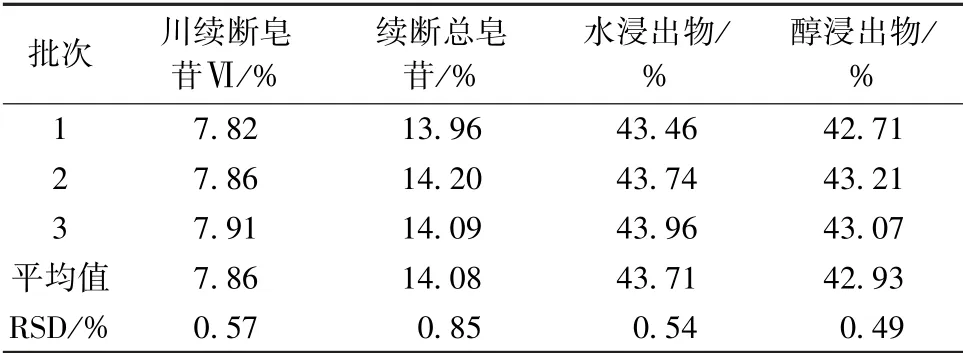
表4 優化工藝下含有量測定結果(n=3)Tab.4 Results of content determination under optimized process (n=3)
多指標綜合評價符合中藥多功效的用藥特點,也可體現中醫藥思維的整體觀念。 本研究采用該方法優化續斷切制工藝, 所得最佳條件為取烘干減重50% “發汗” 后于60 ℃下干燥的藥材, 加入4 倍量水軟化6 h, 取出, 稍潤, 橫切3 mm 厚片,70 ℃下烘干, 川續斷皂苷Ⅵ、 續斷總皂苷、 水浸出物、 醇浸出物含有量分別為7.86%、 14.08%、43.71%、 42.93%, 四者均高于傳統工藝, 可知優化工藝穩定可行, 可用于該藥材加工。

