FNA對短程硝化污泥菌群結構的影響
高春娣,趙 楠,安 冉,韓 徽,張 娜,彭永臻
?
FNA對短程硝化污泥菌群結構的影響
高春娣*,趙 楠,安 冉,韓 徽,張 娜,彭永臻
(北京工業大學環境與能源工程學院,城鎮污水深度處理與資源化利用技術國家工程實驗室,北京 100124)
在SBR反應器增加游離亞硝酸(FNA)預處理單元,投加濃度為1.2mgHNO2-N/L的FNA進行缺氧攪拌4.5h,連續處理3d,考察短程硝化污泥中FNA對氨氧化菌(AOB),絲狀菌和微生物菌群結構的影響.研究表明,FNA對AOB有短時抑制作用,并能夠抑制優勢絲狀菌(微絲菌屬)和(噬纖維菌)的增殖,分別由5.1%和1.1%下降到0.78%和幾乎不可見.SVI從281mL/g降低到100mL/g左右.NAR能夠維持在90%左右,短程硝化不受到破壞.高通量結果顯示,FNA處理后微生物菌群結構多樣性與豐度出現下降,但(陶厄氏菌屬)和出現了增殖,分別增加到5.58%和7.82%,同步硝化反硝化(SND)作用明顯,這使得即便只有短程硝化,總氮去除率依然能達到60%以上.
短程硝化;污泥膨脹;污泥沉降性能;絲狀菌;AOB;微生物菌群結構;SND
短程硝化反硝化存在節省25%的曝氣能耗、減少40%的碳源投加量以及減少污泥產量等優點[1-2],因此被廣泛地應用于實際生活污水處理[3-6].短程硝化反硝化技術是將硝化反應控制并維持在亞硝酸鹽階段,不進行亞硝酸鹽至硝酸鹽的轉化[7].在這一過程中,亞硝酸鹽是必不可少的中間產物,積累率最高可達90%以上[2].當前關于亞硝酸鹽對硝化作用的影響多圍繞對硝化菌,也就是氨氧化菌(AOB)和亞硝酸鹽氧化菌(NOB)的影響展開.有研究表明,超過一定濃度的亞硝酸鹽對微生物以及污泥沉降性能具有一定的影響[8-13],也有研究表明是亞硝酸鹽的質子化產物游離亞硝酸(FNA)對微生物種群具有抑制作用,而非亞硝酸鹽[9,14].研究發現FNA對AOB,NOB,反硝化菌和厭氧氨氧化菌等均有影響[14-19],并且FNA對微生物的抑制作用還會影響到污泥中微生物菌群結構的變化[20],利用這種抑制特性能夠實現短程硝化[21-23].
隨著短程硝化反硝化研究和應用的不斷深入,隨之而來的污泥膨脹問題也越來越突出.由于亞硝酸鹽的積累會使污泥的沉降性能惡化[11],這就導致無論是在實驗室規模研究,還是在實際應用中,污泥膨脹都時有發生.而現有研究中又缺乏FNA對絲狀菌影響的相關報道,并且關于活性污泥系統中微生物對FNA影響適應性的研究也較少[14].針對這一現狀,本研究采用增加FNA預處理單元的方法,專門考察短程硝化污泥中FNA對絲狀菌和硝化菌等微生物菌群的抑制作用以及對這種抑制作用的適應性.
1 材料與方法
1.1 試驗裝置
試驗裝置為SBR反應器,由圓柱形有機玻璃制成,有效容積8L.反應器上部固定電動攪拌器,底部裝有曝氣盤并連接轉子流量計和空氣壓縮機,可直接調控溶解氧(DO)量,進、排水口連接蠕動泵自動進水、電動閥自動排水.溶氧儀裝有DO和pH值探頭,實時監測反應過程DO和pH值的變化.試驗裝置見圖1.

圖1 試驗裝置示意
1.貯水箱;2.蠕動泵;3.電動水閥;4.攪拌器;5.空氣泵;6.曝氣盤;7.WTW 溶氧儀;8.pH值探頭;9.DO 探頭;10.加熱棒;11.空氣轉子流量計;12.FNA預處理單元
1.2 試驗水質及接種污泥
試驗種泥為馴化良好的短程硝化污泥,沉降性能良好,SV在40%左右.進水水質為某高校家屬區實際生活污水,平均C/N<3.0為低碳氮比生活污水.水質參數如表1所示.
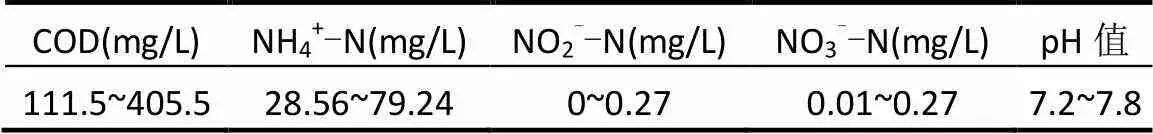
表1 實際生活污水的水質參數
1.3 試驗運行方案
第I 階段:污泥膨脹的誘發(1~40d)
將短程硝化污泥投加到SBR反應器中,污泥濃度維持在2500~3000mg/L,排水比為50%,維持溫度在24℃左右.通過低DO(0.5~1.0mg/L),低負荷運行條件來誘發污泥膨脹.運行方式為進水,好氧攪拌,沉淀30min,排水,每天運行4個周期.運行過程中,pH值隨著亞硝化反應的進行不斷下降,當亞硝化過程完成后,曝氣作用將水中的CO2吹脫導致pH值上升,出現pH值的突變點,此突變點即為氨谷點.通過實時監測pH值變化,來控制好氧曝氣時長,從而實現對氨谷點的實時控制.
第II階段:FNA預處理(41~43d)
從發生膨脹的SBR反應器中取出全部泥水混合物,靜沉后去除上清液,污泥用去離子水離心(4000r/min,5min)洗絳3次消除污泥中NH4+和NO2-等干擾,用去離子水定容至1.0L,控制溫度為24℃,一次性投加NaNO2儲備液使NO2-濃度為5.1g/L,FNA濃度為1.2mgHNO2-N/L,缺氧攪拌4.5h,反應進行中通過投加0.1mol/L的HCl和NaOH控制pH值在7.0±0.05.反應結束后,用去離子水離心洗泥3次.洗泥結束后投加泥到SBR反應器中,運行方式同第I階段.每天進行一次,共運行3d.FNA濃度根據公式(1)計算[24]:

(2)
式中:NO2-為亞硝酸鈉的濃度,mg/L;為反應器內的溫度,℃.
第III階段:反應器正常運行階段(44~72d)
溫度為室溫(20~21℃),與第I階段運行方式相同,每天運行4個周期,共運行29d.
1.4 試驗分析指標及方法
水樣分析項目中NH4+,NO2-,NO3-使用Lachat QuikChem8000流動注射自動測定儀(Lachat Instruments, Milwaukee,USA).MLSS按國家標準方法測定[25].DO和pH值采用WTW溶解氧測定儀(Multi340i型)測定.絲狀菌普通鏡檢通過革蘭式染色法,所用儀器為OLYMPUS-BX61顯微鏡,并通過Image-Pro Plus軟件分析細菌的大小和形態.采用Fast DNASpin Kit for Soil(QBIOgen Inc,Carlsba,CA,美國)DNA提取試劑盒提取反應器活性污泥樣品的總DNA.MiSeq高通量測序實驗流程包括:完成基因組DNA 提取,進行PCR 擴增,并將PCR 產物進行檢測定量,構建MiSeq文庫,最終進行MiSeq測序并進行微生物菌群結構分析.
1.5 數據分析方法
本試驗中亞硝酸鹽積累率的計算如式(3):
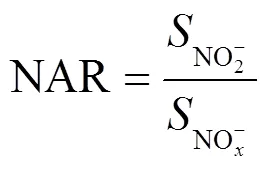
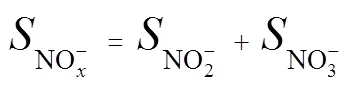
式中:NAR為亞酸鹽積累率,%;NO-為氮氧化物的濃度,mg/L;NO2-為亞硝酸鹽的濃度,mg/L;NO3-為硝酸鹽的濃度,mg/L.
2 結果與討論
2.1 FNA對污泥沉降性能的影響

圖2 FNA預處理前、后SV和SVI的變化情況
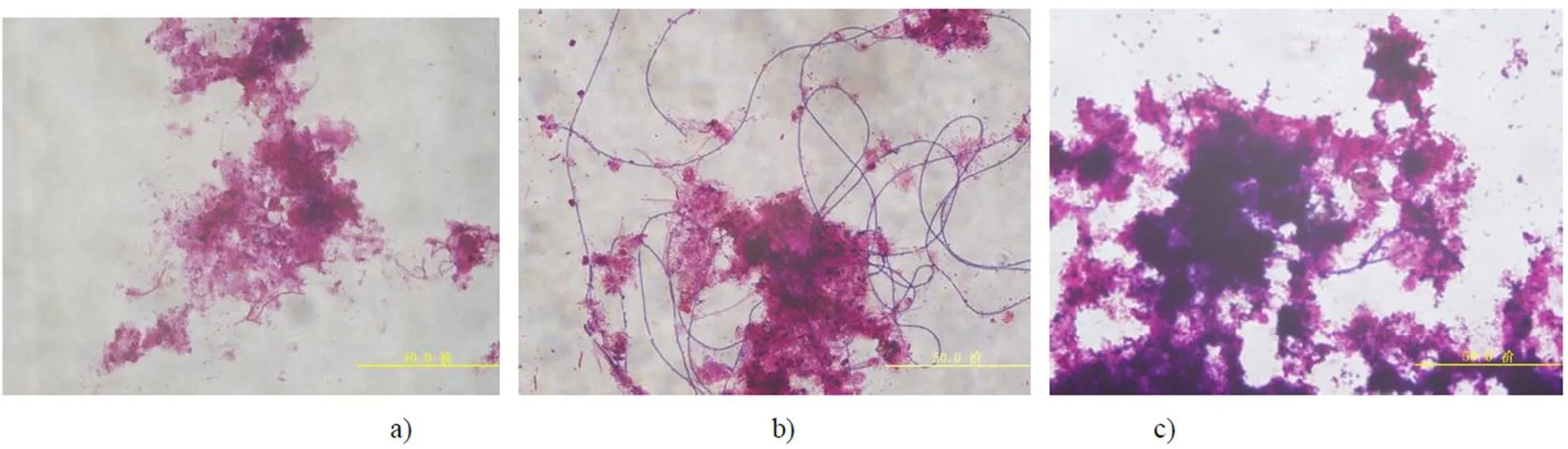
圖3 革蘭氏染色圖片
a)接種污泥革蘭氏染色圖片;b)膨脹污泥SVI值為280的革蘭氏染色圖片;c)停止FNA預處理,系統穩定運行SVI值為100的革蘭氏圖片
在第I階段短程硝化污泥接種初期,系統內污泥的SVI為138mL/g左右(如圖2所示),由于采用低DO運行結合低碳氮比進水,絲狀菌在與菌膠團細菌對營養物質的競爭中處于優勢而大量繁殖,在試驗第15~40d,SVI逐漸上升,第40d達到281mL/g.圖3絲狀菌鏡檢可看出,種泥(圖3a)中只有少量的絲狀菌,菌膠團結構密實,發生膨脹后(圖3b)大量絲狀菌增殖,菌絲從菌膠團中伸出使菌膠團結構松散.由于絲狀菌的大量繁殖,活性污泥的沉降性能惡化導致污泥流失.第II階段的第1d,SVI就下降近50%,達到115mL/g,并在第III階段SVI穩定維持在100mL/g左右.圖3c,較膨脹階段的污泥,第III階段污泥中的菌絲大量減少,污泥沉降性能良好,盡管采用與第I階段相同的運行方式,污泥的沉降性能也沒有惡化.分析原因,認為是FNA對優勢絲狀菌與菌膠團活性的抑制具有差異性,其中優勢絲狀菌對FNA敏感度要高于菌膠團,所以當優勢絲狀菌活性受到FNA抑制時,菌膠團在營養物質的攝取過程中具有優勢而加快增殖,從而使污泥的沉降性能能夠得到改善.由此可見FNA對優勢絲狀菌的抑制具有長期不可恢復性,并能夠有效改善污泥沉降性能惡化的問題.
2.2 FNA對NH4+-N、氮氧化物去除效果的影響
反應器始終在低DO條件下運行,由于AOB對氧的親和力較強[26-27],加之種泥短程硝化性能良好,所以從圖4可看出,第I階段氨氮去除率穩定上升,達90%以上,NH4+-N平均出水在5mg/L左右, NO2--N積累率(NAR)維持在90%以上,短程硝化效果良好.第II階段中的第1d,AOB活性受到抑制,出水NH4+-N為13.79mg/L,相較于階段I增加了8.79mg/L.相關文獻表明,AOB的FNA抑制濃度為0.50~0.63mgHNO2-N/L[28-29],試驗中FNA濃度為1.2mgHNO2-N/L,而從第III階段的第2d,AOB的活性開始逐漸恢復,出水NH4+-N達到2~5mg/L,并在之后的運行中穩定維持在0~4mg/L,說明FNA對AOB活性的抑制具有短時性,當停止FNA抑制后,AOB的活性能夠得以恢復.其次種泥是短程硝化污泥,即污泥硝化菌AOB占有優勢,而NOB含量低,且FNA對NOB抑制作用要強于AOB[28],加之低DO條件運行,使得污泥中的NOB含量逐漸降低,變得微乎其微,所以在第III階段中,出水NO3-接近于0.06mg/L左右,從而污泥NAR能夠維持在95% 以上,并穩定維持短程硝化,使得受到FNA抑制的污泥仍能夠保持良好的短程硝化的性能.

圖4 系統運行不同階段NH4+-N,NO2--N,NO3--N濃度和NAR的變化
好氧運行模式下,理論上只進行到硝化階段無法進行TN的去除.從圖4、5中可看出,第I階段TN去除率達到80%左右,是因為污泥在低DO條件下,系統中存在好氧反硝化菌,發生了同步硝化反硝化(SND)[30],使TN得以去除.第III階段的第1d,TN去除率為0,之后開始升高,并在第15d之后最高達到60%左右,但始終低于第I階段.原因可能是FNA對好氧反硝化菌也具有短時抑制作用且活性無法得到完全恢復或污泥中出現能夠適應高濃度FNA的好氧反硝化菌,但其反硝化能力要弱于第I階段的好氧反硝化菌.
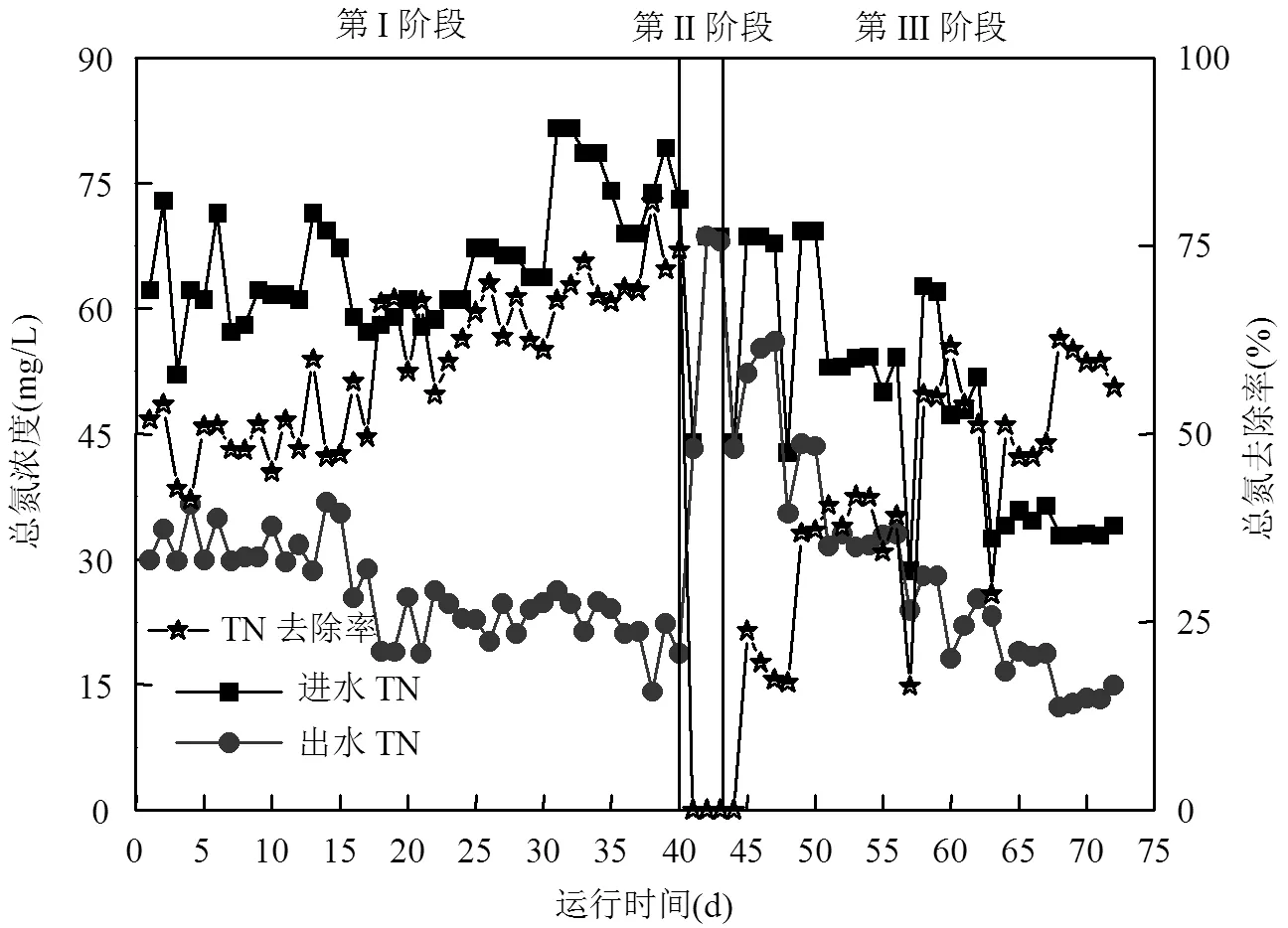
圖5 系統運行不同階段TN濃度和去除率的變化
2.3 活性污泥種群結構的分析
為了探究污泥在3個階段微生物種群結構的變化情況,分別取第0d種泥,第40d膨脹污泥和第72d污泥樣品,分別記為1,2,3,進行MiSeq高通量測序技術分析.
從3個污泥樣品中分別獲得了30242,52902, 33531條優化序列,有效序列平均長度為441,符合MiSeq高通量測序技術要求.3個泥樣分別為970, 1084,1102個OTUs.如表2所示,Ace,Chao,Sobs代表微生物菌群豐度指數,可看出,2 號泥樣中微生物種群豐度有所上升,這有可能是絲狀菌的大量增殖或膨脹系統中出現了新微生物菌種導致.而3號泥樣豐度下降,也再次證明了FNA對微生物具有一定的抑制作用.相關文獻報道[22,31],微生物種群Shannon多樣性指數,可用來估算污泥中微生物多樣性和均一性.2號泥樣的Shannon指數與種泥相比僅有輕微的下降,說明發生膨脹后,其微生物的多樣性與均一性變化可忽略不計.但3號泥樣中微生物菌群的多樣性、均一性均下降,說明FNA對微生物菌群的多樣性與均一性產生抑制作用.
含有絲狀菌菌屬的3個菌門Bacteroidetes(擬桿菌門),Actinobacteria(放線菌門)和Chloroflexi(綠彎菌門),在污泥膨脹后分別由24.27%,5.5%,5.29%上升至27.60%,8.52%和12.2%.而第III階段Bacteroidetes下降幅度最大,由27.6%下降至7.67%, Chloroflexi也下降為原來的50%左右.圖6中,污泥膨脹后優勢菌(微絲菌屬)和(噬纖維菌)分別由3.2% 上升到5.1%,由幾乎不可見增長到了1.1%,而第III階段,分別下降至0.78%和幾乎不可見.但絲狀菌(鏈球菌)在前2個階段中幾乎沒有,當FNA處理后增長至3.1%.說明FNA對部分絲狀菌具有抑制作用尤其是優勢菌和.
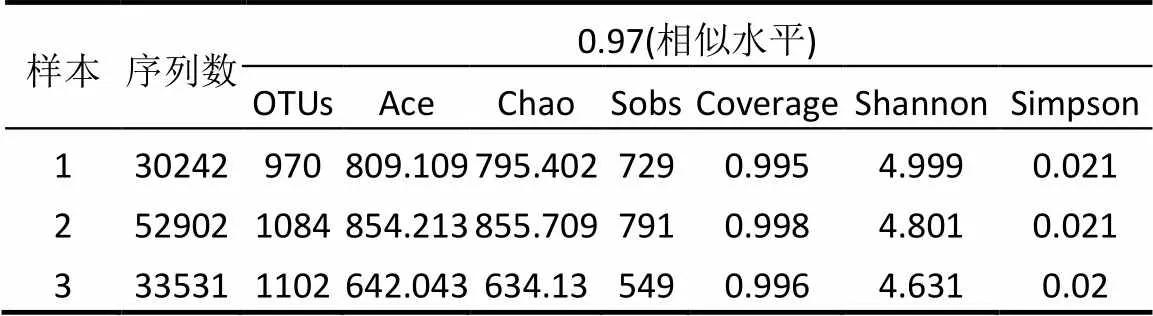
表2 不同階段反應中污泥樣品多樣性指數統計
如圖7可知,Proteobacteria(變形菌門)在3個階段中均占有很大的優勢,分別為39.44%,30.63%, 67.86%.Proteobacteria包括β綱,α綱,δ綱,γ綱,這4種綱中含有能夠進行硝化反硝化菌屬,其中β綱,γ綱包括氨氧化菌屬,也正因如此3個階段中污泥具有良好的去除氮物質的性能.污泥膨脹后Proteobacteria含量下降,主要因為此時絲狀菌處于優勢,使Proteobacteria在競爭底物中處于劣勢,導致其含量下降.第III階段Proteobacteria含量上升,因為FNA對微生物具有抑制作用,使能夠適應高濃度FNA的Proteobacteria菌屬占據優勢并得以增殖.

圖6 MiSeq高通量測序序列在屬水平上的分布
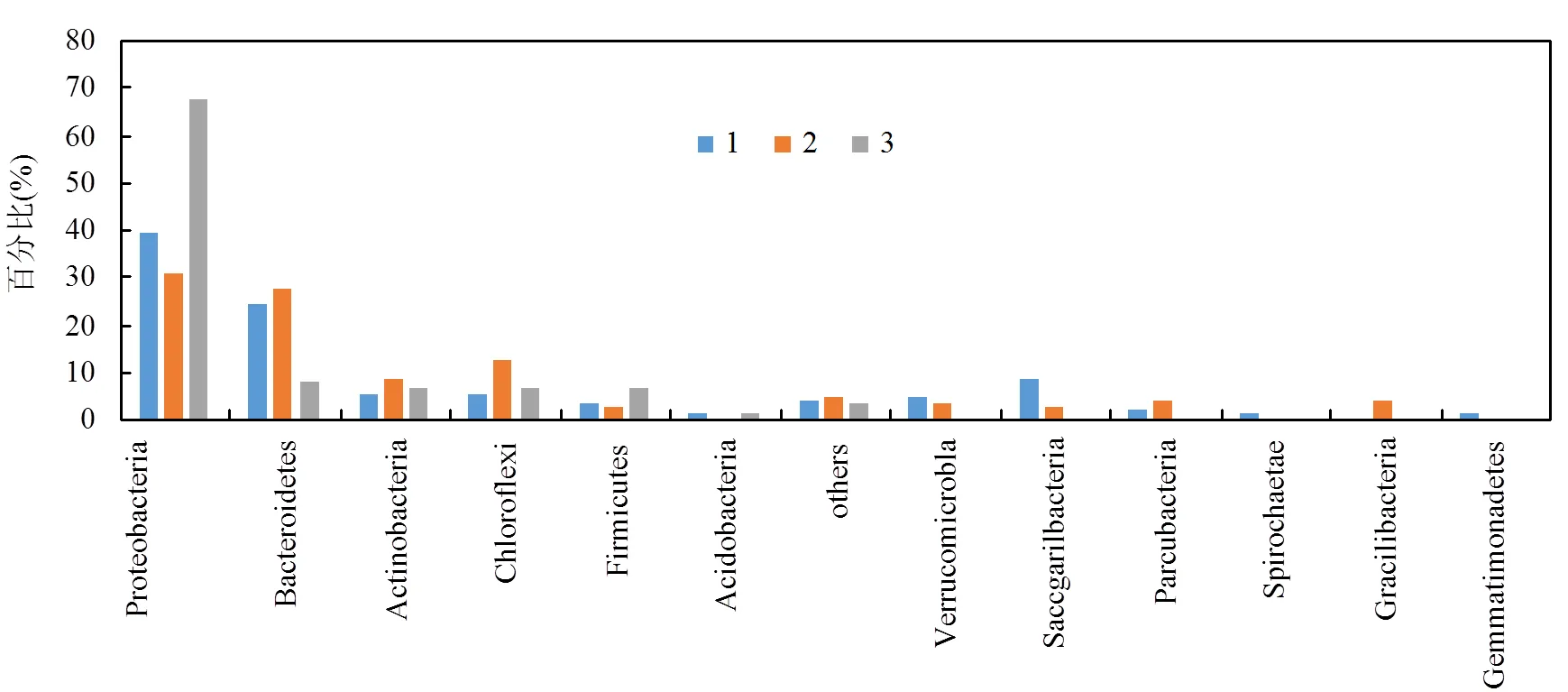
圖7 MiSeq高通量測序序列在門水平上的分布
圖6中(陶厄氏菌屬)是β綱下能夠利用[32-34].污泥膨脹后由8.57%減少至0.52%,第III階段上升至5.58%.具有反硝化功能的兼性厭氧菌[35-36],第I階段和第III階段中分別為4.5%和7.82%,而第II階段僅占0.6%,即經過FNA處理后,污泥中含量增加了7.22%.好氧反硝化菌(海生桿菌屬)[37]在種泥和第III階段中均幾乎不可見,而發生膨脹后,其含量增長至6.8%.由此可見,高濃度FNA對增長具有抑制作用且不可恢復,而具有好氧反硝化功能的和能夠適應高濃度FNA,并在第III階段中含量上升,這也是在第III階段中仍能發生SND的主要原因之一.但FNA對微生物種群結構具有影響,以及和反硝化能力要弱于的原因,導致了第III階段中TN去除率要明顯低于第I階段的80%,僅維持在60%左右.
3 結論
3.1 對于短程硝化過程中發生的絲狀菌污泥膨脹,FNA對絲狀菌增殖有顯著的抑制作用.短程硝化污泥經過FNA濃度為1.2mgHNO2-N/L,4.5h的預處理后,優勢絲狀菌由5.1%下降至0.78%,由1.1%減少到幾乎不可見.SVI迅速從281mL/g降低到100mL/g左右,且NAR能夠維持在90%左右,短程硝化不受到破壞.
3.2 FNA對AOB和好氧反硝化菌均有抑制作用,當FNA為1.2mgHNO2-N/L時,對AOB的抑制作用是短時且可恢復的,但對的抑制作用具有不可恢復性.
3.3 FNA能夠影響微生物的種群結構,使得污泥中微生物的多樣性、均一性以及物種豐度下降.對高濃度FNA的抑制具有較強的適應能力,在FNA處理結束之后,污泥中占微生物菌群的67.86%,污泥中具有反硝化功能的和含量上升,使在第III階段中仍能夠發生SND,保證了良好的TN去除效果.
[1] Gao C D, Fan S X, Jiao E L, et al. Operation and optimization of an alternating oxic-anoxic shortcut nitrification-denitrification system [J]. Advanced Materials Research, 2014,1030-1032:387-390.
[2] 高春娣,王惟肖,李 浩,等.SBR法交替缺氧好氧模式下短程硝化效率的優化[J]. 中國環境科學, 2015,35(2):403-409. Gao C D, Wang W X, Li H, et al. Optimization of short-range nitrification efficiency in alternate anoxic aerobic mode by SBR method [J]. China Environmental Science, 2015,35(2):403-409.
[3] Peng Y Z, Chen Y, Peng C Y, et al. Nitrite accumulation by aeration controlled in sequencing batch reactors treating domestic wastewater [J]. Water Science and Technology, 2004,50(10):35-43.
[4] Peng Y Z, Zhu G B. Biological nitrogen removal with nitrification and denitrification via nitrite pathway [J]. Appl. Microbiol. Biot., 2006, 73(1):15-26.
[5] 高春娣,李 浩,焦二龍,等.交替好氧缺氧短程硝化及其特性 [J]. 北京工業大學學報, 2015,41(1):116-122. Gao C D, Li H, Jiao E L, et al. Alternate oxic-anoxic mode realizing nitritation and its characterization [J]. Journal of Beijing University of Technology, 2015,41(1):116-122.
[6] Yang Q, Peng Y Z, Liu X H, et al. Nitrogen removal via nitrite from municipal wastewater at low temperatures using real-time control to optimize nitrifying communities [J]. Environmental Science Technology, 2007,41(23):8159-8164.
[7] Fdzpolanco F, Villaverde S, Garcia P A. Temperature effect on nitifying bacteria activity in biofilters-activation and free ammonia inhibition [J]. Water Science and Technology, 1994,3030(11):121-130.
[8] Ruiz G, Jeison D, Chamy R. Nitrification with high nitriteaccumulation for the treatment of wastewater with high ammoniaconcentration [J]. Water Research, 2003,37(6):1371?1377.
[9] Zhou Y, Oehmen A, Lim M, et al. The role of nitrite and free nitrous acid (FNA) in wastewater treatment plants [J]. Water Research, 2011, 45(15):4672-4682.
[10] Guo J H, Peng Y Z, Wang S Y, et al. Effective and robust partial nitrification to nitrite by real-time aeration duration control in an SBR treating domestic wastewate [J]. Process Biochemistry, 2009,44(9): 979?985.
[11] Musvoto E V, Lakay M T, Casey T G, et al. Filamentous organism bulking in nutrient removal activated sludge systems.Paper 8: The effect of nitrate and nitrite [J]. Water S A, 1999,25(4):397-407.
[12] Ma Y, Peng Y Z, Wang S Y, et al. Achieving nitrogen removal via nitrite in a pilot-scalecontinuous pre-denitrification plant [J]. Water Research, 2009,43(3):563-572.
[13] 宋姬晨,王淑瑩,楊 雄,等.缺/好氧條件下亞硝酸鹽的存在對污泥沉降性能的影響[J]. 中南大學學報(自然科學版), 2014,45(4): 1361-1368. Song J C, Wang S Y, Yang X, et al. Influence of nitrite on sludge settleability under anoxic and aerobic conditions [J]. Journal of Central South University (Science and Technology), 2014,45(4):1361-1368.
[14] 李 璐,馬 娟,宋相蕊.FNA在污水生物脫氮除磷中的抑制效應[J]. 工業水處理, 2014,34(6):5-9. Li L, Ma J, Song X R, et al. Inhibitory effect of free nitrous acid (FNA)on wastewater biological denitrification and dephosphorization [J]. Industrial Water Treatment, 2014,34(6):5-9.
[15] 劉甜甜,劉 牡,王淑瑩,等.鹽度耦合FNA對短程反硝化過程中N2O還原的影響[J]. 中南大學學報(自然科學版), 2013,44(8):3561- 3568. Liu T T, Liu M, Wang S Y, et al. Impact of salinity coupling FNA on N2O reduction during denitrification via nitrite [J]. Journal of Central South University (Science and Technology), 2013,44(8):3561-3568.
[16] Zahedi S, Romero-Güiza M, Icaran P, et al. Optimization of free nitrous acid pre-treatment on waste activated sludge [J]. Bioresource Technology, 2017,252:216-220.
[17] Egli K, Fanger, U, Alvarez, P J J, et al. Enrichment and characterization of an anammox bacterium from a rotating biological contactor treating ammonium-rich leachate [J]. Archives of Microbiology, 2001,175(3):198-207.
[18] Yoshida Y, Takahashi K, Saito T et al. The effect of nitrite on aerobic phosphate and denitrifying activity of phosphate-accumulating organisms [J]. Water Science and Technology, 2006,53(6):21-27.
[19] Pijuan M, Ye L, Yuan Z. Free nitrous acid inhibition on the aerobic metabolism of poly-phosphate accumulating organisms [J]. Water Research, 2010,44(20):6063-6072.
[20] 馬琳娜,劉文龍,張 瓊,等.游離亞硝酸(FNA)對A2O污泥菌群結構的影響[J]. 中國環境科學, 2017,37(7):2566-2573.Ma L N, Liu W L, Zhang Q, et al. Effect of free nitrous acid (FNA) on microorganism community structures of A2O sludge [J]. China Environmental Science, 2017,37(7):2566-2573.
[21] 韓曉宇,張樹軍,甘一萍,等.以FA與FNA為控制因子的短程硝化啟動與維持[J]. 環境科學, 2009,30(3):809-814. Han X Y, Zhang S J, Gan Y P, et al. Start up and maintain of nitritation by the inhibition of FA and FNA [J]. Environmental Science, 2009,30(3):809-814.
[22] Strous M, Kuenen J G, Jetten M S M. Key physiology of anaerobic ammonium oxidation [J]. Applied and Environmental Microbiology, 1999,65(7):3248-3250.
[23] 馬 斌,委 燕,王淑瑩,等.基于FNA處理污泥實現城市污水部分短程硝化[J]. 化工學報, 2015,66(12):5054-5059. Ma B, Wei Y, Wang S Y, et al. Achieving partial nitritation in sewage treatment system based on treating activated sludge by FNA[J].CIESC Journal, 2015,66(12):5054-5059.
[24] Anthonisen A C, Loehr R C, Prakasam T, et al. Inhibition of nitrification by ammonia and nirous-acid [J]. Journal Water Pollution Control Federation, 1976,48(5):835-852.
[25] Walter W G . Standard methods for the examination of water and wastewater (11th ed.) [J]. American Journal of Public Health & the Nations Health, 1961,51(6):940.
[26] Laanbroek H J, Bodelier P L E, Gerards S. Oxygen consumption kinetics of Nitrosomonas europaea and Nitrobacter hamburgensis grown in mixed continuous cultures at different oxygen concentrations [J]. Archives of Microbiology, 1994,161(2):156-162.
[27] 高春娣,孫大陽,安 冉,等.間歇曝氣下短程硝化耦合污泥微膨脹穩定性[J]. 環境科學, 2018,39(7):3271-3278. Gao C D, Sun D Y, An R, et al. Stability of nitritation combining with limited filamentous bulking under intermittent aeration [J]. Environmental Science, 2018,39(7):3271-3278.
[28] 張宇坤,王淑瑩,董怡君,等.游離氨和游離亞硝酸對亞硝態氮氧化菌活性的影響[J]. 中國環境科學, 2014,34(5):1242-1247. Zhang Y K, Wang S Y, Dong Y J, et al. Effect of FA and FNA on activity of nitrite-oxidising bacteria [J]. China Environmental Science, 2014,34(5):1242-1247.
[29] Vadivelu V M, Keller J, Yuan Z G. Effect of free ammonia and free nitrous acid concentration on the anabolic and catabolicprocesses of an enriched Nitrosomonas culture [J]. Biotechnology and bioengineering, 2006,95(5):830-839.
[30] 周丹丹,馬 放,董雙石,等.溶解氧和有機碳源對同步硝化反硝化的影響[J]. 環境工程學報, 2007,1(4):25-28. Zhou D D, Ma F, Dong S S, et al. Influences of DO and organic carbon on smiultaneous nitrification and denitrification [J]. Chinese Journal of Environmental Engineering, 2007,1(4):25-28.
[31] Navarro R R, Hori T, Inaba T, et al. High-resolution phylogenetic analysis of residual bacterial species of fouled membranes after NaOCl cleaning [J]. Water Research, 2016,94:166-175.
[32] 高晨晨,游 佳,陳 軼,等.絲狀菌污泥膨脹對脫氮除磷功能菌群的影響[J]. 環境科學, 2018,39(6):2794-2801. Gao C C, You J, Chen Y, et al. Effect of denitrification and phosphorus removal microorganisms in activated sludge bulking caused by filamentous bacteria [J]. Environmental Science, 2018,39(6):2794- 2801.
[33] Thomsen T R, Kong Y, Nielsen P H. Ecophysiology of abundant denitrifying bacteria in activated sludge [J]. Fems Microbiology Ecology, 2010,60(3):370-382.
[34] 鄭林雪,李 軍,胡家瑋,等.同步硝化反硝化系統中反硝化細菌多樣性研究[J]. 中國環境科學, 2015,35(1):116-121. Zheng L X, Li J, Hu J W, et al. Analysis of denitrifying bacteria community composition in simultaneous nitrification and denitrification systems [J]. China Environmental Science, 2015,35(1): 116-121.
[35] Spring S, Jackel U M, Kampfer P. Ottowia thiooxydans gen nov sp nov a novel facultatively anaerobic, N2O-producing bacterium isolated from activated sludge, and transfer of Aquaspirillum gracile to Hylemonella gracilis gen nov comb nov [J]. Int. J. Syst. Evol. Microbiol., 2004,54(1):99-106.
[36] 蔡麗云,黃澤彬,須子唯,等.處理垃圾滲濾液的SBR中微生物種群與污泥比阻[J]. 環境科學, 2018,39(2):880-888. Cai L Y, Huang Z B, Xu Z W, et al. Microbial communities and sludge specific resistance in two SBRs treating leachate [J]. Environmental Science, 2018,39(2):880-888.
[37] 李 楊,王 芳,楊海滟,等.高通量測序研究李氏禾生態浮床凈化污水的微生物群落結構變化[J]. 西南農業學報, 2018,31(9):1903- 1911. Li Y, Wang F, Yang H Y, et al. Study on microbial community composition and variation based on high throughput sequencing under leersia hexandra swartz rcological floating bed [J]. Southwest China Journal of Agricultural Sciences, 2018,31(9):1903-1911.
Effect of FNA on microorganism community structures of partial nitrification sludge.
GAO Chun-di*, ZHAO Nan, AN Ran, HAN Hui, ZHANG Na, PENG Yong-zhen
(National Engineering Laboratory for Advanced Municipal Wastewater Treatment and Reuse Technology, College of Environmental and Energy Engineering, Beijing University of Technology, Beijing 100124, China)., 2019,39(5):1977~1984
The long-term effects on ammonia-oxidizing bacteria (AOB), filamentous bacteria and microorganism community structures in partial nitrification sludge was investigated by adding a pretreatment unit of free nitrous acid (FNA) in the sequence bath reactor (SBR) for three days at 1.2mg HNO2-N/Lfor 4.5. The results showed that FNA had the short-time effect on AOB,andof the dominant filamentous bacteria were also decreased from 5.1% and 1.1% to 0.78% and almost invisible. Sludge volume index (SVI) maintained at 110mL/g dropping from 281mL/g, and the nitrite accumulation rate (NAR) was kept at around 90%, indicating the partial nitrification was not undermined. Furthermore, High-throughput sequencing results showed that the diversity and uniformity of microorganism community decreased. However, the proliferation ofandincreased to 5.58% and 7.82%. Simultaneous nitrification and denitrification (SND) had significant effects, and the total nitrogen removal rate was nevertheless maintained more than 60% even only with partial nitrification.
partial nitrification;sludge bulking;sludge settleability;filamentous bacteria;AOB;microorganism community structures;SND
X172
A
1000-6923(2019)05-1977-08
高春娣(1973-),女,河北唐山人,教授,博士,主要研究方向為城鎮污水深度處理與資源化利用,絲狀菌污泥膨脹機制與控制.發表論文38篇.
2018-10-15
國家自然科學基金資助項目(51478012);北京市科技重大專項(Z181100005318001)
*責任作者, 教授, gaochundi@bjut.edu.cn

