兩種不同檢測系統(tǒng)測定血清降鈣素原的比較實驗研究
田剛 丁俊杰 宋敏

摘要:目的? 探討三聯(lián)生物微陣列化學發(fā)光檢測系統(tǒng)測定血清降鈣素原(PCT)結(jié)果的可靠性。方法? 以羅氏Cobas e 601電化學發(fā)光檢測系統(tǒng)為參照系統(tǒng),三聯(lián)生物微陣列化學發(fā)光檢測系統(tǒng)為待評估系統(tǒng),對血清PCT濃度進行測定并進行統(tǒng)計分析。結(jié)果羅氏電化學發(fā)光檢測系統(tǒng)血清 PCT日內(nèi)精密度的變異系數(shù)(CV)為5.33%~7.88%,日間CV為5.62%~8.56%。三聯(lián)生物微陣列化學發(fā)光檢測系統(tǒng)的日內(nèi)CV為4.93%~7.28%,日間CV為5.47%~8.90%。兩種檢測系統(tǒng)有較好的相關性(回歸方程y=1.174x+0.213,P<0.05),相關系數(shù)r2為0.997。在醫(yī)學決定水平(PCT為0.50 ng/ml和2.0 ng/ml)處的Kappa值分別為0.878(P=4.60×10-7)和0.933(P=7.72×10-8),陽性符合率分別為94.44%和100.00%,陰性符合率分別為93.33%和95.45%。結(jié)論? 三聯(lián)生物微陣列化學發(fā)光免疫分析法與羅氏電化學發(fā)光法測定血清PCT結(jié)果相關性和一致性好,可用于臨床血清PCT的快速檢測。
關鍵詞:降鈣素原;血清;羅氏電化學發(fā)光法;三聯(lián)生物微陣列化學發(fā)光免疫分析法
中圖分類號:R346? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? 文獻標識碼:A? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ?DOI:10.3969/j.issn.1006-1959.2019.06.055
文章編號:1006-1959(2019)06-0169-03
Abstract:Objective? To investigate the reliability of the triple biomicroarray chemiluminescence detection system for the determination of serum procalcitonin (PCT) results. Methods? The Roche Cobas e 601 electrochemiluminescence detection system was used as the reference system. The triple biomicroarray chemiluminescence detection system was used as the system to be evaluated. The serum PCT concentration was measured and statistically analyzed. Results? The coefficient of variation (CV) of intra-day precision of PCT in the Roche electrochemiluminescence detection system was 5.33%~7.88%, and the daytime CV was 5.62%~8.56%. The intra-day CV of the triple biomicroarray chemiluminescence detection system was 4.93%~7.28%, and the daytime CV was 5.47%~8.90%. The two detection systems have a good correlation (regression equation y=1.174x+0.213, P<0.05) and the correlation coefficient r2 is 0.997. The Kappa values at the medical decision level (PCT 0.50 ng/ml and 2.0 ng/ml) were 0.878 (P=4.60×10-7) and 0.933 (P=7.72×10-8), respectively. The positive coincidence rates were 94.44% and 100.00%, the negative coincidence rate was 93.33% and 95.45%.Conclusion? The triple biomicroarray chemiluminescence immunoassay and Roche electrochemiluminescence method have good correlation and consistency in the determination of serum PCT results, which can be used for rapid detection of clinical serum PCT.
Key words:Procalcitonin;Serum;Roche electrochemiluminescence;Triple biomicroarray chemiluminescence immunoassay
降鈣素原(procalcitonin,PCT)是目前公認的細菌感染的標志物[1]。臨床上,PCT常用于膿毒血癥、感染性休克的輔助診斷,在小兒顱內(nèi)感染[2],血流感革蘭氏陰、陽性菌[3],凝固酶陰性葡萄球菌血流感染和污染血標本[4]等的鑒別診斷中發(fā)揮著重要作用。早期及時、準確測定血清PCT水平對及時發(fā)現(xiàn)潛在的細菌感染、積極指導臨床用藥和術后感染監(jiān)測等均有重要意義。目前,由于儀器、試劑盒測定方法和實驗室檢測能力的差異,導致血清PCT測定結(jié)果仍有較大差異。為積極響應國家對國產(chǎn)儀器的研發(fā)、轉(zhuǎn)化與應用,本研究以我院常用的羅氏電化學發(fā)光檢測系統(tǒng)為參考檢測系統(tǒng),首次對江蘇三聯(lián)生物工程有限公司生產(chǎn)的微陣列化學發(fā)光免疫分析系統(tǒng)測定血清PCT結(jié)果的準確性和一致性進行評估,為該儀器及配套試劑的臨床應用提供依據(jù)。
1材料與方法
1.1研究對象? 收集西南醫(yī)科大學附屬醫(yī)院檢驗科2018年3月12日~28日臨床測定無溶血、黃疸、脂血的血清樣品共66份。依據(jù)美國臨床實驗室標準化協(xié)會(CLSI)EP-9A《用患者樣品進行方法學比對及偏倚評估-批準指南》及CLSI EP15-A文件的要求,采用參考檢測系統(tǒng)和比對檢測系統(tǒng)在室內(nèi)質(zhì)控均在控下同時測定血清PCT濃度[5]。本研究采用患者檢測后剩余血清做方法學比對,對患者無任何損害和潛在風險,故不再提交倫理委員會審評及受試者知情同意書。
1.2儀器與試劑? 采用羅氏Cobas e601電化學發(fā)光檢測系統(tǒng)及其配套PCT試劑為參考檢測系統(tǒng),試劑盒批號為(LOT:30297504)。江蘇三聯(lián)生物全自動生物芯片分析儀(SLXP-002)及配套試劑為待比對檢測系統(tǒng),試劑盒批號為(LOT:C180307k01)。采用羅氏配套質(zhì)控品(LOT:0027316),低、高質(zhì)控靶值分別為0.47 ng/ml和9.23 ng/ml。
1.3質(zhì)量控制? 按照儀器標準操作程序嚴格對儀器進行維護、保養(yǎng)、室內(nèi)質(zhì)控,在質(zhì)控結(jié)果在控時測定待檢樣品,獲得測定結(jié)果。
1.4測定方法? 分別采用兩套系統(tǒng)對66份臨床血清樣品進行測定并進行統(tǒng)計分析。血清標品均采用美國BD公司真空采血管(含促凝劑)3.5 ml,采樣后及時送檢,3500 r/min,離心10 min分離血清并在6 h完成測定。室內(nèi)質(zhì)控在控下,分別采用高(6.33 ng/ml)、低濃度(0.58 ng/ml)血清樣品連續(xù)測定20次,計算均值(x)、標準差(s)和CV(%);將高、低值血清樣品各分裝20支,-20℃凍存。每日隨機解凍高、低值血清樣本1支并隨標本測定,連續(xù)測定10 d,評價兩種檢測系統(tǒng)的天間精密度。參照試劑說明書,以靶值±10%為日間CV%的允許范圍,其中系統(tǒng)誤差(SE%)小于靶值±20%為臨床可接受標準[6]。
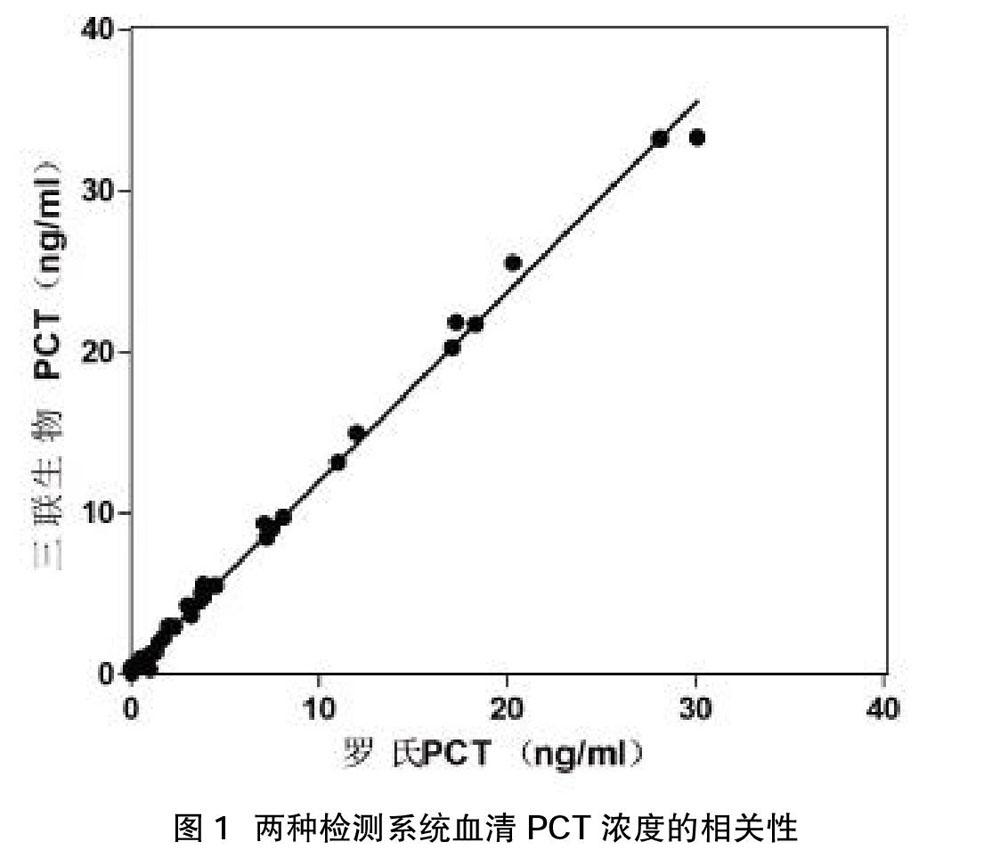
1.5統(tǒng)計學分析? 數(shù)據(jù)分析采用SPSS 17.0軟件完成,由于羅氏Cobas e601為電化學發(fā)光法,三聯(lián)生物為間接酶化學發(fā)光,故采用Pearson相關系數(shù)評價兩種檢測系統(tǒng)的相關性,若相關系數(shù)r2≥0.950(P<0.05),說明兩種方法相關性好。在血清PCT濃度分別為0.50 ng/ml、2.0 ng/ml時,用?字2檢驗計算兩類方法的一致性(Kappa值)、陽性符合率、陰性符合率和一致性系數(shù)(K),K>0.75則提示兩類方法的一致性好,0.4 2結(jié)果 2.1精密度分析? 羅氏電化學發(fā)光檢測系統(tǒng)測定低值和高值血清PCT樣品的日內(nèi)精密度的CV為7.88%和5.33%,日間精密度CV為8.56%和5.62%。三聯(lián)生物全自動生物芯片分析儀測定測定低值和高值血清PCT樣品的日內(nèi)精密度的CV為7.28%和4.93%,日間精密度的CV為8.90%和5.47%,均符合臨床要求。 2.2相關性分析? 以參考檢測系統(tǒng)血清PCT濃度為x,比對檢測系統(tǒng)血清PCT濃度為y,進行回歸分析。血清PCT濃度的回歸方程為y=1.174x+0.213,r2=0.997(P<0.05),見圖1。 2.3兩種檢測系統(tǒng)樣品符合率比較? 以血清PCT濃度分別為0.50 ng/ml、2.0 ng/ml為臨界值(cut-off值),計算陽性和陰性符合率,陽性符合率分別為94.44%和100.00%,陰性符合率分別為93.33%和95.45%。 2.4兩種檢測系統(tǒng)一致性分析? 對以上數(shù)據(jù)進行?字2檢驗并計算Kappa系數(shù)(K),兩種檢測系統(tǒng)血清PCT濃度分別以0.50 ng/ml(表1)、2.0 ng/ml(表2)為臨界值(cut-off值)的K值為0.878(P=4.60×10-7)和0.933(P=7.72×10-8),K均>0.75,說明兩種方法有很好的一致性。 3討論 PCT是116個氨基酸組成的分子量為12.7 kD的激素原,在正常人體血清含量極低,細菌感染后顯著增高[7]。研究表明,動物和人體發(fā)生菌血癥時血清PCT水平顯著升高,尤其是膿毒血癥和感染性休克[8,9]。血清PCT水平<0.50 ng/ml時預示低風險的嚴重膿毒血癥或感染性休克,PCT水平>2.0 ng/ml時預示高風險的嚴重膿毒血癥或感染性休克。本研究以血清PCT水平分別為0.50 ng/ml和2.0 ng/ml為cut-off值進行方法學比對,兩種方法的陽性、陰性符合率均>93.0%,Kappa系數(shù)均>0.75(P<0.05),提示兩類方法有良好的符合率和一致性。 隨著國產(chǎn)儀器的研發(fā)和推廣,基于不同檢測原理測定血清PCT的方法日新月異,這不僅要求測定結(jié)果準確、可靠,同時需降低成本,節(jié)約時間,降低患者經(jīng)濟負擔。本實驗室待評估系統(tǒng)PCT定量檢測試劑盒采用微陣列化學發(fā)光免疫分析原理,以活化處理的硬基質(zhì)玻片為芯片基質(zhì),通過特殊處理將單克隆抗體固定在基質(zhì)玻片上捕獲待測抗原,再加入辣根過氧化物酶標記抗體形成雙抗夾心結(jié)構(gòu),最后加入發(fā)光檢測液,酶促間接化學發(fā)光。本方法具有樣品用量少、靈敏,特異,快速等優(yōu)點,尤其適用于床旁快速定量檢測。參考檢測系統(tǒng)測定血清PCT為雙抗體免疫磁珠電化學發(fā)光法。通過生物素和三聯(lián)吡啶釕標記的單克隆PCT抗體結(jié)合待測血清中PCT形成雙抗體夾心法,再通過生物素結(jié)合鏈霉親和素包被的免疫磁珠,電極吸附、分離,電化學發(fā)光檢測。該方法,具有靈敏度高,結(jié)果穩(wěn)定等優(yōu)點。兩者比較,三聯(lián)生物微陣列化學發(fā)光免疫分析法具有更低的儀器、試劑和耗材成本,可用于臨床血清PCT快速測定。 由于兩種系統(tǒng)檢測原理不同,不能直接采用CLSI EP9-A3文件進行醫(yī)學決定水平處的偏倚評估和配對比較測定結(jié)果。因此,本研究采用相關分析對兩類方法進行比較,r2>0.950(P<0.05),表明兩種方法相關性良好。該結(jié)果提示,在驗證的數(shù)據(jù)分布范圍內(nèi)可通過回歸分析并結(jié)合參考值及對比方法的系統(tǒng)誤差在控,間接判斷兩套系統(tǒng)的可比性和臨床可接受性。由于現(xiàn)有文獻未見三聯(lián)生物微陣列化學發(fā)光免疫分析法測定血清降鈣素原參考區(qū)間的相關報道,故后續(xù)需嚴格按照CLSI C28-A3文件建立該方法正常人的參考區(qū)間、大樣本驗證并結(jié)合臨床制定新的臨界值。
綜上所述,三聯(lián)生物微陣列化學發(fā)光免疫分析系統(tǒng)與羅氏電化學發(fā)光檢測系統(tǒng)有很好的可比性和一致性,可用于臨床血清PCT的快速定量分析。
參考文獻:
[1]Wong D,Rubinshtein R,Keynan Y.Alternative cardiac imaging modalities to echocardiography for the diagnosis of infective endocarditis[J].Am J Cardiol,2016,118(9):1410-1418.
[2]孫裕平,馬少春,喬凌燕,等.降鈣素原和基質(zhì)金屬蛋白酶-9在小兒顱內(nèi)感染中的改變及其價值探討[J].中華急診醫(yī)學雜志,2016,25(12):1305-1308.
[3]張群,胡曉波.降鈣素原在革蘭陽性菌和革蘭陰性菌感染鑒別診斷中的價值探討[J].檢驗醫(yī)學,2015,30(11):1113-1118.
[4]楊菲,蔡成森,張險峰,等.降鈣素原鑒別血液科患者凝固酶陰性葡萄球菌血流感染與污染的臨床價值[J].中國感染與化療雜志,2018,18(1):48-52.
[5]王臣玉,楊麗萍,陳磊,等.兩種降鈣素原檢測系統(tǒng)比較實驗研究[J].現(xiàn)代檢驗醫(yī)學雜志,2017,32(4):143-144.
[6]周曉娜,王愛林,孫淑艷.兩種血清降鈣素原檢測系統(tǒng)的方法學對比及偏差評估[J].南方醫(yī)科大學學報,2014,34(5):683-685.
[7]Memar MY,Varshochi M,Shokouhi B,et al.Procalcitonin: The marker of pediatric bacterial infection[J].Retour Au Numéro,2017(96):936-943.
[8]Gao L,Liu X,Zhang D,et al.Early diagnosis of bacterial infection in patients with septicopyemia by laboratory analysis of PCT, CRP and IL-6 [J].Experimental & Therapeutic Medicine,2017,13(6):3479-3483.
[9]Hu C,Zhou Y,Liu C,et al.Pentraxin-3, procalcitonin and lactate as prognostic markers in patients with sepsis and septic shock[J].Oncotarget,2018,9(4):5125-5136.
收稿日期:2018-12-24;修回日期:2018-1-6
編輯/錢洪飛

