沙利度胺影響腫瘤壞死因子受體表達(dá)對(duì)大鼠慢性坐骨神經(jīng)縮窄的鎮(zhèn)痛效應(yīng)
蘇曉英 陳素明 周飛仁 王清秀
(1綿陽(yáng)市第三人民醫(yī)院 四川省精神衛(wèi)生中心,四川 綿陽(yáng) 621000;2同濟(jì)大學(xué)醫(yī)學(xué)院附屬上海市東方醫(yī)院麻醉科)
凡涉及軀體感覺神經(jīng)系統(tǒng)的損傷或疾病而引起的慢性疼痛即神經(jīng)病理性疼痛(NP)〔1〕,其臨床表現(xiàn)以疼痛過(guò)敏、感覺異常、自發(fā)性疼痛等為主要癥狀,患者常因劇烈疼痛而痛苦不堪〔2,3〕。對(duì)于NP的發(fā)病機(jī)制,目前國(guó)內(nèi)外的探究熱點(diǎn)主要圍繞分子神經(jīng)生物學(xué)機(jī)制,包括炎癥介質(zhì)作用、中樞敏化、中樞去抑制等〔4,5〕。其中,炎癥介質(zhì)作用中研究較為普遍的是細(xì)胞因子腫瘤壞死因子(TNF)〔6〕,而TNF受體(TNFR)的表達(dá)來(lái)體現(xiàn)其效應(yīng)高低〔7,8〕。可見,體內(nèi)TNFR(包括TNFR1、TNFR2)表達(dá)水平與NP發(fā)病密切相關(guān),在傷害性信號(hào)傳導(dǎo)通路中起關(guān)鍵作用。沙利度胺曾因其強(qiáng)致畸作用引起新生兒先天性四肢殘缺而一度被禁用,現(xiàn)代醫(yī)學(xué)研究發(fā)現(xiàn)在一定劑量下,沙利度胺具有鎮(zhèn)靜止癢、免疫調(diào)節(jié)、抗腫瘤等多方面的作用〔9,10〕。沙利度胺可減弱TNFR1、TNFR2 mRNA及蛋白的表達(dá)并調(diào)節(jié)TNF誘導(dǎo)的其他細(xì)胞因子分泌〔11〕,減輕炎癥反應(yīng),這極可能與其鎮(zhèn)痛機(jī)制相關(guān)。而目前沙利度胺與TNFR表達(dá)對(duì)NP的鎮(zhèn)痛作用尚未得到驗(yàn)證,其劑量效應(yīng)關(guān)系需要進(jìn)一步探究。本文擬分析慢性坐骨神經(jīng)縮窄(CCI)大鼠不同劑量下沙利度胺對(duì)TNFR表達(dá)水平的影響,以評(píng)估沙利度胺與TNFR的鎮(zhèn)痛效果。
1 材料與方法
1.1實(shí)驗(yàn)動(dòng)物及分組 清潔級(jí)成年雄性SD大鼠50只,體重200~250 g,購(gòu)于上海西普爾必凱實(shí)驗(yàn)動(dòng)物有限公司。隨機(jī)分為5組各10只:假手術(shù)組(S組)、CCI組(C組)、低劑量沙利度胺組(L組)、中劑量沙利度胺組(M組)、高劑量沙利度胺組(H組)。S組暴露坐骨神經(jīng)不結(jié)扎,其余4組建造CCI模型。
1.2大鼠CCI模型建造 實(shí)驗(yàn)大鼠腹腔注射1%戊巴比妥鈉(40 mg/kg)麻醉,固定于手術(shù)臺(tái)并確保器械消毒;在大鼠右下肢股后中部切開皮膚,沿肌肉紋理鈍性分離股二頭肌進(jìn)而暴露坐骨神經(jīng)干。近分叉處采用鉻制腸線做4個(gè)疏松結(jié)扎,每個(gè)結(jié)扎環(huán)間距大約1 mm。結(jié)扎程度以大鼠大腿肌肉輕微抽出為標(biāo)準(zhǔn),不影響血管血運(yùn)。創(chuàng)面消毒沖洗后逐層縫合,術(shù)后分籠喂養(yǎng)。
1.3術(shù)后處理 根據(jù)預(yù)實(shí)驗(yàn)結(jié)果,L組劑量20 mg/kg,M組50 mg/kg,H組100 mg/kg;采用固定灌胃器每日1次處理實(shí)驗(yàn)大鼠,術(shù)后灌胃持續(xù)1 w。
1.4大鼠機(jī)械性痛閾與熱痛閾測(cè)定 機(jī)械性痛閾測(cè)量:所有大鼠于手術(shù)前,手術(shù)后1、2、3及4 w測(cè)定并記錄其機(jī)械性痛閾與熱痛閾。機(jī)械性痛閾采用von Frey纖維,使尼龍纖維毛垂直刺激大鼠右足底皮膚,逐漸加壓,刺激持續(xù)時(shí)間不超過(guò)4 s;陽(yáng)性反應(yīng)為大鼠出現(xiàn)添足、縮足、抬足等躲避行為,反之為陰性反應(yīng),以出現(xiàn)陽(yáng)性反應(yīng)的壓力值為機(jī)械性痛閾。操作重復(fù)5次,取其平均值。
熱痛閾測(cè)量:熱痛閾以紅外線為輻射源,將實(shí)驗(yàn)大鼠置于輻射熱測(cè)痛儀中,穩(wěn)定5 min后,紅外線照射大鼠右側(cè)足底部皮膚,記錄大鼠出現(xiàn)縮足的潛伏期并防止過(guò)度輻射燙傷大鼠。重復(fù)操作3次,每次間隔10 min,取平均值。
1.5TNFR表達(dá)產(chǎn)物測(cè)定 于手術(shù)后第4周,處死所有實(shí)驗(yàn)大鼠,取其脊髓背角組織,測(cè)定其TNFR1、TNFR2 mRNA及蛋白質(zhì)含量。
1.5.1Western印跡檢測(cè)TNFR蛋白含量 采用GE蛋白印跡系列儀器,一抗TNFR1、TNFR2單克隆抗體及二抗辣根過(guò)氧化物酶標(biāo)記單克隆抗體購(gòu)于碧云天生物有限公司。
脊髓背角組織經(jīng)機(jī)械分散后溶于十二烷基硫酸鈉(SDS)凝膠加樣緩沖液,于4℃,1 200 r/min離心15 min,取上清液作為檢測(cè)樣品并按常規(guī)方法進(jìn)行SDS-聚丙烯酰氨凝膠電泳(PAGE);用轉(zhuǎn)膜緩沖液平衡5 min后轉(zhuǎn)膜,將蛋白質(zhì)從凝膠轉(zhuǎn)移到聚偏二氟乙烯(PVDF)膜上;加入封閉液(5%脫脂牛奶)室溫下封閉2 h;棄封閉液,用0.01 mol/L磷酸鹽緩沖液(PBS)洗膜3次,每次5 min;浸入第一抗體溶液液(稀釋1∶1 000)TNFR1、TNFR2兔抗人單克隆抗體,4℃反應(yīng)12 h;次日棄一抗,0.01 mol/L PBS洗膜,加入辣根過(guò)氧化物酶二抗稀釋液,室溫下反應(yīng)1 h。以β-actin蛋白為內(nèi)參蛋白,分析4組蛋白相對(duì)表達(dá)量。
1.5.2實(shí)時(shí)熒光定量PCR測(cè)定TNFR mRNA含量 采用ABI stepone Real-time PCR儀,總RNA提取試劑盒、逆轉(zhuǎn)錄試劑盒購(gòu)于北京天根有限公司。Trizol試劑提取組織上清液樣本總RNA,加入等體積異丙醇后振蕩混勻,離心10 min,收集沉淀。75%乙醇清洗沉淀,超凈臺(tái)風(fēng)干,而后用焦碳酸二乙酯(DEPC)溶解,逆轉(zhuǎn)錄合成cDNA。選用β-actin為內(nèi)參基因,檢測(cè)各組TNFR1、TNFR2 mRNA的Ct值,運(yùn)用公式2-△△CT計(jì)算4組目的基因的相對(duì)表達(dá)量,操作重復(fù)3次。實(shí)驗(yàn)中,內(nèi)參基因及各目的基因引物序列如表1。
1.6統(tǒng)計(jì)方法 應(yīng)用SPSS19.0軟件進(jìn)行重復(fù)測(cè)量方差分析和Pearson相關(guān)性分析。
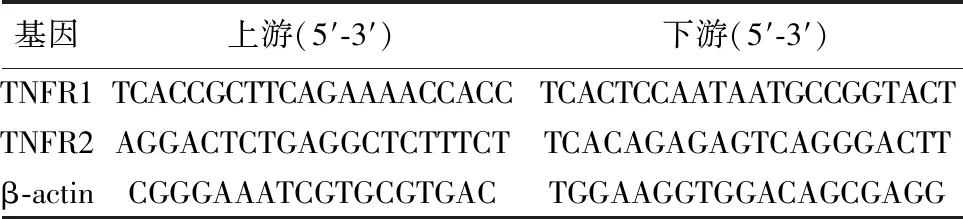
表1 實(shí)時(shí)熒光定量PCR檢測(cè)TNFR基因表達(dá)的引物序列
2 結(jié) 果
2.1術(shù)后不同時(shí)間點(diǎn)下各組機(jī)械性痛閾與熱痛閾的變化 S組在術(shù)前術(shù)后的機(jī)械性痛閾與熱痛閾均無(wú)明顯改變(P>0.05),其余4組術(shù)后痛閾、熱閾均有明顯下降(P<0.05);C組術(shù)后第4周時(shí)機(jī)械性痛閾較術(shù)后第1周明顯升高(P<0.05),而術(shù)后其他時(shí)間點(diǎn)下的機(jī)械性痛閾與術(shù)后各時(shí)間點(diǎn)的熱痛閾無(wú)明顯差異(P>0.05);L組、M組、H組在術(shù)后機(jī)械性痛閾、熱痛閾隨時(shí)間呈上升趨勢(shì)(P<0.05)。術(shù)后C組對(duì)比S組,機(jī)械性痛閾與熱痛閾明顯降低(P=0.000);C組術(shù)后的機(jī)械性痛閾、熱痛閾顯著低于L組(P<0.01);機(jī)械性痛閾、熱痛閾相比,H組顯著高于M組(P=0.000),M組顯著高于L組(P=0.000),見表2。
2.24組TNFR1、TNFR2 mRNA及蛋白相對(duì)表達(dá) 與C組比較,L組、M組及H組TNFR1 mRNA和蛋白含量均明顯降低(P<0.05);H組TNFR1基因表達(dá)產(chǎn)物含量最低,其次為M組,L組相比于前兩組,TNFR1 mRNA與蛋白表達(dá)水平略高(P<0.05);而各組TNFR2基因表達(dá)產(chǎn)物,mRNA與相應(yīng)蛋白含量無(wú)明顯差別(P>0.05),見表3、圖1。
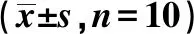
表2 各組不同時(shí)間機(jī)械性痛閾、熱痛閾測(cè)量值
機(jī)械性痛閾F①-②組內(nèi)=15.103,P①-②組內(nèi)=0.000;F②-③組內(nèi)=7.287,P②-③組內(nèi)=0.000;F③-④組內(nèi)=6.432,P③-④組內(nèi)=0.000;F④-⑤組內(nèi)=8.045,P④-⑤組內(nèi)=0.000;熱痛閾:F①-②組內(nèi)=11.651,P①-②組內(nèi)=0.000;F②-③組內(nèi)=3.393,P②-③組內(nèi)=0.001;F③-④組內(nèi)=5.445,P③-④組內(nèi)=0.000;F④-⑤組內(nèi)=5.673,P④-⑤組內(nèi)=0.000;與術(shù)前相比:1)P<0.05;與術(shù)后第1周相比:2)P<0.05
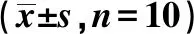
表3 4組TNFR mRNA及蛋白表達(dá)比較
1)與C組相比;2)與L組相比;3)與M組相比:均P<0.05
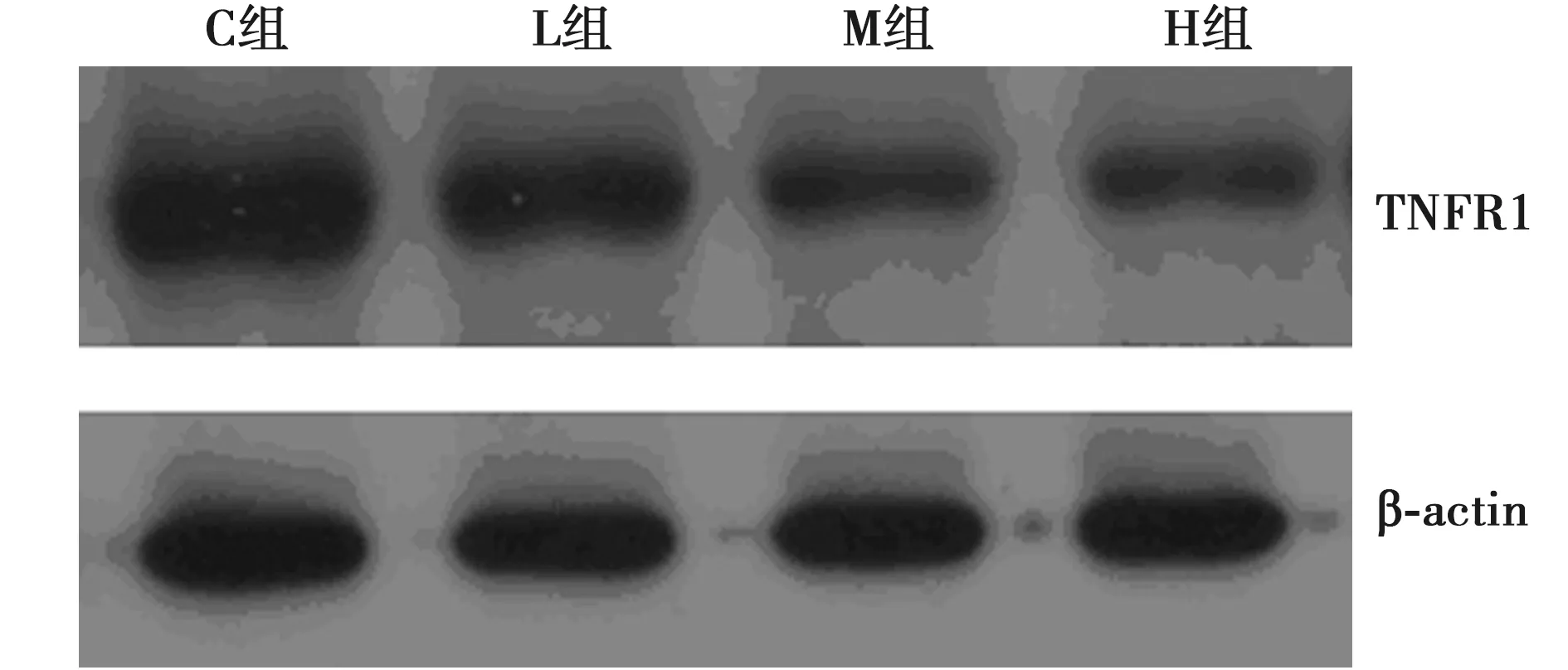
圖1 4組TNFR1蛋白印跡
2.3沙利度胺劑量濃度與TNFR1 mRNA相對(duì)表達(dá)水平的相關(guān)性 隨著沙利度胺濃度的增加,組織細(xì)胞中mRNA相對(duì)表達(dá)水平不斷下降,二者呈明顯負(fù)相關(guān)(r=-0.497,P=0.036),見圖2。
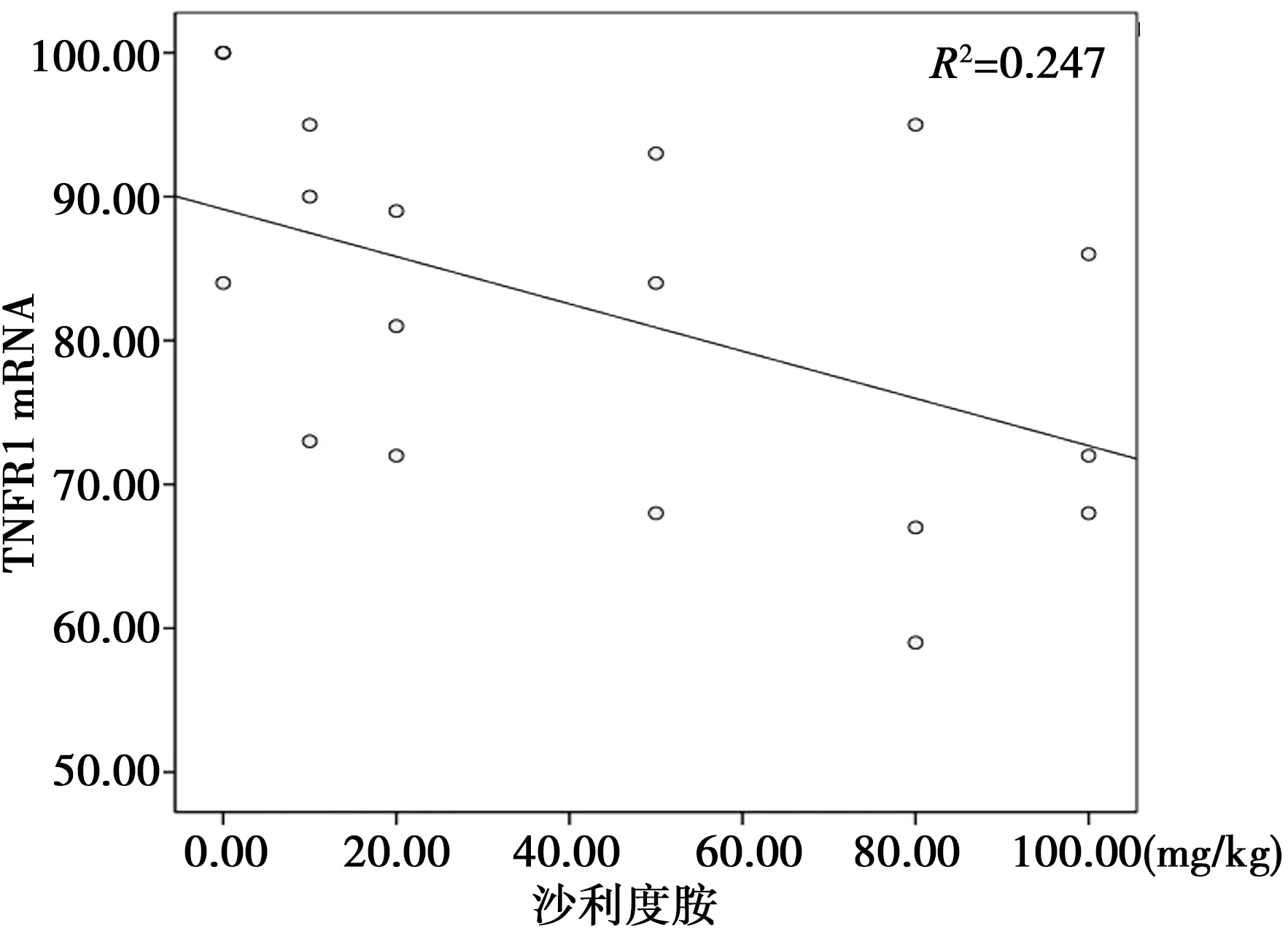
圖2 沙利度胺濃度與TNFR1 mRNA相對(duì)表達(dá)水平的相關(guān)性
3 討 論
目前,臨床治療NP的首要原則是緩解患者疼痛,而傳統(tǒng)的鎮(zhèn)痛藥卻難以達(dá)到理想效果,阿片類藥物雖效果明確,但其不良反應(yīng)嚴(yán)重,無(wú)法成為一線藥物〔12〕,而非甾體抗炎藥只對(duì)部分患者有效,其安全性尚未得到證實(shí)〔13〕。現(xiàn)今較為深入研究的細(xì)胞機(jī)制有傷害性疼痛傳導(dǎo)通路及其相關(guān)的基因、蛋白、細(xì)胞因子等,其中,促炎細(xì)胞因子TNF因在傷害性傳導(dǎo)通路中起關(guān)鍵作用備受關(guān)注〔14,15〕。而TNF的最終作用效應(yīng)由其受體水平?jīng)Q定〔16〕,因此,TNFR表達(dá)水平與NP存在密切關(guān)系。
沙利度胺是臨床常見的鎮(zhèn)靜藥,具有鎮(zhèn)靜、止癢、抗炎、抑制血管生成的功能〔17,18〕。Moreira 等〔19〕在所研究的動(dòng)物模型中提出沙利度胺的鎮(zhèn)靜機(jī)制極可能是通過(guò)下調(diào)TNFR水平實(shí)現(xiàn)的。機(jī)械性痛閾與熱痛閾是大鼠CCI模型中常見的測(cè)量指標(biāo)〔20,21〕,其測(cè)量值能較好地反映大鼠疼痛程度,間接反映藥物的鎮(zhèn)痛效果。本研究提示沙利度胺的鎮(zhèn)痛效應(yīng)極可能與其劑量相關(guān),劑量高,鎮(zhèn)靜效果相對(duì)較好。
TNFR包括TNFR1、TNFR2兩大類,兩者介導(dǎo)不同的信號(hào)傳導(dǎo)途徑,其中,TNFR1可表達(dá)于所有類型的細(xì)胞上,與TNF結(jié)合發(fā)揮生物活性;而TNFR2的功能與結(jié)構(gòu)尚未得到深入剖析。本實(shí)驗(yàn)提示沙利度胺可能具有下調(diào)TNFR1表達(dá)水平的功能,且TNFR1表達(dá)水平受沙利度胺劑量的影響,這極可能與沙利度胺對(duì)大鼠NP模型的鎮(zhèn)痛機(jī)制相關(guān)。TNFR2并不作用于傷害信號(hào)轉(zhuǎn)導(dǎo)通路,對(duì)TNF的生物活性無(wú)明顯影響。本文提示不同劑量的沙利度胺可能影響TNFR1 mRNA的表達(dá),隨著沙利度胺劑量的升高,抑制TNFR1 mRNA水平的效果越明顯。
本實(shí)驗(yàn)尚有不足之處,研究劑量過(guò)少,大鼠NP模型單一;同時(shí),傷害傳導(dǎo)通路涉及基因、細(xì)胞因子較多,沙利度胺是否完全通過(guò)下調(diào)TNFR mRNA及蛋白對(duì)NP大鼠產(chǎn)生鎮(zhèn)痛效果尚未可知,是否存在其他影響因子尚不明確。日后的實(shí)驗(yàn)中將細(xì)分沙利度胺濃度、納入更多大鼠NP模型,進(jìn)一步研究沙利度胺對(duì)NP大鼠模型的影響及作用機(jī)制。
綜上,沙利度胺可能通過(guò)影響TNFR1表達(dá)對(duì)大鼠CCI模型產(chǎn)生鎮(zhèn)痛效應(yīng),且其劑量與TNFR1表達(dá)水平可能相關(guān),有望作為神經(jīng)病理性疼痛的治療靶點(diǎn)之一,具有潛在臨床治療價(jià)值。

