氨基酸碘鹽中碘含量測定方法的研究
程月紅,任雪梅,于艷艷,王健,吳珍珍,鮑連艷,高牡丹
(山東省食品藥品檢驗研究院,山東 濟南 250101)
食鹽是人們日常生活中不可缺少、無法代替的必備調味品,多年來食鹽市場供需穩定,缺乏開發潛力且利潤逐漸壓縮,食鹽生產企業的生存和發展后勁不足,急切需要尋找新的經濟增長點。多品種鹽的出現,滿足了消費者的需求、豐富了食鹽市場,成為食鹽企業新的盈利點[1]。多品種鹽指添加營養強化劑、調味輔料或經特殊工藝加工制得的食鹽,主要品種有強化營養鹽、調味鹽、低鈉鹽、味精鹽、竹鹽等[2],本文研究的氨基酸碘鹽屬于強化營養鹽。食鹽攝入量過多會誘發多種疾病,如使高血壓、骨質疏松[3]、胃病、腎病、呼吸道疾病[4]等發病率大大增加,嚴重影響人體健康。我國居民高鹽膳食形成的口重習慣很難在短期內糾正,而氨基酸碘鹽的出現,因其減鹽不減咸、增味又增鮮的特點,短期內快速有效的減少了居民對食鹽的攝入量,達到了減鹽的目的。除此之外,氨基酸碘鹽含有人體必需的8 種氨基酸,營養豐富,對特定人群的氨基酸缺乏癥狀、偏食、厭食有緩解作用。
碘是人體必需的元素之一,在機體內不能合成,只能從食物中獲取,其主要生理功能通過甲狀腺素完成,人體嚴重缺乏時,甲狀腺組織呈增生性腫大[5],導致孕婦死胎、流產、早產及胎兒先天性畸形,兒童智力低下,發育遲緩等。當碘攝入量過多時,會引發甲狀腺結節[6]、甲狀腺功能亢進[7]等各種疾病,嚴重影響人體健康。食鹽加碘執行GB 26878-2011《食品安全國家標準食用鹽碘含量》,根據《食鹽加碘消除碘缺乏危害管理條例》普及供應添加碘酸鉀的碘鹽,根據不同地區加碘要求不同,加碘水平必須滿足相應地區的要求,因此準確檢測食鹽中碘尤為重要,目前檢測食鹽中碘的方法主要有光度法[8-10]、安倍法[11]、離子色譜法[12]、光譜法[13]等。這些方法需要使用儀器,或者操作較為繁瑣,本研究探討一種測定碘含量的簡單滴定方法,該檢測方法準確可靠,能夠為監管部門提供堅實有力的技術支持,利于食鹽中碘的管理,確保人們合理膳食。
1 材料與方法
1.1 材料與儀器
氨基酸碘鹽、精制碘鹽:均由超市購買;膠原蛋白(酸水解膠原蛋白得到氨基酸)、草酸、磷酸(體積分數為85%)、碘化鉀、次氯酸鈉溶液(有效氯10 %)、淀粉、硫代硫酸鈉標準滴定溶液(濃度為0.100 2 mol/L,臨用前稀釋50 倍):上海安譜實驗科技股份有限公司。本方法所用試劑均為分析純,水為GB/T 6682-2008《分析實驗室用水規格和試驗方法》規定的一級水。
MS204S 電子天平(精度 0.1 mg):梅特勒-托利多公司;DL-1 電子萬用爐:北京市永光明醫療儀器有限公司。
1.2 試驗方法
1.2.1 試驗原理
試樣加入沉淀劑除去氨基酸,溶液中碘離子在酸性條件下用次氯酸鈉氧化成碘酸根,草酸除去多余的次氯酸鈉,碘酸根氧化碘化鉀中碘離子生成單質碘,以淀粉溶液為指示劑,用硫代硫酸鈉標準滴定溶液滴定,計算試樣中碘的含量。
1.2.2 樣品處理
稱取一定量試樣,加水充分溶解后轉移到容量瓶中,加入沉淀劑,加水至刻度,搖勻,靜置約30 min,過濾,棄去初濾液,濾液備用。
1.2.3 碘的測定
準確移取一定量上述濾液于的三角瓶中,加入2 mL草酸-磷酸混合液,搖勻,加入1 mL 次氯酸鈉溶液,用水沖洗瓶壁,然后放在調溫電爐上加熱至沸騰并保持30 s,取下放入冰水浴中迅速冷卻到30 ℃以下。加入5 mL 碘化鉀溶液,搖勻,立即用硫代硫酸鈉標準滴定溶液滴定至淺黃色,加入1 mL 淀粉指示劑,繼續滴定至藍色剛剛消失為終點。同時做試劑空白。
1.2.4 碘含量測定條件的考察
1.2.4.1 沉淀劑種類對碘含量測定結果影響的考察
準確稱取一定質量的氨基酸碘鹽5 份,分別選用5 mL 的50%三氯乙酸、5 mL 的106 g/L 亞鐵氰化鉀和5 mL 的 220 g/L 乙酸鋅、20 mL 的甲醇、20 mL 的無水乙醇為沉淀劑,每加入一種試劑都充分搖勻,稀釋到200 mL,搖勻,靜置,過濾,準確移取 50 mL 濾液,按照1.2.3 的步驟測定,平行測定3 次計算其平均值為測定結果。
1.2.4.2 不同稱樣量、沉淀劑用量、沉淀時間對碘含量測定結果影響的考察
準確稱取氨基酸碘鹽 5、10、15、20、25 g,加入亞鐵氰化鉀和乙酸鋅 1、2、3、4、5、6 mL,沉淀時間為 10、15、20、25、30 min 的條件下檢測碘含量,考察不同稱樣量、沉淀劑用量、沉淀時間對碘含量的影響。每組進行3次平行測定,所得結果為3 次測定的平均值。
2 結果與分析
2.1 探討氨基酸碘鹽中碘的檢測
為了準確檢測氨基酸碘鹽中碘含量,采用多種處理方法,首先按照GB 5009.42-2016《食品安全國家標準食鹽指標的測定》[14]要求,樣品溶解后(不是完全溶解,底部沉有黃色不溶物)直接加入草酸-磷酸混合液、次氯酸鈉等測定,發現加入碘化鉀后,溶液顏色不是純藍色而是灰藍色,滴定近終點時,反應遲緩,根據顏色變化很難確定終點。考慮到黃色不溶物可能影響滴定反應,分別采取吸取上層清液和過濾后濾液進行測定,結果都在10 mg/kg 左右,與實際含量相差甚遠。由此推測,被過濾掉的黃色不溶物,可能是氨基酸與碘反應的產物,是使碘含量偏低的主要原因。為了消除氨基酸的影響,嘗試加入沉淀劑三氯乙酸沉淀蛋白質(因氨基酸本身是小分子蛋白質),結果約為25 mg/kg,因此推測沉淀蛋白質消除了氨基酸的影響。
2.2 氨基酸對測定碘的影響
為了證試氨基酸影響碘的測定,本文分別測定了精制碘鹽、精制碘鹽加氨基酸、精制碘鹽加氨基酸后沉淀除去氨基酸3 種情況下的碘含量,結果見表1。

表1 氨基酸對測定碘的影響Table 1 Effect of amino acids on the determination of iodine
樣品處理過程中發現,加有氨基酸的精制碘鹽不能完全溶解,與氨基酸碘鹽類似,有不溶性物質,過濾除去,滴定時終點反應緩慢,檢測結果與精制碘鹽相比明顯偏低,且平行性較差。分析精制碘鹽加氨基酸后沉淀除去氨基酸的檢測結果,和精制碘鹽相比,結果非常接近,由此證實了氨基酸影響碘的測定,并且可通過加入沉淀劑去除氨基酸,提高測定碘的準確性。
2.3 檢測條件優化
為了更準確的檢測氨基酸碘鹽中碘的含量,對樣品處理條件進行優化。
2.3.1 稱樣量對碘含量測定結果的影響
稱樣量不同對碘含量測定結果有較大影響,結果見圖1。
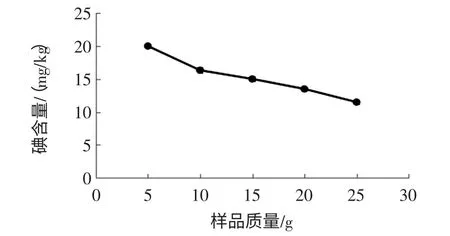
圖1 不同稱樣量檢測結果Fig.1 Different sample weight test results
由圖1所示,隨著樣品量的增加,檢測結果呈下降趨勢。根據2.2 分析結果,氨基酸影響碘的測定推測,樣品量越大,氨基酸沉淀不徹底,使碘的檢測結果降低。由于稱樣量少于5 g 時,檢測誤差較大,綜合考慮,稱樣量為5 g 時最佳。
2.3.2 不同沉淀劑對碘含量測定結果的影響
考察不同沉淀劑對碘含量測定結果的影響,結果見圖2。
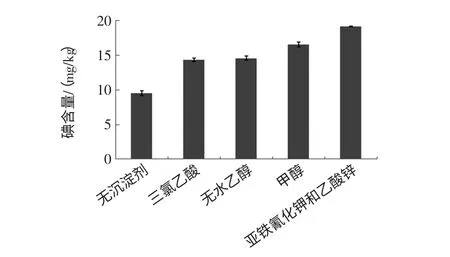
圖2 不同沉淀劑檢測結果Fig.2 Different precipitant test results
如圖2所示,與不加任何沉淀劑的檢測結果相比,加入沉淀劑后檢測值均升高,亞鐵氰化鉀和乙酸鋅為最佳沉淀劑,檢測結果最高。三氯乙酸主要沉淀大分子蛋白質[15],而氨基酸主要是小分子蛋白質,沉淀效果較差。有機溶劑能降低水的介電常數,使具有表面水層的生物大分子脫水,相互聚集沉淀,同樣對氨基酸小分子蛋白質沉淀效果較差。
2.3.3 沉淀劑用量對碘含量測定結果的影響
沉淀劑用量不同對碘含量測定結果的影響,結果見圖3。
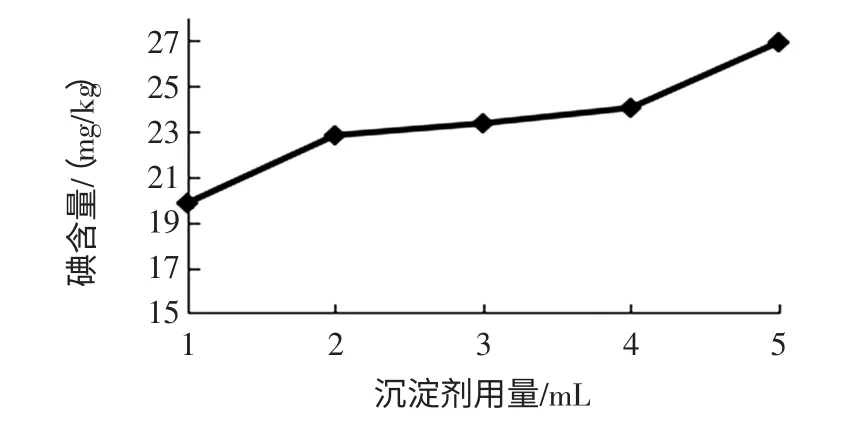
圖3 不同沉淀劑用量檢測結果Fig.3 Different precipitation agent dosage test results
如圖3所示,隨著沉淀劑的增加檢測結果呈上升趨勢,但沉淀劑增加到6 mL 時,試液在煮沸時出現沉淀,且滴定時反應慢,顏色變化緩慢,終點難以判斷,因此得出最佳沉淀劑用量為5 mL。
2.3.4 沉淀時間對碘含量測定結果的影響
沉淀時間對碘含量測定結果的影響,結果見圖4。
沉淀時間即陳化時間,陳化過程中,沉淀晶粒會不斷變大,其比表面減小,吸附雜質質量小,同時小晶粒溶解,原來吸附、吸留或包夾的雜質或目標物,重新進入溶液。沉淀時間越長,大晶粒越大,小晶粒溶解更完全,檢測碘的結果會更高。如圖4所示,隨著沉淀時間的變長,碘的檢測值越高,超過30 min 檢測值僅有微量變化,考慮到檢測周期不易太長,提高工作效率,故選擇最佳沉淀時間為30 min。
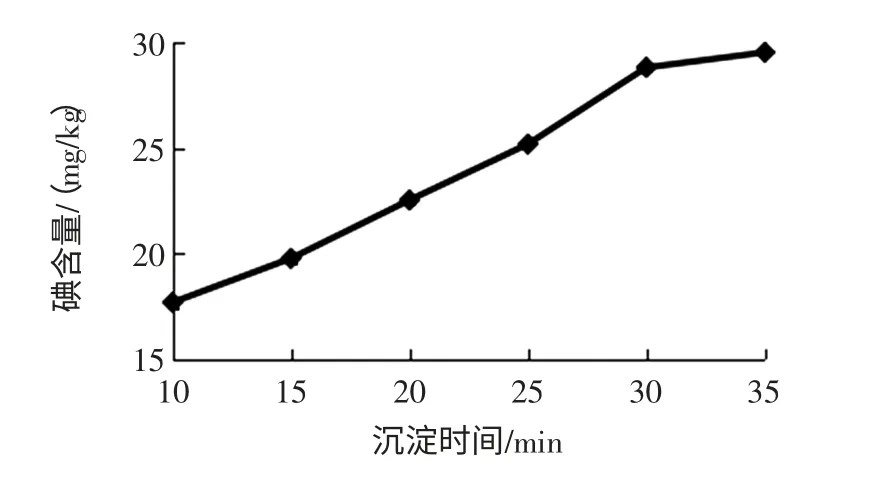
圖4 不同沉淀時間檢測結果Fig.4 Different precipitation time test results
2.4 精密度和重復性
在優化條件下,即稱樣5 g,分別加入5 mL 亞鐵氰化鉀溶液和乙酸鋅溶液,沉淀30 min,平行測定20 次,檢測結果按從小到大順序排列見表2。
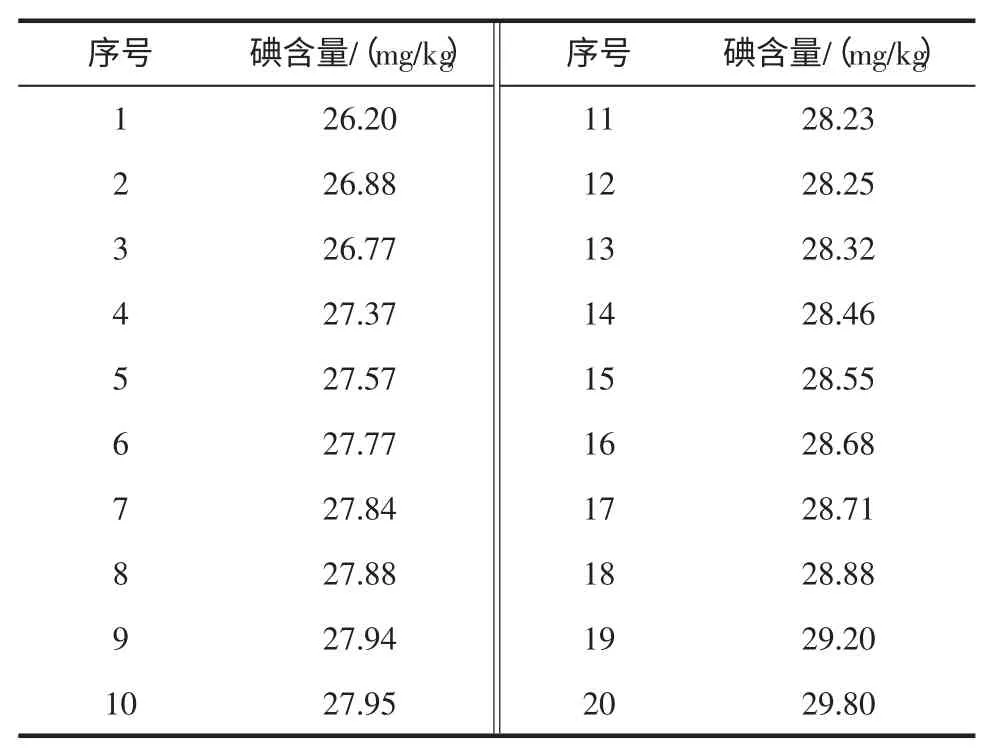
表2 試驗結果分析Table 2 Analysis of test results
根據格魯布斯法,從小到大排列20 個檢測數據,計算其平均值和標準偏差,假設第一個數據和最后一個數據為可疑值,由

查表 T0.05,20=2.56,T0.01,20=2.88,有此判定 20 個檢測值中不存在需要剔除的可疑值。因此檢測結果的平均值為28.06 mg/kg,標準偏差為0.85%,相對標準偏差為3.03 %,相對標準偏差小于7.5 %,符合GB/T 27417-2017《合格評定化學分析方法確認和驗證指南》對實驗室內變異系數的要求[16]。最大相對偏差為6.6%,符合國標方法GB 5009.42-2016 的精密度要求(10%),精密度和重復性良好。
2.5 與國標方法比對
相同的被測樣品(氨基酸碘鹽),采用GB 5009.42-2016 中的氧化還原滴定法,測定氨基酸碘鹽中碘的含量,結果見表3。

表3 國標方法檢測結果分析Table 3 Analysis of test results of national standard methods
由表3所示,采用GB 5009.42-2016 氧化還原滴定法檢測結果為9.80 mg/kg,與本文討論方法的檢測值28.06 mg/kg 相差甚遠,說明國標方法不適用于氨基酸碘鹽中碘的測定。
2.6 加標回收試驗
采用本文所述的方法,以氨基酸碘鹽為研究對象,進行加標回收試驗。加入0.154 7 mg/mL 的碘酸鉀溶液2 mL,平行測定6 次,計算回收率為90.4%~98.8%,均滿足GB/T 27404-2008《實驗室質量控制規范食品理化檢測》[17]對回收率范圍的要求。
3 結論
按照國標方法GB 5009.42-2016 檢測氨基酸碘鹽中的碘,檢測結果遠低于實際水平。本文通過考察多種方法,找到影響測定碘的關鍵物質即氨基酸。為了消除氨基酸的影響,首先考察了不同沉淀劑:三氯乙酸、無水乙醇、甲醇、亞鐵氰化鉀和乙酸鋅對檢測結果的影響,確定最佳沉淀劑為亞鐵氰化鉀和乙酸鋅。為了進一步優化檢測方法,進而對稱樣量、沉淀劑用量、沉淀時間進行考察,得到最佳檢測條件。在優化條件下,對本文所述方法進行確認,主要包括精密度和重復性、與國標方法比對、加標回收試驗,最后得出結論本方法準確度較高,精密度和重復性優于GB 5009.42-2016 的標準要求,且設備要求簡單、操作簡單易行,便于在企業和基層檢驗機構推廣應用。

