甲烷二氧化碳自熱重整工藝分析
劉俊義,祝 賀,張 軍
(1.山西潞安礦業(集團)有限責任公司,山西 長治 046204;2.中國科學院上海高等研究院低碳轉化科學與工程重點實驗室,上海 201203)
合成氣是一種重要的碳一化工原料氣,可以合成甲醇、甲酸甲酯、二甲醚、合成油等化工產品。以天然氣為原料重整制備合成氣,按照O 原子供應原料不同可分為:(1)水蒸氣為氧原料的濕重整SMR;(2)O2為氧原料的甲烷部分氧化POM;(3)CO2為氧原料的干重整;(4)上述兩種或三種物質為氧原料的耦合重整。
其中水蒸氣重整SMR,最早于1926 年成功工業化,但所得合成氣的n(H2)/n(CO)高(約為3),該工藝過程能耗高、投資大、設備龐大、生產成本高、活性組分為Ni 的催化劑面臨嚴重的積炭問題[1,2]。甲烷部分氧化POM,包括非催化部分氧化和催化部分氧化,非催化部分氧化為了獲得甲烷的高轉化率和最小的揮發分,要求溫度控制在1573 K 以上[3],不僅浪費資源并且對反應器材質的要求苛刻,催化部分氧化在催化床層中存在熱點并且容易發生爆炸[4],因此難以得到廣泛的工業應用。CO2干重整,同時利用溫室氣體二氧化碳和甲烷作為原料,原料來源廣泛,變廢為寶,獲得低n(H2)/n(CO)的合成氣,引起學術界和產業界的廣泛關注[5-7]。
CO2干重整的重難點包括催化劑和高溫條件下熱量供給等。制備高活性、高選擇性、高穩定性、耐熱性能好的催化劑是現階段國內外研究的重點,已取得了很多有意義的結果[8]。許崢等[7]根據CO2干重整可能包括的化學反應及熱力學數據指出,重整反應CH4+CO2=2CO+2H2是獨立的吸熱反應,高溫對反應有利,且只有t>645℃才是熱力學上可行的反應。甲烷部分氧化釋放的高溫熱量用于滿足干重整吸熱的能量所需,實現甲烷二氧化碳自熱重整(CO2/CH4/O2重整),將是一個高效節能的方法,這也是目前研究的熱點[9]。
本項目組前期通過熱力學Gibbs 自由能、計算流體力學CFD 方法等對自熱重整反應器進行了研究,并且在山西潞安進行了萬方級的中試實驗[10]。本文通過熱力學方法對甲烷二氧化碳自熱重整過程進行研究,分析其產物性質、轉化率等主要特點,為原料選擇、工藝條件、催化劑設計等提供幫助和指導。
1 二氧化碳自熱重整分析方法
甲烷二氧化碳自熱重整主要反應有:

反應(1)為甲烷燃燒反應。反應(2)為CO2-CH4重整反應,反應(3)為H2O-CH4重整反應,水蒸氣可為入口原料或過程產生,反應(2)和反應(3)均為可逆反應。反應(4)為逆水煤氣變換反應,是體系達到平衡的主要依據。
雖然甲烷二氧化碳自熱重整反應體系涉及諸多組分,只要反應器設計合理、催化劑性能優良,最終化學反應達到或者接近化學平衡,其產物及組成是確定的。
本項目組成功采用國內外在能源、化工等領域廣泛應用軟件Aspen plus 對甲烷二氧化碳自熱重整過程進行模擬分析[10],本文將采用Gibbs 自由能方法對CH4-CO2自熱重整過程進行多方面的分析,包括合成氣中CH4含量、二氧化碳轉化率、n(H2)/n(CO)、臨界性能等的研究分析。
相律是多組分多相平衡體系所遵循的普遍規律,帶有化學反應體系普遍的相律基本方程為:
F=2-π+N-r-S
其中:F 為自由度,π 為相數,N 為組分數,r 為獨立反應數,S 為補充方程式數。
CH4-CO2自熱重整體系中,不考慮碳,相數π=1,體系組分數N=6,獨立反應數r=3,由于絕熱過程氧供給決定平衡溫度,則補充方程式數S=1。因此,不考慮積炭的甲烷二氧化碳自熱重整體系自由度F=2-1+6-3-1=3。
2 結果與討論
2.1 CH4含量
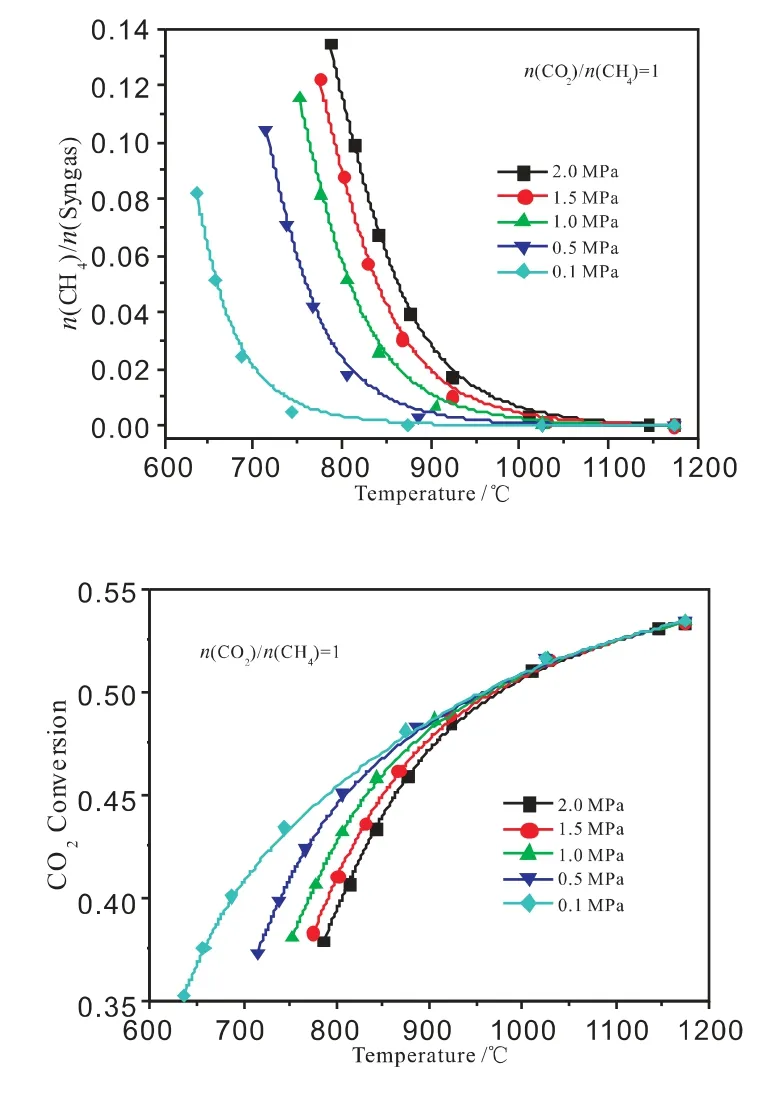
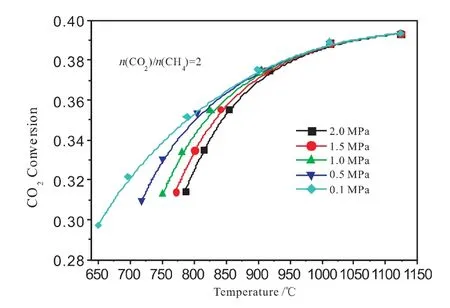
圖2 不同n(CO2)/n(CH4)時溫度、壓力對CO2轉化率的影響
不同n(CO2)/n(CH4)時,溫度、壓力對二氧化碳轉化率的影響見圖2。從圖2 可以看出:隨著平衡溫度的增加,二氧化碳轉化率增加;隨著轉化壓力的增加,二氧化碳轉化率降低;隨著原料氣n(CO2)/n(CH4)的增加,二氧化碳轉化率降低。
從反應(2)可知,重整反應是反應分子數增加的吸熱反應。因此,溫度增加有利于重整反應正向進行,溫度增加二氧化碳轉化率增加;增加壓力促進重整反應逆方向進行,壓力增加二氧化碳轉化率降低。原料氣n(CO2)/n(CH4)增加,有利于重整反應的進行,由于原料氣CH4恒定,雖然CO2轉化量增加,但二氧化碳轉化率卻降低。
2.3 氫碳比n(H2)/n(CO)
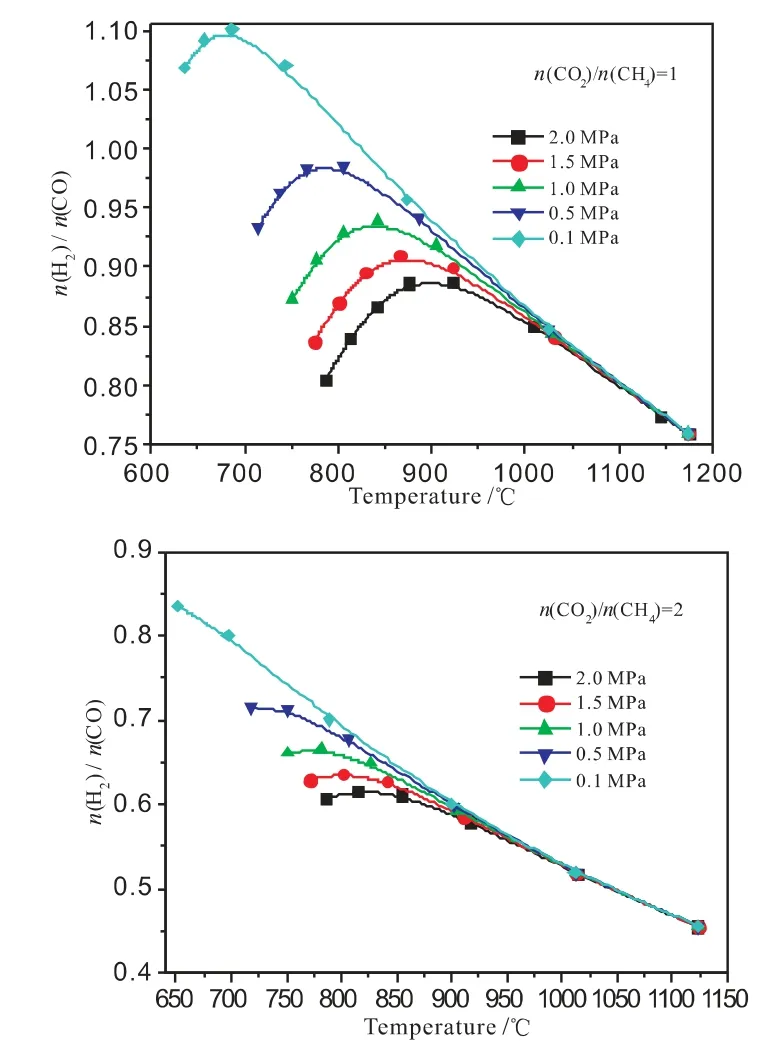
圖3 不同n(CO2)/n(CH4)時,溫度、壓力對合成氣n(H2)/n(CO)的影響
不同n(CO2)/n(CH4)時,溫度、壓力對合成氣n(H2)/n(CO)的影響見圖3。從圖3 可以看出:壓力增加,n(H2)/n(CO)降低;溫度對n(H2)/n(CO)的影響不是單調遞增或遞減;與溫度、壓力相比,n(CO2)/n(CH4)顯著影響n(H2)/n(CO)數值,n(CO2)/n(CH4)=1,n(H2)/n(CO)數值約0.9;n(CO2)/n(CH4)=2,n(H2)/n(CO)數值約0.6。
2.4 臨界性能
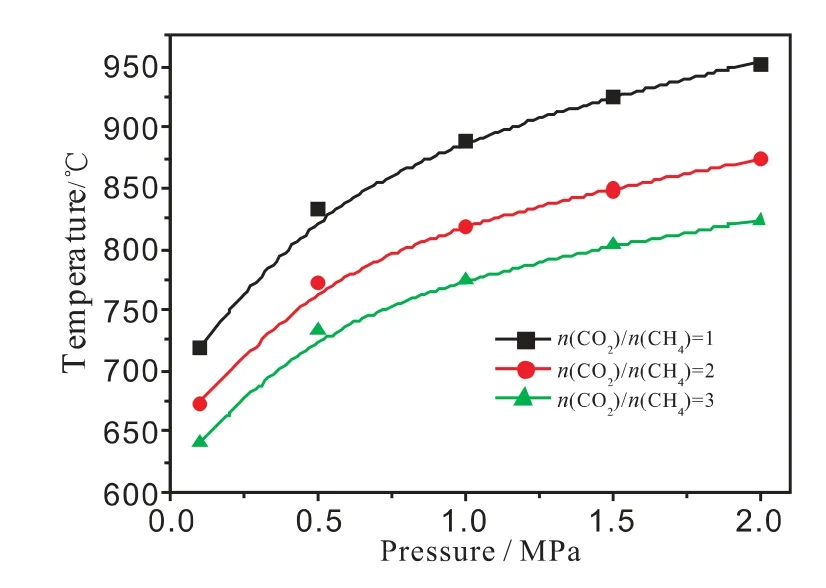
圖4 臨界條件時,n(CO2)/n(CH4)、重整溫度與壓力的關系
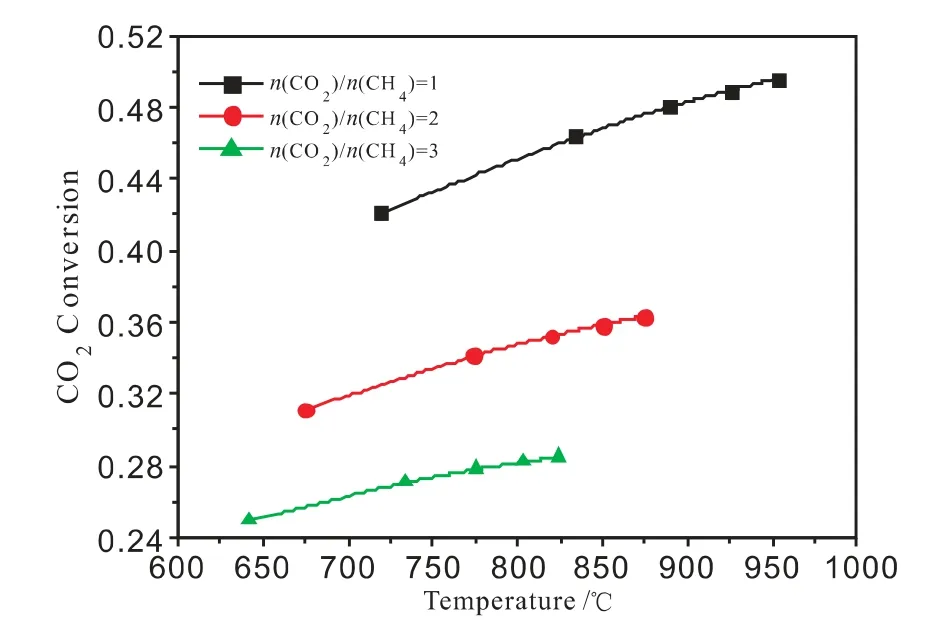
圖5 臨界條件時,n(CO2)/n(CH4)、重整溫度與二氧化碳轉化率的關系
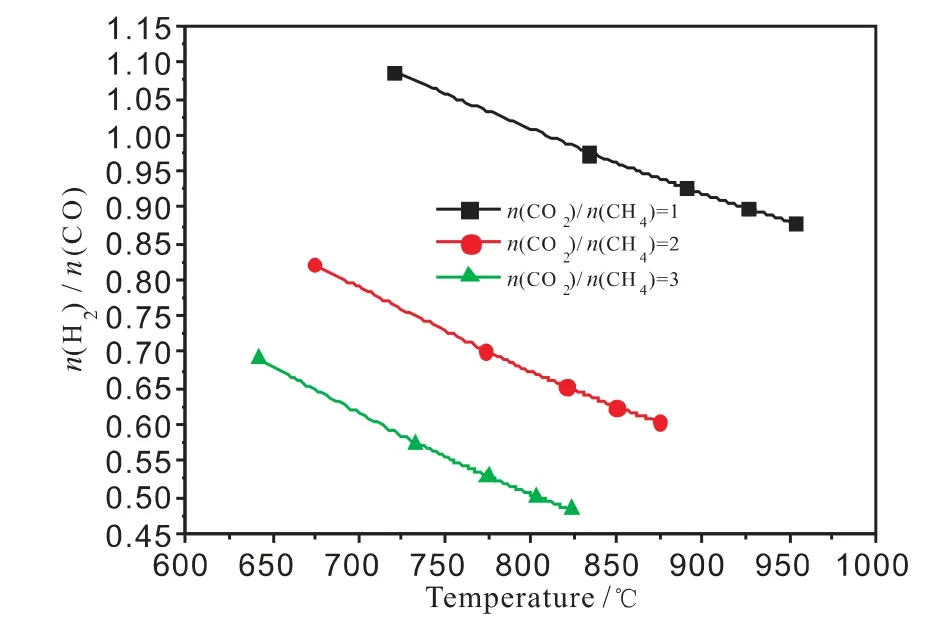
圖6 臨界條件時n(CO2)/n(CH4)、重整溫度與n(H2)/n(CO)的關系
重整工藝過程,合成氣中CH4含量的要求對工藝過程的原料氣組成、平衡溫度、操作壓力等參數有重要的制約作用。定義重整出口合成氣中甲烷含量為1%時為臨界條件。研究臨界條件下合成氣性質、二氧化碳轉化率、n(H2)/n(CO)等參數對工業過程及催化劑的研發有重要的指導意義。
根據前面分析可知,不考慮積炭,甲烷二氧化碳自熱重整體系自由度F=3,除合成氣中甲烷含量為1%之外,再提供兩個獨立條件就可確定反應體系其余參數。圖4~圖6 分別為臨界條件下n(CO2)/n(CH4)、重整平衡溫度與壓力、二氧化碳轉化率、單位甲烷的CO2轉化量以及n(H2)/n(CO)等重整過程特性參數的關系。
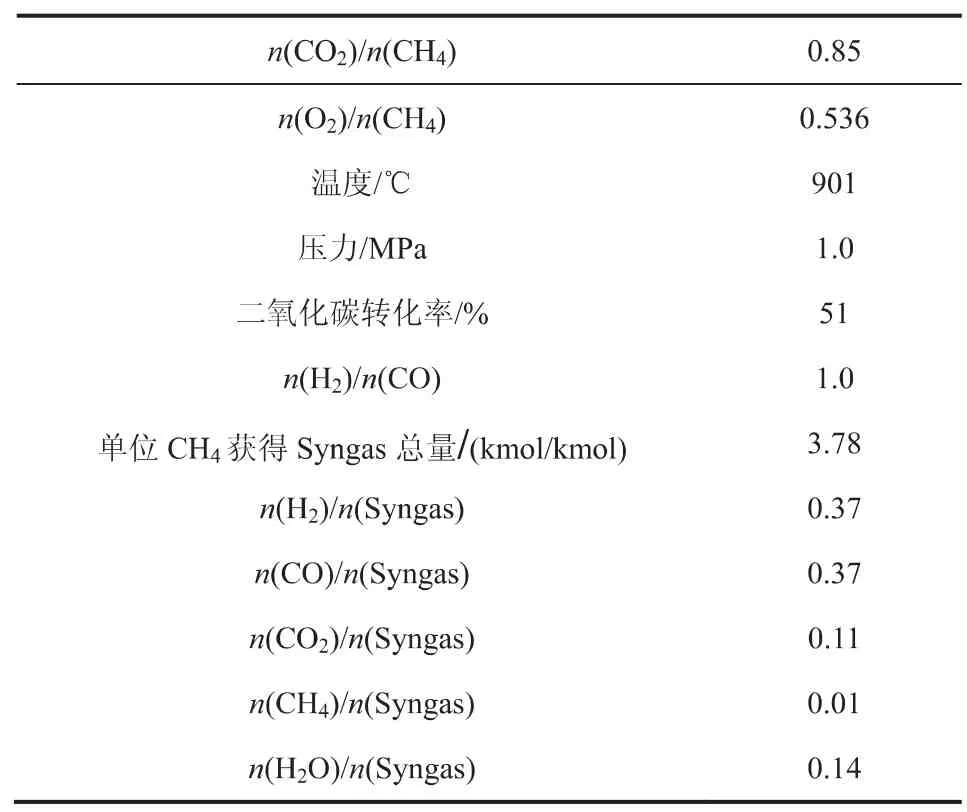
表1 滿足某丙醛合成氣制備的甲烷二氧化碳自熱重整工藝過程詳細計算參數
根據臨界條件時的關系圖,從圖4~圖6 即可直接插值獲得相關的工藝操作參數,指導工業條件選擇及催化劑研發。例如根據魏音等[11]的調研,在總壓為1.0MPa、進料n(C2H4):n(CO):n(H2)=1:1:1 的條件下發生氫甲酰化反應合成丙醛,則可假設上游合成氣的特性為:壓力約為1.0MPa,n(H2)/n(CO)約為1,合成氣甲烷含量1%。則從圖5~圖7 可知,工藝條件大致確定為:n(CO2)/n(CH4)約為1,重整平衡溫度約890℃,CO2的轉化率約48%。經詳細計算,滿足乙烯氫甲酰化催化合成丙醛的甲烷二氧化碳自熱重整制備合成氣的工藝過程參數見表1,結果與通過臨界條件關系圖的結果吻合。
2.5 水蒸氣的影響
水蒸氣對甲烷二氧化碳自熱重整有較大影響。以n(CO2)/n(CH4)=1、壓力2.0MPa、氧碳比n(O2)/n(CH4)恒定時,改變n(H2O)/n(CH4),結果見表2。n(H2O)/n(CH4)增加,主要發生了水煤氣變換反應(CO+H2O→CO2+H2),即反應物CO 減少,產物H2、CO2增加。從表2 可以看出,隨著水碳比n(H2O)/n(CH4)增加,水蒸氣增加,重整平衡溫度降低,出口合成氣CH4含量增加,n(H2)/n(CO)增加,CO2轉化率降低并且可能由正值轉為負值、H2O 轉化率由負值轉為正值。少量或適量水蒸氣可以保護轉化爐內關鍵設備、調節產物n(H2)/n(CO),過量水蒸氣則CO2轉化率為負值,變為傳統蒸汽重整。
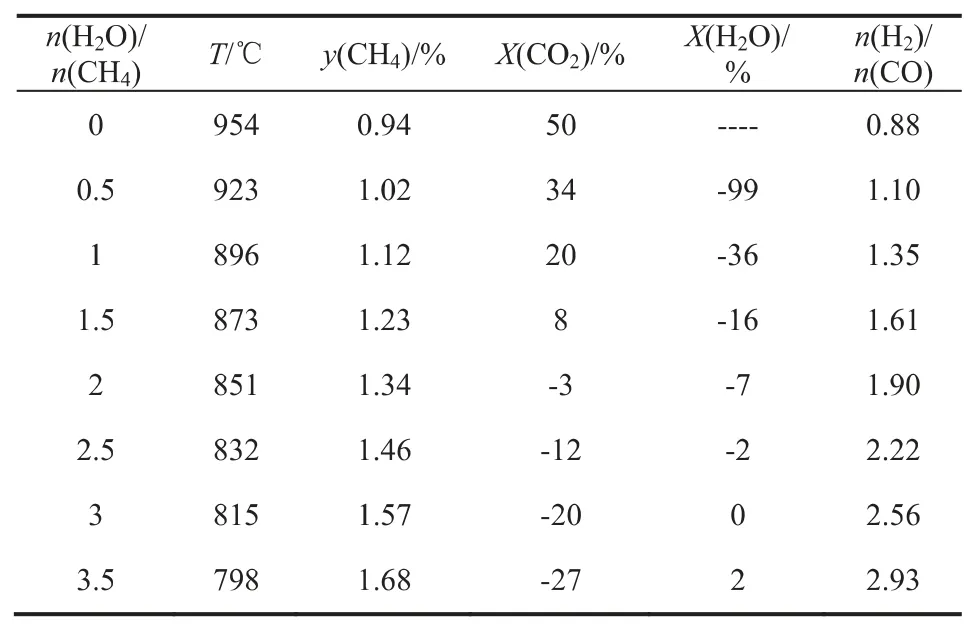
表2 H2O 對甲烷二氧化碳自熱重整工藝過程的影響(n(CO2)/n(CH4)=1、n(O2)/n(CH4)恒定)
3 結論
(1)甲烷二氧化碳自熱重整過程反應復雜,而采用最小化Gibbs 自由能的方法進行熱力學平衡分析可簡單、高效獲得重整過程的相關參數。
(2)甲烷二氧化碳自熱重整過程,溫度增加,合成氣中甲烷含量減少、二氧化碳轉化率增加;壓力增加,合成氣中甲烷含量增加、二氧化碳轉化率降低;n(CO2)/n(CH4)增加,合成氣中甲烷含量減少、二氧化碳轉化率降低;溫度、壓力對n(H2)/n(CO)有影響,但n(CO2)/n(CH4)顯著影響n(H2)/n(CO)數值。
(3)定義出口合成氣中甲烷含量1%為臨界條件,分析臨界條件時n(CO2)/n(CH4)、重整平衡溫度與壓力、二氧化碳轉化率以及n(H2)/n(CO)等重整過程特性參數的關系圖,通過圖可直接插值獲得相關的特性參數。根據一個乙烯氫甲酰化合成丙醛時對合成氣性質要求的案例,通過臨界條件下各參數特性的關系初步了解甲烷二氧化碳自熱重整的工藝條件,并采用詳細計算進一步驗證該方法可取。
(4)少量或適量水蒸氣可以保護甲烷二氧化碳自熱重整轉化爐內關鍵設備、調節產物n(H2)/n(CO)。

