不同初加工方法對黃精品質的影響研究
朱新焰 叢琨 石亞娜 包和超 張智慧 王家金 錢均祥 季鵬章


摘 要 目的:探索不同初加工方法對黃精品質的影響, 優化不同等級、不同形態黃精的初加工方法。方法:經不同干燥法及煮制法、蒸制法處理黃精后,利用硫酸-苯酚法對指標性成分黃精多糖進行含量測定,同時考察藥材醇溶性浸出物、水溶性浸出物及總灰分的含量,篩選最佳初加工工藝。結果:經不同方法處理后,各級黃精樣品均符合2015年版《中國藥典》(一部)對黃精多糖(≥7%)、醇溶性浸出物(≥45%)及總灰分含量(≤4%)的要求;從干燥方式來看,微波干燥法優于烘箱干燥法;對不同形態(個狀及片狀)黃精樣品而言,片狀黃精品質優于個狀黃精;而對于初加工方法而言,蒸制法優于煮制法。黃精“統貨”蒸制、煮制時間分別在20、15 min時,黃精多糖含量達到較高值。結論:通過對不同的初加工方法分別進行探討,初步得到了黃精的個狀、片狀及“統貨”樣品進行高效初加工的方法,可為有效利用黃精資源提供一定的科學依據。
關鍵詞 黃精;初加工;品質評價;黃精多糖
ABSTRACT? ?OBJECTIVE: To explore the effects of different primary processing methods on quality change of Polygonatum sibiricum, and to optimize primary processing method of P. sibiricum with different grades and shapes. METHODS: After processed with different drying methods, boiling method and steaming method, sulfuric acid-phenol method was used to determine the contents of indicator component P. sibiricum polysaccharide in samples. The contents of ethanol-soluble extract, water-soluble extract and total ash were investigated. The optimal primary processing methods were screened. RESULTS: After processed with different methods, the contents of polysaccharide (≥7%), ethanol-soluble extract (≥45%) and total ash (≤4%) of samples at all levels conformed to the requirements of the 2015 edition of Chinese Pharmacopoeia (part Ⅰ); from aspect of drying method, microwave drying method was better than oven drying method;for P. sibiricum with different morphologies (individual and lamellar), the quality of lamellar samples of P. sibiricum was better than that of individual P. sibiricum. As primary processing method, steaming was better than boiling. The contents of P. sibiricum polysaccharide were in relatively high level, when the steaming and boiling time of gradeless and uniformly-priced goods of P. sibiricum were 20 and 15 minutes respectively. CONCLUSIONS: By discussing the different primary processing methods, high-efficient primary processing method for the individual and lamellar samples of P. sibiricum as well as gradeless and uniformly-priced goods of P. sibiricum are preliminarily obtained, which can provide a scientific basis for the effective utilization of P. sibiricum resources.
KEYWORDS? ?Polygonatum sibiricum; Primary processing; Quality evaluation; P. sibiricum polysaccharide
黃精為百合科植物黃精(Polygonatum sibiricum Red.)的干燥根莖,為2015年版《中國藥典》(一部)[1]收錄的品種,為中藥黃精來源之一,又稱“雞頭黃精”“雞頭參”等。黃精是我國傳統藥食同源性的滋補中藥,其味甘,性平,具有養陰潤肺、補脾益氣及抗炎、抗腫瘤、抗病毒等功效[2]。
現有文獻關于黃精的初加工工藝或方法種類繁多,以蒸煮法為主[3-4]。如賀海花等[5]考察了不同蒸制方法和時間對黃精中多糖含量的影響;楊琳[6]和王景媛等[7]嚴格控制蒸煮時間,對多糖、浸出物及灰分含量分別進行了研究。2015年版《中國藥典》(一部)僅對黃精多糖、浸出物等指標作了規定,尚未涉及初加工的技術參數。盡管對加工前后黃精中成分的含量變化有一些研究報道,但不同加工工藝、方法對不同等級、不同形態的黃精中化學成分的影響尚缺乏系統的研究,相對應的加工工藝也缺乏相應的技術參數[8],特別是同一品種不同形態黃精藥材的加工工藝研究鮮見報道。藥材加工后,指標性成分的含量能直觀地反映出其品質的優劣[9]。黃精的化學成分研究表明,黃精品質的判斷依據主要以黃精多糖、醇溶性浸出物、水溶性浸出物、總灰分的含量等為指標[6]。為此,本研究采用黃精(P. sibiricum Red.)為對象,通過對不同形態的藥材(片狀、個狀)進行分級后,按不同方法進行初加工,再分別測定各工藝方法下黃精多糖、醇溶性浸出物、水溶性浸出物、總灰分等指標的含量,以期優化出黃精的蒸制、煮制及干燥的初加工工藝參數,為黃精初加工工藝的優化提供理論依據。
1 材料
1.1 儀器
150B型高速中藥粉碎機(瑞安市永歷制藥機械有限公司);DRHH-2型數顯恒溫水浴鍋(上海雙捷實驗設備有限公司);FA1004型電子分析天平(上海舜宇恒平科學儀器有限公司);GZX-GF101-3-BS-Ⅱ型電熱恒溫鼓風干燥箱(上海躍進醫療器械有限公司);TDL-40B型低速臺式大容量離心機(上海安亭科學儀器廠);752N型紫外分光光度計(上海儀電分析儀器有限公司);SX-4-10型箱式電阻爐(大龍醫療設備有限公司);KSW型電爐溫度控制器(北京市永光明醫療儀器廠); G90F25CN3L-C2(G1)型微波爐(廣東格蘭仕微波爐電器制造有限公司)。
1.2 藥品與試劑
D-葡萄糖對照品(中國食品藥品檢定研究院,批號:110833-201205,含量以99.5%計);無水乙醇、苯酚、濃硫酸等均為分析純,水為純化水。
1.3 藥材
黃精藥材分別采自云南保山(批號:20150117-2,家種)、云南文山(批號:20150104-1,家種)、云南臨滄(批號:20150108-2,家種),經云南省農業科學院藥用植物研究所季鵬章研究員鑒定為百合科植物黃精(P. sibiricum Red.)的全草。
2 方法
2.1 材料預處理
將3年生新鮮黃精去除地上部分,取其根莖,洗凈泥沙,除去根,供凈選用。選取無病蟲害、無腐爛破損且塊大肥潤、色黃、斷面呈角質透明的黃精原料,稱定質量并作好記錄,供分級使用。
2.2 樣品分級
依據“2.1”材料預處理方法和已有的分級方法[6]將個狀黃精分為:一級,70 g以上;二級,20~70 g;三級,20 g以下。依據對片狀黃精加工的文獻報道[2,6],片狀黃精的切片厚度<1 cm。
2.3 干燥方法及時間的篩選
取同一級別相同質量的黃精樣品分別進行烘箱和微波法干燥,依照材料預處理、樣品分級結果和現有文獻報道[5-6,8],設定烘箱溫度為50 ℃,微波則使用中火(功率為550 W),干燥后取出,分別進行多糖等內在指標含量檢測與分析,比較兩種干燥方法的優劣,確定干燥方法。黃精樣品經煮/蒸制后,依照材料預處理、樣品分級結果和現有文獻報道[5-6,8],8~26 min左右即可干燥該類藥材,設定個狀樣品干燥時間為6~30 min不等,每隔2 min為1個時間梯度;設定片狀樣品干燥時間為3~12 min不等,每隔1 min為1個時間梯度。干燥后取出晾涼,用高速中藥粉碎機進行粉碎,過120目篩后進行多糖等內在指標檢測與分析,確定各級樣品的最佳干燥時間。
2.4 煮制、蒸制法的時間篩選
2.4.1 煮制法單因素試驗 依照材料預處理、樣品分級結果和現有文獻報道[5-6],黃精藥材樣品在沸水中煮制11~17 min左右時可至透心,故選取沸水煮制透心時間區間為:黃精個狀10~20 min、片狀10~15 min,每隔1 min為1個時間梯度,優選最佳煮制時間。每次處理隨機稱取各級樣品300 g,用水量以沒過樣品為準,水沸時放入樣品,計時,煮好后,取出晾涼,一次處理完后再換水處理下一批。隨后進行干燥,用高速中藥粉碎機進行粉碎,過120目篩后進行多糖等內在指標的檢測與分析。
2.4.2 蒸制法單因素試驗 依照材料預處理、樣品分級結果和現有文獻報道[5-6],黃精藥材樣品在沸水中蒸制16~24 min左右時可至透心,故選取沸水蒸制透心時間區間為:黃精個狀15~25 min、片狀15~20 min,每隔1 min為1個時間梯度,優選最佳蒸制時間。每次處理隨機稱取各級樣品300 g,水沸時于蒸籠中放入樣品,計時,蒸好后,取出晾涼,一次處理完后再換水處理下一批。隨后進行干燥,用高速中藥粉碎機進行粉碎,過120目篩后進行多糖等內在指標的檢測與分析。
2.5 黃精“統貨”初加工的工藝篩選
使用“2.1”項下方法對黃精凈選后,按照產地傳統的粗放型初加工方式進行處理,即不對藥材進行分等級、分大小及不切片處理,以“統貨”形式初加工。根據3年生黃精個體大小和文獻報道[5-6,8],設置15、20、25、30 min等4個時間段,每隔5 min為1個時間梯度,分別進行煮制和蒸制,隨后進行干燥,用高速中藥粉碎機進行粉碎,過120目篩后進行多糖等內在指標的檢測與分析。
2.6 多糖含量測定
采用硫酸-苯酚法測定。
2.6.1 多糖提取與供試品溶液的制備 精密稱取經初加工處理的黃精粉末0.25 g于100 mL燒杯中,加50 mL水,用保鮮膜和皮筋封口,置于沸水浴中連續提取1 h,取出冷卻后濾過,取濾液5 mL于50 mL離心管中,加無水乙醇30 mL搖勻,靜置1 h,4 000 r/min離心10 min,棄去上清液,沉淀以50~60 ℃熱水復溶,放冷,用水定容于100 mL量瓶中,搖勻,即得供試品溶液[10-11]。
2.6.2 標準品溶液的制備 精密稱取105 ℃干燥至恒定質量的D-葡萄糖對照品33 mg,置于100 mL量瓶中,加水溶解并稀釋至刻度,即得葡萄糖標準品溶液。
2.6.3 苯酚溶液的制備 精密稱取苯酚5 g,置于100 mL量瓶中,水浴加熱溶解,加適量水快速稀釋至刻度(避免揮發),混勻,即得。
2.6.4 測定波長的選擇 按“2.6.1”“2.6.2”項下方法制備供試品及標準品溶液各適量,分別加水至1 mL,置于冰水浴中,依次加入“2.6.3”項下苯酚溶液1 mL和濃硫酸5 mL,搖勻,置水浴中加熱10 min后,取出,冷卻至室溫,隨后在400~700 nm波長范圍內進行掃描。結果,兩者均在490 nm波長附近均有最大吸收,即以490 nm為檢測波長。
2.6.5 線性關系考察 使用移液槍精密吸取葡萄糖標準品溶液0.1、0.2、0.3、0.4、0.5、0.6 mL,置于10 mL具塞試管中,各加水至1 mL,按“2.6.4”項下方法顯色后,作為系列標曲標準品溶液;另取2 mL水,同法處理,作為空白對照溶液。將上述溶液于490 nm波長下測定吸光度,以葡萄糖質量濃度(x,mg/mL)為橫坐標、吸光度(y)為縱坐標進行線性回歸,得回歸方程為 y=0.830 5x-0.004 5(r=0.999 0,n=6),表明葡萄糖檢測質量濃度的線性范圍為0.004 71~0.027 2 mg/mL。
2.6.6 精密度試驗 使用移液槍精密吸取葡萄糖標準品溶液0.5 mL,共6份,按“2.6.5”項下方法顯色并測定吸光度。結果,吸光度的RSD為1.19%(n=6),表明儀器精密度良好。
2.6.7 穩定性試驗 分別精密量取標準品及供試品溶液0.5 mL,各 6份,按“2.6.5”項下方法顯色,并每隔15 min 測定1次吸光度,共計6次。結果,標準品溶液和供試品溶液吸光度的RSD分別為0.98%和1.06%(n=6),表明兩者在90 min內穩定性良好。
2.6.8 重復性試驗 精密稱取經初加工處理的黃精粉末0.25 g,共6份,按“2.6.1”項下方法制備供試品溶液,再按“2.6.5”項下方法顯色并測定吸光度。結果,吸光度的RSD為 1.18%(n=6),表明該方法重復性良好。
2.6.9 加樣回收試驗 精密稱取經初加工處理且干燥至恒定質量的黃精粉末9份,按“2.6.1”項下方法制備供試品溶液。再精確稱取葡萄糖對照品0.105 g,置于100 mL量瓶中,配成質量濃度為1.05 mg/mL的溶液。精密吸取上述供試品溶液各0.5 mL,置于刻度比色管中,分別精密加入定量的上述葡萄糖溶液,再按“2.6.5”項下方法顯色并測定吸光度,計算加樣回收率。結果,平均加樣回收率為99.84%,RSD為1.56%(n=9),表明該法準確性較高,符合含量測定要求[12]。
2.6.10 樣品測定 精密稱取經初加工處理的黃精粉末適量,按“2.6.1”項下方法提取多糖并制備供試品溶液,再按“2.6.5”項下方法顯色并測定吸光度,按回歸方程計算含量[13-14]。
2.7 浸出物及總灰分的測定
分別按2015年版《中國藥典》(四部)[15]的方法測定醇溶性、水溶性浸出物以及總灰分的含量。
3 結果
3.1 干燥方法篩選結果
微波及烘箱干燥的醇溶性浸出物平均含量分別為55.66%、52.81%,水溶性浸出物平均含量分別為 62.64%、59.17%,總灰分平均含量為3.12%、3.39%,均符合2015年版《中國藥典》(一部)的要求[1]。微波干燥樣品的多糖平均含量普遍高于烘箱干燥,故后續試驗將采取微波干燥法進行干燥,結果見表1。
3.2 不同加工方法對各級黃精品質的影響
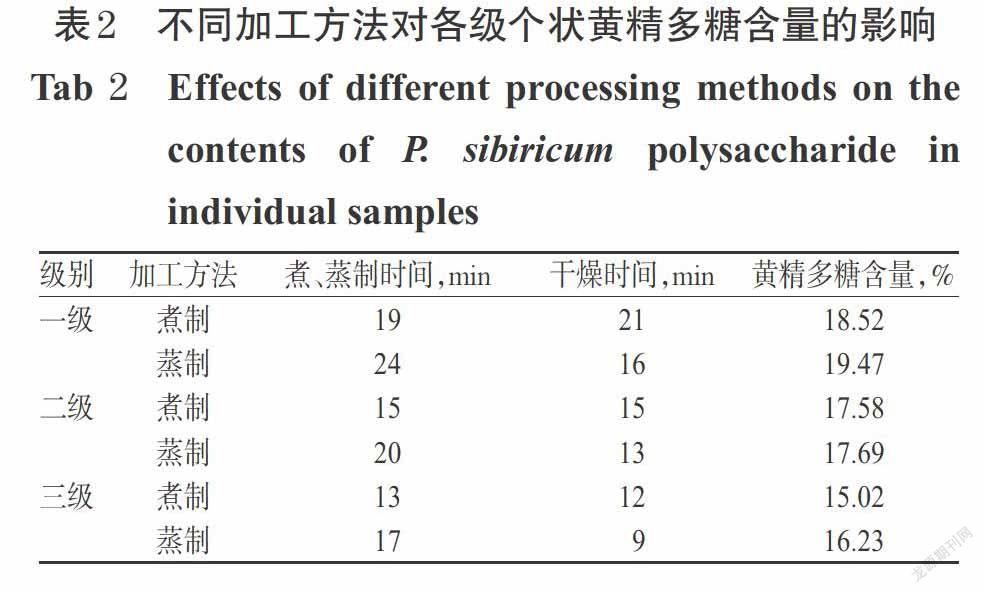
3.2.1 個狀各級黃精初加工方法比較 對黃精個狀各級樣品進行煮制與蒸制,依據干燥方法篩選結果,進行微波干燥后(下同),按“2.6.1”項下方法制備供試品溶液,每個品種選取3個批次,每個批次進行3次重復試驗,分別測定黃精多糖等含量等指標,取平均值。結果,蒸、煮法的醇溶性浸出物平均含量分別為58.39%、57.63%,水溶性浸出物平均含量分別為59.17%、62.64%,總灰分平均含量分別為3.39%、3.12%,均符合2015年版《中國藥典》(一部)的要求[1];黃精多糖含量以一級最高,二級次之,三級較低;且蒸制法的黃精多糖含量均比煮制法高,詳見表2。
3.2.2 片狀黃精初加工方法比較 分別對黃精片狀各級樣品進行煮制與蒸制,依據預試驗結果進行微波干燥后,按“2.6.1”項下方法制備供試品溶液,每個品種選取3個批次,每個批次進行3次重復試驗,分別測定黃精多糖含量等指標,取平均值。結果,蒸、煮法的醇溶性浸出物平均含量分別為70.43%、70.30%,水溶性浸出物平均含量分別為65.41%、61.64%,總灰分平均含量分別為2.86%、2.80%,均符合2015年版《中國藥典》(一部)的要求[1];蒸制法的黃精多糖含量均比煮制法高,提示對于片狀樣品蒸制法優于煮制法,詳見表3。
由表2、表3可見,黃精個狀、片狀樣品均以蒸制法為宜,各級樣品最佳蒸制時間分別是:黃精個狀一、二、三級樣品分別為24、20、17 min;片狀為14 min。同一級別樣品,煮制法的微波干燥時間要長于蒸制法,干燥時間隨樣品大小或級別的降低而降低,與相關研究報道[5-6,16]基本一致。此外本研究結果還顯示,在采用相同的初加工方法處理時,片狀樣品的黃精多糖含量普遍高于個狀樣品。
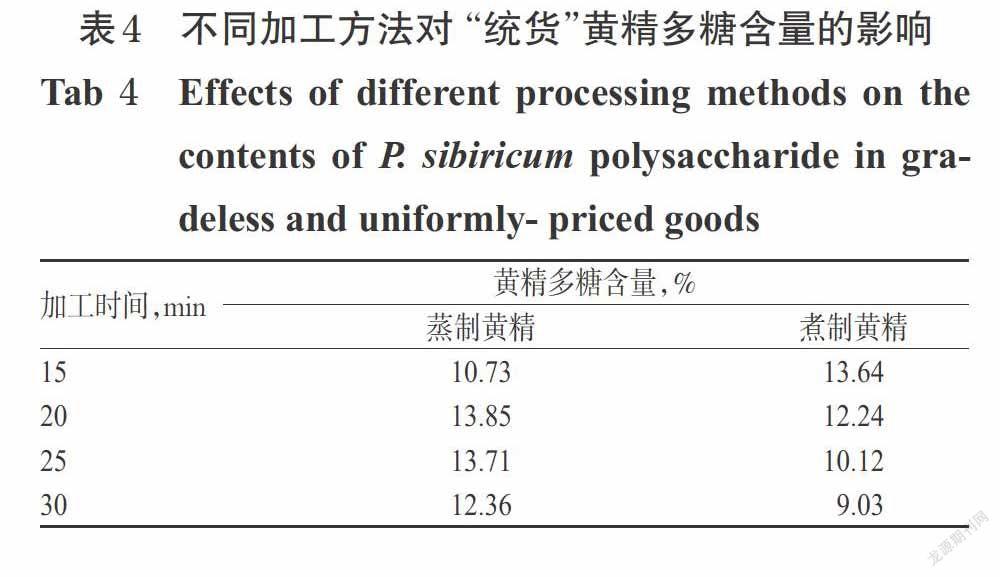
3.3 不同加工方法對黃精“統貨”品質的影響及時間優化結果
在初加工時間段內用蒸、煮法處理“統貨”黃精樣品時,其醇溶性浸出物平均含量分別為56.20%和55.37%,水溶性浸出物平均含量分別為64.05%和62.12%,總灰分平均含量分別為3.21%和3.14%,均高于2015年版《中國藥典》(一部)的要求[1]。采用蒸制法時,黃精多糖含量先上升至最大值,在20~25 min時開始下降;采用煮制法時,黃精多糖含量呈下降趨勢。蒸制法黃精多糖含量高于煮制法,即黃精蒸制及煮制時間分別在20 min及15 min左右時,多糖含量最高,詳見表4。
本研究通過對黃精藥材進行詳細分級后,采取了一系列的初加工方法探索;同時,對黃精“統貨”進行了初加工工藝的優化,初步得到了黃精各級藥材的初加工方法及相關參數,可為傳統的產地初加工提供參考依據。結果顯示:(1)黃精切片后初加工的品質優于個狀初加工的品質。無論是蒸制法還是煮制法,片狀加工時間均短于個狀,且片狀樣品的多糖含量均高于個狀藥材。這與切片后增大了藥材與水分子或水蒸氣接觸的表面積有關,接觸面積的增大使得藥材溫度在短時間內升至水溫,內部相關酶的活性被充分抑制,化學成分也得到了極大的保留,從而相應減少了成分的損失[5]。(2)蒸制法優于煮制法。在藥材個體較大、處理時間相對較長的初加工中,蒸制黃精品質高于煮制黃精品質,原因有二:一是蒸制時,藥材不與水直接接觸,而水溫到100 ℃ 時才會產生蒸氣,水蒸氣要使藥材內部各種酶類達到滅活的效果,往往需要較長的時間,所以使用該法初加工的藥材,其化學成分含量達到最高值所需要的時間要長于煮制法;二是煮制時,藥材直接與沸水接觸,使得藥材化學成分含量可在較短的時間內到達最高值。而隨著煮制時間延長至黃精透心,其水溶性成分也隨之流失,損失較大,這是煮制時黃精含量在較短時間內迅速升高,而后又降低的主要原因[5-6]。(3)微波干燥法優于烘箱干燥法。烘干是由表及里的干燥過程,但干燥后的外層會直接影響藥材內部水分的蒸發,溫度過高和時間過長均會使部分糖分損失,進而影響藥材的品質[8,14];而微波干燥則剛好相反,是由內到外的干燥形式,干燥時間更易控制,且干燥徹底、均勻,干燥用時短,大大減少了有效成分的損失[14,17]。
綜上,本研究通過對不同的初加工方法分別進行探討,初步得到了黃精的個狀、片狀及“統貨”樣品的初加工工藝參數,可為有效利用黃精資源提供一定的科學依據。本課題組后續將對黃精藥材的加工工藝特別是深加工方面進行深入研究。
參考文獻
[ 1 ] 國家藥典委員會.中華人民共和國藥典:一部[S]:2015年版.北京:中國醫藥科技出版社,2015:306-307.
[ 2 ] 段秀彥.黃精藥材企業質量標準研究[D].楊凌:西北農林科技大學,2016.
[ 3 ] 姜程曦,洪濤,熊偉.黃精產業發展存在的問題及對策研究[J].中草藥,2015,46(8):1247-1250.
[ 4 ] 蘇文田,劉躍鈞,蔣燕鋒,等.黃精產業發展現狀與可持續發展的建議[J].中國中藥雜志,2018,43(13):2831-2835.
[ 5 ] 賀海花,楊云,王爽,等.不同蒸制方法和時間對黃精中多糖含量的影響[J].中藥材,2009,32(6):861-862.
[ 6 ] 楊琳.黃精的產地初加工工藝研究[D].楊凌:西北農林科技大學,2015.
[ 7 ] 王景媛,翟思程,王昌利,等.黃精產地加工與炮制一體化可行性探討[J].現代中醫藥,2017,37(5):105-108.
[ 8 ] 衡銀雪,鄭旭煦,殷鐘意,等.不同干燥方法對黃精干燥特性和品質的影響[J].食品工業科技,2018,39(7):158-161、167.
[ 9 ] 張洪坤,王其豐,郭長達,等.不同加工方法牡丹皮中7種指標性成分的含量測定及質量評價[J].中國藥房,2018,29(22):3063-3068.
[10] 徐兵兵,于勇杰,吳帆,等.黃精多糖研究綜述[J].中國野生植物資源,2015,34(4):38-41、46.
[11] 梁引庫.黃精多糖提取工藝的研究[J].中國農學通報, 2012,28(12):269-272.
[12] 朱新焰,字淑慧,王家金,等.白及與2種近緣種的多糖組織化學定位及含量測定研究[J].中藥材,2018,41(12):2774-2778.
[13] 藍松.苯酚-硫酸法測定黃精多糖含量研究[J].廣東化工,2013,40(18):132-133.
[14] 郭未艷,孫秋燕,徐曉紅,等.滇黃精多糖提取的工藝組合及其優化[J].時珍國醫國藥,2013,24(6):1391-1393.
[15] 國家藥典委員會.中華人民共和國藥典:四部[S].2015年版.北京:中國醫藥科技出版社,2015:202、204.
[16] 陳麗霞,王建科,耿曉玲.綜合評分法優選黃精蒸制工藝[J].微量元素與健康研究,2017,34(5):38-40.
[17] 彭星星,王德群,彭華勝.歷代本草中“九蒸九曬”藥材加工的沿革與變遷淺談[J].皖西學院學報,2018,34(2):92-99.
(收稿日期:2018-12-20 修回日期:2019-08-09)
(編輯:余慶華)

