廣西發酵酸筍氣味物質提取方法優化及比較分析
郭榮燦,王成華,江虹銳,余 煉,劉小玲,*,趙謀明,2,*
(1.廣西大學輕工與食品工程學院,廣西南寧 530004; 2.華南理工大學輕工與食品學院,廣東廣州 510641)
竹筍是一種傳統食材,被廣泛應用于我國、印度及東南亞國家的菜肴烹煮中[1-3]。發酵竹筍是針對鮮竹筍儲藏困難的問題而誕生的自然發酵產物。在廣西,發酵酸筍是重要的食物原料。酸筍一個重要的特征就是其發酵酸味,該氣味具有很強的地區嗜好性,對其推廣產生了阻礙。對酸筍氣味組成進行研究,有利于對發酵酸筍進行性能改良、品質控制以及按嗜好進行市場細分,對推廣地區特色產品有很大的意義。
隨著檢測儀器和技術的不斷進步,氣味成分的提取濃縮技術也在不斷豐富。常見的氣味物質提取方法有液液萃取法(LLE)、同時蒸餾萃取法(SDE)、頂空固相微萃取法(HS-SPME)等。LLE操作簡單,但是耗時長,該方法也用于非揮發性物質的提取[4],可能會引入非揮發性化合物,從而干擾實驗結果。SDE法是通過同時加熱樣品及萃取溶劑,使揮發組分與溶劑蒸氣混合,從而達到萃取的目的,該方法對含量低的揮發成分萃取效果較好,但需要保持沸騰,很容易造成氣味物質的變化[5]。頂空固相微萃取法不需要高溫加熱,實驗裝置簡單,但萃取物質類型易受到萃取頭涂層種類的影響[6]。目前,對廣西發酵酸筍氣味的研究匱乏,提取方法各有優劣,用何種方法提取氣味物質效果最好尚無研究結論。本文使用氣相色譜-質譜聯用儀(GC-MS)分別對LLE、SDE、HS-SPME法提取的發酵酸筍氣味物質的萃取峰面積和萃取物質種類進行優化和比較,旨在尋找最優的氣味物質提取方法,為進一步展開深入的風味研究提供方法支持。
1 材料與方法
1.1 材料與儀器
發酵酸筍樣品及其發酵液 廣西南寧市五里亭菜市場;氯化鈉 國藥集團化學試劑有限公司;二氯甲烷、正己烷 天津富宇精細化工有限公司、乙醚 江蘇沭陽恒潤精細化工有限公司;以上試劑 均為分析純。
7890B-5977A氣相色譜-質譜聯用儀、DB-Wax彈性石英毛細管色譜柱 美國Agilent公司;Milli-Q水凈化系統 德國Merck公司;75 μm CAR/PDMS固相微萃取頭、85 μm PA固相微萃取頭、100 μm PDMS固相微萃取頭、65 μm PDMS/DVB固相微萃取頭、手動固相微萃取握柄 美國Supelco公司;HY-5A回旋式振蕩搖床 常州朗越儀器制造有限公司;JYL-C16V食品研磨機 山東九陽股份有限公司;RCT B S025數顯恒溫磁力攪拌裝置、T25 digital均質機 美國IKA公司;LG10-2.4A離心機 北京京立離心機有限公司;5418 R高速離心機 德國Eppendorf公司;DZTW調溫加熱套 北京市永光明醫療儀器有限公司;AL204電子天平 梅特勒-托利多儀器(上海)有限公司。
1.2 實驗方法
1.2.1 LLE法提取發酵酸筍香氣物質及條件優化
1.2.1.1 香氣物質的提取 參考馮云子[7]的LLE條件,設計實驗如下:將50 g酸筍通過食品研磨機粉碎成糊,與50 mL發酵酸液混合后,置于1000 mL錐形瓶中。加入100 mL鹽水與100 mL萃取劑,在振蕩搖床上振蕩20 h后,通過分液漏斗取有機層,置于500 mL錐形瓶中。加入適量無水硫酸鈉除水,用保鮮膜封口后,于振蕩搖床上振蕩1 h,之后通過濾紙過濾。使用注射器將1 mL濾液通過0.22 μm有機相膜過濾到GC-MS進樣瓶(2 mL)中,進行GC-MS分析。
1.2.1.2 萃取溶劑的選擇 由于溶劑對萃取效果有一定的影響,故分別采用二氯甲烷(極性)、乙醚(極性)、正己烷(非極性)按照初始條件,添加17.00%氯化鈉溶液,對萃取峰面積及萃取物質種類進行對比。
1.2.1.3 樣品離子濃度的優化 適量的氯化鈉溶解在水中會增加樣品的離子濃度,從而降低揮發性化合物在水中的溶解度,促進其向有機相溶劑的傳質過程。以初始條件為基礎,使用最佳溶劑作為溶劑,分別添加0.00%、17.00%、飽和氯化鈉溶液,對比萃取峰面積及萃取物質種類。
1.2.2 SDE法提取發酵酸筍香氣物質及條件優化
1.2.2.1 香氣物質的提取 參考馮云子[7]的SDE條件,設計實驗如下:將50 g酸筍通過食品研磨機粉碎成糊,與50 mL發酵酸液混合后置于 500 mL圓底燒瓶中,加入一定量的氯化鈉溶液稀釋樣品,連接在同時蒸餾萃取裝置上,通過加熱套加熱并保持微沸。另在250 mL圓底燒瓶中添加100 mL萃取溶劑,連接在同時蒸餾裝置上后,通過恒溫水浴鍋保持溶劑微沸。連續提取一定時間后,冷卻至室溫,取有機相部分置于500 mL錐形瓶中。加入適量無水硫酸鈉,用保鮮膜封口后于振蕩搖床上振蕩1 h,之后通過濾紙過濾。使用注射器將1 mL濾液通過0.22 μm有機相膜過濾到GC-MS進樣瓶(2 mL)中,進行GC-MS分析。
1.2.2.2 萃取溶劑的選擇 在初始條件的基礎上,使用100 mL 17.00%氯化鈉溶液稀釋樣品后,分別使用二氯甲烷(水浴溫度45 ℃)、乙醚(水浴溫度40 ℃)、正己烷(水浴溫度75 ℃)作為萃取溶劑,萃取時間為2 h,對比萃取峰面積及萃取物質種類。
1.2.2.3 樣品離子濃度的優化 以初始條件為基礎,分別添加100 mL的0.00%、17.00%、飽和氯化鈉溶液稀釋樣品,使用最佳溶劑作為萃取劑,萃取時間為2 h,對比萃取峰面積及萃取物質種類。
1.2.2.4 稀釋液添加量的優化 由于同時蒸餾萃取法涉及樣品的加熱,如不對樣品進行稀釋,加熱過程中可能會造成樣品焦糊,影響萃取效果,故在初始條件的基礎上,分別添加50、100、150及200 mL的最佳濃度氯化鈉溶液,使用最佳溶劑作為萃取劑,萃取時間為2 h,對比萃取峰面積及萃取物質種類。
1.2.2.5 萃取時間的優化 在以上條件均選取最佳萃取條件后,分別對比萃取1、2、3及4 h的萃取峰面積及萃取物質種類。
1.2.3 HS-SPME萃取法提取發酵酸筍香氣物質及條件優化
1.2.3.1 香氣物質的提取 參考Kim等[8]的HS-SPME實驗條件,實驗設計如下:樣品前處理:將100 g發酵酸筍固體經食品研磨機粉碎后與100 mL發酵酸液混合,在冰水浴下通過均質機以8000 r/min均質1 min。勻漿放入離心管中,以5000 r/min離心15 min后取上清液,再經10000 r/min離心30 min,放入樣品瓶中備用。
萃取:取樣液3 mL放入15 mL頂空樣品瓶,與等體積超純水混合,加入氯化鈉和磁力轉子,于300 r/min轉速下磁力攪拌,水浴平衡30 min,分別使用經過老化的萃取頭萃取一定時間后,通過手動進樣口進樣,在250 ℃下釋放5 min,通過GC-MS測定結果。
1.2.3.2 萃取針頭的選擇 本實驗篩選了四種具有不同固定相涂層的萃取頭,分別為85 μm PA(Polyacrylate,聚丙烯酸酯,強極性)、75 μm CAR/PDMS(Carboxen/Polydimethylsiloxane,碳分子篩/聚二甲硅氧烷,中極性)、65 μm PDMS/DVB(Polydimethylsiloxane/Divinylbenzene,聚二甲硅氧烷/二乙烯基苯,中極性)、100 μm PDMS(Polydimethylsiloxane,聚二甲硅氧烷,非極性),在樣品中加入0.60 g氯化鈉,于50 ℃下萃取30 min。萃取頭使用一臺氣相色譜柱進樣口作為老化裝置,使用氮氣吹掃保持環境惰性,老化時間及溫度按照Supelco公司的推薦條件進行,具體見表1。
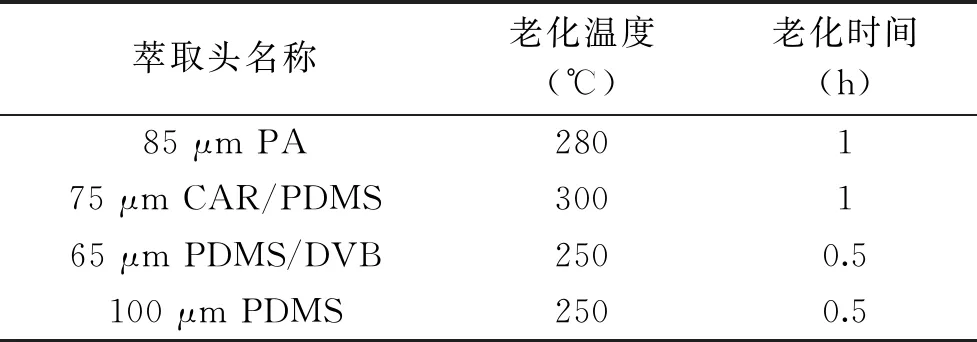
表1 固相微萃取頭的老化溫度和時間Table 1 Aging temperature and time for SPME fiber
1.2.3.3 樣品離子濃度的優化 使用最佳萃取頭,在樣品中分別加入相當于樣品質量0%(0.00 g)、1%(0.60 g)、2%(1.20 g)、3%(1.80 g)氯化鈉,于50 ℃下萃取30 min。對比萃取峰面積及萃取物質種類。
1.2.3.4 萃取溫度的優化 使用最佳萃取頭,在樣品中加入最佳添加量的氯化鈉,分別于30、40、50、60 ℃下萃取30 min,對比萃取峰面積及萃取物質種類。
1.2.3.5 萃取時間的優化 在上述最佳條件下分別萃取10、20、30、40 min,對比萃取峰面積及萃取物質種類。
1.2.4 揮發性成分的GC-MS測定 GC條件:色譜柱使用DB-Wax(60 m×0.25 mm×0.25 μm),進樣器溫度250 ℃,LLE及SDE法樣品通過自動進樣器進樣1 μL,溶劑延遲8 min;HS-SPME法為手動進樣,解吸時間為5 min。柱箱升溫程序:40 ℃保持2 min,以5 ℃/min的速度上升到120 ℃,保持2 min,再以7 ℃/min的速度上升到220 ℃,保持5 min,最后以7 ℃/min的速度上升到240 ℃,保持5 min。
MS條件:質譜條件為傳輸線溫度250 ℃。離子能級70 ev,采用SCAN(全掃描)模式,掃描質荷比范圍為35~395。LLE及SDE法樣品設置3 min的溶劑延遲。
定性與定量方法:色譜圖通過MassHuter軟件積分并與NIST14譜庫比對,取匹配度在80%以上的物質進行分析。通過積分法計算絕對峰面積,并通過峰面積歸一化法計算相對含量。
1.3 數據處理
本文實驗進行兩次平行實驗,峰面積數據以平均值形式表示,提取物質總數數據取平行組中最大值,相對含量以百分比形式呈現。數據通過SPSS軟件進行統計計算,總離子流圖通過Origin軟件進行繪制。
2 結果與討論
2.1 LLE法的萃取效果及條件優化
2.1.1 不同溶劑對LLE萃取酸筍揮發性物質效果的影響 正己烷、乙醚和二氯甲烷3種不同極性溶劑在LLE法中對酸筍中揮發性成分的萃取效果如表2所示。由表2可知,不同溶劑萃取酸筍揮發性物質的總峰面積由大到小分別為:乙醚>正己烷>二氯甲烷。而萃取物質種類由多至少分別為:乙醚>二氯甲烷>正己烷。非極性溶劑正己烷的萃取總峰面積雖較極性溶劑二氯甲烷大,但其萃取的物質種類少于兩種極性溶劑,推測與相似相溶原理有關,在醬油的香味成分萃取上也存在香味物質以極性物質為主的情況[7]。故考慮到萃取物質的多樣性,正己烷并不適合作為發酵酸筍氣味物質的萃取溶劑使用。而在極性溶劑方面,極性較強的乙醚無論是萃取總峰面積還是物質總類優于二氯甲烷。綜上所述,乙醚是通過液液萃取法萃取酸筍揮發性氣味成分的最佳溶劑。

表2 不同溶劑對LLE萃取酸筍揮發性物質效果的影響Table 2 Effect of different solvents on extraction efficiencies of volatile compounds from bamboo shoots by LLE
2.1.2 不同樣品離子濃度對LLE萃取酸筍揮發性物質效果的影響 向樣品中添加0.00%、17.00%和飽和氯化鈉溶液在LLE法中對酸筍中揮發性成分的萃取效果如表3所示。從表3可以看出,隨著氯化鈉溶液濃度由增加0%增加至飽和,萃取總峰面積由4.22×109Ab·s逐漸增加至6.76×109Ab·s,而提取物質總數也由29增加至34種。這與增加離子強度會抑制揮發性物質在水相中的溶解度的理論符合[9],故采取添加飽和氯化鈉溶液作為最佳離子濃度條件。
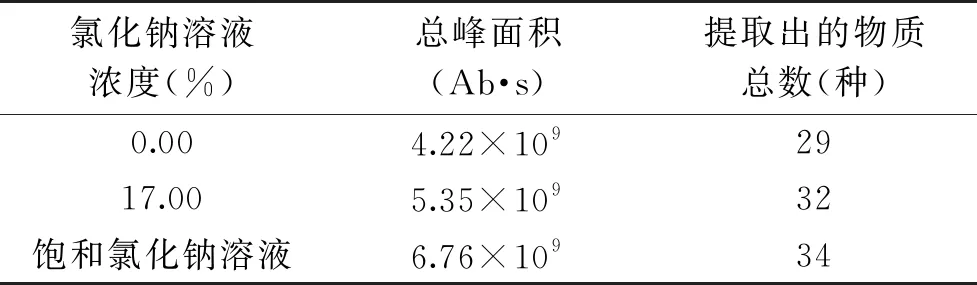
表3 不同離子濃度對LLE萃取 酸筍揮發性物質效果的影響Table 3 Effect of different salt concertrations on extraction efficiencies of volatile compounds from bamboo shoots by LLE
2.2 SDE法的萃取效果及條件優化
2.2.1 不同溶劑對SDE萃取酸筍揮發性物質效果的影響 正己烷、乙醚和二氯甲烷3種不同極性溶劑在SDE法中對酸筍中揮發性成分的萃取效果如表4所示。由表4可知,不同溶劑萃取酸筍揮發性物質的總峰面積由大到小分別為:二氯甲烷>乙醚>正己烷。而萃取物質種類由多至少分別為:二氯甲烷>乙醚>正己烷。極性溶劑正己烷萃取在總峰面積和物質種類方面均劣于非極性溶劑,故非極性溶劑正己烷并不適合作為SDE法萃取發酵酸筍氣味物質的萃取溶劑。在極性萃取溶劑方面,乙醚的萃取物質總峰面積(6.64×108Ab·s)和萃取的物質種類(19種)均少于二氯甲烷(1.09×109Ab·s,22種)。推測原因為SDE法中的萃取過程為將樣品與溶劑同時加熱,揮發性成分在通過加熱后以氣態形式與溶劑蒸氣混合,故最終萃取液中不包含難揮發性組分,而在LLE過程中則由于樣品與萃取液的直接接觸,造成了難揮發性成分能夠從水相轉移至有機相,LLE中萃取的物質種類普遍多于SDE的原因也可以解釋為此。因此在SDE法萃取實驗中,二氯甲烷的萃取效果優于乙醚,這與通過SDE法萃取豆瓣醬和東方鲀的氣味物質的實驗結果一致[10-11]。綜上所述,二氯甲烷是通過同時蒸餾萃取法萃取酸筍揮發性氣味成分的最佳溶劑。

表4 不同有機溶劑對SDE萃取 酸筍揮發性物質效果的影響Table 4 Effect of different organic solvents on extraction efficiencies of volatile compounds from bamboo shoots by SDE
2.2.2 不同樣品離子濃度對SDE萃取酸筍揮發性物質效果的影響 向樣品中添加0.00%、17.00%和飽和氯化鈉溶液在SDE法中對酸筍中揮發性成分的萃取效果如表5所示。從表5可以看出,與LLE實驗中鹽含量變化引起萃取效果變化的規律類似,隨著氯化鈉溶液濃度的增加,無論是物質種類還是物質總質量均在上升,在飽和食鹽水中達到最佳(1.62×109Ab·s,24種),故采取添加飽和氯化鈉溶液作為最佳離子濃度條件。
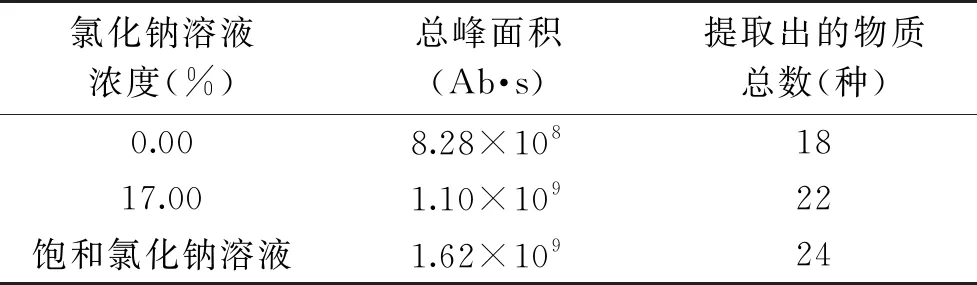
表5 不同離子濃度對SDE萃取 酸筍揮發性物質效果的影響Table 5 Effect of different salt concertrations on extraction efficiencies of volatile compounds from bamboo shoots by SDE
2.2.3 不同稀釋液添加量對SDE萃取酸筍揮發性物質效果的影響 向樣品里添加50、100、150、200 mL的飽和氯化鈉溶液,對萃取效果的影響如表6所示。從表6可以看出,當添加的稀釋液體積為50 mL時,其萃取的物質總數為23種,僅比最多的100 mL組少1種,且萃取的物質總質量(以總峰面積表示)最高(1.95×109Ab·s)。由于SDE法的樣品涉及保持沸騰狀態的加熱過程,如不添加一定量的稀釋液稀釋樣品,會造成樣品焦糊。在實驗過程中,50 mL組在萃取后期出現焦糊現象,萃取樣品也散發著焦糊氣味,故其總峰面積大可能是由于稀釋不足,發生焦糊現象時產生了新的不良氣味物質引起的,因此該稀釋液添加量不適合進行SDE萃取。在未發生焦糊現象的組(100~200 mL)中,隨著飽和氯化鈉溶液添加量的增加,萃取物質的總峰面積在從1.61×109Ab·s逐漸下降到9.26×108Ab·s,萃取的物質總數也從24種減少到22種,這說明當加入150 mL或更多飽和氯化鈉溶液后,稀釋液體積過大造成樣品被過分稀釋,影響了萃取效果。綜上所述,100 mL為SDE法最適氯化鈉溶液添加量。

表6 不同稀釋液添加量對SDE萃取 酸筍揮發性物質效果的影響Table 6 Effect of different volumes of diluent on extraction efficiencies of volatile compounds from bamboo shoots by SDE
2.2.4 不同樣品萃取時間對SDE萃取酸筍揮發性物質效果的影響 對樣品進行1、2、3、4 h的提取,萃取效果如表7所示。從表7中可以看出,萃取時間為1 h的樣品萃取物質總峰面積及提取出的物質總數均最少(7.47×108Ab·s,20種),說明1 h的萃取時間明顯不足,揮發性物質與溶劑蒸氣混合時間短,難以完全萃取揮發性成分。理論上同時蒸餾萃取過程由于萃取液蒸氣和水蒸氣的冷卻回流,萃取液和樣品水溶液的總量在裝置中維持不變,提取過程是無損失的循環過程,故延長提取時間可以增加揮發性物質和萃取劑蒸氣的混合次數,從而增加提取效果[12],但在實際實驗中由于密封條件無法完全達到理論狀態,水蒸氣和萃取溶劑蒸氣會少量泄露,經過長時間的實驗有可能造成樣品焦糊或有機萃取溶劑不足的狀態,且長時間的加熱過程可能會破壞揮發性氣味物質。在萃取時間超過2 h的情況下,隨著時間的增加,總峰面積保持在1.62×109Ab·s左右,2~3 h提取物質總數的變化并不明顯(24種),在加熱4 h的時候提取出的物質總數還減少了1種。故可以看出,提取2 h已經可以較為充分地提取出酸筍樣品中的揮發性成分,故最佳萃取時間選擇為2 h。

表7 不同萃取時間對SDE萃取 酸筍揮發性物質效果的影響Table 7 Effect of different extraction time on extraction efficiencies of volatile compounds from bamboo shoots by SDE
2.3 HS-SPME法的萃取效果與條件優化
2.3.1 不同萃取頭對HS-SPME萃取酸筍揮發性物質效果的影響 四種不同涂層的萃取頭進行實驗,對比萃取效果,結果如表8所示。由表8可以看出,強極性萃取頭PA總峰面積較高,中極性萃取頭PDMS/DVB和CAR/PDMS的萃取總峰面積次之,非極性萃取頭PDMS萃取總峰面積最低。從萃取的物質總數來說,PDMS/DVB的萃取效果最好(39種),較PA萃取頭多了11種,從萃取效果完整性方面考慮,選擇65 μm PDMS/DVB為最佳萃取頭。
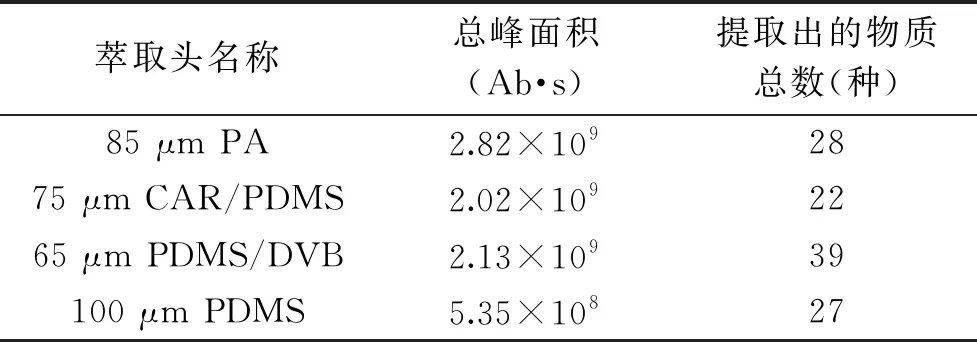
表8 不同萃取頭對HS-SPME萃取 酸筍揮發性物質效果的影響Table 8 Effect of different SPME fibers on extraction efficiencies of volatile compounds from bamboo shoots by HS-SPME
2.3.2 不同樣品離子濃度對HS-SPME萃取酸筍揮發性物質效果的影響 由于向水相溶液中添加鹽離子,可以通過增加離子強度,降低疏水性化合物在水中的溶解度,促進其析出,故在HS-SPME實驗中通常都會添加一定量的氯化鈉以增加萃取效果[13]。本實驗中研究了向樣品中分別加入相當于樣品質量0%(0.00 g)、1%(0.60 g)、2%(1.20 g)、3%(1.80 g)氯化鈉對萃取效果的影響。由表9可知,在添加氯化鈉量為0.00~1.20 g之間時,隨著添加氯化鈉質量的上升,總峰面積由1.88×109Ab·s上升至3.21×109Ab·s,萃取的物質總數也由38種上升至41種,而在將氯化鈉添加量增加至1.80 g時,萃取效果(3.21×109Ab·s,41種)與1.20 g時(3.23×109Ab·s,41種)相差不大。故可知在添加氯化鈉質量為1.20 g時,已經達到了將酸筍中的揮發性物質通過HS-SPME萃取出來的萃取效果。根據在醬油方面的對HS-SPME與鹽濃度的研究[7],當氯化鈉濃度上升到一定濃度,會對部分揮發性物質,特別是小分子揮發性物質產生抑制作用,如繼續增加氯化鈉濃度有降低萃取效果的可能,故在此選擇1.20 g作為最佳氯化鈉添加量。
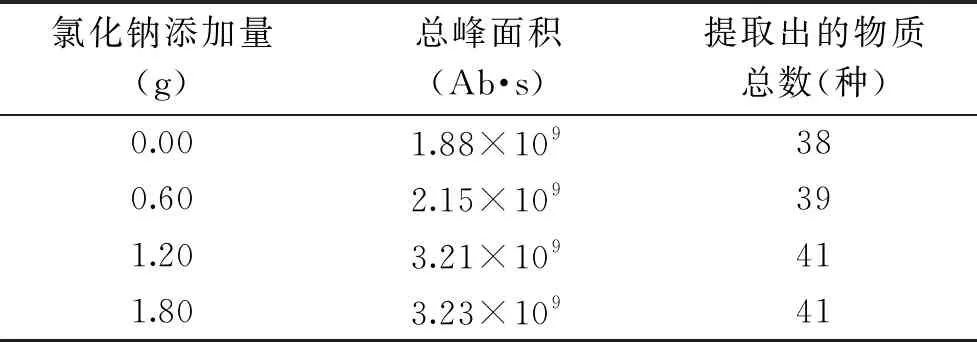
表9 不同離子濃度對SPME萃取 酸筍揮發性物質效果的影響Table 9 Effect of different salt concertrations on extraction efficiencies of volatile compounds from bamboo shoots by HS-SPME
2.3.3 不同萃取溫度對HS-SPME萃取酸筍揮發性物質效果的影響 本實驗分別在30、40、50及60 ℃進行萃取,對比萃取效果,結果如表10所示。由表10所示,萃取溫度由30 ℃上升到50 ℃之間時,萃取總峰面積由2.23×109Ab·s上升至3.20×109Ab·s,提取出的物質總數由34種上升至41種。但當萃取溫度上升到60 ℃時(3.22×109Ab·s,41種),萃取效果相較于50 ℃時(3.20×109Ab·s,41種)沒有明顯的變化。HS-SPME通過加熱使樣品中的揮發性物質析出,分散在樣品上方的空氣中,再通過萃取頭吸附揮發性物質,在這個過程中,萃取溫度的提高對揮發性物質的析出有加速作用,且部分揮發性物質必需達到一定的溫度才能充分揮發,故過低的溫度會降低萃取效果,而過高的溫度會造成頂空部分水蒸氣含量過高,加速萃取頭使用壽命的損耗。故可以得知,在進行HS-SPME萃取時,萃取溫度達到50 ℃時,已經足以對發酵酸筍的揮發性組分進行充分的萃取。

表10 不同萃取溫度對HS-SPME 萃取酸筍揮發性物質效果的影響Table 10 Effect of different extraction temperatures on extraction efficiencies of volatile compounds from bamboo shoots by HS-SPME
2.3.4 不同萃取時間對HS-SPME萃取酸筍揮發性物質效果的影響 在本實驗中在采取上述實驗選取出的最佳條件下,分別對樣品分別萃取10、20、30、40 min,對比萃取效果,結果如表11所示。灌服狹果茶藨子果實乙酸乙酯萃取物Ⅱ低、中劑量由表11可知,隨著溫度提取時間的增加,在30 min時提取物質的總峰面積達到3.21×109Ab·s,提取出的物質總數為41種,再繼續增加提取時間至40 min,提取物質總峰面積為3.23×109Ab·s,相較30 min時增加并不多,而物質種類沒有增加,說明提取時間為30 min已充分提取揮發性物質。

表11 不同萃取時間對HS-SPME 萃取酸筍揮發性物質效果的影響Table 11 Effect of different extraction time on extraction efficiencies of volatile compounds from bamboo shoots by HS-SPME
足夠的萃取時間可以讓固相微萃取頭與頂部空氣進行充分傳質,直到達到動態平衡則萃取完全,故一定的萃取時間是必要的。但由于用于萃取的樣品酸筍液水分含量較高,萃取過程中會產生大量水蒸氣,長時間令萃取頭暴露在有水蒸氣的環境中,會加速萃取頭使用壽命的損耗,故萃取時間在萃取充分的條件下也應該盡量縮短。故選擇30 min作為最佳提取時間。
2.4 不同提取方法對酸筍揮發性風味物質提取效果的比較分析
由2.1~2.3中的結論,分別采用LLE、SDE及HS-SPME的最佳條件進行萃取實驗。3種萃取方法的萃取物質詳表如表12,總離子流圖如圖1。
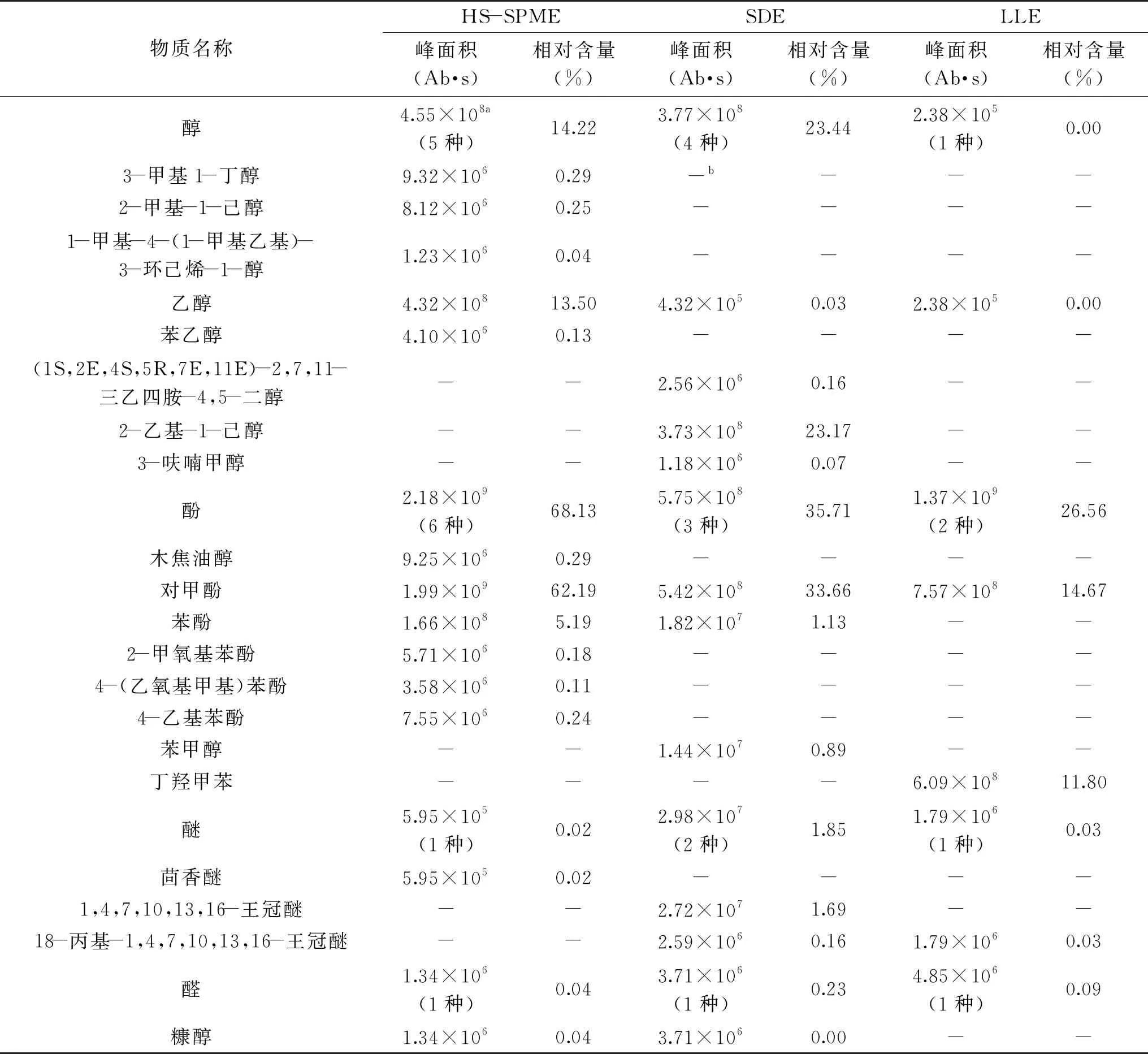
表12 不同提取方法酸筍揮發性風味物質的結果比較Table 12 The comparison results of volatile compounds from fermented bamboo shoots by different extraction methods
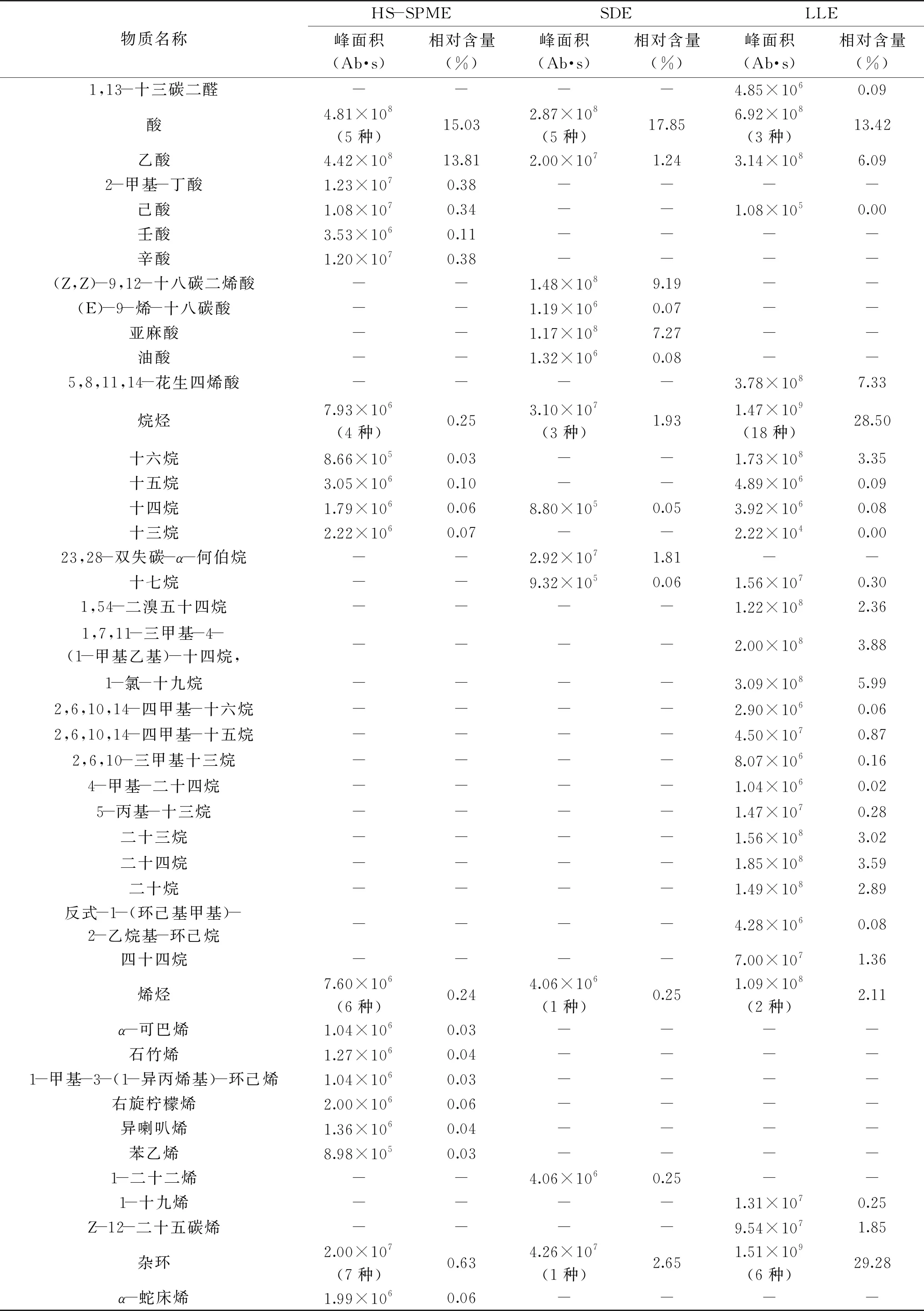
續表
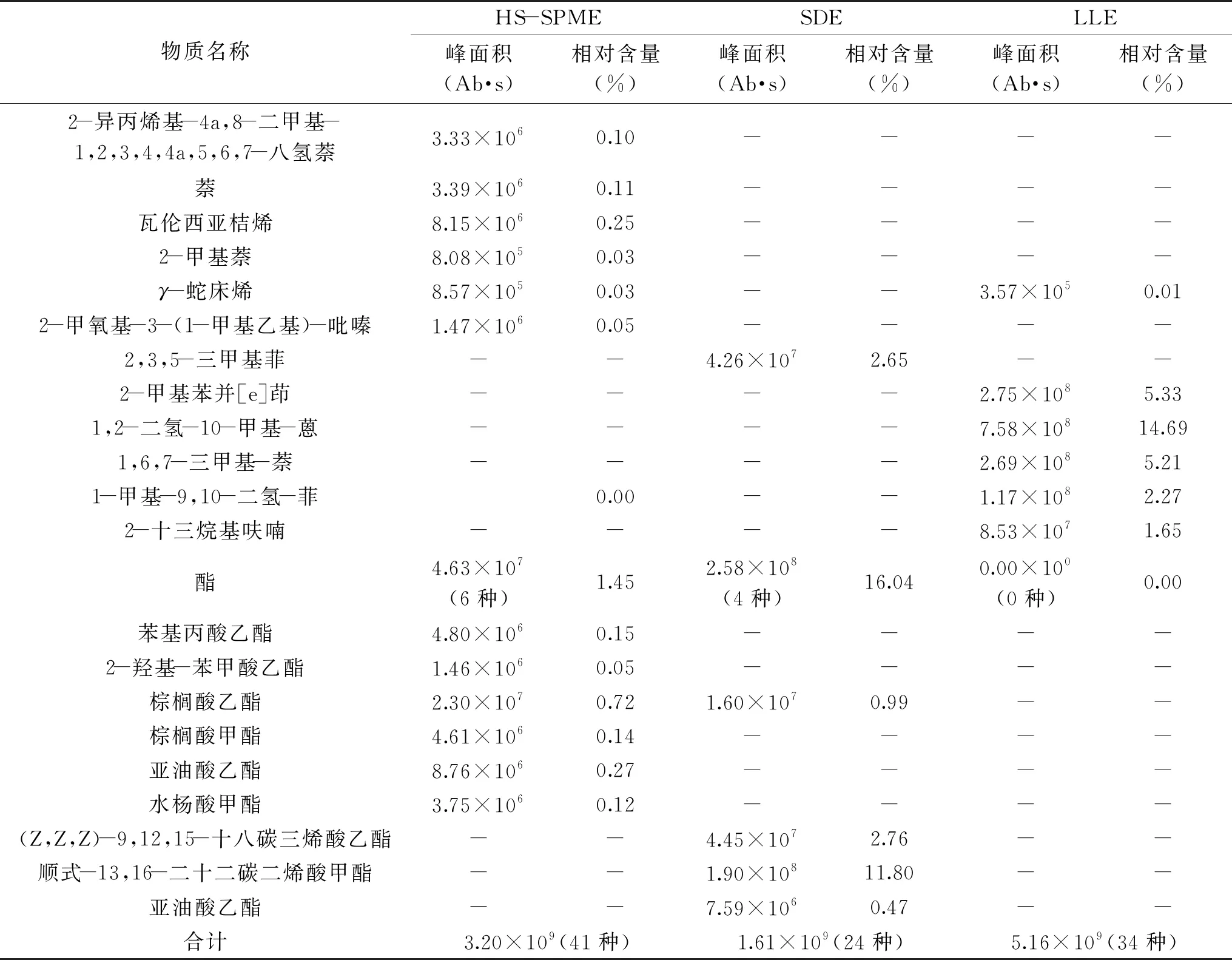
續表
由表12可知,萃取物質峰面積最大為LLE法,HS-SPME法次之,最后是SDE法,萃取物質種類由多到少順序則為HS-SPME法、LLE法、SDE法。無論是萃取物質峰面積還是萃取物質種類,均為SDE法效果最不理想。
相較于其他兩法,通過LLE法萃取的物質中,雜環類化合物相對含量最高(29.28%),一些雜環物質具有氣味活性如吡嗪、呋喃,但在本實驗LLE法萃取出的雜環化合物中,含量最高的為2-甲基苯并[e]茚、1,2-二氫-10-甲基-蒽、1,6,7-三甲基-萘等高沸點的化合物,揮發性較差,對氣味物質貢獻有限。烷烴類化合物種類較多(18種),占到了其萃取物質總數(34種)的一半以上,而該種物質的相對含量為第二,占到了28.50%,其中含有大量高碳數的烷烴,沸點較高。根據酒類、發酵乳制品、發酵調味品及發酵泡菜等其他發酵食品氣味的研究[14-17],烷烴類化合物由于大多數沸點較高或嗅聞閾值較高,在食品當中難以覺察,對氣味貢獻較小。而醇(1種)、酚(2種)、酸(3種)、烯(2種)等物質種類較少,這幾類物質的相對含量均小于以上兩種物質,相對含量之和為42%,而該類物質則通常作為對呈味起貢獻作用的物質存在[14-17]。這可能是由于LLE法引入了過多的非揮發性物質,故在GC-MS分離鑒定過程中掩蓋了含量較少的揮發性氣味物質。而另外兩法在原理上通過萃取以氣態形式存在的揮發性物質,沒有直接與樣品接觸,沒有出現這一問題。
SDE法萃取出的物質中相對含量最高的為酚類(35.71%)、醇類次之(23.44%),再到酸類(17.85%)和酯類(16.04%),合計達到93.04%。同上文所述,這幾類物質常被認為對氣味貢獻較大。在SDE萃取的這幾類物質中,含量較高的對甲酚、乙酸、3-呋喃甲醇等均是常見被報道的呈味物質。
HS-SPME法萃取物質峰面積相對較大,萃取出的物質種類最為豐富,且其中有著起氣味貢獻作用潛力的醇(5種)、酚(6種)、酸(5種)、烯(6種)、酯(6種)類物質較多,相對含量由多至少依次為酚(68.13%)、酸(15.03%)、醇(14.22%)及其他,前3類物質的相對含量達到了97.38%,其中含量較高的對甲酚、苯酚、乙酸、乙醇均是發酵食品中常見的氣味物質[14-17]。
可見對于揮發性物質的萃取效果上,LLE法雖然獲取的峰面積最大,但其萃取出的物質中氣味貢獻度較低的高沸點雜環類和烷烴類所占比例較高,而SDE法和HS-SPME法萃取物質種類則更多地集中在氣味貢獻度較高的強揮發性低沸點物質上。
對比圖1可以明顯看出,自25 min開始直至結束,LLE對應的總離子流色譜圖(圖1A)上出現較多雜峰,該現象并未在另外兩組色譜圖(圖1B、C)中出現,同時LLE萃取的萃取液相較于SDE萃取得到的樣液顏色偏黃,故認為在萃取過程中由于LLE法為萃取液與樣品液直接接觸,除含量偏少的揮發性氣味物質外,LLE法也將諸如色素等含量更高的非揮發性有機物萃取了出來,引起了雜峰偏多現象,這與前文中LLE法萃取物質中非氣味貢獻物質種類較多的情況相對應。這些雜峰的引入會掩蓋目標物質在色譜圖中的分離效果,同時也降低了質譜系統的鑒定精確度,這也就能解釋為何通過LLE法獲得的總峰面積最大,但通過質譜鑒定準確度高于80%的物質數低于HS-SPME法。
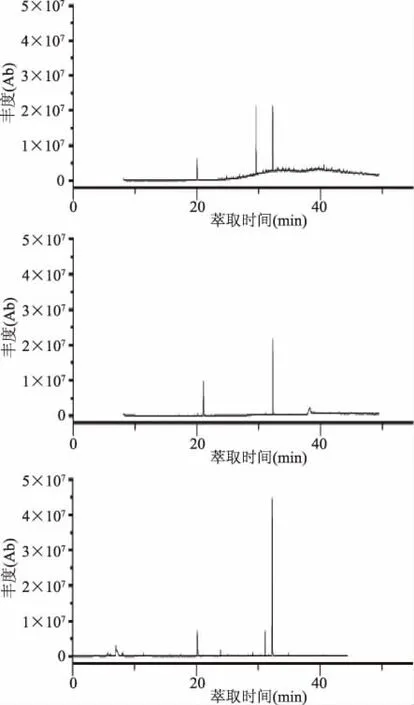
圖1 LLE、SDE及HS-SPME法 提取酸筍氣味物質總離子流色譜圖Fig.1 Total ion chromatogram of fermented bamboo shoots volatiles obtained by LLE,SDE and HS-SPME注:A圖為LLE法總離子流圖;B圖為SDE法總離子流圖; C圖為HS-SPME法總離子流圖。
綜上所述,LLE法萃取物質種類多,總峰面積最大,但對氣味起貢獻作用的物質相對含量偏低;SDE法萃取的物質中對氣味起貢獻作用的物質相對含量較高,但其萃取物質種類和總峰面積均在三法中最低;HS-SPME法萃取物質種類最多,總峰面積大,且萃取物質種類集中在對氣味起貢獻作用的物質上,故認為HS-SPME法是萃取發酵酸筍氣味物質的最佳方法。
3 結論
本研究主要優化了LLE、SDE、HS-SPME法在萃取發酵酸筍氣味物質方面的最佳萃取條件,并通過對比3種方法的萃取效果,選擇最佳的萃取發酵酸筍氣味物質的方法,結論如下:LLE法使用乙醚作為提取溶劑,稀釋液使用飽和氯化鈉溶液提取效果最佳。SDE法采用二氯甲烷作為提取溶劑,稀釋液采用100 mL飽和氯化鈉溶液,提取2 h效果最佳。HS-SPME法采用65 μm PDMS/DVB萃取頭,添加1.2 g氯化鈉,在50 ℃下水浴萃取30 min萃取效果最佳。各萃取法使用以上條件,可使得萃取峰面積及萃取物質種類達到最大。對比3種萃取方法,由于LLE法直接接觸樣品液,傳質效果好,萃取物質峰面積最大(5.16×109Ab·s),且萃取物質種類多(34種),但其中對氣味貢獻作用低的高沸點雜環類和烷烴類物質所占比重較大(相對含量達到57.78%);而SDE法萃取物質集中在對氣味貢獻度較高的酚、醇、酸、酯類物質上(相對含量達到93.04%),但其峰面積最小(1.61×109Ab·s),萃取物質種類最少(24種);HS-SPME對揮發性成分的萃取峰面積較高(3.20×109Ab·s),同時該法萃取的物質種類最為豐富(41種),且其中酚、酸、醇類物質相對含量高(97.38%),故HS-SPME法為萃取發酵酸筍氣味物質的最佳方法。

