降鈣素基因相關肽的胃黏膜保護機制的研究進展
羅雙慧 劉 巍 曾志琴 胡楚鵬 許寧銀 黃 安 奚 濤 邢瑩瑩
中國藥科大學生命科學與技術學院,江蘇南京 211198
胃潰瘍是全球普遍的胃腸道疾病之一。胃潰瘍的病理生理學涉及胃黏膜的攻擊性和保護性因素之間的不平衡[1]。頻繁暴露于各種有害的刺激很容易導致胃黏膜損傷,這些有害刺激包括外在因素(如乙醇、非甾體類抗炎藥、幽門螺桿菌和缺血再灌注損傷)和內在因素(如胃酸、胃蛋白酶和炎癥趨化因子)[2-3]。加強胃黏膜的保護機制有助于預防胃潰瘍。在正常生理條件下,胃黏膜依賴多種保護機制維持結構的完整性,并通過黏膜防御系統抵御外來有害刺激[4]。除了胃黏膜屏障外,許多內源性物質(包括神經遞質和局部自體活性物質等)有助于保護胃黏膜免受炎癥、氧化應激和細胞凋亡的影響。其中,降鈣素基因相關肽(calcitonin gene-related peptide,CGRP)是辣椒素敏感性感覺神經的主要傳遞物,是公認的胃黏膜保護物質[5]。本文論述CGRP 對胃黏膜保護的相關作用機制,重點闡述通過刺激CGRP 釋放減少胃黏膜損傷的最新研究進展。
1 降鈣素基因相關肽的生物特性
CGRP 是人類用基因重組技術發現的第一個活性多肽[6],通過選擇性剪接降鈣素基因(CALCA)產生。它含有37 個氨基酸,分子量約為3800 D(圖1)[7],主要有2 個亞型:α-CGRP 和β-CGRP。α-CGRP 主要分布在外周神經系統,而胃腸神經的內在神經元主要表達β-CGRP。2 種亞型由不同的基因編碼,但具有較高的序列相似性,因此生物學功能相似[8]。CGRP 主要的合成部位是背根神經節(DRG),在感覺神經細胞胞體合成,以軸漿運輸方式運送到神經末梢,與P 物質、神經激肽共同存儲在突觸小體內。在感覺神經末梢或胞體胞膜上存在的辣椒素受體(TRPV1),是調節CGRP合成與釋放的關鍵受體(圖2)[9]。
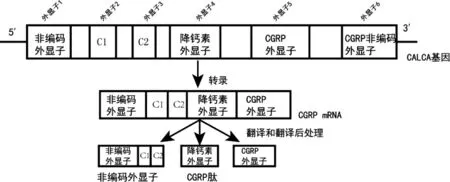
圖1 CGRP 肽的剪接和翻譯后加工
TRPV1 是主要在感覺神經中表達的非選擇性陽離子通道,它們在CGRP 陽性纖維中高度共表達[10]。當該通道受到刺激開放時,細胞外的陽離子(主要包括鈉離子和鈣離子)內流,導致胞質內鈣離子濃度增加,鈣離子作為第二信使,促使P 物質和CGRP 釋放,引發一系列重要的生物學反應(圖2)。盡管人們已經充分認識到CGRP 的合成受TRPV1 激活的調節,但確切的機制仍然未知。
由于外周辣椒素敏感感覺神經的存在,CGRP 廣泛分布于心血管、胃腸道和呼吸系統并發揮多種功能。CGRP 是迄今為止發現的最有效的血管擴張器,它的藥效比其他血管舒張藥(如腺苷、P 物質或乙酰膽堿)的效力高約1000 倍[11]。除此之外,CGRP 還具有抗凋亡、抗血小板聚集、抗氧化、抗增殖和抗衰老的特性,可以保護機體內的多種系統,使其能夠抵御相關疾病的高危因素。
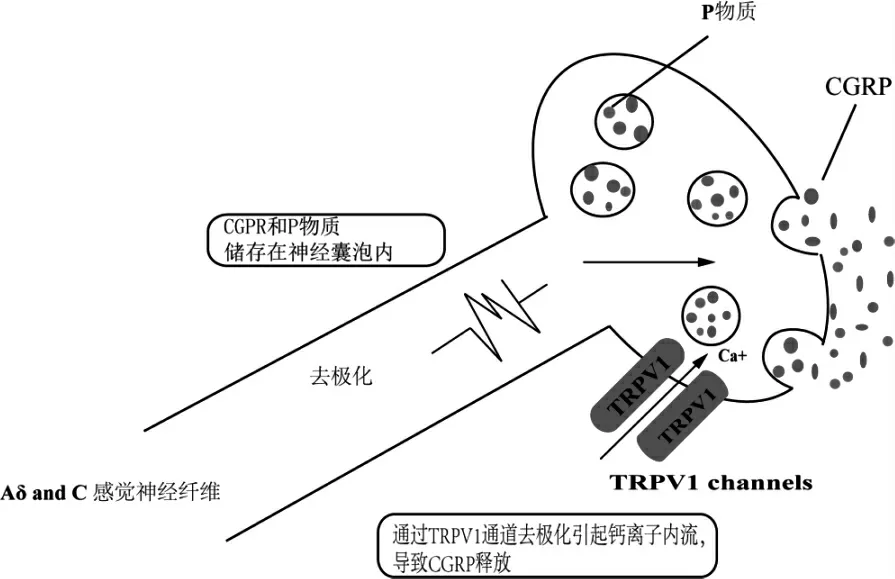
圖2 TRPV1 通道的調節作用
2 降鈣素基因相關肽對胃黏膜的生物影響
2.1 CGRP 與胃酸分泌
早期的研究表明,CGRP 是一種有效的胃酸分泌抑制劑[5]。胃黏膜損傷與胃酸的分泌增加密切相關,動物實驗和臨床觀察均證實顱腦損傷和燒傷后,胃液中氫離子濃度增加,應用抗酸劑及抑酸劑可有效地預防和治療應激性胃潰瘍。胃酸分泌的增加與神經中樞和下丘腦損傷引起的神經內分泌失調、血清胃泌素增高、CGRP 減少有關[13]。在小鼠模型中,五肽胃泌素或腦池內促甲狀腺素釋放激素外源地刺激小鼠的胃酸分泌,而CGRP 能減少63%~78%的胃酸分泌[14]。CGRP受體在胃黏膜細胞中普遍表達,靜脈注射CGRP 受體拮抗劑,CGRP8-37 或CGRP 抗體能完全阻止CGRP對胃酸分泌抑制的影響[15]。CGRP 能夠減少基礎泌酸量,降低胃蛋白酶活性和胃液消化活動度,可用于消化性潰瘍的治療。
2.2 CGRP 與胃黏膜血流
CGRP 是一種廣譜擴血管物質。使用氫氣清除技術控制大鼠的基礎胃黏膜血流量在35~50 mL/(min·100 g)范圍內,用大鼠α-CGRP(15、75 pmoL/min)以劑量依賴方式灌注能顯著增加胃黏膜血流量,但對平均動脈血壓的影響很小[16]。CGRP 增加血流量主要分為兩種機制:一種是CGRP 與內皮細胞上的受體結合,上調一氧化氮合酶(NOS)產生一氧化氮(NO)[10]。NO穿過細胞膜,活化平滑肌內可溶性鳥苷酸環化酶,經cGMP 通路活化蛋白激酶G,后者可作用于Ca2+-ATP酶,使細胞內游離鈣離子濃度下降,舒張平滑肌[17]。CGRP 也可通過前列環素活化cAMP/PKA 途徑,發揮舒張血管的作用,cAMP 升高的程度與血管舒張反應的強弱密切相關。另一種是CGRP 可以不經過內皮,直接與血管平滑肌細胞上的受體結合,通過cAMP 活化PKA或通過激活血管平滑肌細胞膜上的K+-ATP 通道來實現[7]。格列本脲是三磷酸腺苷敏感鉀通道的抑制劑,它能有效削弱CGRP 對胃黏膜血流量的增加效果,這也說明CGRP 提高血流量需要通過激活三磷酸腺苷敏感鉀通道[18]。
2.3 CGRP 與胃腸運動
大量實驗證明,胃黏膜損傷及肌肉牽拉等傷害性刺激均可引起感覺神經元釋放CGRP,激活蠕動反射的效應器(如調節神經元和運動神經元),也可直接作用于受刺激部位的平滑肌。CGRP 對大部分胃腸道運動起抑制作用,主要涉及的機制有以下兩種:一種是對腸段的縱向和圓形肌肉的直接松弛作用;另一種是刺激蠕動反應的神經元(如非腎上腺素能非膽堿能抑制神經元),釋放其他抑制型神經遞質,如NO 和血管活性腸肽,間接影響腸蠕動[17]。不僅如此,CGRP 在傷害性刺激下被釋放到局部,作為脊髓抑制反射通路的一部分,進而激活脊髓傳入神經纖維,抑制胃腸運動[19]。胃腸道依賴于CGRP 這種保護劑對血流量的增加和對胃腸道蠕動的調節,有助于改善胃局部微循環并恢復胃潰瘍造成的胃黏膜損傷。
3 CGRP 與抗炎和抗凋亡機制的相關性
研究表明,CGRP 的下調和胃潰瘍的發病機制有關,而目前許多藥物是通過上調CGRP 表現出抗潰瘍活性[20]。由檸檬酸桿菌獲得的富含鞣花單寧的成分對大鼠乙醇誘導的消化性潰瘍發揮胃保護作用,其機制包括增加CGRP 表達,小鼠體內CGRP 表達增加呈檸檬酸桿菌劑量依賴性[21]。辣椒素敏感的感覺神經細胞纖維受刺激后釋放CGRP,后者提高胃黏膜組織中前列環素、前列腺素E2水平從而抑制中性粒細胞的活化和肥大細胞的脫顆粒,減少組胺等炎癥介質的釋放,在減輕胃腸道炎癥方面起重要作用[22-23]。
不僅如此,CGRP 也通過抗炎和抗凋亡的機制保護大鼠胃黏膜免受缺血再灌注損傷。在小鼠缺血再灌注損傷模型中,腹腔注射3 μg/kg 的CGRP 能顯著減少缺血再灌注損傷引發的胃黏膜水腫、出血、細胞凋亡、黏膜分離和炎癥細胞浸潤[24-25]。在局灶性腦缺血再灌注誘導的胃黏膜損傷模型中也有類似的結果。CGRP 主要通過促進生長抑素表達的上調和胃泌素表達的下調來改善局部內環境,對缺血再灌注誘導的胃黏膜損傷發揮保護作用[26]。
在其他研究中,CGRP8-37 的全身給藥加劇了吲哚美辛或乙醇誘導的黏膜損傷[27],表明內源性CGRP對胃黏膜防御至關重要。在存在NOS 抑制劑亞硝基左旋精氨酸甲酯的情況下,CGRP 的胃保護作用明顯減弱。進一步的研究發現,CGRP 能夠通過減少主要內源性NOS 抑制劑(不對稱二聚體γ-精氨酸)來增加NO[28]。NO 是一種重要的胃黏膜保護因子,具有擴張血管、調節免疫應答、調節神經遞質釋放等作用[29]。因此,CGRP/NO 途徑可能成為CGRP 對胃黏膜有益作用的另一個機制。
CGRP 基因敲除模型進一步證實了CGRP 在維持胃黏膜完整性和增強潰瘍愈合中的重要作用。研究表明,在CGRP 敲除小鼠中,完全不存在由胃先前暴露于輕度刺激物誘導的適應性CGRP 介導的胃腸保護作用[30]。辣椒素去神經支配,導致傳入神經末梢釋放CGRP 削弱,加重了浸水-束縛應激引發的胃黏膜損傷[5]。這些報告提供趨同的證據,即CGRP 對胃黏膜完整性和防御有益。實際上許多肽(例如肽YY、腎上腺髓質素、胰島淀粉樣多肽、胰高血糖素樣肽等)可能都是通過CGRP 釋放增加的共同機制提供針對乙醇誘導損傷的胃保護[31]。
4 總結
CGRP 不僅能抑制胃酸分泌,調節胃腸運動,還能通過舒張血管和抗炎、抗凋亡等機制來修復應激性胃損傷。CGRP 的分泌增加能調節腸胃蠕動,有效保護胃黏膜防御刺激物。從辣椒素到合成的辣椒素酯,尋找胃腸道疾病的治療策略方面在刺激內源性CGRP釋放的基礎上取得了很大的進展。神經元和免疫細胞的雙向調節作用協調宿主對病原體入侵的機制,也為我們提供了新的思考方向。然而,辣椒素在自然水環境中很容易分散,半衰期短,可迅速在血液中被清除。因此,提高辣椒素的穩定性或尋找合適的類似物是未來研究中的主要任務。使用CGRP 治療的另一個難題是,作為一種多肽,CGRP 口服利用度低,難以從大量相似的內源性分子中鑒定出來進行量化。此外,CGRP治療在給藥和代謝方面還面臨很多挑戰。

