少見部位神經內分泌癌的CT及MRI表現
瞿姣, 袁欣, 趙衛, 李德艷, 楊亞英
發生于消化道及肺以外的神經內分泌癌少見,且文獻多見側重于描述其病理或臨床特征的個案報道,鮮有分析少見部位神經內分泌癌影像學特征的文章。本文通過回顧性分析31例少見部位神經內分泌癌的影像學資料并復習相關文獻,旨在提高對本病的認識。
材料與方法
1.臨床資料
回顧性分析我院2009年3月-2018年12月經手術病理證實并有完整臨床及影像學資料的少見部位神經內分泌癌31例。男24例,女7例,男女比例3.4∶1;年齡 4~86(54.90±20.90)歲。31例中病變位于鼻腔鼻竇7例,縱隔14例,腎臟2例,膀胱4例,前列腺2例,肝臟1例,卵巢1例。所有患者均經取材活檢或手術病理獲得組織學及免疫組化結果。
2.檢查儀器及方法
本組31例中20例術前行CT平掃+增強檢查,1例行MRI平掃+增強檢查,6例同時行CT平掃+增強及MRI平掃+增強檢查,4例同時行CT平掃及MRI平掃+增強檢查。CT檢查采用Siemens 64排或128排螺旋CT掃描儀,管電壓100~120 kV,管電流150~250 mAs;增強掃描:經肘靜脈按流率2.5 mL/s注射對比劑碘海醇(1.5 mL/kg×體重)后跟注生理鹽水30 mL,頭頸部及胸部行動脈期及靜脈期雙期增強掃描,腹盆腔行動態增強掃描。磁共振掃描:平掃采用快速自旋回波(TSE),獲得軸面、冠狀面T2WI、冠狀面壓脂T2WI及軸面T1WI,增強掃描:以流率1.5~2.0 mL/s經肘靜脈靜脈注入Gd-DTPA(0.2 mmol/kg)后行增強軸面、冠狀面及矢狀面T1WI,層厚為1~5 mm,層間距為1 mm;9例行DWI掃描,b值取0,800~1000 s/mm2。
3.圖像分析
由2名高年資放射科診斷醫師共同閱片,回顧性分析所有病例的CT及MRI圖像,意見有分歧時通過討論達成一致。觀察并記錄病變部位、大小、形態、密度/信號、強化特征及周圍結構侵犯、骨質破壞、淋巴結轉移情況。
結 果
本組31例,臨床表現均無特殊性。影像形態學特征見表1:病灶均表現為類圓形或不規則軟組織腫塊(圖1~7),最大徑線范圍2.7~11.6 cm,平均(6.90±2.52) cm,中位數6.0 cm,29例≥4 cm。密度、信號不均,CT平掃表現為以中等密度為主的混雜密度影,磁共振T1WI呈等或稍低信號,T2WI呈以等或稍高信號為主的混雜信號,8例DWI高b值擴散受限呈混雜高信號,ADC圖為低信號。增強后5/31呈不均勻輕度強化,13/31呈不均勻中等程度強化,13/31呈不均勻明顯強化,1例時間-信號強度曲線(time intensity curve,TIC)呈流出型;14例縱隔神經內分泌癌中,12例見分隔樣強化或小血管穿行征(圖1、2)。28/31的病灶內見不同形態壞死區(圖3~6),僅2/31于病灶邊緣見小斑片狀鈣化。31例均伴周圍組織侵犯,其中7例發生于鼻腔鼻竇的神經內分泌癌周圍侵犯以骨質破壞為主(7/7)且均表現為膨脹性與浸潤性破壞并存,未見明顯骨質硬化(圖3b);發生于縱隔的病變均伴有周圍結構侵犯(14/14),以頭臂靜脈、上腔靜脈及心包受侵多見(12/14)。31例中,17/31伴淋巴結轉移,轉移淋巴結與原發灶強化方式一致。1例肝臟神經內分泌癌,表現為肝內多個腫塊,累及肝左右葉及膽囊,增強動脈期呈不均勻中度強化,靜脈期持續強化(圖7)。1例卵巢神經內分泌癌,表現為右附件區稍低密度腫塊伴子宮及右輸尿管受侵、右腎靜脈旁淋巴結轉移。
病理免疫組織化學結果提示嗜鉻素A(CgA) 、突觸素(Syn)、神經元特異性烯醇化酶(NSE) 、CD56陽性表達比例分別為67.7%、93.5%、25.8%、38.7%。
討 論
神經內分泌癌(neuroendocrine carcinoma,NEC)是起源于黏膜上皮及黏膜下腺體上皮細胞的一類能夠攝取胺的前體(氨基酸)并通過脫羧作用合成和分泌胺及多肽激素的罕見惡性腫瘤[1],好發于消化道和肺部,常見部位包括胃(類癌)、肺(小細胞癌)、胰(胰島細胞癌)[2],發病機制尚不明確。WHO將其分為類癌、分化好的神經內分泌癌(不典型類癌)、分化差的神經內分泌癌(包括小細胞癌和大細胞神經內分泌癌)[3]。原發于鼻腔鼻竇、縱隔、肝臟、腎臟、膀胱、前列腺及卵巢的NEC罕見且臨床癥狀無特殊性,僅部分小細胞NEC可出現皮膚潮紅、哮喘和腹瀉等類癌綜合征表現。

表1 31例NEC的影像形態學特征
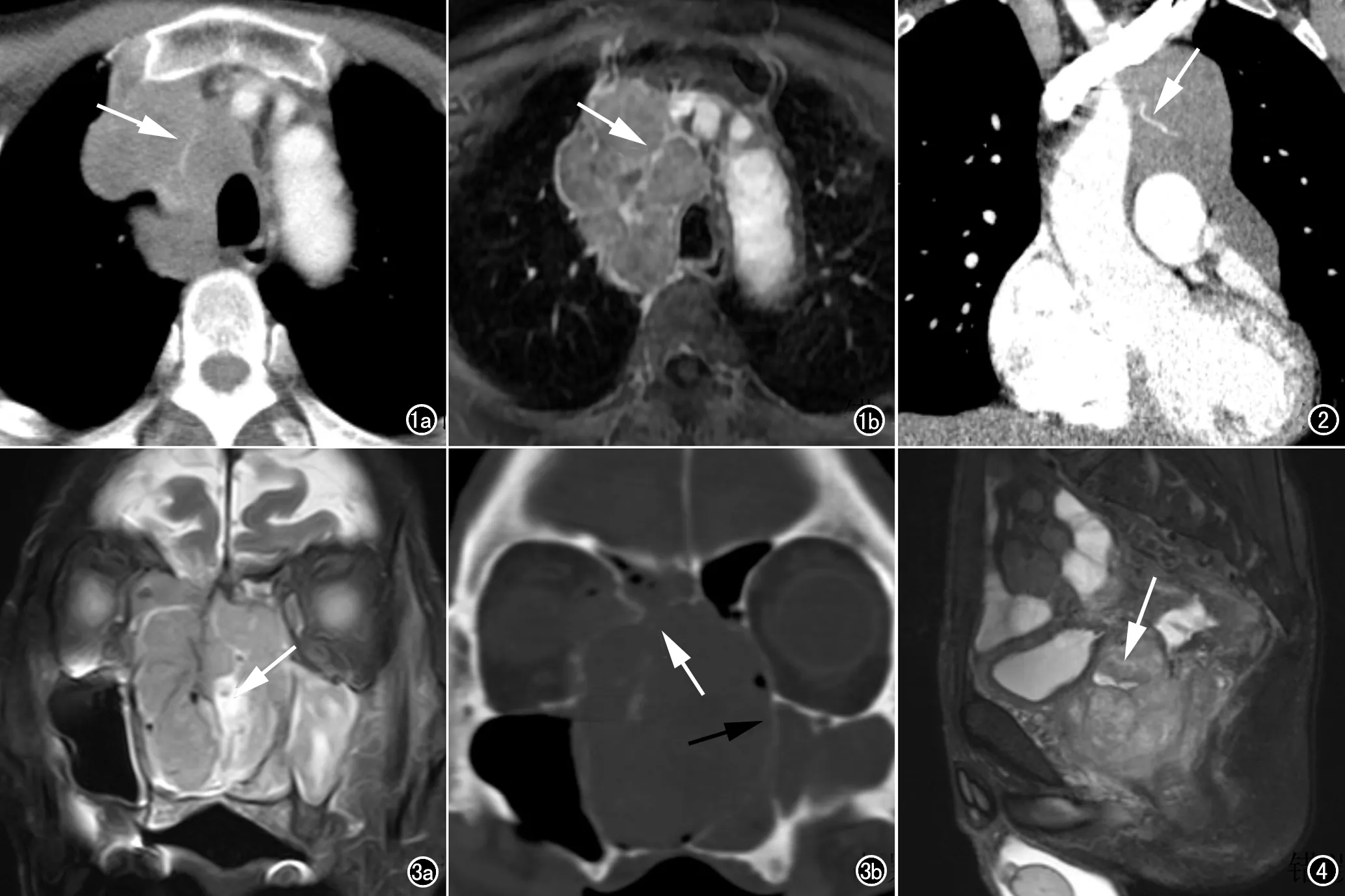
圖1男,61歲,縱隔低分化NEC。a) CT增強掃描示右側前中縱隔軟組織腫塊內線樣明顯強化區(箭);b) MRI軸面T1WI增強亦顯示病灶內多發分隔樣強化(箭)。 圖2男,39歲,前上縱隔NEC。冠狀面CT增強圖像示腫塊內小血管穿行征(箭)。 圖3男,80歲,鼻腔鼻竇NEC。a) MRI冠狀面壓脂T2WI圖像示雙側鼻腔、篩竇及左側上頜竇混雜稍高及高信號腫塊,其內見片狀壞死區(箭); b) CT平掃冠狀面骨窗圖像示雙側上頜竇內側壁、鼻中隔、鼻甲、篩竇各壁骨質膨脹性吸收(黑箭)與浸潤性破壞(白箭)并存,未見骨質增生硬化。 圖4男,82歲,前列腺NEC。MRI矢狀面T2WI示前列腺混雜稍高及高信號腫塊,體積大,侵犯精囊腺、膀胱后壁及直腸前壁,病灶內見條片狀T2WI高信號壞死區(箭)。
NEC光鏡下腫瘤細胞排列呈團巢狀、柵欄狀、小梁狀等[4],結合神經元特異性烯醇化酶(NSE)、嗜鉻素A(CgA)、突觸素(Syn)及CD56等標記物陽性表達可確診;其中CgA對NEC具有高度特異性,Syn被視為診斷分化良好的NEC最具敏感性的指標[5],而高密度NSE的表達往往提示該病[2]。NEC各亞型的生物學行為、組織惡性程度不同,故不同病理分型的NEC治療方法及預后各異。
分析本組少見部位神經內分泌癌的影像學特征并結合相關文獻發現因神經內分泌癌侵襲力強,早期易擴散,因此在CT及MRI上常表現為浸潤性生長的軟組織腫塊,體積通常較大且極易侵犯鄰近結構,易發生淋巴結轉移及遠處轉移。其密度和信號表現各異,以實性成分多見[6],壞死常見,這與組織學上NEC伴有廣泛的出血和壞死相符[4]。病灶內偶見鈣化,可能為局部組織營養不良所致[7]。強化程度文獻報道不一,但與分化程度有關且大致有以下趨勢:高分化腫瘤多為均勻強化,而大部分低分化腫瘤呈不均勻強化[8-9]。本組31例均表現為軟組織腫塊影,體積較大,壞死率達90.3%,以片狀壞死多見,僅2例見鈣化,增強后均表現為不均勻強化,周圍組織侵犯率高達100%,54.8%伴淋巴結轉移,與文獻相符。
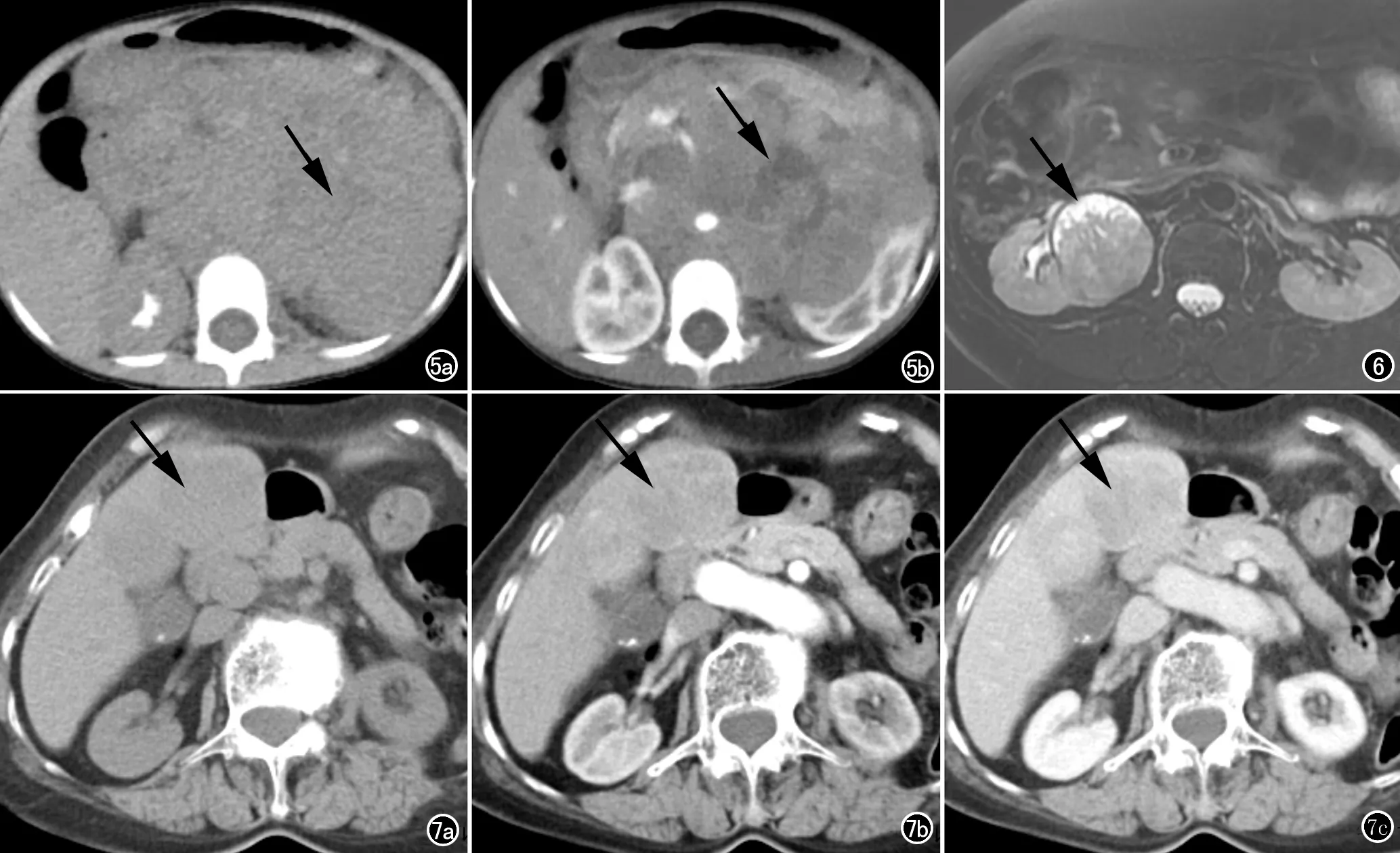
圖5女,4歲,左腎NEC。a)腹部CT平掃軸面圖像示左腎巨大腫塊(箭),邊界不清;b)增強掃描腫塊呈不均勻中度強化,其內見片狀壞死區(箭),周圍結構廣泛受侵。 圖6女,54歲,右腎NEC。MRI軸面脂肪抑制T2WI示右腎混雜稍高及高信號腫塊,其內見片狀壞死(箭),右側腰大肌顯示不清。 圖7女,80歲,肝臟NEC。a) CT平掃示肝臟多個低密度腫塊(箭);b) 增強動脈期病灶呈不均勻中度強化(箭);c)增強靜脈期病灶持續強化(箭)。
除上述共性外,不同部位的NEC影像表現差異較大。
縱隔NEC:好發于前縱隔,易侵犯縱隔大血管及心包等結構[10],常于病灶內出現線樣、分隔樣強化或瘤內細小血管強化影即“瘤內血管穿行征”[11],病理提示為腫瘤內部豐富的纖維血管分隔,此征象罕見于前縱隔其他腫瘤[7]。本組14例縱隔NEC,周圍組織受侵率為100%,以心包、頭臂靜脈及上腔靜脈受累最為多見,其中12例于病灶內見小血管穿行或線樣、分隔樣強化。
鼻部NEC:文獻顯示鼻部NEC好發于鼻腔、篩竇及上頜竇, 常伴壞死,病灶極易侵犯竇壁骨質且膨脹性骨質破壞吸收與浸潤性破壞并存、骨質輪廓可見且不伴骨質硬化是其有別于其他惡性腫瘤的特征表現[12,13];本組7例鼻部NEC,病變壞死率為85.7%,以灶性及小片狀壞死多見,周圍骨質均以膨脹性及浸潤性破壞并存且未見骨質增生硬化,與文獻相符。
單純的前列腺NEC以PSA水平升高不顯著、腫塊較大伴鄰近組織受侵及淋巴結轉移為特點[14],本組2例病灶體積較大且均伴膀胱、精囊腺、直腸下段侵犯及盆腔、髂窩淋巴結轉移(圖4),其中1例PSA 3.04 ng/mL,處于正常值范圍,另一例同時合并前列腺上皮源性惡性腫瘤,PSA 41.2 ng/mL。
既往報道的腎類癌約26%見鈣化,約75%增強后強化不明顯,動脈造影顯示為乏血供腫瘤[15],多早期出現局部侵犯和淋巴結轉移,本組2例腎臟NEC中1例見斑片狀鈣化,增強后2例均呈中度強化,均伴不同程度的周圍結構侵犯。
肝臟NEC:文獻報道的肝臟NEC多表現為肝內腫塊伴囊變壞死[16],一般無肝硬化,動脈期實性部分呈輕中度強化,靜脈期持續強化有助于疾病的診斷[1]。本組1例肝臟NEC,無肝硬化征象,病灶內見不規則壞死區,增強動脈期實性部分呈不均勻中度強化,靜脈期持續強化,與文獻相符。
本組31例術前影像診斷均考慮惡性腫瘤,但未定具體病理類型,可能與筆者對本病的認識不夠充分有關。
綜上所述,NEC可發生于全身各處,CT及MRI具有一定的特點:病灶表現為大腫塊,壞死常見,鈣化少見,極易侵犯周圍結構。鼻腔鼻竇神經內分泌癌周圍骨質膨脹性與浸潤性破壞并存且不伴骨質硬化,縱隔NEC伴分隔樣強化或瘤內血管穿行征較具特征性。CT結合MRI優勢互補,能充分顯示病變的范圍,周圍侵犯程度及骨質破壞情況,有助于NEC的診斷。