基于TOPSIS分析與多組分定量的感冒靈制劑質量控制研究
肖日傳,匡艷輝,鄭捷,王德勤
(廣州白云山和記黃埔中藥有限公司,廣東 廣州 510515)
感冒靈制劑是一種經典的中西藥復方制劑,市面上的劑型主要包括顆粒劑、膠囊劑和片劑3種,如復方感冒靈顆粒、復方感冒靈片、感冒靈膠囊等,在臨床上應用十分廣泛,常用于治療頭痛、發熱等由感冒引起的各種癥狀,現收載于《中華人民共和國衛生部藥品標準中藥成方制劑》[1]。作為中西藥合用的典范,感冒靈制劑在不斷臨床實踐中,得到了廣泛認可。研究表明,由于中藥組分的加入,中西藥組方配伍后起到了非常明顯的協同作用,特別是在抗感染和抑菌方面[2],同時也在一定程度上制約了西藥成分的毒性或不良反應[3]。
以顆粒劑為例,感冒靈顆粒和復方感冒靈顆粒所用西藥原料相同,均為對乙酰氨基酚、咖啡因和馬來酸氯苯那敏,但在中藥原料方面兩者有所不同,感冒靈顆粒中的中藥成分為三叉苦、金盞銀盤、野菊花和崗梅,復方感冒靈顆粒中則為金銀花、五指柑、野菊花、三叉苦、南板藍根和崗梅。現行標準中,感冒靈3種劑型含量測定項均以西藥成分對乙酰氨基酚為主要指標,或增加一種成分如咖啡因或綠原酸為控制指標;現有研究也多對西藥成分對乙酰氨基酚、咖啡因和馬來酸氯苯那敏中的一種或者幾種進行測定,如丁宏珍[4]和吳小輝[5]對感冒靈顆粒中對乙酰氨基酚的質量分數進行了測定,蔡松濤等[6]報道了感冒靈片中對乙酰氨基酚、馬來酸氯苯那敏、咖啡因化藥成分的質量分數檢測;或者僅有增加來源于中藥原料的綠原酸成分測定的少量研究,如夏方亮等[7]對復方感冒靈膠囊中對乙酰氨基酚和綠原酸的質量分數進行了檢測,倪坤儀等[8]在檢測復方感冒靈片3種化藥成分的基礎上,增加了綠原酸成分的質量分數測定。
綜上可知,中西藥復方制劑的質量控制以測定多個組分為趨勢,且中藥成分的作用不容忽視。本文以綠原酸、木犀草苷、蒙花苷、異綠原酸B和異綠原酸C作為檢測指標,其中綠原酸、異綠原酸B與異綠原酸C來源于野菊花、金盞銀盤或金銀花,蒙花苷來源于野菊花,木犀草苷來源于野菊花或金銀花。探討感冒靈多種劑型5種成分同時測定的質量分析方法,并基于質量分數測定結果,采用TOPSIS法進一步對不同批次樣品進行比較和分析,以期為建立一種更全面、系統的感冒靈制劑整體質量評控的技術體系奠定基礎,為其質量標準的完善提升提供數據支撐。
1 儀器與材料
Agilent 1260高效液相色譜儀及DAD檢測器(美國Agilent公司);KQ-600VDB型雙頻數控超聲波清洗器(昆山市超聲儀器有限公司);CP225D十萬分之一電子分析天平(賽多利斯科學儀器有限公司)。
綠原酸(批號110753-201415)、木犀草苷(批號111720-200905)購自中國食品藥品檢定研究院,異綠原酸B(批號MUST-18031602)、異綠原酸 C(批號MUST-18031603)、蒙花苷(批號MUST-17071710)購自成都曼斯特生物制品有限公司。乙腈為色譜純,其余試劑為分析純。感冒靈制劑來自不同生產廠家的不同劑型,各批次樣品信息見表1。
2 方法與結果
2.1 色譜條件
Agilent Eclipse Plus C18(4.6 mm×250 mm,5 μm)色譜柱;流動相為乙腈(A)-0.1%(體積分數)H3PO4水溶液(B),梯度洗脫:0~10 min,13%A;10~15 min,13%A→20%A;15~20 min,20%A;20~40 min,20%A→30%A;40~50 min,30%A→60%A。體積流量:1 mL/min;柱溫:30 ℃;檢測波長:327 nm(綠原酸、異綠原酸B和異綠原酸C),334 nm(蒙花苷),350 nm(木犀草苷);進樣量:10 μL。
2.2 混合對照品溶液的制備
分別精密稱取各對照品適量,加甲醇溶液溶解,制成含綠原酸43 μg/mL、木犀草苷35 μg/mL、異綠原酸B 42 μg/mL、異綠原酸C 42 μg/mL、蒙花苷64 μg/mL的混合對照品溶液,于4 ℃冰箱保存備用,臨用前經0.22 μm微孔濾膜濾過,即得。
2.3 供試品溶液的制備
取各感冒靈制劑(片劑需除去糖衣、膠囊劑取內容物、顆粒劑直接取樣),置研缽中研細,過3號篩。分別精密稱取各批樣品3 g,置具塞錐形瓶中,精密加入甲醇25 mL,密塞,稱定質量,超聲處理(功率250 W,頻率45 kHz)30 min。放冷后稱定質量,用甲醇補足減失的質量,搖勻、濾過,取續濾液,即得。
2.4 方法學考察
2.4.1 線性關系的考察 精密吸取“2.2”項下混合對照品溶液2、4、6、8、10、12 μL,分別注入液相色譜儀中,按“2.1”項下色譜條件測定。以進樣量為橫坐標,峰面積為縱坐標,繪制標準曲線,進行回歸分析,回歸方程及相關系數見表2。
表1 36批感冒靈制劑來源信息表
Table1Source information table of 36 batches of Ganmaoling preparations

編號制劑名稱廠家批號規格每日用量/gS1感冒靈顆粒廣東A117120110 g/袋30S2北京B2017072710 g/袋30S3安徽C17070810 g/袋30S4四川D17010110 g/袋30S5廣西E1180130210 g/袋30S6廣西E22017110110 g/袋30S7廣西E31711020210 g/袋30S8廣東A2D18F00910 g/袋30S9廣東A317125110 g/袋30S10廣西E418020910 g/袋30S11云南F2017111510 g/袋30S12廣東A42017010110 g/袋30S13廣東A52017081810 g/袋30S14廣東A62017020510 g/袋30S15廣西E418012810 g/袋30S16廣西E518020410 g/袋30S17河南G2017050410 g/袋30S18廣東A71801046H10 g/袋30S19廣東A81808022H10 g/袋30S20感冒靈膠囊吉林A1712010.5 g/粒3S21黑龍江B201802020.5 g/粒3S22廣西C1802010.5 g/粒3S23江西D18042610.5 g/粒3S24復方感冒靈顆粒河北A18033114 g/袋42S25廣西B18034714 g/袋42S26廣東C17123714 g/袋42S27復方感冒靈片廣西A11712010.32 g/片3.84S28江西B12017121710.32 g/片3.84S29江西B22018030120.32 g/片3.84S30廣西A21710030.32 g/片3.84S31廣西A31703010.32 g/片3.84S32廣東C1201612090.32 g/片3.84S33廣東C275017010.32 g/片3.84S34廣東C31707130.32 g/片3.84S35廣東C431707080.32 g/片3.84S36廣東C51705020.32 g/片3.84
表2 感冒靈制劑5種化學成分的線性關系考察
Table2Linear relationships of five chemical constituents in Ganmaoling preparations

化合物檢測波長/nm回歸方程r線性范圍/μg綠原酸327Y=2.615 33×105X-3.108×1030.999 50.086 0~0.516 0木犀草苷350Y=1.673 97×105X+1.889 2×1040.999 70.070 0~0.420 0異綠原酸B327Y=2.748 35×105X+3.104 9×1040.999 60.084 0~0.504 0異綠原酸C327Y=3.416 71×105X-2.632 0×1040.999 60.084 0~0.504 0蒙花苷334Y=2.418 77×105X-1.184 2×1040.999 60.128 0~0.768 0
2.4.2 精密度試驗 精密吸取“2.2”項下混合對照品溶液10 μL,連續進樣6次,分別計算5種成分峰面積的RSD值,考察儀器精密度,結果綠原酸、木犀草苷、異綠原酸B、異綠原酸C、蒙花苷峰面積的RSD值分別為1.34%、0.39%、0.45%、1.24%、0.47%,表明儀器精密度良好。
2.4.3 重復性試驗 取同一批次感冒靈制劑(感冒靈顆粒,批號170101),按“2.3”項下方法平行制備6份供試品溶液,按“2.1”項下色譜條件進樣測定,計算峰面積的RSD值。結果綠原酸、木犀草苷、異綠原酸B、異綠原酸C、蒙花苷峰面積的RSD分別為2.52%、1.93%、2.46%、1.61%、2.13%,表明方法重復性良好。
2.4.4 穩定性試驗 取同一批感冒靈樣品(感冒靈顆粒,批號170101),按“2.3”項下方法制備供試品溶液,按“2.1”項下色譜條件分別于0、2、4、6、8、10、12、24 h進樣分析,記錄色譜圖,計算峰面積的RSD值。結果綠原酸、木犀草苷、異綠原酸B、異綠原酸C、蒙花苷峰面積的RSD值分別為1.90%、2.41%、1.56%、2.23%、0.40%,表明供試品溶液在24 h內穩定。
2.4.5 加樣回收率試驗 取已知質量分數的感冒靈樣品粉末6份(感冒靈顆粒,批號170101),每份約1.5 g,置具塞錐形瓶中,分別精密加入綠原酸、木犀草苷、異綠原酸B、異綠原酸C、蒙花苷對照品0.290、0.321、0.556、0.528、0.584 mg,按“2.3”項下方法制備供試品溶液,按“2.1”項下色譜條件測定,分別計算各成分加樣回收率及RSD值。結果綠原酸、木犀草苷、異綠原酸B、異綠原酸C、蒙花苷的平均加樣回收率分別為99.72%、99.08%、109.32%、112.21%、98.66%,RSD值分別為2.42%、1.64%、1.95%、2.77%、3.02%,表明方法加樣回收率良好。
2.5 樣品測定
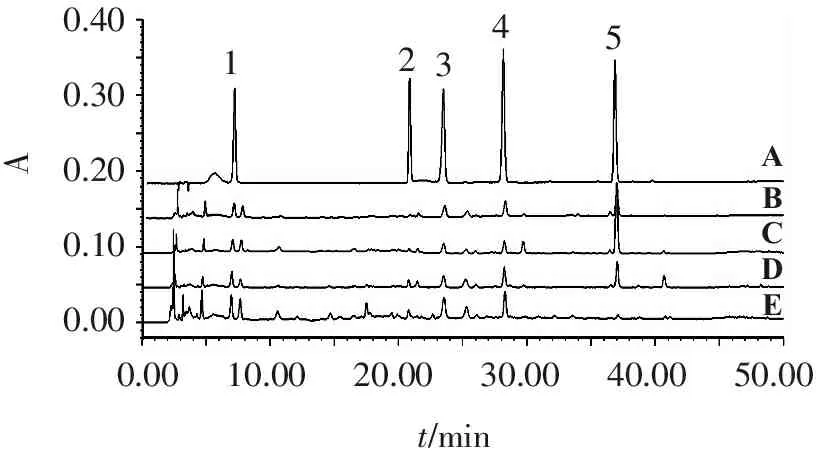
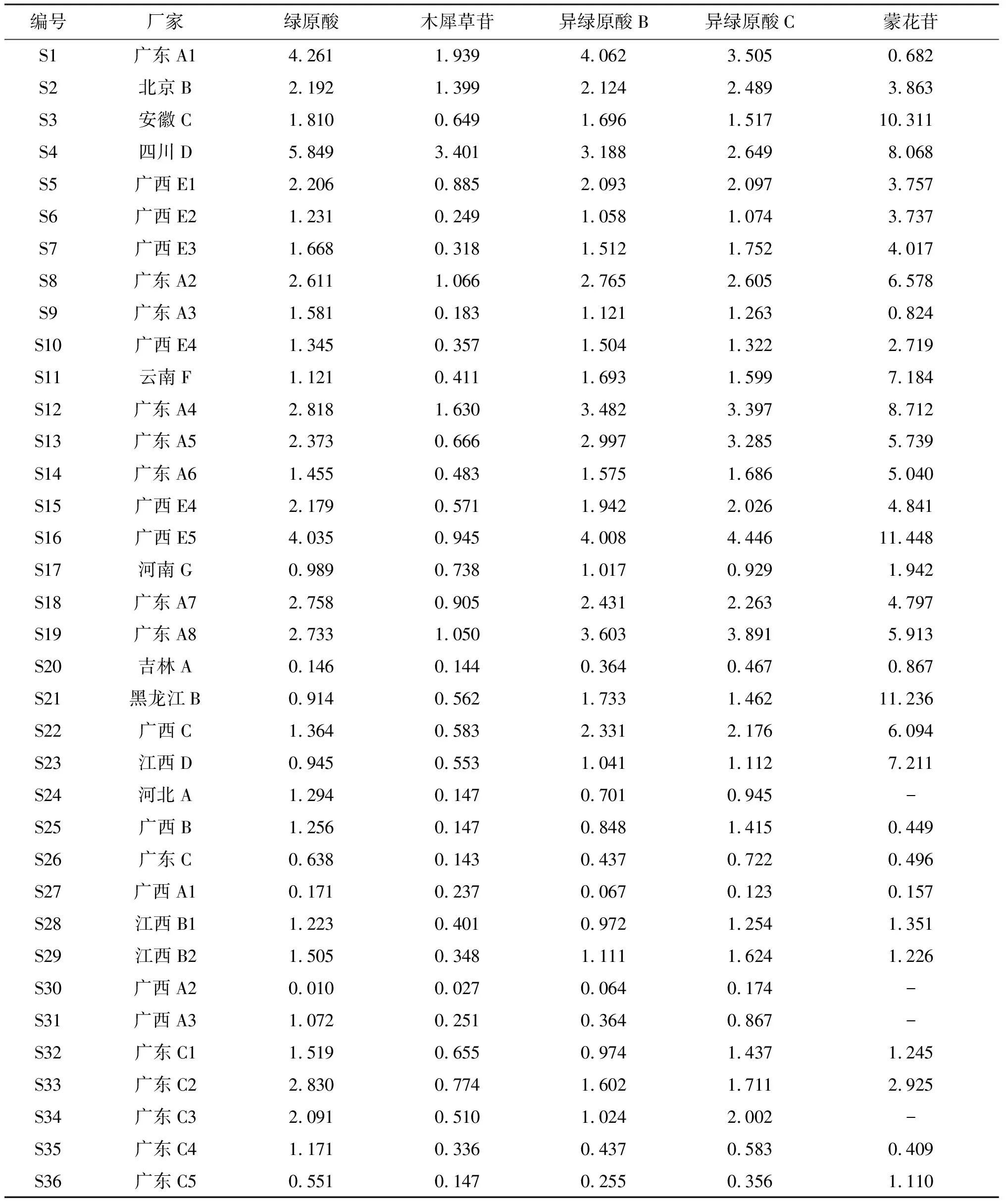
取36批感冒靈制劑樣品,按“2.3”項下方法制備供試品溶液,按“2.1”項下色譜條件測定。以外標法計算綠原酸、木犀草苷、異綠原酸B、異綠原酸C和蒙花苷5種化學成分的質量分數,得到感冒靈顆粒、感冒靈膠囊、復方感冒靈顆粒和復方感冒靈片的質量分數測定結果(以每日服用量計算,顆粒劑規格為10 g/袋,日服用量為30 g;膠囊劑規格為0.5 g/粒,日服用量為3 g;復方顆粒劑規格為14 g/袋,日服用量為42 g;片劑規格為0.32 g/片,日服用量為3.84 g)。見表3。供試品與混合對照品溶液不同波長下的色譜圖見圖1~3。
0.400.300.200.100.00AABC0.0010.0020.0030.0040.0050.00t/minDE12345
1.綠原酸; 2.木犀草苷; 3.異綠原酸B; 4.異綠原酸C; 5.蒙花苷。
A.混合對照品溶液; B.感冒靈顆粒溶液; C.感冒靈膠囊溶液; D.復方感冒靈片溶液; E.復方感冒靈顆粒溶液。
圖1感冒靈4種制劑的HPLC色譜疊加圖(327 nm)
Figure1HPLC chromatographic overlay charts of four Ganmaoling preparations (327 nm)
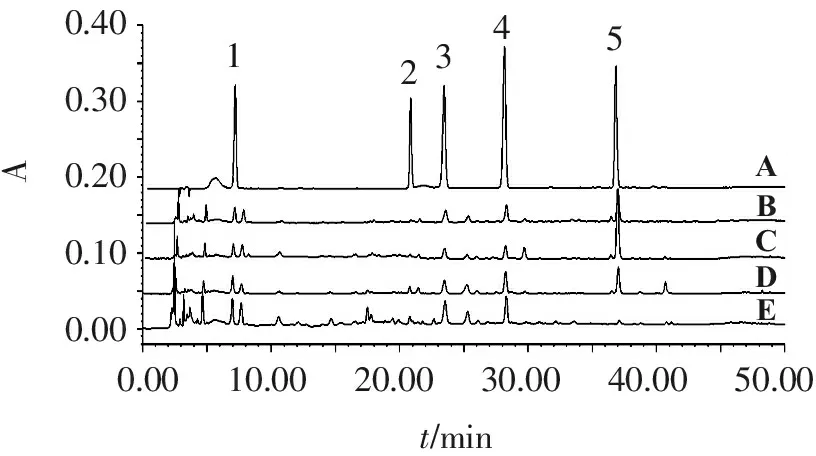
0.400.300.200.100.000.0010.0020.0030.0040.0050.00t/minABCDEA12345
1.綠原酸; 2.木犀草苷; 3.異綠原酸B; 4.異綠原酸C; 5.蒙花苷
A.混合對照品溶液; B.感冒靈顆粒溶液; C.感冒靈膠囊溶液; D.復方感冒靈片溶液; E.復方感冒靈顆粒溶液。
圖2感冒靈4種制劑的HPLC色譜疊加圖(334 nm)
Figure2HPLC chromatographic overlay charts of four Ganmaoling preparations (334 nm)

0.0010.0020.0030.0040.0050.00t/min0.400.300.200.100.00ABCDEA12345
1.綠原酸; 2.木犀草苷; 3.異綠原酸B; 4.異綠原酸C; 5.蒙花苷。
A.混合對照品溶液; B.感冒靈顆粒溶液; C.感冒靈膠囊溶液; D.復方感冒靈片溶液; E.復方感冒靈顆粒溶液。
圖3感冒靈4種制劑的HPLC色譜疊加圖(350 nm)
Figure3HPLC chromatographic overlay charts of four Ganmaoling preparations (350 nm)
表3 感冒靈制劑質量分數測定結果
Table3Determination results of mass fraction of Ganmaoling preparations 日服用量/mg
編號廠家綠原酸木犀草苷異綠原酸B異綠原酸C蒙花苷S1廣東A14.2611.9394.0623.5050.682S2北京B2.1921.3992.1242.4893.863S3安徽C1.8100.6491.6961.51710.311S4四川D5.8493.4013.1882.6498.068S5廣西E12.2060.8852.0932.0973.757S6廣西E21.2310.2491.0581.0743.737S7廣西E31.6680.3181.5121.7524.017S8廣東A22.6111.0662.7652.6056.578S9廣東A31.5810.1831.1211.2630.824S10廣西E41.3450.3571.5041.3222.719S11云南F1.1210.4111.6931.5997.184S12廣東A42.8181.6303.4823.3978.712S13廣東A52.3730.6662.9973.2855.739S14廣東A61.4550.4831.5751.6865.040S15廣西E42.1790.5711.9422.0264.841S16廣西E54.0350.9454.0084.44611.448S17河南G0.9890.7381.0170.9291.942S18廣東A72.7580.9052.4312.2634.797S19廣東A82.7331.0503.6033.8915.913S20吉林A0.146 0.144 0.364 0.467 0.867 S21黑龍江B0.914 0.562 1.733 1.462 11.236 S22廣西C1.364 0.583 2.331 2.176 6.094 S23江西D0.945 0.553 1.041 1.112 7.211 S24河北A1.294 0.147 0.701 0.945 - S25廣西B1.256 0.147 0.848 1.415 0.449 S26廣東C0.638 0.143 0.437 0.722 0.496 S27廣西A10.1710.2370.0670.1230.157S28江西B11.2230.4010.9721.2541.351S29江西B21.5050.3481.1111.6241.226S30廣西A20.0100.0270.0640.174-S31廣西A31.0720.2510.3640.867-S32廣東C11.5190.6550.9741.4371.245S33廣東C22.8300.7741.6021.7112.925S34廣東C32.0910.5101.0242.002-S35廣東C41.1710.3360.4370.5830.409S36廣東C50.5510.1470.2550.3561.110
2.6 基于TOPSIS法的不同批次間感冒靈制劑質量評價
TOPSIS法又稱為逼近理想解排序法、理想點法[9-10],是一種理想目標相似性的順序選優技術,已在醫藥領域有廣泛應用[11-12]。因這4種產品3類劑型的處方原料不相同,其處方劑量也不同,以制劑共有的中藥原料野菊花為例,顆粒劑和膠囊劑中所含野菊花的生藥量分別為2.46 g/袋和1.23 g/粒,片劑和顆粒劑(復方)所含野菊花的生藥量分別為0.781 g/片和3.1 g/袋,故藥材所含成分的質量分數實際有較大偏差。將其換算成每日服用量后,3種劑型所含野菊花的生藥用量則較為相近。
為體現制劑整體臨床療效,本試驗以36批樣品中每日服用量所含5種化學成分的質量分數為指標,首先建立規范化矩陣,對矩陣數據進行無量綱化處理得到規格化向量[13]。由于該制劑現行標準尚未涉及中藥各成分,且無明確的中藥藥效成分,多認為多組分協同起效,故定義此5種成分的權重值均等,進而可以得到加權后的規格化值。根據矩陣確立正理想解(最優值)和負理想解(最劣值),計算評價對象即各批樣品與正負理想解的歐氏距離,以樣品指標和正理想解的相對接近程度Ci值來評價各批樣品的質量優劣。Ci值越接近1,則認為質量越好[14]。見表4。
結果顯示,3類劑型由于涵蓋2種原料處方,且處方劑量也不同,綜合評價值Ci呈現出較大的差異。為排除處方不同的影響,進一步對同一原料處方進行分析評價,發現不同生產廠家之間整體差異減小,從顆粒劑和膠囊劑制劑產品來看,以S4批次樣品質量最好;從片劑和顆粒劑復方制劑來看,以S33批次樣品質量最好。此外,同一處方同一劑型內不同廠家生產的感冒靈產品質量良莠不齊,或少部分批次評價結果明顯較差,其原因可能與中藥材的來源、品質差異及制劑成型制備工藝的選擇等有關。
3 討論
3.1 色譜條件的建立
本實驗在流動相的選擇上,考察了甲醇-水、甲醇-0.1%(體積分數,下同)醋酸、甲醇-0.1%H3PO4、乙腈-水、乙腈-0.1%醋酸、乙腈-0.1%H3PO4等不同系統流動相對供試品溶液各成分分離的影響。通過對比色譜圖,以乙腈-H3PO4為流動相效果最好,而乙腈-0.1%H3PO4和乙腈-0.2%H3PO4無明顯差別,為了減少對色譜柱的損傷,選擇H3PO4體積分數低的洗脫系統。實驗中所采用的二極管陣列檢測器,可以同時檢測樣品在所有波長的吸收情況,通過對樣品進行全波長掃描,對各波長下的光譜圖基于光譜吸收、文獻比對和化合物極性等分析,得到蒙花苷的最大吸收波長為334 nm,木犀草苷的最大吸收波長為350 nm,綠原酸、異綠原酸B、異綠原酸C的最大吸收波長為327 nm。三處波長基線平穩、色譜圖峰形好、各成分均達到有效分離,故選擇327、334、350 nm作為檢測波長,以充分反映感冒靈制劑中藥組分信息和實際質量分數。

表4 感冒靈制劑的TOPSIS分析結果Table 4 TOPSIS Results of Ganmaoling preparations
Ci*為顆粒劑與膠囊劑兩者比較,Ci**為片劑與顆粒劑(復方)兩者比較。
3.2 供試品溶液制備條件的優化
對供試品的制備條件進行優化,通過比較不同超聲處理時間(10、20、30、40、60 min)對色譜峰結果的影響發現,隨著超聲時間的延長,各色譜峰峰面積有所增加,30 min以后峰面積差異縮小,故確定超聲時間為30 min。采用甲醇作為提取溶劑,色譜峰型較好,相比水或乙醇作溶劑提取雜質少。
3.3 數據分析
感冒靈制劑是常用的中西藥復方制劑,西藥成分的高質量分數與中藥成分的低質量分數是導致該制劑整體質量難控制的主要原因。本著多種成分兼顧、多個劑型統一標準、多種方法共同分析的整合理念,本試驗對不同批次感冒靈顆粒、感冒靈膠囊、復方感冒靈顆粒、復方感冒靈片4類制劑中的綠原酸、木犀草苷、異綠原酸B、異綠原酸C、蒙花苷進行了測定和化學計量分析。按照每天所服用的制劑中所含有的藥材量計算,通過對比發現,同一劑型內各批次所含5種化學成分質量分數的差異不大,均以蒙花苷和綠原酸2種成分質量分數居高;而不同劑型各成分質量分數差異較大。以復方感冒靈片劑和復方感冒靈顆粒劑為例,由于該復方制劑處方中同時含有野菊花和金銀花,所以片劑和復方顆粒劑所含綠原酸類成分質量分數理論上應大于顆粒劑和膠囊劑,但實際上并沒有。這可能是組方原料不同與每日服用量差異所導致,復方片劑雖原料生藥量大于顆粒劑,但其每日服用量卻小于顆粒劑。
因此,為了更科學地評價不同劑型,統一采用能體現藥品臨床療效和實際用途的每日服用量為指標進行TOPSIS分析。結果顯示,同一原料處方條件下,不同生產廠家或不同批次感冒靈產品質量良莠不齊。為更好地控制該制劑整體質量,必須保證中藥原料的均一性和道地性,確保臨床合理用藥。
本研究建立了感冒靈制劑整體質量評價模型,以多個指標對感冒靈產品進行了質量評價,符合中藥多組分協同的整體觀念。TOPSIS法用于多指標決策分析,將多個指標簡化成一個綜合評價值,提高了分析的科學準確性,實現了對感冒靈制劑整體質量的控制。

