芻議氣壓變化在化學實驗中的應用與防范
寧夏
氣壓是氣體壓強的簡稱。氣壓產生的原因是大量氣體分子對器壁持續的、無規則的撞擊,氣壓變化在科學研究和日常生活中都有廣泛的應用。在中學化學實驗中可應用氣壓變化保障實驗順利進行,但也要防范氣壓變化對實驗造成干擾。
一、引起氣壓變化的原因分析
引起氣壓變化的原因主要有溫度、容器的體積、氣體物質的量等。分析如下:
1.容器體積(V)和氣體物質的量(n)不變時,氣體壓強(p)與溫度(T)成正比;
2.溫度(T)和氣體物質的量(n)不變時,氣體壓強(p)與容器體積(V)成反比;
3.溫度(T)和容器體積(V)不變時,氣體壓強(p)與氣體物質的量(n)成正比。
二、應用氣壓變化保障實驗順利進行
1.應用在裝置氣密性的檢查中
裝置的氣密性良好是保障實驗順利進行的前提。檢查裝置氣密性的原理是通過改變溫度或氣體的體積從而改變壓強,再通過氣泡的產生、水柱的形成、液面的升降等現象來判斷裝置的氣密性是否良好。
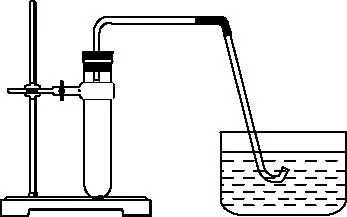
圖1
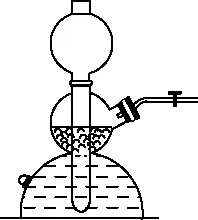
圖2
圖1裝置氣密性檢查的原理是容器體積(V)和氣體物質的量(n)都不變時,氣體壓強(p)與溫度(T)成正比。方法是將導管伸入水中,用手捂熱(或用酒精燈微熱)試管,如果導氣管末端產生氣泡,松手后(或撤去酒精燈)導管末端有一段水柱形成,則證明裝置氣密性良好。
圖2裝置氣密性檢查的原理是溫度(T)和氣體物質的量(n)都不變時,氣體壓強(p)與體積(V)成反比。方法是關閉導氣管,向球形漏斗中加水,使漏斗中的液面高于容器內的液面,一段時間后,如果液面差不變,則證明裝置氣密性良好。
其他裝置氣密性檢查的原理和方法參見上述論述。
2.應用在部分物質的順利制備中
利用密閉體系中產生的氣體會形成較大壓強的原理可實現部分實驗的順利進行。
制備一定量的H2時,可用圖3裝置。將Zn粒放到有孔塑料板上,長頸漏斗中加入稀H2SO4,稀H2SO4與Zn粒接觸產生氫氣。通過關閉彈簧夾(氣體增多,氣壓增大,長頸漏斗中液面上升,液體與固體分離,反應停止)或打開彈簧夾(氣體減少,氣壓減小,長頸漏斗中液面下降,液體與固體接觸,反應發生)控制反應的停止和發生。
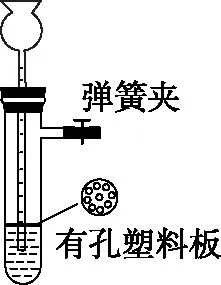
圖3
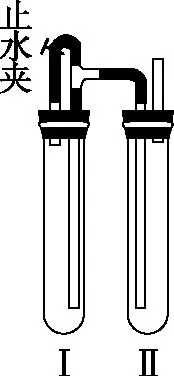
圖4
制備一定量Fe(OH)2白色沉淀時,可用圖4裝置。在試管Ⅰ中加入鐵屑和少量稀H2SO4,試管Ⅱ里加入大量NaOH溶液,當試管Ⅱ中持續產生氣泡時,關閉止水夾,由于Ⅰ中氣體量增加,氣壓增大,試管Ⅰ中溶液就會進入試管Ⅱ中,使試管Ⅱ中產生大量Fe(OH)2白色沉淀。并且由于試管Ⅱ中的O2已經被生成的H2排干凈,所以生成的Fe(OH)2白色沉淀能保持較長時間,不被氧化。
3.應用在理解物質性質或反應原理中
(1)用來理解噴泉實驗原理
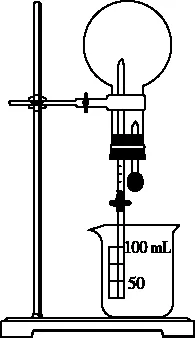
圖5
噴泉實驗可以說明氣體的溶解性或與其他試劑的反應情況。中學化學中常見的噴泉實驗裝置如圖5所示,燒瓶內氣體溶解于燒杯中的試劑或與燒杯中的試劑發生反應,導致燒瓶內氣體分子數目急劇減少,燒瓶內氣壓急劇降低,外界大氣壓將燒杯內的水通過導管壓至燒瓶內形成噴泉。
為保證實驗的順利發生所采取的措施主要有兩種:一是打開止水夾,在燒瓶上敷熱毛巾,使燒瓶內氣壓增大,氣體分子與燒杯中的試劑接觸進而溶解或發生反應,使燒瓶內壓強減小,短時間形成壓強差,形成噴泉;二是打開止水夾,擠壓膠頭滴管,使燒瓶內氣體與燒杯中的試劑接觸進而溶解或發生反應,燒瓶內氣體溶解或與試劑發生反應,導致燒瓶內氣體的量瞬間減少,短時間內產生壓強差,形成噴泉。
(2)用來理解鋼鐵腐蝕原理
因環境不同,鋼鐵發生的腐蝕主要有吸氧腐蝕和析氫腐蝕兩種類型。
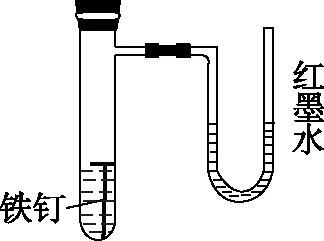
圖6
如圖6所示,鐵釘在試管中發生的腐蝕類型可以根據右側U形管內左右兩邊的液面高低來判斷。發生析氫腐蝕時,試管內產生氫氣導致氣壓增大,U形管內紅墨水液面左低右高;發生吸氧腐蝕時,試管內消耗氧氣導致氣壓減小,U形管內紅墨水液面左高右低。
上述幾方面主要是通過人為造成壓強差來確保后續實驗的順利進行或利用實驗過程中自然形成的壓強差來理解相關反應原理。但也有很多實驗需要防范因氣壓變化對實驗造成的干擾和影響。
三、防范氣壓變化對實驗造成干擾
1.防范氣壓變化對準確量取氣體體積的影響
氣體的體積隨溫度和壓強的變化而發生變化。一定量的氣體的體積是指氣體的溫度、產生的壓強分別與室溫和大氣壓一致情況下的體積。
圖7為量氣裝置之一。某化學課外活動小組利用如圖7所示的裝置將NO2和O2的混合氣通入水中反應,并測定反應后混合氣的體積。在讀取量氣管體積時應注意以下兩點:一是冷卻至室溫(溫度影響氣體的體積);二是上下移動量氣管,使前后兩次讀數時均保持量氣管內液面和球形容器內液面相平(當量器管內液面高于球形容器內液面時,因球形容器內氣體壓強高于外界大氣壓,所收集氣體的體積偏小;當量器管內液面低于球形容器內液面時,因球形容器內氣體壓強低于外界大氣壓,所收集氣體的體積偏大)。
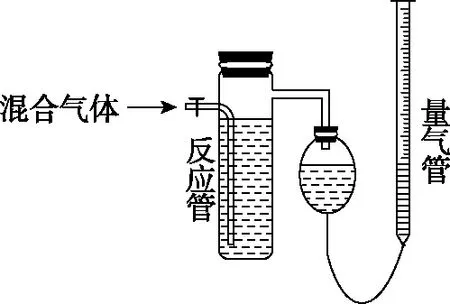
圖7
2.防止在實驗過程中因氣壓變化而發生意外
(1)防止氣壓變化致使液體發生倒吸
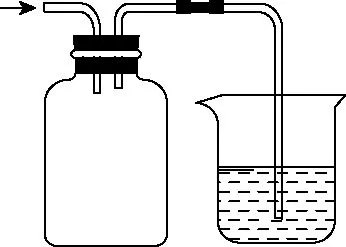
圖8
如圖8,當氣體被燒杯內的溶液吸收或反應后,會瞬間造成反應容器的壓強低于外界大氣壓,空的試劑瓶就可以防止燒杯內的液體進入氣體發生裝置。
如圖9,CO還原CuO的實驗結束后是先撤去酒精燈還是先停止通CO涉及氣壓變化問題。如果先停止通CO,后撤去酒精燈,由于撤去酒精燈后溫度降低,直玻璃管內就會產生低壓,瓶內液體就會倒吸至直玻璃管內。所以應該是先撤去酒精燈,待直玻璃管冷卻至室溫后,再停止通入CO。
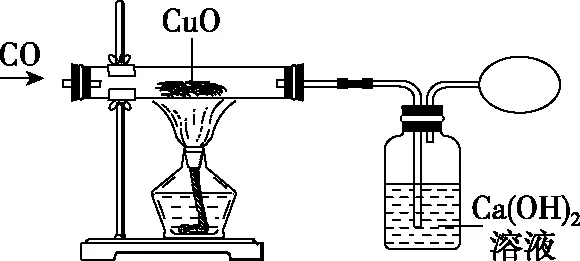
圖9
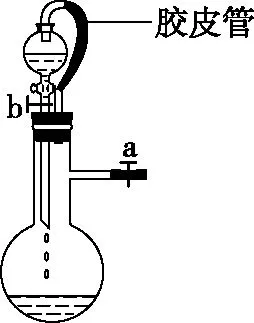
圖10
(2)防止氣壓變化導致液體不能順利流下
如圖10,當燒瓶內產生氣體時,若沒有膠皮管,燒瓶內的氣壓增大會導致漏斗內液體較難順利流下。膠皮管的作用就是平衡壓強,使漏斗內的液體順利流下。
(3)防止氣壓變化導致塞子脫落
如圖11,當錐形瓶內氣壓過大時有可能導致錐形瓶橡膠管脫落。錐形瓶內插入導管并加入一定量的水就可以防止錐形瓶內氣壓過大導致橡膠塞脫落。
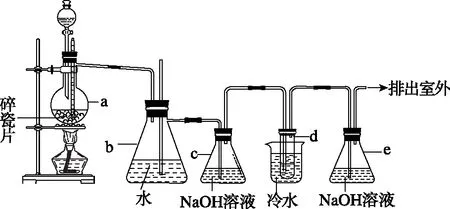
圖11
四、與氣壓變化有關的高考試題賞析
整理近幾年高考實驗試題,與壓強差有關的問題設置主要是利用壓強差保障后續實驗順利進行和防止壓強差對實驗造成干擾兩類。
1.利用壓強差保障后續實驗順利進行
【例1】(2018·全國卷Ⅰ·26節選)醋酸亞鉻[(CH3COO)2Cr·2H2O]為磚紅色晶體,難溶于冷水,易溶于酸,在氣體分析中用作氧氣吸收劑。一般制備方法是先在封閉體系中利用金屬鋅作還原劑,將三價鉻還原為二價鉻;二價鉻再與醋酸鈉溶液作用即可制得醋酸亞鉻。實驗裝置如圖所示。回答下列問題:

(3)打開K3,關閉K1和K2。c中亮藍色溶液流入d,其原因是___________________>。
【答案】c中產生H2使壓強大于大氣壓
【解析】二價鉻與醋酸鈉溶液反應的前提是c中的溶液能夠進入d中與醋酸鈉溶液混合。當c中的壓強大于d中的壓強就可以實現c中的溶液流入d中發生反應。即當打開K3,關閉K1和K2時,c中鋅粒與鹽酸反應產生的氫氣排放不出去,產生了較大的壓強,將c中生成的亮藍色溶液壓入d中。
【例2】(2017·全國卷Ⅰ·26節選)凱氏定氮法是測定蛋白質中氮含量的經典方法,其原理是用濃硫酸在催化劑存在下將樣品中有機氮轉化成銨鹽,利用如圖所示裝置處理銨鹽,然后通過滴定測量。


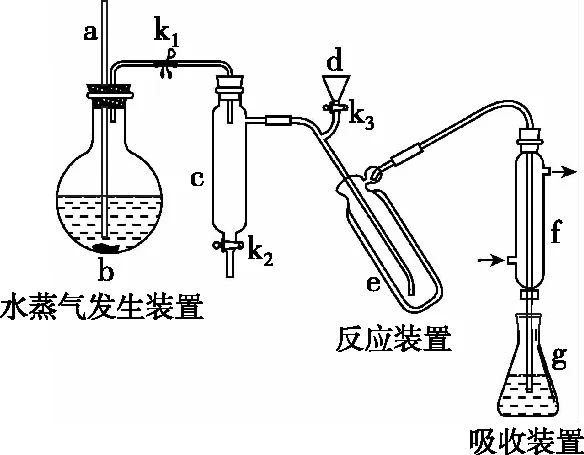
回答下列問題:
(3)清洗儀器:g中加蒸餾水;打開k1,關閉k2、k3,加熱b,蒸氣充滿管路;停止加熱,關閉k1,g中蒸餾水倒吸進入c,原因是____________________;打開k2放掉水。重復操作2~3次。
【答案】(3)c中溫度下降,管路中形成負壓
【解析】儀器的干凈程度是后續實驗順利進行的前提。當c裝置中的壓強低于g裝置中壓強時,錐形瓶中的液體可以倒流入c中進而起到清洗儀器的作用。即由于停止加熱,c、e及其所連接的管道內水蒸氣冷凝為水后,使氣壓小于外界大氣壓,在大氣壓的作用下,錐形瓶內的蒸餾水流入c中。
2.防止壓強差對后續的實驗造成干擾
【例3】(2019·全國卷Ⅰ·27節選)硫酸鐵銨[NH4Fe(SO4)2·xH2O]是一種重要鐵鹽。為充分利用資源,變廢為寶,在實驗室中探究采用廢鐵屑來制備硫酸鐵銨,具體流程如下(略):
回答下列問題:
(2)鐵屑中含有少量硫化物,反應產生的氣體需要凈化處理,合適的裝置為________(填標號)。
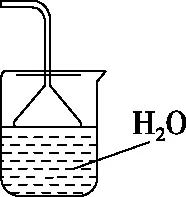
A

B
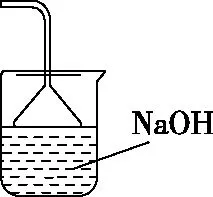
C
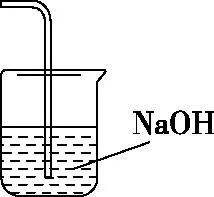
D
【答案】C
【解析】由于鐵屑中含有少量硫化物,所以產生的氣體為H2S。H2S氣體在水中的溶解性較差,可以利用NaOH溶液來吸收H2S氣體。但當吸收速率過快時,會導致整個導管內的壓強降低進而發生溶液倒吸,干擾實驗順利進行。采用倒扣的漏斗進行吸收,可以避免發生倒吸。
【例4】(2016·江蘇卷·21B節選)焦亞硫酸鈉(Na2S2O5)是常用的抗氧化劑,在空氣中、受熱時均易分解。實驗室制備少量Na2S2O5的方法:在不斷攪拌下,控制反應溫度在40℃左右,向Na2CO3過飽和溶液中通入SO2,實驗裝置如下圖所示。
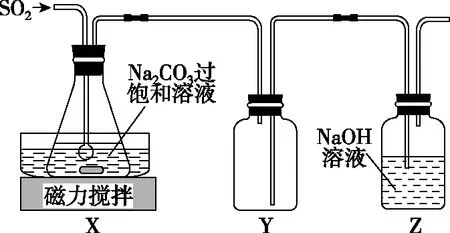

(2)裝置Y的作用是_________________。
【答案】(2)防止倒吸
【解析】由于SO2是大氣污染物,最后盛有NaOH溶液的Z裝置是用來吸收SO2氣體的。SO2很容易和NaOH溶液發生反應,導致裝置X中壓強減小,易發生溶液的倒吸,因此裝置Y的作用是防止發生倒吸。
實驗探究是學生獲取化學知識的重要手段,是提高學生學科核心素養的重要手段。梳理氣壓變化在化學實驗中的應用與防范,呈現了基于原理分析的理性思考過程。從知識、原理到應用,只有教會學生怎樣思考問題、分析問題,才是真正教會了學生如何學習。

