火腿腸中亞硝酸鹽的測定
趙俊英
(隴東學院 化學化工學院,甘肅 慶陽 745000)
食品中亞硝酸鹽含量超標是倍受關注的食品安全問題之一[1]。國內外檢測食品中亞硝酸鹽的方法很多,主要有分光光度法[2]、氣相分子吸收光譜法[3]、干式化學分析法[4]、電化學法[5]等。氣相分子吸收光譜法更適用于液態食品中亞硝酸鹽含量的測定,干式化學分析法更適用于初步的檢測,電化學法雖然測定時間短,操作簡單但適用的范圍有限,而分光光度法結果準確,操作簡便,因此本文采用分光光度法對生活中常見的火腿腸中的亞硝酸鹽含量進行了測定。
1 實驗部分
1.1 儀器與試劑
721分光光度計(上海第三分析儀器廠),電子天平(北京賽多利斯天平有限公司),酸度計(上海儀電科學儀器股份有限公司),電爐,容量瓶,移液管等。
亞鐵氰化鉀(AR),乙酸鋅(AR),硼砂(AR),鹽酸(AR),氫氧化鈉(AR),對氨基苯磺酸(AR),亞硝酸鈉(AR),鹽酸萘乙二胺(AR)。
1.2 樣品處理
取適量的火腿腸,用小刀切碎,放入研缽中碾碎,準確稱取5.0克經碾碎、混勻的樣品,置于50mL燒杯中。加12.5mL硼砂飽和溶液,攪拌均勻,以70℃左右的水將樣品洗入500mL容量瓶中,置沸水浴中加熱15min,冷卻至室溫。邊轉邊加入5mL 106g·L-1亞鐵氰化鉀溶液,最后加入5mL 220g·L-1乙酸鋅溶液。
2 實驗數據分析
2.1 波長的確定
室溫下于50mL容量瓶中,加入1mL 5μg·mL-1標準亞硝酸鹽和2mL 4g·L-1對氨基苯磺酸,待其重偶化3min后加1mL 2g·L-1鹽酸萘乙二胺,定容,靜置25min,待反應完全后,在520~580nm范圍內,以10nm為梯度,測量其吸光度,數據見表1。以波長為橫坐標,吸光度為縱坐標,作圖,見圖1。由圖1可知,吸光度在520~540nm波長范圍內隨波長增大而增大,在540~580nm波長范圍內隨波長減小而減小,實驗得出在波長在540nm處吸光度最大,因此選擇540nm作為測量波長。

表1 波長對吸光度的影響

圖1 波長對吸光度的影響
2.2 pH值的確定
在室溫下于50mL容量瓶中,加入1mL標準亞硝酸鹽和2mL對氨基苯磺酸,待其重偶化3min后加1mL鹽酸萘乙二胺,待反應完全后,調節pH值,測定不同pH值下的吸光度,數據見表2。以pH值為橫坐標,吸光度為縱坐標,作圖,見圖2。由圖2可知,吸光度在pH值為0.5~1.0時逐漸增大,在1.0~1.4時逐漸減小,因此選擇控制pH值為1.0。

圖2 pH值對吸光度的影響

表2 pH值對吸光度的影響
2.3 鹽酸萘乙二胺用量的確定

表3 鹽酸萘乙二胺用量對吸光度的影響
在室溫下于7個50mL容量瓶中,分別加入1mL標準亞硝酸鹽和2mL對氨基苯磺酸,待其重偶化3min后,相應加入0.5,1.0,1.5,2.0,2.5,3.0,3.5mL鹽酸萘乙二胺,測量其吸光度,數據見表3。根據表3的數據,以鹽酸萘乙二胺的量為橫坐標,吸光度為縱坐標,作圖,見圖3。由圖3可知,鹽酸萘乙二胺用量在0.5~1.0mL時逐漸增大,在1~1.5mL時減小并趨于平衡,因此本文選擇鹽酸萘乙二胺加入量為1mL。
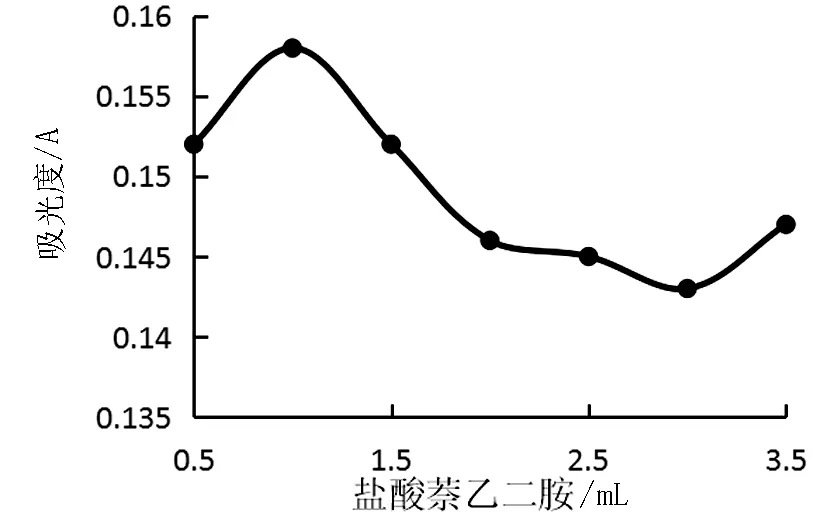
圖3
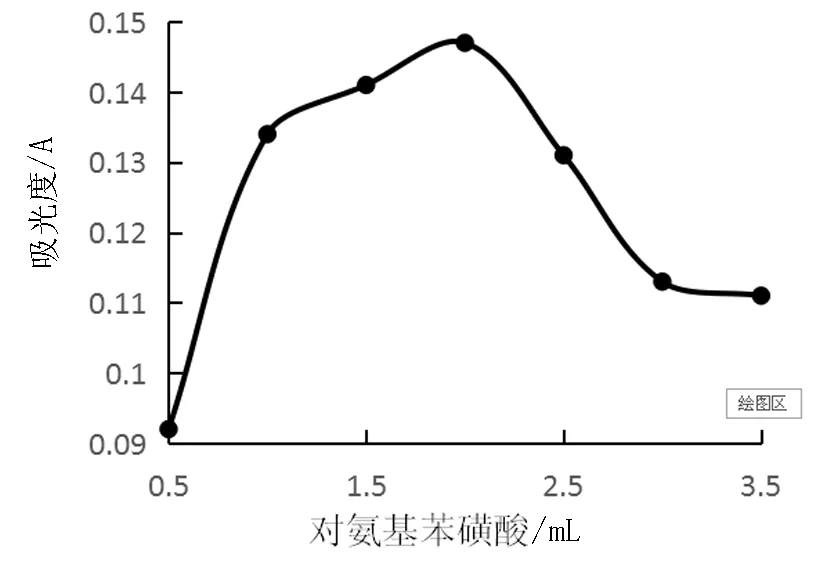
圖4 對氨基苯磺酸用量對吸光度影響
2.4 對氨基苯磺酸用量對吸光度影響
在室溫下于7個50mL容量瓶中,分別加入1mL標準亞硝酸鹽,相對應的加入0.5,1.0,1.5,2.0,2.5,3.0,3.5對氨基苯磺酸,待其重偶化3min后加1mL鹽酸萘乙二胺,定容,靜置25min,測量其吸光度,數據見表4。以對氨基苯磺酸的量為橫坐標,吸光度為縱坐標,作圖,見圖4。由圖4可知對氨基苯磺酸在小于1.0mL大于2.0mL時吸光度較低,在1.0~2.0mL時吸光度較好因此本文取2mL對氨基苯磺酸進行重偶化。

表4 對氨基苯磺酸用量對吸光度的影響
2.5 重偶化時間的確定

表5 重偶化對吸光度的影響
在室溫下在6個50mL容量瓶中,分別加入1mL標準亞硝酸鹽和2mL對氨基苯磺酸,待其重偶化后加1mL鹽酸萘乙二胺,分別測量重偶化時間在2,3,4,5,6,7min時的吸光度,數據見表5。以重偶化時間為橫坐標,吸光度為縱坐標,作圖,見圖5。由圖5可知重偶化時間在3~4min吸光度最大,在大于5min后吸光度降低明顯,本文中控制重偶化時間為3~4min。

圖5 重偶化時間對吸光度影響
2.6 顯色時間的確定
在室溫下在50mL容量瓶中,加入1mL標準亞硝酸鹽和2mL對氨基苯磺酸,待其重偶化3min后加1mL鹽酸萘乙二胺,分別測量顯色時間在10,15,20,25,30,35,40min時的吸光度,數據見表6。以顯色時間為橫坐標,吸光度為縱坐標,作圖,見圖6。由圖6可知,隨著時間的延長,吸光度在增加,當顯色時間在20 min后逐漸穩定,并且在25min左右吸光度最大,本文中控制顯色時間為25min左右。

圖6 顯色時間對吸光度影響
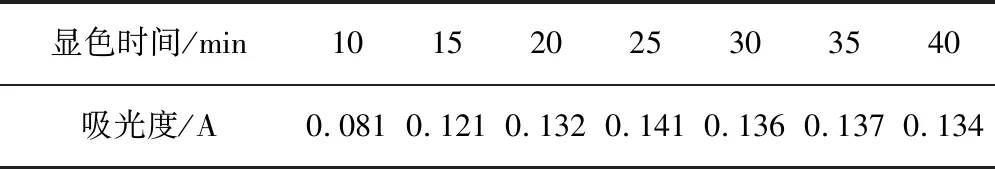
表6 顯色時間對吸光度的影響
2.7 繪制標準曲線
分別吸取0.00,0.20,0.40,0.60,0.80,1.00,1.50,2.00,2.50mL標準亞硝酸鈉,分別加入50mL的容量瓶中。再各加2mL對氨基苯磺酸,混勻,靜置4min后各加入1mL鹽酸萘乙二胺,以空白試劑調節零點,測定吸光度A,數據見表7。以亞硝酸鈉的量為橫坐標,吸光度為縱坐標,作圖,見圖7。可知,亞硝酸鹽含量與吸光度之間的線性關系良好,其線性回歸方程為y=0.0212x+0.0022,相關系數R2=0.9984。

圖7 亞硝酸鈉標準曲線

表7 亞硝酸鈉標準曲線
2.8 樣品測定
取40.0mL的樣液放置于50mL的容量瓶中。按標準曲線測定方法依次加入其它試劑。加水稀釋至刻度,混勻,靜置25min,以蒸餾水調節零點,于波長540nm處測吸光度A,對照標準曲線,計算出樣品中亞硝酸鹽的含量,數據見表8。由表8可知,雙匯王中王、清真雞肉香腸和金雙匯特級火腿腸的亞硝酸鹽含量分別為7.548,6.338,9.273(mg·kg-1),均小于30mg·kg-1,符合國家標準,可放心食用。

表8 不同品牌火腿腸中亞硝酸鹽的含量
2.9 加標回收率實驗
采用三個已檢測的樣品液,分別加入1,2,3μg亞硝酸鈉,測量其吸光度,利用標準曲線方程得出其實際檢測值,根據回收率公式計算回收率。見表9。由表9可知回收率分別為96.96%,93.73%和93.25%,說明該方法回收率效果較好。

表9 回收率實驗結果
3 結論
本文采用分光光度法對生活中常見的三種不同品牌的火腿腸進行了測定,條件為540nm波長,pH值=1,重偶化時間為4min,鹽酸萘乙二胺為1mL,對氨基苯磺酸為2mL,顯色時間為25min。標準曲線為y=0.0213x+0.0022,R2=0.9984。測出雙匯王中王、清真雞肉香腸和金雙匯特級火腿腸的亞硝酸鹽含量分別為7.548,6.338,9.273mg·kg-1,均未超過國家規定的標準30mg·kg-1。

