基于MRI活性骨髓勾畫的非共面調強放療在宮頸癌骨髓保護方面的劑量學優勢
李萍,張書旭,陽露,曾慶星,林曉輝,張國前
1.廣州醫科大學研究生院,廣東廣州510182;2.廣州醫科大學附屬腫瘤醫院放療中心,廣東廣州510095
前言
宮頸癌是女性最常見的惡性腫瘤之一,對于中晚期宮頸癌(ⅡA 期以上)常采用同步放化療的治療模式。既往很多學者研究證實,盆腔腫瘤患者接受同步放化療后,其骨髓抑制的程度與骨髓的照射體積密切相關[1-4]。如何有效減少骨髓照射劑量體積,進而減少放療過程中骨髓抑制的發生率或嚴重程度,成為當前宮頸癌放療的研究熱點之一。人體骨骼中的骨髓分為紅骨髓和黃骨髓兩部分,紅骨髓含有大量造血細胞,具有活躍的造血功能,即造血活性骨髓;而黃骨髓由不具備造血功能的脂肪細胞組成[5]。由于活性骨髓在骨盆腔內分布不均勻、不對稱,且在普通定位CT 圖像上難以辨認,若對整個骨盆進行限量,會大大增加IMRT 計劃的難度。有效區分骨髓腔內造血活性骨髓對于提高放療療效有重大意義。而在T1WI 脂肪抑制序列中,骨髓腔內脂肪含量越高的部位信號強度越低,即無效骨髓呈低信號,造血活性骨髓呈高信號[6],因此,MRI 技術可以有效區分骨髓腔活性骨髓和非活性骨髓。本研究通過利用MRI T1WI 抑脂序列圖像確定盆腔活性骨髓,分別制定常規9 野共面IMRT 計劃和9 野非共面IMRT(NC-IMRT)計劃(其中NC-IMRT 計劃包括7 個共面野和2 個非共面野),比較2 種計劃方案在宮頸癌盆腔骨髓保護方面的劑量學差異,以期為宮頸癌放療骨髓保護提供更好的參考依據。
1 資料與方法
1.1 研究對象
選擇20 例宮頸癌根治術前患者,年齡37~54 歲,平均年齡45.4 歲。其中IIB 期4 例、IIIB 期7 例、IVA期9例。入組條件:患者血常規檢查正常,血紅蛋白≥120 g/L,白細胞≥4.0×109/L,中性粒細胞≥2.0×109/L,血小板≥100×109/L;未曾接受過化療和盆腔放療。
1.2 MRI、CT模擬定位及圖像融合
放療前1周,患者采用仰臥位,雙手抱肘置于額頭,采用飛利浦Achieva l.5T MR 行盆腔增強MRI T1WI 抑脂序列掃描,TR 3 000 ms,TE 120 ms,矩陣288×256,層厚4 mm;隔天采用GE Lightspeed 16 排螺旋CT行盆腔增強掃描,掃描參數:層厚5 mm,層間距5 mm,矩陣512×512,120 kV,220 mA。掃描范圍從第一腰椎上緣到坐骨下結界5 cm。MRI、CT 掃描前利用膀胱容量測量儀檢測患者尿量需達到(300±50)mL。將同一患者的MRI、CT 圖像導入放療計劃系統(Pinnacle V9.10)進行圖像融合。
1.3 有效活性骨髓的勾畫
在MRI T1WI 抑脂序列圖像中富含脂肪的區域表現為低信號,骨盆區域和雙側股骨頭上端內信號高于脂肪低信號的區域即為活性骨髓。由一位臨床經驗豐富醫生,在MRI T1WI 抑脂序列圖像中勾畫出骨盆(包括腰骶骨、髂骨、坐骨、恥骨)和雙側股骨頭上端的有效活性骨髓(圖1a)。勾畫完成后與定位CT圖像(圖1b)進行融合,獲得定位CT 圖像上的有效活性骨髓分布。
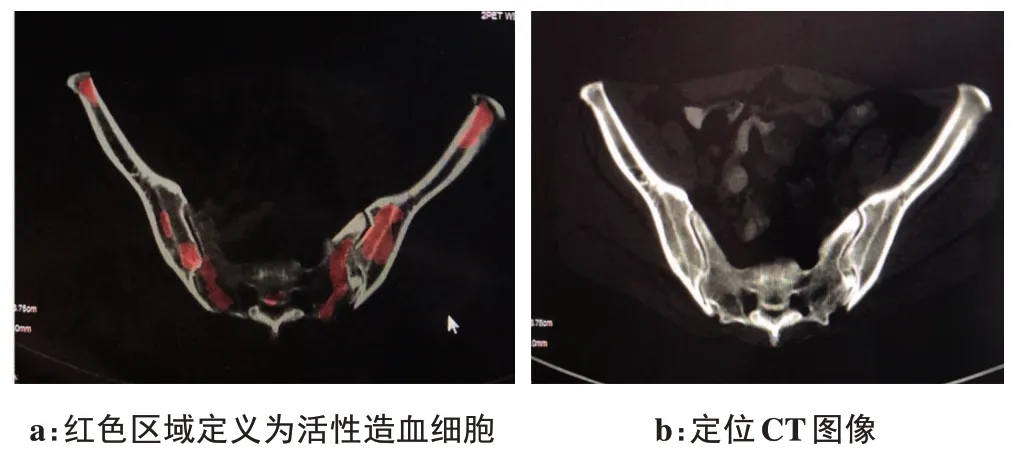
圖1 MRI、CT圖像上有效活性骨髓勾畫示例Fig.1 Examples of active bone marrow segmentations in CT and MRI images
1.4 IMRT與NC-IMRT計劃設計與評估
由同一臨床醫生利用放療計劃系統(Pinnacle V9.10)勾畫治療靶區和危及器官:宮頸癌患者腫瘤靶區(Gross Target Volume,GTV);轉移的淋巴結靶區(Lymph Node Gross Tumor Volume,GTVnd);髂總、髂外、髂內、閉孔、骶前淋巴引流區及宮旁、陰道上1/3及殘端靶區(Clinical Target Volume,CTV);計劃靶區(Planning Target Volume,PTV)為CTV頭腳方向外放1.0 cm,前后左右外放0.5 cm。處方劑量為60 Gy/27次,2.2 Gy/次,5次/周。并給予單獨限量:骨盆有效活性骨髓(Active Bone Marrow,BMACT)V30≤30%(V30為接受30 Gy劑量照射的體積百分比)。其它危及器官限量為:膀胱V40≤50%,直腸V40≤50%,小腸D40≤40 Gy(D40為40%靶區體積接受的照射劑量),雙側股骨頭V30≤30%。
然后由物理師進行IMRT計劃設計:采用6MVX射線,布野方式為9野,照射野的入射角度分別為0°、40°、80°、120°、160°、200°、240°、280°、320°。NC-IMRT 計劃在IMRT計劃的基礎上設計:保證其它照射野角度不變,將IMRT計劃中80°和280°照射野分別轉床90°和270°,為避免在治療過程中機架與患者發生擠壓碰撞,治療床角度改變后機架角度活動范圍也一定程度受限,通過測試,當治療床角度為90°和270°時,機架頭側和腳側的最大活動角度分別為35°和55°。NC-IMRT計劃機架角度根據患者體型個體差異選擇最大活動角度。兩組計劃中靶區GTVnd和CTV的臨床處方劑量分別為60 Gy和50.4 Gy,要求95%的靶區接受100%的處方劑量,均應用相同計劃系統、限制條件和歸一條件。
對于GTVnd和CTV,比較Dmean、Dmax、Dmin、均勻性指數(HI)、適形度指數(CI)。其中HI=D5/D95,D95和D5分別代表95%和5%的靶區體積所得到的絕對劑量比值,HI值越接近1,表明靶區內劑量分布越均勻;CI 為處方劑量包裹的體積與靶區體積的比值,CI 值越接近1,表明適形度越好。比較BMACT低劑量輻射區(V10和V20)和高劑量輻射區(V30、V40和V50)。其它危及器官比較:直腸和小腸Dmax、Dmean、V30、V45,膀胱Dmax、Dmean、V35、V40、V50,兩側股骨頭Dmax、Dmean、V10、V20、V30、V40。此外,還比較了兩種照射方式的機器跳數。
1.5 統計學分析
數據資料以均值±標準差表示,采用SPSS 16.0軟件對IMRT 與NC-IMRT 計劃的劑量學參數進行配對t檢驗分析,P<0.05為差異具有統計學意義。
2 結果
2.1 靶區的劑量學比較
20例患者IMRT和NC-IMRT計劃中,GTVnd的Dmean分別為(6 284.0±9.3)和(6 375.2±10.4)Gy,Dmax分別為(6 294.4±98.3)和(6 386.0±87.5)Gy。CTV 的Dmean分別為(5 360.1±159.0)和(5 400.2±234.7)Gy,Dmax分別為(6 367.5±231.5)和(6 378.7±147.5)Gy,差異均無統計學意義(P>0.05)。對于靶區GTVnd的CI和HI,兩組計劃無明顯差異(P>0.05);PTV靶區CI在NC-IMRT計劃中稍優于MRT計劃,而HI則不及IMRT組(表1)。
表1 IMRT和NC-IMRT計劃的靶區劑量學比較(±s)Tab.1 Dosimetric comparison of target areas between intensitymodulated radiotherapy(IMRT)and non-coplanar IMRT(NC-IMRT)plans(Mean±SD)

表1 IMRT和NC-IMRT計劃的靶區劑量學比較(±s)Tab.1 Dosimetric comparison of target areas between intensitymodulated radiotherapy(IMRT)and non-coplanar IMRT(NC-IMRT)plans(Mean±SD)
?
2.2 有效活性骨髓劑量學比較
對20 例宮頸癌根治性放療患者定位CT 圖像進行骨盆外輪廓勾畫,所得骨盆體積Vpelvix為(600.32±6.88)cm3,同時利用患者T1WI抑制序列MRI 圖像再次進行有效活性骨髓的勾畫,所得體積為(219.38±9.73)cm3。在IMRT 計劃和NC-IMRT 計劃兩種治療方式下,BMACT的受照劑量Dmean分別為(3 679.6±265.0)和(3 466.4±255.1)Gy。相對于IMRT計劃,NC-IMRT 計劃能有效降低骨髓V10、V20、V40、V50,差異有統計學意義(P<0.05),見表2。
表2 IMRT和NC-IMRT計劃骨髓劑量學比較(%,±s)Tab.2 Dosimetric comparison of pelvic bone marrow between IMRT and NC-IMRT plans(%,Mean±SD)

表2 IMRT和NC-IMRT計劃骨髓劑量學比較(%,±s)Tab.2 Dosimetric comparison of pelvic bone marrow between IMRT and NC-IMRT plans(%,Mean±SD)
骨盆骨髓低劑量輻射區骨盆骨髓高劑量輻射區計劃類型V10 V20 V30 V40 V50 IMRT NC-IMRT t值P值99.26±1.02 89.90±2.40 6.776 0.000 93.80±4.21 76.37±3.52 3.272 0.006 77.90±7.55 69.42±9.37 0.486 0.643 46.84±12.06 35.49±10.65 5.983 0.011 5.02±2.88 2.01±1.14 4.081 0.003
2.3 雙側股骨頭劑量學比較
圖2選取了其中1 例患者雙側股骨頭的DVH 圖進行比較,NC-IMRT 計劃有效降低了雙側股骨頭的受照劑量。20 例患者中,IMRT 和NC-IMRT 計劃左側股骨頭平均Dmean分別為(2 999.3±119.9)和(2 596.4±235.5)Gy,其中Dmean的最大差異為19.8%,差異有統計學意義(P<0.05);右側股骨頭IMRT 和NC-IMRT計劃Dmean分別為(2 912.4±146.5)和(2 549.8±226.2)Gy,其中Dmean的最大差異為35.0%,差異有統計學意義(P<0.05)。雙側股骨 頭 的V10、V20、V30、V40如表3所示,結果顯示NC-IMRT 計劃在保護左右側股骨頭具有明顯優勢。
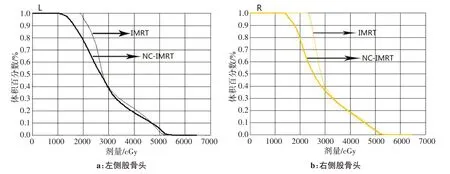
圖2 IMRT和NC-IMRT計劃兩側股骨頭DVH圖比較Fig.2 Dose-volume histogram comparison of bilateral femoral heads between IMRT and NC-IMRT plans
2.4 其它危及器官劑量學比較
分別比較IMRT 和NC-IMRT 兩種照射方式下,膀胱、直腸、小腸各危及器官的受照劑量,結果如表4所示。NC-IMRT 計劃減少了膀胱的Dmax和V30(P<0.05);對于小腸劑量一定程度上有所增加,但二者差異沒有統計學意義(P>0.05)。

表3 IMRT和NC-IMRT計劃左右側股骨頭受照劑量比較Tab.3 Comparison of doses to bilateral femoral heads between IMRT and NC-IMRT plans
2.5 機器跳數比較
IMRT 和NC-IMRT 計劃的平均機器跳數分別為793±84 和766±112(P>0.05),NC-IMRT 技術沒有明顯增加機器跳數。
3 討論
宮頸癌發病率在女性惡性腫瘤中僅次于乳腺癌,在生殖道惡性腫瘤中居首位。據2017年美國癌癥協會最新統計數據顯示,宮頸癌患病率在美國為0.6%(1/161),其中小于49 歲病人約占0.3%(1/371),患病率較往年未見明顯下降,且發病群體趨于年輕化[7]。對于中晚期(IIB 期以上)宮頸癌患者通常采用同步放化療。對于根治性放療而言,為了達到臨床靶區的有效生物劑量,通常GTV 給量為60 Gy,CTV為50.4 Gy,在保證臨床靶區高劑量的同時,靶區周邊的器官如直腸、膀胱、骨盆也不可避免受照射,尤其是骨盆骨髓,臨床上3~4級的血液學不良反應常使得治療中斷或無法繼續治療,有可能影響到患者的預后。如何有效降低盆腔骨髓的受照體積和劑量,從而降低骨髓抑制的程度和發生率成為當然的熱門研究話題[8]。
骨盆是整個盆腔的骨性支架,正常人體內超過1/2有效活性骨髓位于髂骨、骶骨、股骨近端及低位腰椎[9-10],普通定位CT不足以區分骨盆內活性和非活性骨髓[11],若要實現放療過程中更好地保護骨盆內活性骨髓,只能對全骨盆大范圍進行限量[12],這就增加了達到臨床靶區治療劑量的難度。研究中,MRI勾畫的有效活性骨髓體積較整個骨盆體積小,僅對小體積的活性骨髓進行劑量限制,既能保證靶區劑量,又能有效地降低活性骨髓的劑量,從而降低血液學不良反應發生率。盡管MRI技術在區分有效活性骨髓方面發展比較成熟,但當體內有效活性骨髓含量相對較少時,MRI的敏感度不及SPECT和PET-CT[13-15]。由于目前SPECT所用的藥物核素99Tcm標記的硫膠體在臨床應用上有所限制,暫時未能開展該試驗。而PET-CT價格昂貴,考慮到患者的經濟負擔問題,因此,相關試驗也暫未采用。當條件許可時,擬進一步探討PET-CT在活性骨髓識別方面的優勢。
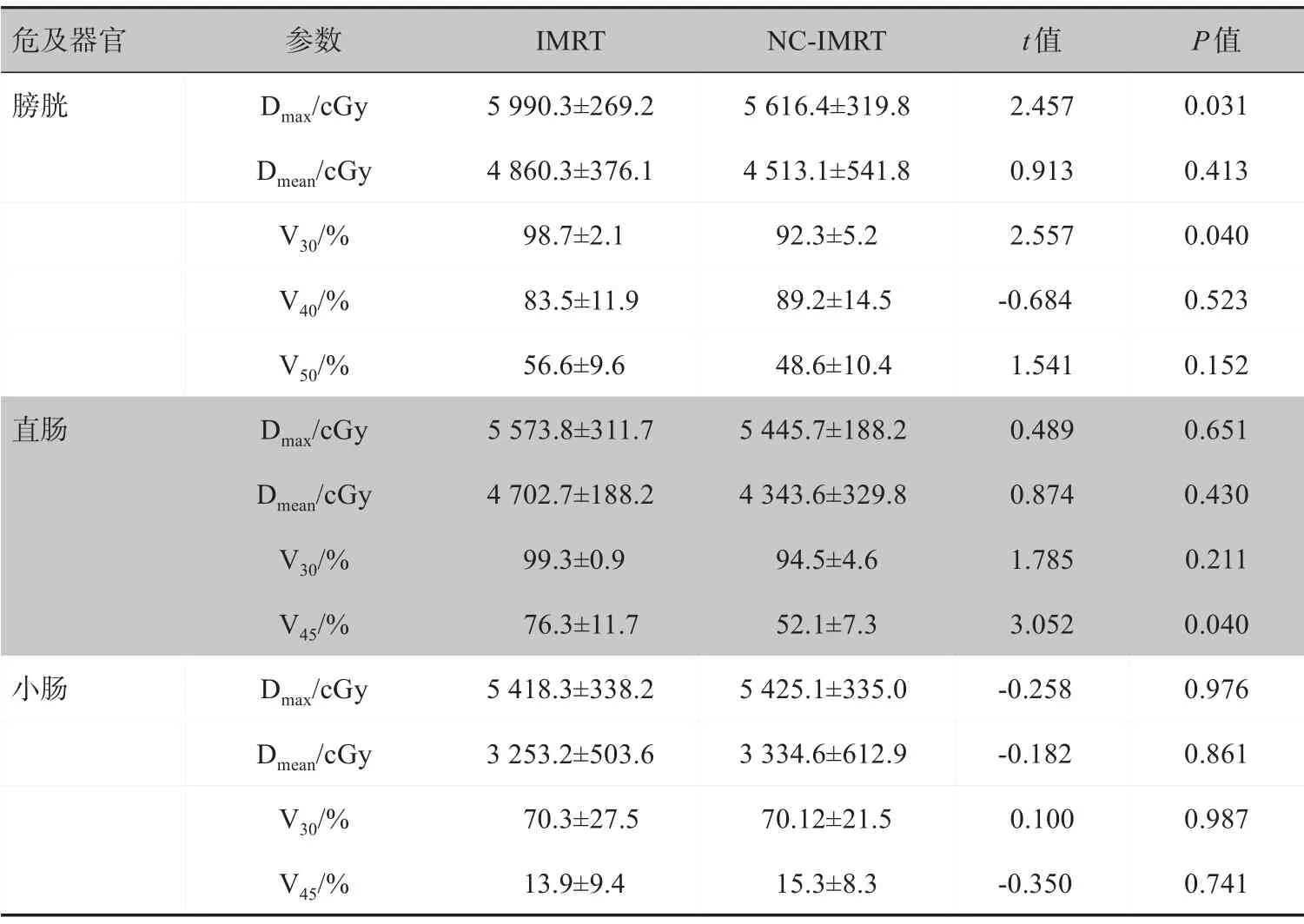
表4 兩組計劃其它危及器官劑量學差異比較Tab.4 Comparison of the dose-volume parameters of organs-at-risk between IMRT and NC-IMRT plans
非共面技術已廣泛應用于腫瘤的放射治療中[16-19]。研究中筆者利用非共面技術優化劑量分布,探討該技術在保護危及器官方面的劑量學優勢。研究發現,相對于IMRT 計劃,NC-IMRT 計劃有效降低了BMDACT的V10、V20、V40、V50;同時,還降低了雙側股骨頭受照劑量;其它危及器官,如膀胱、直腸Dmean也均有降低,小腸的受照劑量較IMRT 計劃略有升高,但差異無統計學意義。Mauch 等[20]發現低劑量射線對于骨髓腔內的造血干細胞相當敏感,低劑量輻射通過損傷造血干細胞,使骨髓腔內有效造血骨髓發生急性和慢性改變,從而造成骨髓抑制和外周全血細胞降低。本次試驗通過MRI 指導勾畫出活性骨髓,改變外照射入射角度,從而有效降低了骨盆骨髓高低劑量輻射區的照射劑量。
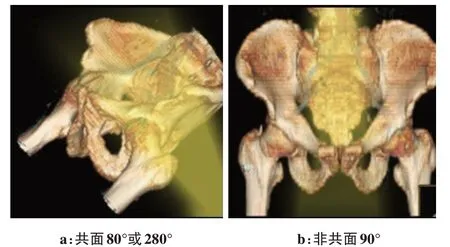
圖3 共面野和非共面野光野示意圖Fig.3 Images of coplanar field and non-coplanar field
綜上所述,NC-IMRT計劃相對IMRT計劃在保護盆腔骨髓方面有一定的劑量學優勢,如圖3a所示,當共面計劃照射,機架角側面出束時,整個骨盆基本暴露于照射野中,從而使骨盆照射劑量急劇增加,當改成非共面照射(圖3b)時,光野分別沿著骨盆出入口方向照射,在一定程度上減少了骨盆和雙側股骨頭照射體積,從而更好地保護骨盆和雙側股骨頭,降低了臨床發生急性血液學不良反應的發生率。當然非共面照射在實施過程中相對于共面照射來說耗費時間長,增加了臨床實施的難度,在質控上也有一定的難度。
致謝:本項目受到廣州市醫學重點學科(2017-2019年)腫瘤治療學及實驗腫瘤學項目資助。

