基于氮摻雜石墨烯量子點/硫化鎘納米晶電化學發光傳感器檢測硫化氫
杜方凱 張慧 譚學才 馮德芬 羅燕妮


摘?要?以檸檬酸和氨水為原料,用水熱法制備了氮摻雜石墨烯量子點(NGQDs),與硫化鎘納米晶(CdS NCs)復合,構建了固態電化學發光(ECL)傳感器,用于硫化氫(H2S)的檢測。采用紫外-可見吸收光譜和熒光光譜對NGQDs和CdS NCs進行了表征,同時對傳感器的ECL和電化學行為進行了系統研究。結果表明,以H2O2為CdS NCs的共反應試劑時,NGQDs可增強CdS NCs的ECL信號,并且NGQDs/CdS NCs的穩定性增加。H2S存在下,S2與過量的Cd2+發生鍵合作用,ECL值降低。在最優條件下, ECL變化值與H2S濃度(2.0×1010~2.0×105 mol/L)的對數呈良好的線性關系,檢出限為6.7×1011 mol/L。采用本傳感器測定血清中H2S濃度,加標回收率為92.7%~103.8%。
關鍵詞?電化學發光;石墨烯量子點;硫化鎘納米簇;硫化氫
1?引 言
硫化氫(H2S)是一種無色、易燃、水溶性氣體,具有臭雞蛋的特有氣味,傳統意義上被認為是有毒氣體[1]。然而,最近的研究證明,H2S是一種人類或其它生物體內可以產生的氣態信號,除一氧化氮(NO)和一氧化碳(CO)外,H2S被認為是第三種氣體信號分子[2],在心血管系統、中樞神經系統、呼吸系統,胃腸系統以及內分泌系統等方面起著重要的調節作用[3~7]。H2S濃度異常可能導致一些疾病,如胃粘膜損傷、肝硬化和阿爾茨海默氏病[8~10]等。現有的檢測H2S的方法有比色法[11]、磷光法[12]、氣相色譜法[13]、熒光法[14]和電化學發光法[15]等。其中,電化學發光技術具有儀器較簡單、快速、靈敏度高、線性范圍寬等優點,引起了廣泛關注[16,17]。目前的電化學發光體系中,魯米諾及三聯吡啶釕因水溶性好、發光效率高、穩定性好而成為常用的發光試劑。然而,這些發光試劑價格昂貴、對環境污染大, 制約了電化學發光技術的發展。 因此, 構建價格低廉、易于合成、可固定于電極表面的發光試劑具有重要的意義。
半導體納米晶體(NCs)作為一種新型ECL發光試劑,與傳統的分子發光試劑相比,具有尺寸/表面陷阱控制發光、抗光漂白穩定性好等優點,但NCs的ECL發光強度通常較低,限制了其廣泛應用。納米材料(如碳納米管[18]、石墨烯[19]、金納米粒子[20]、銀納米粒子[21])與NCs制備復合材料,是提高ECL發光效率的有效途徑之一。此外,加入共反應試劑是另一種有效法,如Zhang等[22]報道共反應試劑H2O2可極大地增強CdS NCs的ECL強度。
氮摻雜石墨烯量子點(NGQDs)作為新型碳納米材料,具有良好的生物相容性、優異的細胞膜通透性和理想的光學性能,引起了廣泛關注[23,24]。近年來,已開發出具有優異熒光特性的NGQDs用于電化學發光分析傳感領域[25,26],但改善其水溶性、簡化改性過程、產生高而穩定的ECL信號仍然是研究的重點。
本研究將NGQDs與CdS NCs簡單混合制備其復合物,修飾于電極表面,顯示了較強的ECL強度。樣品中存在H2S時,電極的ECL響應強度減弱,基于此建立了檢測H2S的ECL分析方法,用于牛血清中H2S濃度的定量檢測,效果良好。本研究結果對復雜生物樣品中H2S的檢測具有重要的參考價值。
2?實驗部分
2.1?儀器與試劑
JEM-2100(HR)型高分辨率透射電子顯微鏡(日本JEOL 公司); MPI-EⅡ型電致化學發光檢測儀(西安瑞邁電子科技有限公司); CHI660E電化學工作站(上海辰華儀器有限公司); Agilent Cary 60紫外可見分光光度計(美國Agilent Technologies公司); F-4600熒光分光光度計(日本Hitachi公司);KQ218型超聲清洗儀(昆山市超聲儀器有限公司); PHS-3E型pH計(上海精密科學儀器有限公司); FD-1000型冷凍干燥機(埃朗科技國際貿易有限公司); H1850R型冷凍離心機(湖南湘儀公司)。電化學測試采用三電極體系:修飾的玻碳電極(GCE)為工作電極(φ=3.00 mm),Ag/AgCl電極(飽和KCl)為參比電極,鉑電極為輔助電極
Na2S·9H2O、Cd(NO3)2·4H2O(阿拉丁生物科技有限公司); 殼聚糖(上海伯奧生物科技有限公司); 牛血清(浙江天杭生物有限公司); 乙腈(成都科龍化工試劑廠); 谷胱甘肽(上海瑞永生物科技有限公司);K2S2O8(上海化學試劑有限公司)。 其它試劑均為國產分析純,實驗用水為超純水。
2.2?NGQDs的制備
參照文獻[27]的方法制備NGQDs: 將25 mg檸檬酸溶于12.5 mL水,快速加入500 μL氨水,加入25 mL反應釜中,200℃反應3 h,冷卻至室溫,超聲30 min,用0.22 μm 微孔濾膜過濾并透析(MWCO: 3500 Da)至中性,備用。
2.3?CdS NCs的制備
參照文獻[22]的方法制備CdS NCs。 將186.0 mg Cd(NO3)2·4H2O溶于30 mL 水中,攪拌下加熱至70℃; 將596.0 mg Na2S·9H2O溶解于30 mL 水中,并將此溶液緩慢注入Cd(NO3)2溶液中,立即產生黃色沉淀。將混合液置于70℃反應3 h后,產物離心,沉淀用乙醇和水各洗滌2次。將最終產物超聲溶解于水中,9000 r/min離心10 min,收集上層黃色溶液,于4℃保存,備用。
2.4?修飾電極的制備
在專用麂皮上依次用1.0、0.3和0.05 μm的Al2O3粉末對GCE進行處理,再用HNO3(50%,V/V)、乙醇及水超聲清洗,室溫下用氮氣吹干,待用。將適量NGQDs與CdS NCs混合,攪拌1 h。取適量混合液滴涂于處理好的GCE表面上,室溫下自然晾干。將適量殼聚糖醋酸溶液(6.67 mg/mL)滴涂于NGQDs/CdS NCs/GCE電極表面,烘干。將修飾好的電極放入不同濃度的Na2S溶液(作為H2S來源[14])中,37℃下孵育7 min。在含有10 mmol/L H2O2的PBS(0.1 mol/L, pH=9.0)中用電化學發光檢測儀進行檢測,光電倍增管電壓600 V,掃描范圍
1.5~0 V,掃速為50 mV/s。
2.5?血清中H2S的檢測
將1 μL不同濃度的H2S標準溶液加入到90 μL牛血清中。分別向其中加入60 μL CH3CN,沉淀血清中的蛋白,6000 r/min離心1 min。將140 μL上清液加入到280 μL 40%(V/V)CH3CN中,繼續沉淀蛋白,6000 r/min離心5 min。最后,將100 μL上清液樣品加入到400 μL超純水中,將修飾好的電極插入處理好的溶液中,37℃孵育7 min,在含有10 mmol/L H2O2的PBS(0.1 mol/L,pH=9.0)中檢測ECL值。
3?結果與討論
3.1?修飾電極的ECL的機理
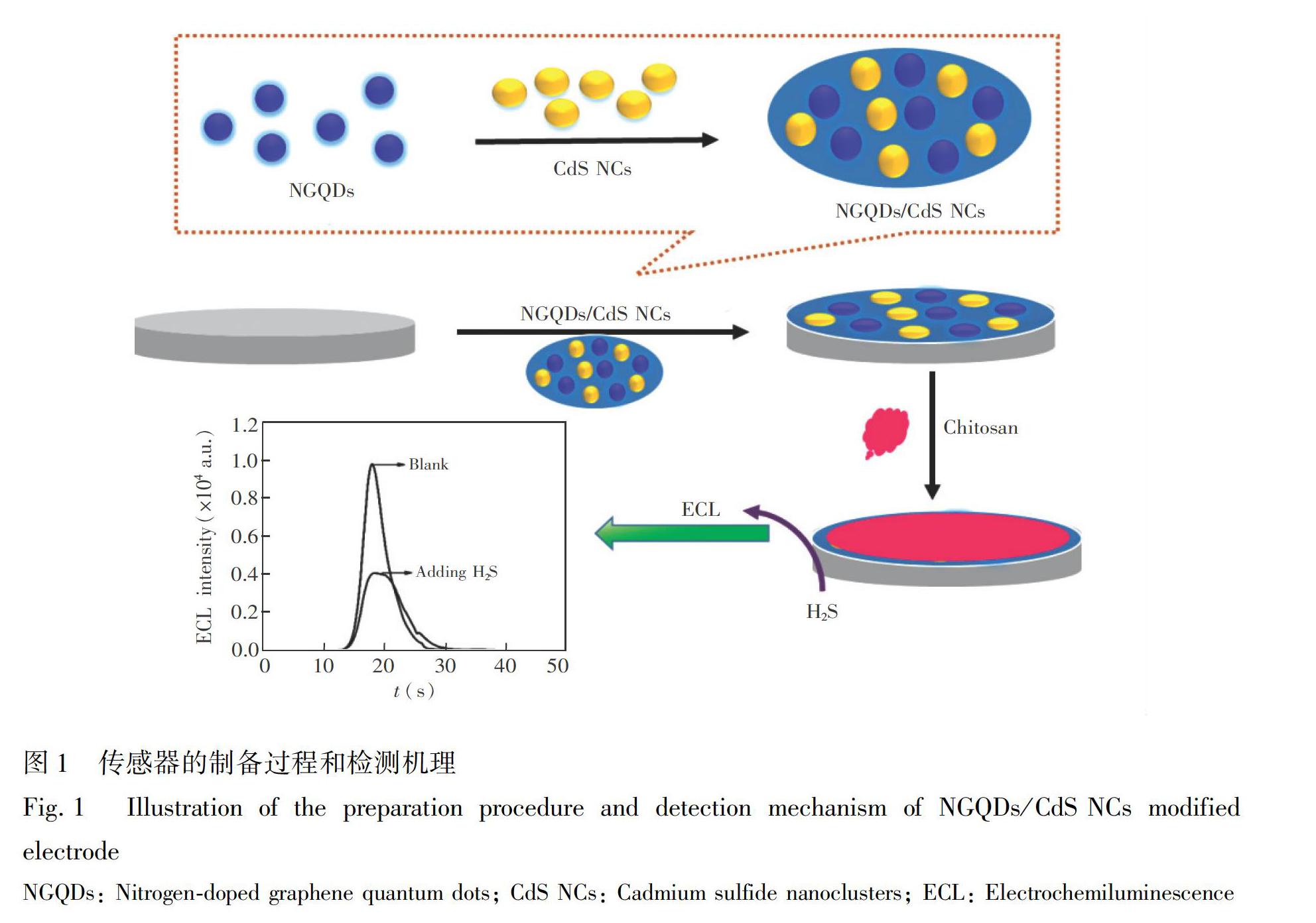
傳感器制備及檢測原理如圖1所示。CdS NCs作為半導體納米晶ECL發光試劑,H2O2為其共反應試劑,可能的反應機理為[18,22]:
CdS+ne
→n(CdS)·-(1)
H2O2+e
→OH
+ OH·(2)
OH· + CdS·-→CdS*+ OH
(3)
CdS* →CdS+hv(4)
3.2?NGQDs與CdS NCs的表征
圖2為NGQDs和CdS NCs的紫外-可見吸收光譜及熒光發射光譜圖。由圖2A可見,NGQDs的特征吸收峰出現在230和345 nm, 230 nm處的吸收峰與π-π*躍遷有關,345 nm處的吸收峰是與CN的n-π*轉變相關,證明N元素成功摻雜到量子點中[28]。在345 nm的激發波長下,NGQDs在440 nm處發射很強的熒光。由CdS NCs的紫外吸收光譜及熒光發射光譜(圖2B)可見,在471 nm處出現CdS NCs的吸收帶, 在511 nm處有最大熒光發射峰。上述結果表明,NGQDs和CdS NCs成功制備。
3.3?NGQDs/CdS NCs修飾電極的電化學發光和電化學行為
采用掃描電子顯微鏡對修飾電極表面的形貌進行了表征。如圖3所示,電極表面修飾了較為均一的Chitosan/NGQDs/CdS NCs膜。不同修飾材料對ECL信號值的影響如圖4A所示,
由圖可知,NGQDs修飾電極幾乎沒有ECL信號(曲線a); CdS NCs/GCE在含有10.0 mmol/L H2O2的0.1 mol/L PBS溶液中表現出較弱的ECL信號強度(曲線b)。根據文獻[29]報道,H2O2可吸附在其氧化CdS NCs表面形成的S缺陷上,從而可以穩定電化學過程中產生的的OH·,產生ECL信號。對比曲線b和曲線c可知,NGQDs的加入使修飾電極具有突出的ECL性質(曲線c)。這可能是由于NGQDs的高導電率和表面豐富的羧基,可與Cd2+配位,穩定表面S缺陷,導致ECL信號增強。經過5.0×106 mol/L H2S溶液孵化后, 修飾電極的ECL有較大幅度的減弱,這是由于CdS的穩定常數(1.25×1026)非常大,S2可將NGQDs從CdS NCs表面競爭下來,降低CdS·的穩定性。這與文獻[22]報道的一致。 NGQDs/CdS NCs混合材料修飾的電極與單個材料修飾的電極相比,ECL值大幅增加。圖4B為不同修飾電極相應的CV圖。CdS NCs修飾的電極在1.24 V出現還原峰,說明CdS NCs在1.24 V處可被還原,產生CdS)·。NGQDs在0.74 V出現弱的還原峰。當二者混合修飾后,在-1.09 V處出現還原峰,且還原峰電流大幅增大,表明CdS NCs更容易被還原。
3.4?實驗條件的優化
探討了影響ECL響應的實驗參數,其中復合材料NGQDs/CdS NCs中NGQDs與CdS NCs的體積比是關鍵因素之一。由圖5A可見, ECL響應值先隨二者體積比增加而增大, 當體積比為0.5時達到最大值,之后逐漸減小。這可能是因為二者體積比較小時,NGQDs的量過少,協同作用不顯著, ECL值降低; 而當二者體積比較大時,參加ECL反應的CdS較少,因此ECL值較低。
NGQDs/CdS NCs的修飾量也是影響實驗的主要因素之一。結果表明(圖5B), 在5.5~8.5 μL范圍內,ECL值先隨修飾量的增加而增大,在修飾量為7.0 μL時達到最大值, 隨后逐漸降低,這是由于過多的修飾材料堆積在電極表面, 阻礙電子的傳遞,使ECL值降低。
檢測溶液中H2O2含量也可影響ECL值。對其含量進行了優化,結果表明(圖5C),當0.1 mol/L PBS中含有10 mmol/L H2O2時ECL值較大,當H2O2含量繼續增加時,ECL值變化較小。 考慮到成本,選擇含有10 mmol/L H2O2的PBS(0.1 mol/L)為反應溶液。
另外,還考察了pH值對ECL響應的影響(圖6A),結果表明,在其它影響因素不變的情況下,ECL響應在pH 7.0~9.5范圍內先隨pH值增加而增大,在pH=9時達到最大; 當pH>9后,ECL值反而降低。這可能是由于pH較低時有利于失去質子,而當pH過高時,影響了H2O2的穩定性。
掃速對ECL響應的影響如圖6B所示,在掃速為50 mV/s時ECL響應值最大。在較低掃速時,形成活性反應中間體的速度較慢,不利于ECL反應的進行,而在過高的掃速下,ECL反應時間縮短,也會導致ECL響應值降低。選擇最佳掃速為50 mV/s。
3.5?線性方程和檢出限
在最佳實驗條件下,用電致化學發光檢測儀檢測電化學發光傳感器對不同濃度H2S的響應情況(圖7)。由NGQDs/CdS NCs修飾電極在不同濃度H2S溶液中的ECL曲線(圖7A)可知,隨著H2S濃度增加,ECL強度逐漸減小。 ECL變化值(ΔECL, ΔECL =ECLblank-ECLH2S)與H2S濃度的線性相關曲線見圖7B,在2.0×1010~2.0×105 mol/L范圍內,H2S濃度的對數與ΔECL呈良好的線性關系,其線性回歸方程為I = 1186.48×lgCH2S+14762.82(R2=0.9995),檢出限(S/N=3)為6.7×10 mol/L。同文獻報道的檢測方法相比(表1),本方法具有更寬的線性范圍或更低的檢出限。
3.6?重現性、穩定性和抗干擾能力
在最優條件下,使用修飾電極對5 μmol/L H2S連續測定10次, ECL強度值的相對標準偏差(RSD)為0.6% (圖8A)。采用相同方法制備7根電極并進行測量,其ECL強度值的RSD為2.1%,表明電極的制備重現性良好。將修飾電極在室溫下放置7天后,再次進行檢測,發光信號值為初始值的88.8%~91.9%, 表明修飾電極具有良好的穩定性。
對修飾電極的選擇性進行了考察。由圖8B可見,濃度為5 μmol/L的胱氨酸、谷胱甘肽、S2O28及Cl對應的ECL響應值與空白實驗對應的ECL響應值相差小,而5 μmol/L H2S的ECL值比空白值降低明顯。干擾測試結果表明,修飾電極對H2S具有良好的選擇性。
3.7?血清中H2S的檢測
為了評估制備的修飾電極的實用性,將修飾電極用于牛血清樣品中H2S的檢測,檢測結果見表2,加標回收率在92.7%~103.8%之間。因此,制備的修飾電極可用于血清樣品中H2S的檢測。
4?結 論
合成了NGQDs/CdS NCs復合材料,NGQDs表現出了優越的電化學性質,而CdS NCs表現出了較高的發光效率。 在2.0×105~2.0×1010 mol/L范圍內,H2S濃度的對數與其相對發光強度呈良好的線性關系,檢出限(S/N=3)為6.7×1011 mol/L。將此電極用于血清中H2S的檢測, 效果良好, 加標回收率在92.7%~103.8%之間。 NGQDs/CdS NCs修飾電極具有良好的穩定性、重現性及抗干擾能力,為體外快速靈敏檢測H2S提供了新方法。
References
1?Reiffenstein R J, Hulbert W C, Roth S H. Annu. Rev. Pharmacol. Toxicol., 1992, 32(1): 109-134
2?Kabil O, Banerjee R. J. Biol. Chem.,2010,285(29): 21903-21907
3?Lefer D J. Proc. Natl. Acad. Sci. USA,2007,104(46): 17907-17908
4?Calvert J W, Elston M, Nicholson C K, Gundewar S, Jha S, Elrod J W, Ramachandran A, Lefer D J. Circulation,2010,122(1): 11-19
5?Abe K, Kimura H. J. Neurosci.,1996,16(3): 1066-1071
6?Kimura H. Mol. Neurobiol.,2002,26(1): 13-19
7?Martelli A, Testai L, Breschi M C, Blandizzi C, Virdis A, Taddei S, Calderone V. Med. Res. Rev.,2012,32(6): 1093-1130
8?Li L, Rose P, Moore P K. Annu. Rev. Pharmacol. Toxicol.,2011,51: 169-187
9?Szabo C. Nat. Rev. Drug Discov.,2007,6: 917-935
10?Kamoun P, Belardinelli M C, Chabli A, Lallouchi K, Chadefaux-Vekemans B. Am. J. Med. Genet. A,2003,116A(3): 310-311
11?Hughes M N, Centelles M N, Moore K P. Free Radical Bio. Med.,2009,47(10): 1346-1353
12?Wu P, Zhang J, Wang S, Zhu A, Hou X. Chemistry,2014,20(4): 952-956
13?Pierre R B, Paula D P, Eric R H. J. Chromatogr. A,1999,830(2): 485-489
14?Qian Y, Zhang L, Ding S, Deng X, He C, Zhu H L, Zhao J. Chem. Sci.,2012,3(10): 2920-2923
15?Doeller J E, Isbell T S, Benavides G, Koenitzer J, Patel H, Lancaster J R, Darley-Usmar V M, Krausa D W. Anal. Biochem.,2005,341(1): 40-51
16?Dong Y P, Wang J, Peng Y, Zhu J J. Biosens. Bioelectron.,2017,64: 530-535
17?WANG Ming-Li, SUN Ya-Nan, GUO Jia-Yi, YANG Xue-Mei, YANG Min-Li. Chinese J. Anal. Chem.,2018,46(5): 780-786
王明麗, 孫亞楠, 郭佳怡, 楊學梅, 楊敏麗. 分析化學,2018,46(5): 780-786
18?Wang X F, Zhou Y, Xu J J, Chen H Y. Adv. Funct. Mater.,2009,19(9): 1444-1450
19?Zhou H, Zhang Y Y, Liu J, Xu J J, Chen H Y. Chem. Commun.,2013,49: 2246-2248
20?Jie G F, Liu P, Zhang S S. Chem. Commun.,2010,46: 1323-1325
21?Wang C, E Y, Fan L, Yang S, Li Y. J. Mater. Chem.,2009,19(23): 3841-3846
22?Zhang Y Y, Zhou H, Wu P, Zhang H R, Xu J J, Chen H Y. Anal. Chem.,2014,86(17): 8657-8664
23?Du Y, Guo S. Nanoscale,2016,8(5): 2532-2543
24?Li L, Wu G, Yang G, Peng J, Zhao J, Zhu J J. Nanoscale,2013,5(10): 4015-4039
25?Nie G M, Wang Y, Tang Y, Zhao D, Guo Q F. Biosens. Bioelectron.,2018,101: 123-128
26?Qi B P, Zhang X R, Shang B B, Xiang D S, Qu W Y, Zhang S H. Carbon,2017,121: 72-78
27?Chen S, Song Y, Li Y, Liu Y, Su X, Ma Q. New J. Chem.,2015,39(10): 8114-8120
28?Cai Z, Li F, Wu P, Ji L, Zhang H, Cai C, Gervasio D F. Anal. Chem.,2015,87(23): 11803-11811
29?Fang Y M, Song J, Zheng R J, Zeng Y M, Sun J. J. Phys. Chen. C,2011,115:9117-9121
Detection of Hydrogen Sulfide Based on Nitrogen-doped
Graphene Quantum Dots/Cadmium Sulfide Nanocrystals
Electrochemiluminescence Sensor
DU Fang-Kai, ZHANG Hui, TAN Xue-Cai*, FENG De-Fen, LUO Yan-Ni
(School of Chemistry and Chemical and Engineering, Guangxi University for Nationalities,
Key Laboratory of Guangxi Colleges and Universities for Food Safety and Pharmaceutical Analytical Chemistry,
Guangxi Key Laboratory of Chemistry and Engineering of Forest Products, Nanning 530006, China)
Abstract?Nitrogen-doped graphene quantum dots (NGQDs) were synthesized by hydrothermal method with citric acid and ammonia as raw materials. A solid-state electrochemiluminescence (ECL) sensor was thus constructed by dropping NGQDs/CdS nanocluster (NCs) composites. The properties of NGQDs and CdS NCs were characterized by UV-Vis absorption spectroscopy and fluorescence spectroscopy. The electrochemiluminescent and electrochemical behaviors of the sensor were studied. The results showed that NGQDs could enhance electrochemiluminescence signal of CdS NCs and the stability of NGQDs/CdS NCs increased when H2S was used as the co-reaction reagent of CdS NCs. In the presence of H2S, S2
bonded with excess Cd2+, and the ECL intensity decreased. Under the optimal conditions, the decrease in electrochemiluminescence intensity varied proportionally with the logarithmic concentration of H2S from 2.0×1010-2.0×105 mol/L, and the detection limit was estimated to be 6.7×1011 mol/L. The sensor was used for the determination of H2S in bovine serum with recoveries of 92.7%-103.8%, which indicated that the proposed sensor had the potential for detection of H2S in practical complex samples.
Keywords?Electrochemiluminescence; Graphene quantum dots; Cadmium sulfide nanoclusters; Hydrogen sulfide
(Received 18 September 2019; accepted 18 November 2019)
This work was supported by the National Natural Science Foundation of China (No. 11904059), the Natural Science Foundation of Guangxi Province, China (Nos. 2017GXNSFBA198026, 2018GXNSFAA294044, 2018GXNSFAA281136), the Key Research and Development Project of Guangxi Province, China (No. AB18126048), the Basic Ability Enhancement Program for Young and Middle-aged Teachers of Guangxi Province, China (No. 2018KY0168), and the State Key Laboratory of Analytical Chemistry for Life Science, Nanjing University (No. SKLACL1810).

