表面增強拉曼光譜活性基底的制備與性質研究
趙博儒 沈勁松 孫志 陳峰 陳智棟 趙健偉


摘?要?建立了無氰電沉積粒徑約20 nm的銀顆粒制備表面增強拉曼光譜活性銀基底的方法, 考察了基底的相關性質。利用電化學循環伏安法在不同的掃描速度下研究此沉積體系的電化學行為, 結果表明, 銀的電沉積過程受擴散控制, 當掃描速度增大時, 氧化峰位略正移, 但還原峰明顯負移。掃描電鏡表征結果表明, 沉積銀層的結晶形狀規則, 分布均勻, 粒徑為(20 ± 10) nm。以甲基橙為探針, 考察了沉積銀基底對拉曼光譜信號的增強作用, 其增強因子為5.2×105。沉積銀基底對羅丹明6G(R6G)分子檢測的線性范圍為1×1012~1×10 mol/L, 相關系數為0.98, 檢出限低于1×1012 mol/L。拉曼光譜Mapping圖表明, 沉積銀活性基底在大范圍內的增強效果均勻。
關鍵詞?沉積銀; 活性基底; 表面增強拉曼散射; 檢出限
1?引 言
拉曼光譜分析對測試樣品無損害, 具有樣品制備簡單、操作方便等優點, 廣泛應用于單分子檢測、化學化工、生物醫學、納米材料等領域[1], 但拉曼散射信號弱, 應用受限。Fleischmann等[2]將有機分子吸附于經粗糙化處理的貴金屬材料表面, 發現拉曼信號顯著增強, 即表面增強拉曼散射(Surface-enhanced Raman scattering, SERS)效應。因此, SERS活性基底的制備成為其應用的關鍵。其中, 銀薄膜相對便宜, 增強效果顯著, 因此應用廣泛。
近年來, 有關銀基底SERS效應和制備方法的研究取得了較大進展。徐存英等[3]在AgNO3中添加離子液體, 通過電化學沉積得到致密的銀沉積層, 具有較好的SERS效應。曾勇明等[4]在玻碳片上沉積銀層, 銀粒子直徑約為1~2 μm, 對探針分子的檢出限達到1.0×107 mol/L, 雖具有SERS效應, 但效果不理想。隨著研究的深入, 研究者開發了許多具有納米結構特征的基底及復合基底。Upender等[5]通過納米團簇沉積制備出了平均粒徑為(157 ± 119) nm的銀膜, 并將其作為表面增強拉曼光譜的活性基底, 具有SERS活性高、重現性好和性能相對穩定的特點, 對羅丹明6G(R6G)的檢出限可達1.0×1016 mol/L, 有望應用于超低濃度分子的檢測, 但其制備過程復雜且成本高, 難以商業化應用。Polavarapu等[6]利用旋涂工藝, 采用油胺-甲苯體系制備了3~5 nm金、銀溶膠, 在退火處理后, 可得到穩定的SERS活性基底。Gu等[7]采用AgNO3/PVP溶液體系在銅基板上合成出枝狀銀納米結晶, 這種SERS基底具有較高的熱穩定性和良好的重現性, 檢測R6G濃度可低至3.2×1011 mol/L。Kosovi等[8]比較了兩種低摻雜p型硅晶片, 一種通過電化學刻蝕獲得微孔硅模板, 另一種浸入HF溶液中獲得具有介孔結構的模板。分別在AgNO3溶液中進行電化學沉積銀納米粒子, 在微孔模板上形成了均勻的納米球形銀層, 在介孔模板上則具有形狀不規則和邊緣銳利的銀聚集體,后者表現出更好的SERS活性。此外, 該基底的局域表面等離子體共振頻帶的峰值更接近激發光源的波長, 在這種共振條件下, R6G的檢出限低至1.0×1015 mol/L。雖然其在SERS領域表現出很大的應用潛力, 但重現性不佳, 難以大規模應用。
雖然制備銀的SERS基底相關的理論研究和實驗方法很多, 但目前多以基礎研究為主。有些SERS基底雖具有低檢出限和寬線性范圍, 但制備過程復雜, 不適宜作為標準化的檢測方法。李貞等[9]對SRES活性基底制備的研究進展進行了評述, 指出了各種制備方法的優點和弊端。
因此, 制備一種SERS效應顯著、穩定性好、靈敏度高的活性基底, 同時開發工藝流程簡單、生產環保、可批量生產、成本低廉的制備方法, 具有重要的理論和實用價值。無氰電沉積銀作為一種電沉積方法, 能夠滿足上述要求。本研究采用循環伏安法、掃描電鏡和拉曼光譜分別對無氰沉積銀體系的電化學行為、沉積銀基底的微觀結構、SERS增強效應及分析檢測性能等進行了詳細的研究。相比商品化的銀膠SERS檢測技術, 本研究采用的銀基底制備方法簡單可靠, 成本低, 性能穩定, 可長期貯存; 電沉積銀層均勻平整, SERS增強效果顯著; 其在測試應用中操作簡便, 響應靈敏, 線性范圍寬, 檢出限低, 具備良好的應用價值。
2?實驗部分
2.1?儀器、試劑與材料
DH7001電化學工作站(江蘇東華測試技術股份有限公司);SU8010場發射掃描電鏡(Scanning electron microscope, SEM, 日本日立公司); DXR2xi型顯微共焦拉曼光譜儀(美國賽默飛世爾科技有限公司); AUY120電子分析天平(日本島津公司); KQ2200DE型數控超聲波清洗器(昆山超聲儀器有限公司)。
ZHL-02無氰鍍銀母液(嘉興銳澤表面處理技術有限公司), 用去離子水稀釋1倍, 作為電沉積工作液; 甲基橙(分析純, 天津市光復科技發展有限公司); 羅丹明6G(Rhodamine 6G, 分析純, 麥克林試劑公司); 其它試劑均為分析純, 使用前未做進一步處理。紫銅片(15 mm×15 mm, 厚度0.8 mm, 嘉興市嘉信醫療器械有限責任公司); 純銀片(15 mm ×15 mm, 厚度0.8 mm, 純度99.99%, 常熟市常宏貴金屬有限公司)。
2.2?電沉積銀基底的制備
以紫銅片作為沉積銀基底, 在45℃下以無水乙醇超聲洗滌15 min, 再以去離子水洗滌。在40℃~50℃加熱條件下, 電流密度3~5 A/dm2, 陰極脫脂5 min, 以去離子水洗滌。在40℃~50℃加熱條件下, 電流密度5~7 A/dm2, 陽極電化學拋光至光亮平滑時, 取出后用大量去離子水洗滌。在溫度(391)℃和電流密度(1.0 0.1) A/dm2條件下, 恒流電沉積銀5 min, 以去離子水洗滌, 吹干, 備用。
2.3?電化學性能測試
電化學實驗在20℃下進行。 以直徑為3.0 mm的玻碳電極為工作電極, 鉑片為對電極, 飽和甘汞電極為參比電極。每次測試前, 玻碳電極用0.05 μm的拋光粉(Al2O3)打磨, 分別用無水乙醇和去離子水超聲清洗15 min。循環伏安曲線測試在工作液中進行, 電位掃描范圍為1.1~1.0 V。
2.4?拉曼光譜表征
將電沉積銀基底在1.0×105 mol/L甲基橙溶液中分別浸泡10、20、30、120、180、240、360和1440 min, 將純銀基底在1×105 mol/L甲基橙溶液中分別浸泡4和24 h。取出, 用去離子水淋洗, 氮氣吹干, 然后進行SERS表征。激發光源為532 nm的氬離子激光, 光譜分辨率小于2 cm1, 激光強度為2.0 mW, 積分時間為0.167 s, 循環10次。
配制1.0×105、1.0×106、1.0×107、1.0×108、1.0×109、1.0×1010、1.0×1011和1.0×1012 mol/L的R6G溶液, 取R6G溶液20 μL, 滴加在電沉積銀基底上, 在室溫下自然干燥, 然后測定拉曼光譜。激發光源為532 nm的氬離子激光, 激光強度為2.4 mW, 積分時間為0.143 s。測量SERS二維成像(Mapping)時, 成像面積為150 m×150 m, 積分時間為0.008 s, 循環5次。
3?結果與討論
3.1?電沉積體系的電化學行為
為研究銀的電沉積過程, 利用循環伏安法在不同的掃速(2~5000 mV/s)下考察了玻碳電極在溶液中的電化學行為。圖1給出了部分掃速下銀在玻碳電極表面的循環伏安圖。
電勢從1.0 V向負方向掃描, 在低掃速2 mV/s時, 0.17 V處出現一個弱的還原峰; 隨掃描速度逐漸增大, 在0.55~1.20 V出現一個明顯的還原峰。此還原峰對應銀離子絡合物在玻碳電極表面的電沉積反應。還原峰的峰位及峰電流均顯著地受到掃描速度的影響。電勢向正方向掃描時, 0~0.25 V可以觀察到明顯的氧化峰, 對應電沉積銀層的氧化溶解。隨著掃描速度不斷增加, 氧化峰逐漸向正電勢方向移動, 但是相對還原峰而言, 移動不明顯; 同時氧化峰電流也相應增高。還原過程較氧化過程更復雜, 包含了去水合作用、絡合物解離過程、銀離子放電等過程。因此, 還原峰對掃描速度的依賴性更強。此特征與其它無氰電沉積銀體系類似[10], 盡管絡合劑種類和溶液濃度會導致具體的峰電位有所不同。
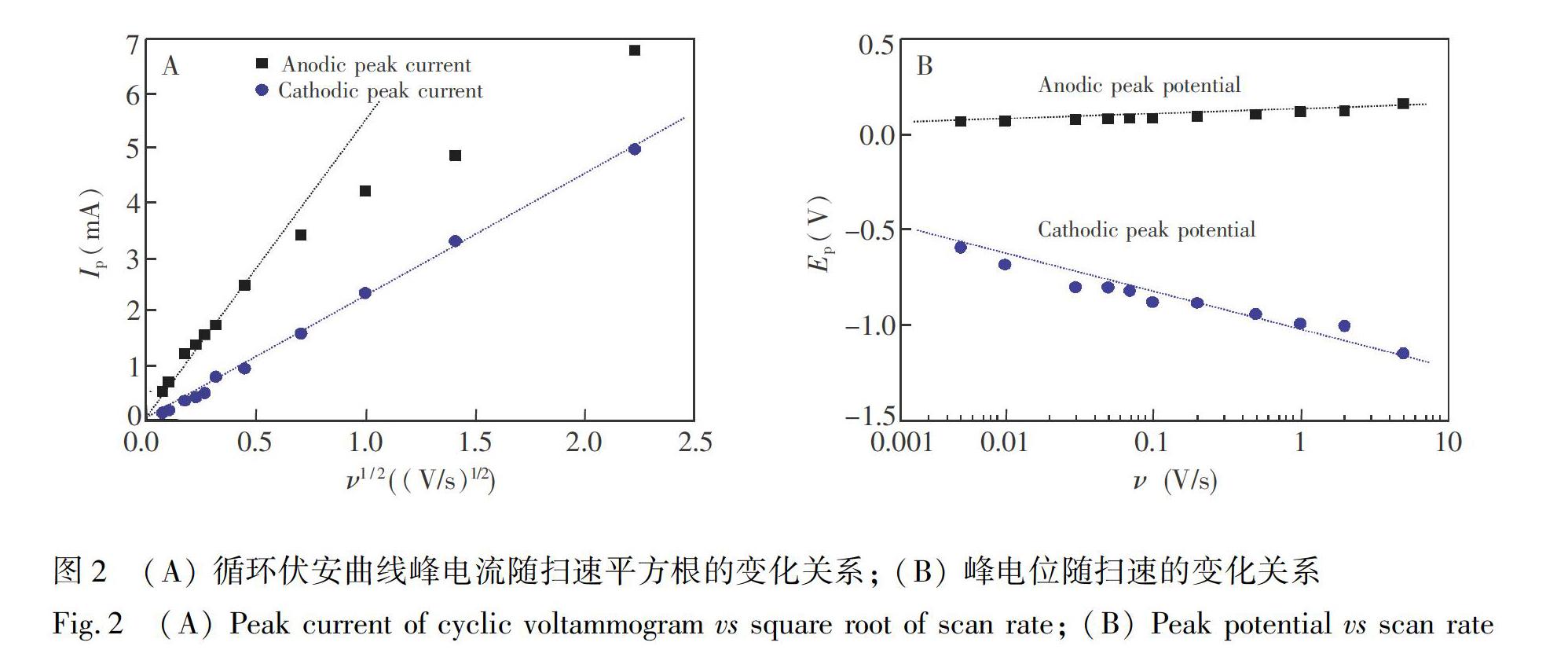
考察了峰電流與掃描速度的關系, 以及峰電位與掃描速度的關系。由圖2A可見, 陰極峰電流與掃描速度的平方根呈良好的線性關系, 符合擴散過程控制的電化學行為中峰電流密度與掃描速度的關系:
jp=0.4958nF32αDv12(RT)-12c(1)
其中, jp為峰電流密度, n為銀在沉積過程中的電子轉移數, F為法拉第常數, α為電荷轉移系數, D為擴散系數, υ為掃描速度, R為氣體常數, T為溫度, c為鍍液中電活性物質的濃度。因此, 可以推斷銀在此體系的電沉積放電過程中受擴散控制[11]。對于氧化峰電流, 因為在較高的掃描速度下, 氧化峰變寬, 導致峰電流在1 V/s后不再線性增加。
由圖2B可見, 雖然氧化峰電位隨掃速增加, 但變化不明顯。掃描速度增加3個數量級, 但峰電位僅增加了94 mV。然而, 還原峰電位隨著掃速的對數呈顯著的線性下降, 進一步表明銀絡合物在電沉積過程中的復雜性。
3.2?電沉積銀基底的形貌和尺寸特征
SERS增強效應主要由電磁場增強和化學增強共同作用, 其中電磁場增強起主導作用, 且電磁場增強中局域表面等離子體共振(Localized surface plasma resonance, LSPR)的貢獻最大。SERS基底中顆粒的形狀、尺寸對LSPR效應的影響尤為顯著[12,13]。電沉積條件下銀基底在不同放大倍數下的SEM圖見圖3, 電沉積銀基底的表面平整、均勻, 與樣品光滑、明亮的外觀一致; 沉積銀層由細小的球形晶粒組成, 形狀較規則, 顆粒尺寸相對均勻, 未出現團聚現象。
對SEM圖中晶粒的粒徑統計分析如圖4所示, 銀晶粒的粒徑主要集中在12~32 nm, 利用高斯分布函數對其擬合, 得到晶粒的粒徑為(20±10) nm。易早等[14]利用原位生長在玻璃基底上制備出平均粒徑100 nm的銀顆粒, 由此制備的基底也具有較好的SERS效應。Wang等[15]采用浸鍍法制備的系列銀/硅納米孔柱陣列(Ag/Si-NPAs)所形成的銀納米結構主要有兩種, 即平均粒徑在70 nm以下和平均粒徑為
0.1~1 μm的基底, 結果表明, 前者的SERS增強效應更明顯。因此, 銀粒徑對于SERS效應影響顯著。本研究所制備的銀基底其晶粒粒徑遠小于原位生長制備的納米銀顆粒, 形狀更為規則, 銀納米粒子因重疊堆積, 顆粒彼此接近, 更易產生等離子體耦合, 增強SERS效應[13]。
3.3?電沉積銀基底的拉曼光譜表征
以甲基橙為探針, 研究了電沉積銀基底的SERS活性, 并與純銀基底對比。結果表明, 電沉積銀基底比甲基橙粉末具有信噪比更高的拉曼特征峰, 表明電沉積銀具有SERS活性。銀是微晶金屬材料, 其晶粒尺度一般大于102 nm, 即使具有SERS活性, 如未經特殊處理, 也不能滿足增強的需求。而通過電沉積獲得的銀基底具有比純銀更加顯著的SERS效應。由圖5可見, 隨著浸泡時間延長, 甲基橙分子的拉曼特征峰的強度增強, 30 min內甲基橙分子吸附速率較快, 隨后吸附速度趨于平緩。浸泡24 h基底的SERS效應不增反減, 甚至出現基線不平的現象, 說明電沉積銀基底在長時間浸泡后, 活性發生變化。在實際應用中, 浸泡時間過長既影響測試, 又影響時效性。因此, 選擇浸泡30~60 min可滿足測試需求。圖5也說明電沉積銀基底對甲基橙分子的吸附是相對緩慢的動力學過程。此結果也預示了SERS效應在電沉積銀基底吸附有機分子的動力學研究中具有良好的應用價值。
平均表面增強因子(Averaged surface enhancement factor, ASEF)可直接反映SERS基底的增強效應, 是拉曼光譜分析的重要指標[12]。利用甲基橙分子在銀表面拉曼光譜的最強峰(1389 cm1)估算銀基底的ASEF, 計算公式如下[13]:
ASEF=Isurf/NsurfIbulk/Nbulk(2)
其中, Isurf為吸附在電沉積銀基底上單層的甲基橙分子在1389 cm1處的積分強度, Ibulk為甲基橙粉末中的分子在1389 cm1處的積分強度, Nsurf和Nbulk分別為激發光束照射區相應的表面和粉末中甲基橙分子的數量。因甲基橙分子的吸附數量難以絕對定量給出, 故本研究以與其尺寸相當的4-巰基苯甲酸分子在銀基底上單層覆蓋的數據為參考[16], 估計在沉積銀基底上單層甲基橙分子的表面濃度為5×1014 molecule/cm2, 激光光束直徑≈1 μm, 由此計算得Nsurf≈8.3×1014 mol。在分母一項中, 甲基橙分子密度為1.28 g/cm3, 激光光束直徑≈1 μm, 其穿透厚度d≈16.5 μm[14], 由此計算得Nbulk≈6.5×1010 mol。將相應的數據代入式(2), 可計算出電沉積銀基底的增強因子達到5.2×105, 表明沉積銀基底具有更好的SERS活性。陸冬蓮等[17]利用銀鏡反應, 在玻璃上沉積200 nm的銀膜, 選擇與銀納米粒子結合作用較弱的巰基苯胺為探針分子, 測得其增強因子≈4.6×105。因此, 本研究制備的無氰電沉積銀基底與其它利用復雜制備方法獲得的基底具有相當的SERS活性。
3.4?電沉積銀基底的檢測線性范圍、檢出限及SERS均勻性
以R6G為探針研究電沉積銀基底的檢測性能。圖6給出了不同濃度下的R6G分子的拉曼光譜圖。由圖6A可見611、775、1183、1308、1360、1506、1568和1649 cm1處R6G的拉曼特征光譜振動峰, 其中, 611 cm1處的強特征峰由苯環面內振動產生[4,15]。隨著溶液樣品濃度的降低, R6G的拉曼振動峰的強度減小, 特征峰峰位未出現明顯的位移, 說明電沉積銀基底具有較好的測試靈敏度和穩定性。圖6B為1×1011 mol/L和1×1012 mol/L R6G的拉曼光譜圖, 即便濃度低至1×1012 mol/L, 仍可觀察到R6G的主要特征峰, 且沒有明顯的移動。R6G在電沉積銀基底的檢出限低于1×1012 mol/L(S/N>3)。陳韶云等[18]采用電化學沉積法制備了樹枝狀銀微納結構的活性基底,R6G檢出限為1×1010 mol/L, 說明電沉積銀基底具有良好的檢測靈敏度和檢出限。
4?結 論
采用工藝簡便、成本低廉的無氰電化學沉積法制備出可批量生產、SERS效應顯著、平顆粒徑約20 nm的銀基底。對此體系的電化學研究的結果表明, 銀的沉積過程受擴散控制, 且還原過程較氧化過程更復雜。本研究分別選擇增強效應較低的甲基橙和活性較高的R6G分子對電沉積銀基底的SERS效應開展系列研究, 結果表明, 電沉積銀基底比純銀具有更好SERS活性。R6G的檢出限低于1×1012 mol/L, 且具有寬的檢測線性范圍。 電沉積銀基底具有良好的均勻性, 保證了測量的一致性和穩定性。
References
1?LUO Zhi-Xun, FANG Yan. Spectroscopy and Spectral Analysis, 2006, 26(2): 358-364
駱智訓, 方 炎. 光譜學與光譜分析, 2006,26(2): 358-364
2?Fleischmann M, Hendra P J, Mcquillan A J. Chem. Phys. Lett.,1974,26(2): 163-166
3?XU Cun-Ying, HUA Yi-Xin, DUAN Yun-Biao, ZHANG Peng-Xiang. Spectroscopy and Spectral Analysis,2009,29(11): 2984-2988
徐存英, 華一新, 段云彪, 張鵬翔.光譜學與光譜分析,2009,29(11): 2984-2988
4?ZENG Yong-Ming, SUN Jian-Jun, CHEN Qi-Zhen, AI Li, LIN Zhi-Bin, REN Bin, TIAN Zhong-Qun. Chinese J. Anal. Chem.,2009,37(s1): 239
曾勇明, 孫建軍, 陳啟振, 艾 莉, 林志彬, 任 斌, 田中群.分析化學,2009,37(s1): 239
5?Upender G, Satyavathi R, Raju B, Shadak A K, Narayana R D, Bansal C. Chem. Phys. Lett.,2011,511(4-6): 309-314
6?Polavarapu L, Manga K K, Yu K, Ang P K, Cao H D, Balapanuru J, Loh K P, Xu Q H. Nanoscale,2011,3(5): 2268-2274
7?Gu H X, Xue L, Zhang Y F, Li D W, Long Y T. ACS Appl. Mater. Interfaces,2015,7(4): 2931-2936
8?Kosovi M, Balarin M, Ivanda M, Derek V, Marcius M, Risti M, Gamulin O. Appl. Spectrosc.,2015,69(12): 1417-1424
9?LI Zhen, XU Wei-Ping, WU Ya-Dong, XU Ting-Juan, JIN Qin-Yu. China Pharmaceutical,2015,24(3): 4-6
李 貞, 徐維平, 吳亞東, 徐婷娟, 金勤玉.中國藥業,2015,24(3): 4-6
10?Liu A, Ren X F, Zhang J, Li D Y, An M Z. RSC Adv.,2016,6(9): 7348-7355
11?Rooij M R. Anti-Corros Method M,2003,50(5): 154-160
12?Gersten J, Nitzan A. J. Chem. Phys.,1980,73(7): 3023-3037
13?Lin X M, Cui Y, Xu Y H, Ren B, Tian Z Q. Anal. Bioanal. Chem.,2009,394(7): 1729-1745
14?YI Zao, LI Kai, HAN Shang-Jun, NIU Gao, YI You-Gen, CHEN Shan-Jun, LUO Jiang-Shan, TANG Yong-Jian. Chin. J. Nonferrous. Met.,2010,20(11): 2221-2227
易 早, 李 愷, 韓尚君, 牛 高, 易有根, 陳善俊, 羅江山, 唐永建.中國有色金屬學報,2010,20(11): 2221-2227
15?Wang Y Q, Ma S, Yang Q Q, Li X J. Appl. Surf. Sci.,2012,258(15): 5881-5885
16?Mohri N, Matsushita S, Inoue M. Langmuir,1998,14(9): 2343-2347
17?LU Dong-Lian, HAN He-You, LIANG Jian-Gong. Chinese J. Anal. Chem.,2010,38(5): 715-718
陸冬蓮, 韓鶴友, 梁建功.分析化學,2010,38(5): 715-718
18?CHEN Shao-Yun, WANG Yuan, LIU Hui, HU Cheng-Long, LIU Xue-Qing, LIU Ji-Yan. Chinese J. Anal. Chem,2017, 45(3): 374-380
陳韶云, 王 圓, 劉 輝, 胡成龍, 劉學清, 劉繼延.分析化學,2017, 45(3): 374-380
Preparation and Properties of Active Substrates for
Surface Enhanced Raman Spectroscopic Analysis
ZHAO Bo-Ru1,3, SHEN Jing-Song2, SUN Zhi1, CHEN Feng*1, CHEN Zhi-Dong3, ZHAO Jian-Wei*1
1(College of Materials and Textile Engineering, Jiaxing University, Jiaxing 314001 China)
2(Jiangsu Donghua Testing Technology Co. Ltd, Taizhou 214500, China)
3(College of Materials Science and Engineering, Changzhou University, Changzhou 213100, China)
Abstract?The silver active substrates with average particle size of about 20 nm for surface-enhanced Raman spectroscopic analysis were prepared using cyanide-free electrochemical deposition method. The electrochemical deposition behavior of the system was studied by cyclic voltammetry at different scanning rates. The results showed that the electrodeposition process of silver was controlled by diffusion. With the increase of scanning rate, the oxidation peak slightly shifted positively, whereas the reduction peak had a significant negative shift. The result of scanning electron microscopy showed that the silver particles were fine, uniform, and regular in shape, and their size was (20±10) nm. Using methyl orange as a probe, the enhancement of Raman spectral signal with the silver-deposited substrate was investigated, and an enhancement factor of 5.2×105 was obtained. The linear range for detection of rhodamine 6G was 1×1012-1×106 mol/L, the correlation coefficient was 0.98, and the limit of the detection was lower than 1×1012 mol/L. Raman spectroscopy mapping also showed that the silver-deposited substrate had a uniform distribution.
Keywords?Silver deposited; Active substrate; Surface enhanced Raman scattering; Limit of detectionReceived 25 June 2019; accepted 31 October 2019)
This work was supported by the Natural Science Foundation of Zhejiang Province, China (Nos. LY19B030006, LY19E090005) and the National Natural Science Foundation of China (Nos. 51861145202, 51802121)

