酪氨酸激酶抑制劑治療老年Ph陽性慢性粒細胞白血病的臨床觀察
楊嵐,任慧娟,韓艷秋
內蒙古醫科大學附屬醫院血液科,內蒙古呼和浩特市010050
慢性髓性白血病(chronic myelogenous leukemia,CML)屬于一種臨床惡性腫瘤,形成于骨髓造血干細胞克隆性增值,PH 染色體(費城染色體) 是CML 細胞遺傳學特征性標記,與BCR-ABL 融合基因作為臨床診斷該癥的必備條件,具有特殊性影響意義[1]。酪氨酸激酶抑制劑(chronic myelogenous leukemia,TKI)屬于低分子多靶點藥物,治療CML 可使患者8年OS率提升至87%,且TKI 治療時可將細胞遺傳學和分子學監測作為預測療效及指導臨床用藥方案的觀察性指標[2]。但TKI 治療時仍有30%左右患者因不良反應等而未獲得最佳治療效果需更換方案。伴隨病情進展,80%CML 患者會伴有克隆演變(CE),為臨床分析慢粒染色體異常的重點問題[3]。雖診療中細胞遺傳學CE對CML 而言屬于一類已知風險性因素,且與預后較差相關,但預后重要性在TKI 治療中尚未進一步明確。美國血液學年會(ASH)于2018年研究中報道無CE 患者6 個月CCyR 顯著高于伴CE 患者,但2組深層分子學反應相近,且CE 似乎并不對5年臨床結局產生影響[4-5]。本研究觀察TKI 治療Ph 陽性老年慢性粒細胞白血病后檢出克隆演變對預后的影響,為治療老年慢性粒細胞白血病提供方法。
1 資料與方法
1.1 一般資料 選取2009年7月-2019年10月期間于內蒙古醫科大學附屬醫院初診為Ph 陽性的慢性髓性白血病(CML)的老年患者780 例,將一線TKI 治療后檢出CCA/Ph-的32 例老年CML患者作為研究對象,所有患者均符合CML 相關診斷標準[4],確診前均行血常規、骨髓細胞形態學、生化、骨髓活檢、細胞遺傳學和分子生物學等項目檢查。32 例患者中男性22 例,女性10 例,年齡為62~85 歲,平均年齡為(73.5±5.6)歲。相關觀察指標和研究過程均經倫理委員會審批通過,患者均簽署知情同意書。
1.2 納入和排除標準 納入標準:(1)均具有完整細胞遺傳學資料;(2)患者Ph 染色體及BCR-ABL 融合基因均為陽性;(3)均行規律性隨訪;(4)臨床依從性均良好;(5)均將TKI 作為一線治療藥,且TKI 治療時檢出CCA/Ph-。符合上述所有選項者納入本研究[5]。排除標準:(1)合并其他惡性腫瘤;(2)確診前6 個月內未行伊馬替尼(IM)治療;(3)第1年時監測頻率<2 次;(4)除TKI 外接受干擾素、骨髓移植或其他抗腫瘤藥物等治療;(5)年齡<16 歲。符合上述任意1 項者不納入本研究。
1.3 方法
1.3.1 治療方法 患者確診后均行甲磺酸伊馬替尼片(商品名:格列衛,瑞士諾華制藥有限公司,注冊證號H20100263,規格:0.1 g)治療,400 mg/次,1 次/d,治療初期行1~2 次/周血常規檢查,根據血象變化酌情增減劑量,直至血象回復平穩或達到血液學完全反應(CHR),隨后每1~3 個月進行1 次。第1年治療時,治療后第3、6 和12 個月行骨髓細胞遺傳學分析,直至到達CCyR,隨后每12 個月1 次。采用RQ-PCR進行BCR-ABL 融合基因檢測,每3 個月1 次,直至達到MMR,隨后每3~6 個月1 次,若發現BCR-ABL轉錄本升高應該每1~3 個月監測1 次。治療反應評價為失敗,警告或疾病進展時需行激酶測序分析突變,評價患者服用依從性。伊馬替尼(IM)耐藥或不能耐受時,綜合考慮患者合并癥與用藥史及病史、BCRABL 激酶區突變類型及經濟情況轉換為二代TKI:尼洛替尼膠囊(NL)(商品名:達希納,瑞士諾華制藥有限公司,注冊證號H20140334,規格:200 mg 或150 mg)或達沙替尼片(DAS)(商品名:施達賽,百時美施貴寶制藥有限公司,注冊證號H20160433,規格:20 mg 或50 mg)治療。
1.3.2 檢驗方法 進行細胞遺傳學檢測。骨髓細胞常規染色體核型分析:抽取肝素抗凝的骨髓5 mL,計數后按1.5×106/mL進行直接法制備然后采用G顯帶技術,方法為使用胰蛋白酶、其他鹽溶液或堿等處理染色體標本,后將其于Giemsa 染液中染色,完畢后染色體上會出現類似于與Q 帶但寬度及亮度均不同的橫紋,使用顯微鏡觀察,則深淺相間的帶形橫紋出現在視野中,因Q 帶和G 帶彼此對應,因此染色體表現為Q帶亮帶對應部分被Giemsa 染液染成深色帶紋,而Q帶暗帶部分呈現為淺色帶紋。分析20 個細胞,按《人類細胞遺傳學國際命名體制[ISCN (1995)]》[6] 進行核型描述,核型分析鑒定至少需2 人共同參與操作。熒光原位雜交技術(FISH):抽取肝素抗凝的骨髓5 mL,制備染色體玻片,目標探針變性,將變性的DNA探針10L 加至標本上,蓋上蓋玻片并封片,制備玻片標本,后將其玻片放置于熒光顯微鏡之下,采用20×物鏡掃描樣品雜交區域,從中選取分散最佳的區域,后采用40×或100×物鏡,并在三色或多色熒光激發觀察,視野中出現不同顏色的熒光圖像,后選擇一定方向進行計數,計數至少300 個間期細胞[7]。分子生物學監測:采用實時定量聚合酶鏈反應(RQ-PCR)法檢測監測BCR-ABL 轉錄本水平,檢測標本可為外周血(不少于8 mL),后采用紅細胞裂解液獲取紅細胞后,收集白細胞,其后使用TRIzol 試劑(美國Invitrogen 公司)處理,經氯仿萃取,后使用異丙醇沉淀獲取RNA。采用基因擴增儀(美國Biorad 公司,型號:伯樂T100)及實時RQ-PCR 檢測儀(美國羅氏公司,型號:LC480)檢測,設置內參基因為ABL。采用BCR-ABL(P210)定量檢測試劑盒(上海源奇生物科技有限公司)獲取標準曲線,后進行標本檢測及計算。BCR-ABL 水平檢測值(BCR-ABL/ABL)=BCR-ABL 拷貝數/ABL 拷貝數×100%。BCR-ABL 國際標準值(IS)=BCR-ABL 水平檢測值×轉換系數(CF)[8]。
1.3.3 療效判定方法 (1)完全血液學反應:患者的WBC 在10×109/L 以下,PLT 在450×109/L 以下,外周血中無髓性不成熟細胞,嗜堿粒細胞<0.05,脾大消失為完全血液學反應(CHR);(2)完全和部分細胞遺傳學反應:患者骨髓中Ph (+) 細胞數為0%即為完全細胞遺傳學反應(CCyR);患者的Ph(+)細胞數≤35%即為部分細胞遺傳學反應(PCyR);(3)主要分子學反應:患者的BCR-ABLIS≤0.01%(ABL 拷貝數>10 000)稱為主要分子學反應(MMR);(4)MR4.5:MR4.5 定義為骨髓或外周血標本連續2 次檢測BCRABLIS≤0.0032%(ABL 拷貝數>32 000)或ABL 拷貝數>32 000 時無法檢測的疾病微小殘留;(5)穩定的 MR4.5:穩定的MR4.5定義為 BCR-ABLIS≤0.0032%,持續至少2年[9-10]。(6)事件定義:總生存(OS) 時間指的是從TKI 開始治療,到任何誘因致使患者死亡或者最后一次隨訪結束;(7)無事件生存(EFS) 時間:從TKI 開始治療,到治療期間發生下述任何1 項事件結束:喪失CHR、CCyR 及MMR;病情已進展到CML 加速期(AP)或者急變期(BP);發展成為Ph 染色體陰性急性髓系白血病(AML);任何誘使患者死亡因素以及隨訪活動結束[11]。
1.3.4 隨訪采用門診、微信、電話或訪視等方式從TKI開始治療時定期隨訪,并與患者預約復查時間[10]。
1.4 觀察指標(1)分析檢出CCA/Ph-老年CML 患者基線資料及CCA/Ph-特征;(2)分析32 例老年患者總體療效;(3)分析32 例老年患者生存情況;(4)影響老年CML 患者生存的單因素分析;(5)影響老年CML 患者生存的多因素分析。
1.5 統計學分析 應用SPSS22.0 統計軟件進行數據處理。計量資料以均數±標準差(±s)表示,采用獨立樣本t 檢驗;計數資料以例數和百分率表示,采用2檢驗。n<40 或T<1 時采用Fisher 檢驗。分析生存情況,將單因素中P<0.05 的影響性因素納入多因素分析,采用Logistic 多元回歸分析影響生存率的因素。P<0.05 為差異有統計學意義。
2 結果
2.1 分析檢出CCA/Ph-老年CML 患者基線資料及CCA/Ph-特征 伴CCA/Ph-老年CML 患者32 例中男性22 例(68.7%)、女性10 例(31.3%)。于TKI 開始治療時,28 例CP、3 例AP、1 例BP;TKI 治療時于14 (3~92) 個月首次出現CCA/Ph-,且有11 例(34.4%)調整藥物為二線NL 或DAS。首次伴CCA/Ph-的克隆比例≥50%有19 例(59.4%),且12 例(37.5%)反復性出現CCA/Ph-,20 例(62.5%)CCA/Ph-出現為一過性(隨訪僅1 次)。CCA/Ph-異常類型:以+8 為主有19 例(59.4%),以-7/7q-為主有5 例(15.6%)。見表1。
2.2 分析32 例老年患者總體療效 32 例伴CCA/Ph-老年CML 患者TKI 治療后均獲取CCyR,獲取中位時間13 (3~59) 個月,且15 例(46.9%) 于初次給藥3個月后檢驗BCR-ABLIS,其水平≤10%。當隨訪中位時間50 (11 ~132) 個月時,患者中75.0% (24/32)療效維持在CCyR;62.5%(20/32)分子學反應為MMR,且獲取中位時間為31 (4-73) 個月。-7/7q-為主的5 例老年患者中l 例應用TKI 治療失敗且首次染色體核型檢出-7、9q-,被確診克隆演變Ph 陰性AML(急性骨髓性白血病),其余3 例患者療效為MMR(2例)及CCyR(1 例)。
2.3 分析生存情況 隨訪中位時間50 個月時32 例患者平均EFS 時間:45 個月,且平均2年、5年的EFS 率分別為(83.5±7.1)%、(52.5±9.3)%。32 例患者中總生存中位時間為50 個月時,平均2年、5年的OS率分別為(92.3±5.1)%、(77.3±9.6)%。32 例患者中3 例(9.4%)死亡:2 例死于Ph 陰性AML,l 例BP 患者死于復發。
2.4 影響老年CML 患者生存的單因素分析32 例老年患者EFS 率(2年)與性別、TKI 給藥3 個月BCRABLIS 水平、CCA/Ph-出現頻率相關(<0.05),OS率(2年)與CCA/Ph-出現頻率相關(<0.05)。CCA/Ph-異常類型組間EFS 率(2年)及OS 率(2年)差異無統計學意義(>0.05),但以-7/7q-為主異常患者的EFS 率(2年)及OS 率(2年)相比以+8 為主異常患者的EFS 率(2年)及OS 率(2年)較低。見表2。
2.5 影響老年CML 患者生存的多因素分析 采用TKI治療時影響老年CML 患者EFS 率的獨立性危險因素是反復出現 CCA/Ph- [OR=4.758,95%CI(1.22-18.591),<0.05]。患者OS 率單因素分析中僅存在1個因素即CCA/Ph-出現頻率(<0.05),因此未進行OS 率的多因素分析。見表3。
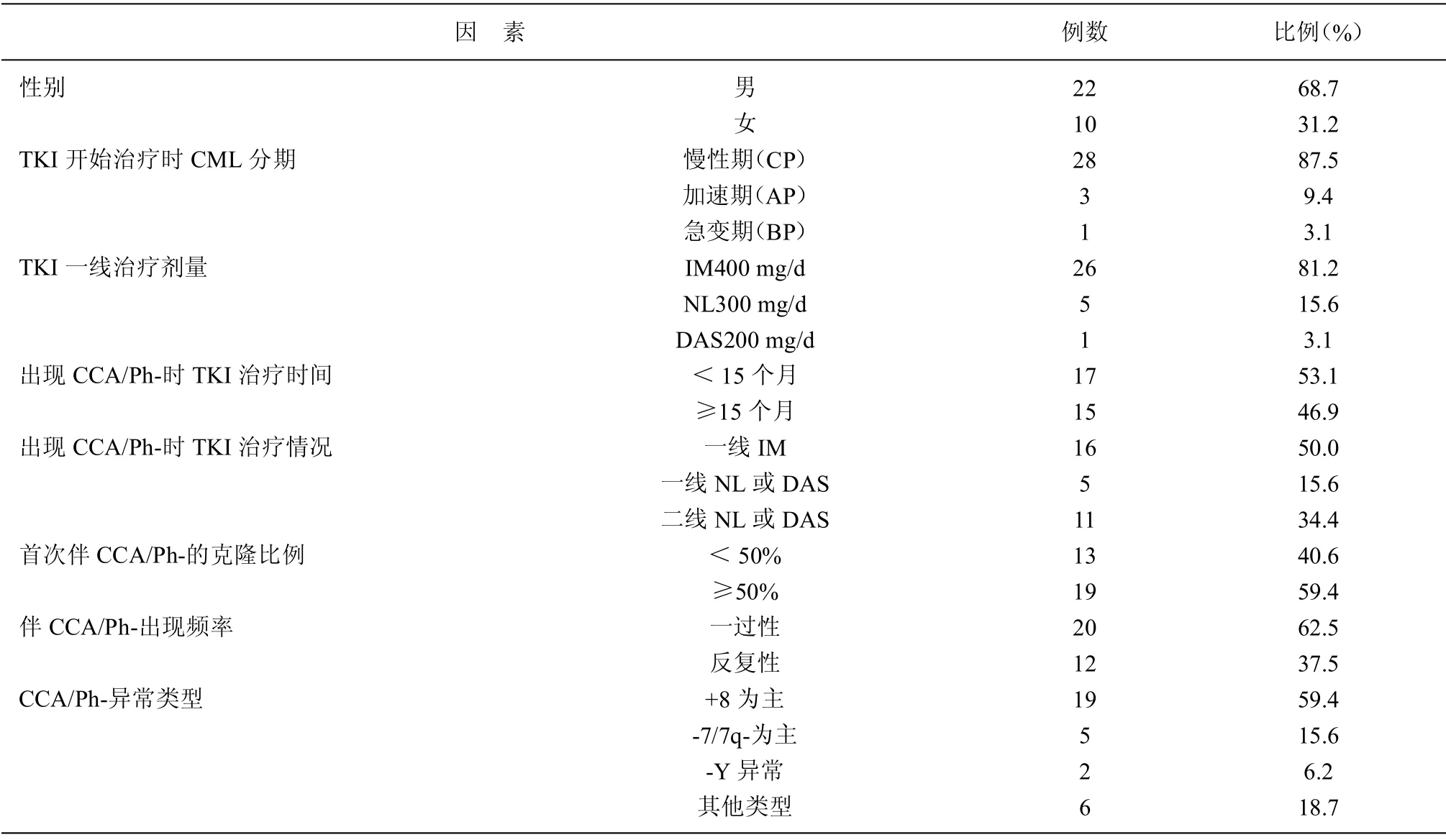
表1 分析檢出CCA/Ph-老年CML 患者基線資料及CCA/Ph-特征

表2 影響老年CML 患者生存的單因素分析

表3 影響老年CML 患者EFS 率的多因素分析
3 討論
CML) 是一種血液惡性腫瘤,其典型特征為Ph陽性染色體出現克隆性增殖演變,其治療主要采用TKI 作為一線藥物,但治療期間伴有Ph 陽性核型反應或Ph 陰性克隆演變,出現上述變化則表明治療失敗或病情進展,提示預后較差[11]。臨床大數據研究[12] 發現TKI 治療CML 時發生CCA/Ph-的幾率為3.5%~10.0%,而本研究發現TKI 治療CML 時CCA/Ph-發生率為4.1%(32/780),二者研究結果相符。
臨床研究[13] 發現在采用TKI 治療CML 時出現CCA/Ph-的時間范圍是7~18 個月,且基本會獲取不同細胞遺傳學反應(CyR)。本研究發現TKI 治療32 例老年CML 患者時于14 個月首次出現CCA/Ph-,而獲取CCyR 的中位時間為13 個月,二者研究結果一致。本研究采用TKI 治療CML 時檢出CCA/Ph-的例數為32 例,CCA/Ph-的染色體異常類型中以+8 為主有19 例(59.4%),以-7/7q-為主有5 例(15.6%),提示本研究780 例CML 患者中檢出CCA/Ph-的克隆演變中以+8 為主,其次為-7/7q-。
大部分臨床研究并未對檢出CCA/Ph-克隆演變對CML 患者預后的影響價值進行仔細的探索,研究相對欠缺,且檢出CCA/Ph-對預后的意義仍處于爭論階段[13-14]。國外臨床研究[15] 報道采用甲磺酸伊馬替尼治療后,療效為PCyR 的CML 患者中檢出克隆演變患者與未檢出患者的5年OS 率及EFS 率比較差異無統計學意義。本研究隨訪50 個月時32 例患者平均EFS 時間45 個月,5年EFS 率為(52.5±9.3)%;OS 平均時間為50 個月,5年OS 率為(77.3±9.6)%。在影響因素分析中將CCA/Ph-的異常類型、CCA/Ph-的出現頻率、出現CCA/Ph-時TKI 治療、伴CCA/Ph-的克隆比例、患者性別及TKI給藥3 個月BCR-ABLIS水平6 項影響因素納入分析,研究上述因素對老年CML 患者2年OS 率及EFS 率的相關性,結果發現,32 例老年患者EFS 率(2年)與性別、TKI 給藥3 個月 BCR-ABLIS 水平及 CCA/Ph-出現頻率相關(P<0.05),OS 率(2年)與CCA/Ph-出現頻率相關(P<0.05)。CCA/Ph-異常類型組間以+8 為主異常與以-7/7q-為主異常的患者生存率存在差異,其原因可能與不同CCA/Ph-異常類型的增殖、CE 特點存在較大差異及CCA/Ph-異常類型存在一定的不穩定性相關[16-18]。
本研究將影響老年CML 患者EFS 率(2年)的單因素納入多因素分析,并采用多元回歸方程分析后發現,采用TKI 治療CML 時影響老年CML 患者EFS率的獨立性危險因素是反復出現CCA/Ph- [OR=4.758,95%CI(1.22-18.591),<0.05]。TKI 作為一線藥物治療CML 時老年CML 患者反復出現CCA/Ph-是影響患者生存的獨立性風險因素。上述研究中發現CCA/Ph-具有較強的遺傳學異質性,因此老年CML 患者在采用TKI 作為一線藥物治療時,若出現CCA/Ph-則需要嚴格篩查患者染色體異常變化,并與該克隆演變的遺傳學特征、獲得的細胞細胞遺傳學反應及分子生物學反應進行綜合性評價患者病情治療及進展情況[19-21]。若治療期間CCA/Ph-反復性出現即≥2 次,則需警惕病情是否存在進展的風險,而在染色體核型檢查中出現以-7/7q-為主的CCA/Ph-則要警惕是否存在病情轉化的風險,并及時為患者調整治療方案[22-24]。
本研究對TKI 作為一線藥物治療CML 且檢出Ph染色體克隆演變的老年CML患者預后情況進行觀察,并綜合細胞遺傳學、分子生物學及臨床檢驗多項技術,分析影響其生存的單因素及多因素,發現TKI 作為一線藥物治療CML時老年CML患者反復出現CCA/Ph-是影響患者生存的獨立性風險因素。但本研究納入樣本數量較少,并未將確診后未采用TKI 作為一線藥物治療的老年CML 患者納入研究,且本研究也并未對TKI二線藥物轉換治療后能否逆轉異常克隆情況進行分析,因此在后續進一步的臨床研究中將上述問題納入其中,進行深入探討。

