響應面法優化超聲輔助提取杜仲葉中的綠原酸
吳紅艷,彭呈軍,鄧后勤,*
(1.湖南農業大學食品科學技術學院,湖南長沙410128;2.慈利縣九九農業開發有限公司,湖南張家界427200)
杜仲(Eucommia ulmoides Oliver),屬杜仲科,具有抗氧化、降血壓[1]、強筋健骨[2]、改善糖代謝、補肝腎[3-4]等功效。現代研究發現,杜仲葉與杜仲皮具有相似的功能成分和藥理作用[5],含有蘆丁[6]、綠原酸、杜仲膠[7]、桃葉珊瑚苷[8]、槲皮素、京尼平苷酸、山奈酚等化學成分,綠原酸和黃酮類化合物是杜仲葉的主要活性成分。綠原酸具有較強的抗衰老、清除自由基、殺菌、抗病毒、抗癌、降血脂、保護心血管等作用[9-14]。因此,杜仲葉綠原酸的提取開發成為研究者關注的重點[15]。
綠原酸屬于半水合物,為針狀結晶水,是由咖啡酸和奎尼酸形成的酯。國內對于杜仲葉綠原酸提取方法的研究較多,主要有超聲波輔助提取法[16]、水提取法[17]、微波輔助提取法[18]、酶提取法[19-20]等,而國外相關的研究較為缺乏。在從植物提取過程中,一般采用極性較強的水[21]、乙醇[22-23]、甲醇、丙酮等提取溶劑。
單因素試驗效率高,但只能確定大致的參數范圍,正交試驗設計可尋找最佳因素水平組合,但是不能給出明確的回歸方程,無法找到最佳組合和響應值的最優值,因此,傳統的單因素試驗和正交試驗已經不能滿足提取工藝優化要求[24],基于響應面分析方法不僅能夠縮短試驗優化時間,而且能夠快速建模,因此,本文在單因素試驗基礎上,通過響應面法分析提取時間、甲醇體積分數、提取溫度、超聲功率對杜仲葉中綠原酸提取得率的影響,以期為杜仲葉綠原酸的提取工藝提供參考。
1 材料與方法
1.1 材料與試劑
杜仲葉8 號:湖南省慈利縣九九農業開發有限公司;綠原酸對照品(純度≥99%):成都曼思特生物科技有限公司。
甲醇(色譜純)、乙酸(優級純)、乙腈(色譜純):國藥集團。
1.2 儀器與設備
安捷倫1100 型高效液相色譜儀:美國安捷倫公司;DTY-A220 型電子天平:美國康州HZ 電子科技有限公司;TF-FD-1L 型冷凍干燥機:上海拓紛機械設備有限公司;KM-300DE 型中文液晶超聲波清洗器:昆山美美超聲儀器有限公司;LH-08B 型中藥粉碎機:浙江省溫嶺市創力藥材器械廠制造。
1.3 試驗方法
1.3.1 樣品的預處理
杜仲葉清洗后于零下80 ℃冷凍干燥機內進行冷凍干燥,用中藥粉碎機將干燥后的杜總葉粉碎后過60目篩,篩過的葉粉在4 ℃冰箱內保存待用。
1.3.2 綠原酸的提取
稱取0.5 g~2.0 g 粉碎均勻的試樣(精確到0.001 g)于25 mL 比色管中,加入20 mL 一定體積分數的甲醇,在一定的超聲功率下提取一定的時間后,用一定體積分數的甲醇定容到 25 mL,混勻,過 0.22 μm 濾膜,濾液供液相色譜分析。試樣中綠原酸的提取得率按下面公式計算:
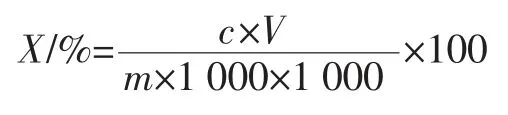
式中:X 表示試樣中綠原酸含量,%;c 表示由標準曲線求得進樣液中綠原酸的濃度,μg/mL;V 表示試樣定容體積,mL;m 表示試樣質量,g。
1.3.3 標準曲線的繪制
稱取綠原酸標準品0.02 g 于10.0 mL 容量瓶中,加流動相溶解并定容至刻度,混勻,制得綠原酸標準儲備液,準確量取1.00 mL 綠原酸標準儲備液于10.0 mL容量瓶中,用流動相稀釋至刻度,混勻,得綠原酸標準使用液,分別吸取綠原酸標準使用液并在容量瓶中定容的濃度分別為 2.00、10.0、20.0、40.0、80.0 μg/mL 標準系列,每個樣品重復3 次,分別進樣,記錄峰面積,繪制標準曲線,得回歸曲線方程為Y=13.206 6x-11.983,R2=0.999 6,其中 Y 為綠原酸峰面積(mAU·S),x 為進樣量(μg/mL),結果表明綠原酸在 2 μg/mL~80 μg/mL范圍內線性關系良好。
1.3.4 單因素試驗
1.3.4.1 考察提取時間
準確稱取0.5 g 杜仲葉粉末于25 mL 試管中,在甲醇體積分數50%,溫度60 ℃,超聲功率180 W 的條件下,分別提取 15、30、45、60、75 min,然后過濾,稀釋相同倍數,待測。
1.3.4.2 考察甲醇體積分數
準確稱取0.5 g 杜仲葉粉末于25 ml 試管中,設置溫度60 ℃,超聲功率180 W,加入體積分數為40 %、50%、60%、70%、80%的甲醇20 mL 于試管中超聲提取45 min。過濾,稀釋相同倍數,待測。
1.3.4.3 考察超聲功率
準確稱取0.5 g 杜仲葉粉末于25 mL 試管中,設置溫度60 ℃,甲醇體積分數50%,在超聲功率分別為150、180、210、240、270 W 的條件下提取 45 min。過濾,稀釋相同倍數,待測。
1.3.5 色譜條件
色譜柱:C18色譜柱(250 mm×4.6 mm,5 μm),柱溫35 ℃,流速 1.0 mL/min,流動相:0.5%乙酸溶液+乙腈=9+1,檢測波長 327 nm,進樣量 20 μL。
1.4 數據處理
采用Design Expert 10(32-bit)軟件設計響應面優化試驗,采用OriginPro 8.5 軟件繪制試驗數據圖。
2 結果與分析
2.1 單因素試驗
2.1.1 提取時間對提取得率的影響
在溫度60 ℃,提取功率180 W,甲醇體積分數50%的條件下,考察提取時間對提取得率的影響,結果如圖1 所示。
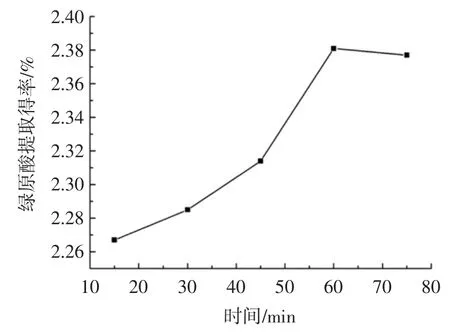
圖1 提取時間對提取得率的影響Fig.1 Effect of extraction time on extraction yield of chlorogenic acid
從圖1 可以看出,在超聲波輔助提取的作用下,綠原酸的提取得率隨時間變長而逐步增加,在60 min 時達到最大值,隨后減小。這可能是因為提取時間的延長,可能導致綠原酸的結構被破壞[25]以及雜質的溶出。因此,選擇最佳提取時間為60 min。
2.1.2 甲醇體積分數對提取得率的影響
在溫度60 ℃,提取功率180 W,提取時間45 min條件下,考察甲醇體積分數對提取得率的影響,結果如圖2 所示。
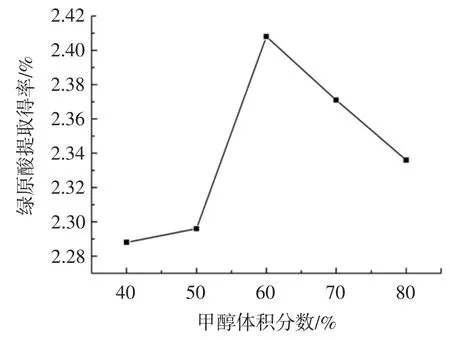
圖2 甲醇體積分數對提取得率的影響Fig.2 Effect of methyl alcohol mass fraction on extraction yield of chlorogenic acid
從圖2 可以看出,綠原酸提取得率在甲醇體積分數為60%左右最高。由于綠原酸結構特殊,含有很多極性不同的化學鍵,往往通過分子內酯基遷移或水解而產生異構化,彼此最適合的溶劑極性各不相同。因此,綠原酸的提取得率會隨著甲醇體積分數的增加先增大后減小。李輝等[26]比較了水、甲醇、乙醇、乙酸乙酯、丙酮等不同極性的溶劑對杜仲葉綠原酸提取率的影響,發現以甲醇為溶劑時,綠原酸提取率最高,丙酮為提取劑時提取率最低,用水提取時,植物中的蛋白質、淀粉等也會被提取出來,導致綠原酸提取率較低。
2.1.3 超聲功率對提取得率的影響
在溫度60 ℃,甲醇體積分數50%,提取45 min 的條件下,考察超聲功率對提取得率的影響,結果如圖3所示。
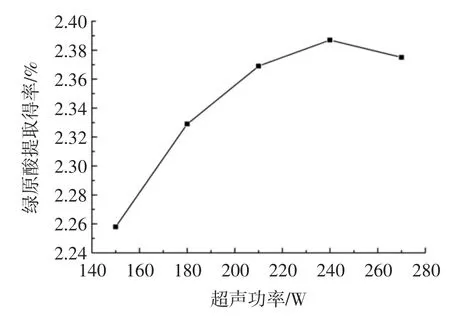
圖3 超聲功率對提取得率的影響Fig.3 Effect of ultrasound power on extraction yield of chlorogenic acid
從圖3 可以看出,綠原酸的含量與超聲功率呈正相關,隨著超聲功率的增大,綠原酸的含量逐漸增大,在功率較低的條件下,其增大不是很明顯,在240 W 時達到最大值。因此,選擇240 W 為最佳超聲提取功率。
2.1.4 提取溫度對提取得率的影響
在甲醇體積分數50%,提取功率180W,提取45min條件下,考察溫度對提取得率的影響,由于超聲清洗儀器在低于40 ℃溫度不穩定,故只選擇4 個因素水平,結果如圖4 所示。
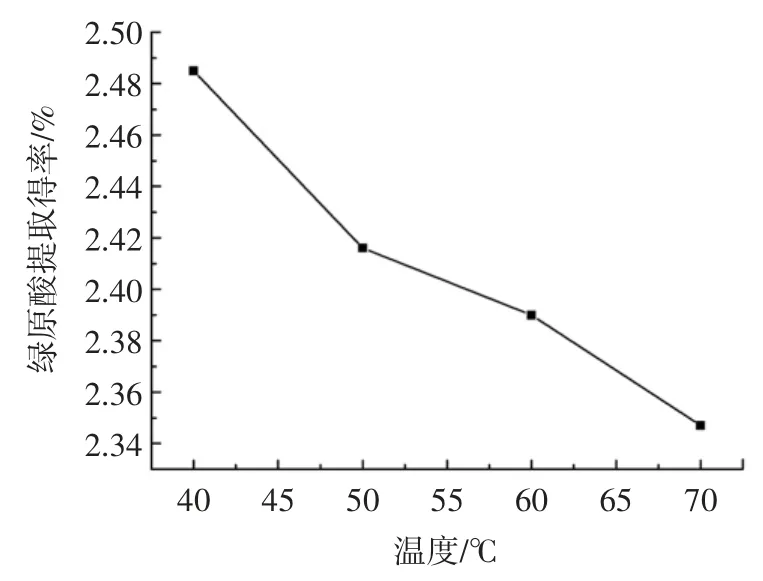
圖4 提取溫度對提取得率的影響Fig.4 Effect of extraction temperature on extraction yield of chlorogenic acid
從圖4 可以看出,綠原酸的提取得率與提取溫度呈負相關,隨著提取溫度的升高,綠原酸的提取得率逐漸降低,這是因為綠原酸為熱敏性物質,本身不穩定,在高溫條件下,其分子結構中的酯鍵、不因素飽和雙鍵等不穩定部分發生斷裂,失去活性,從而降低得率[27],所以適宜的提取溫度為40 ℃,而曾橋等[28]研究了杜仲葉茯磚茶中綠原酸最佳提取溫度為60 ℃,這是因為兩者采用的試驗原料不同,茯磚茶在加工過程中會經過汽蒸渥堆、干燥等高溫處理過程,因此茯磚茶中綠原酸的最佳提取溫度會相對偏高。
2.2 響應面優化杜仲葉中綠原酸的提取工藝
2.2.1 響應面試驗設計及結果
選取提取時間(A)、甲醇體積分數(B)、超聲功率(C)對杜仲葉中綠原酸的提取工藝進行優化。具體設計方案見表1。

表1 響應面試驗因素水平表Table 1 Factors and levels in response surface design
為優化超聲輔助提取杜仲葉中綠原酸的工藝條件,采用經典的三因素三水平Box-Behnken 試驗設計,在單因素試驗基礎上,精密稱取0.5 g 左右的杜仲葉粉末于比色管中,由于超聲清洗儀在低于40 ℃時溫度不穩定,所以選取提取時間(A)、甲醇體積分數(B)、超聲功率(C)對杜仲葉中綠原酸的提取工藝進行優化。具體結果表2。
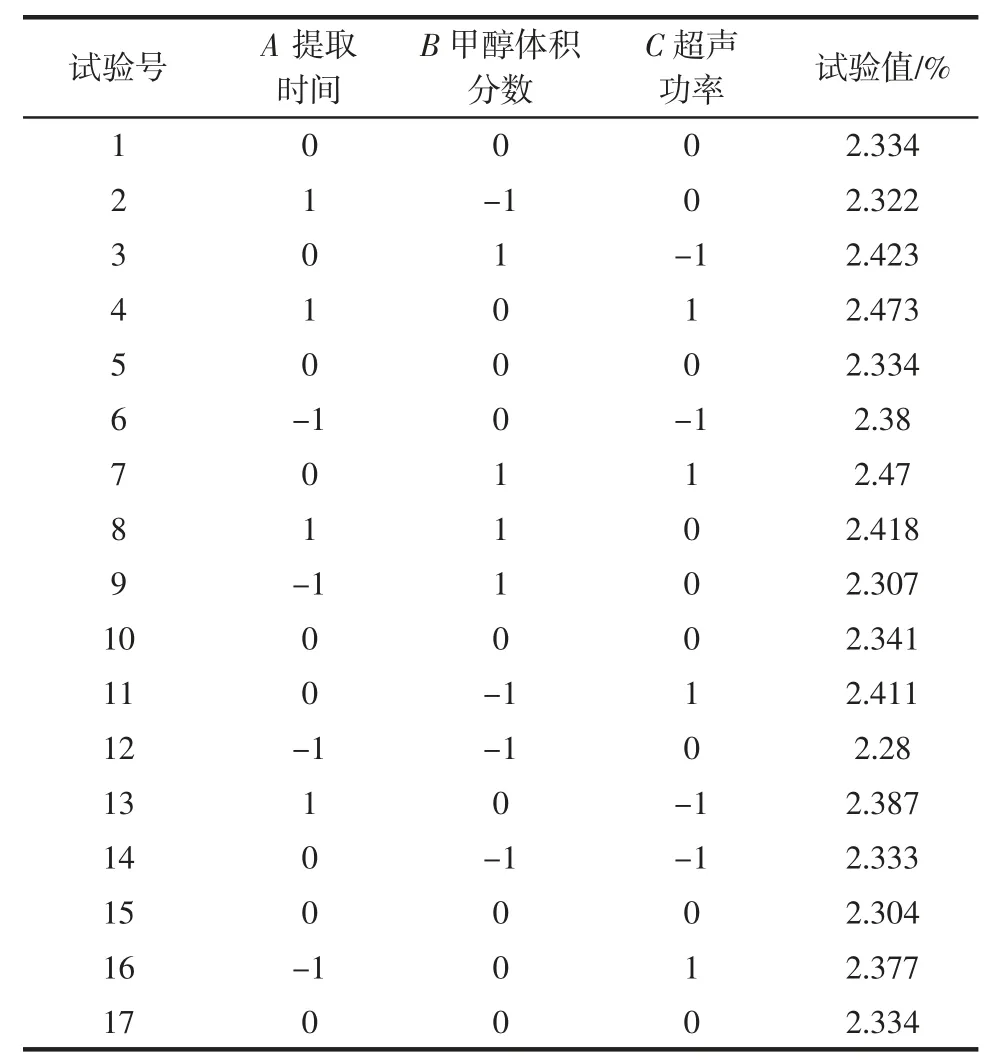
表2 響應面試驗方案及結果Table 2 Scheme and experimental results of response surface design
2.2.2 模型評價
利用Design-Expert 軟件對表2 試驗數據進行二次多項式回歸擬合,得到的數學模型為:
Y=23.29+0.32A+0.34B+0.26C+0.17AB+0.22AC-0.078BC-0.013A2+0.037B2+0.76C2
模型方差分析結果和各項系數顯著性檢驗結果列于表3。
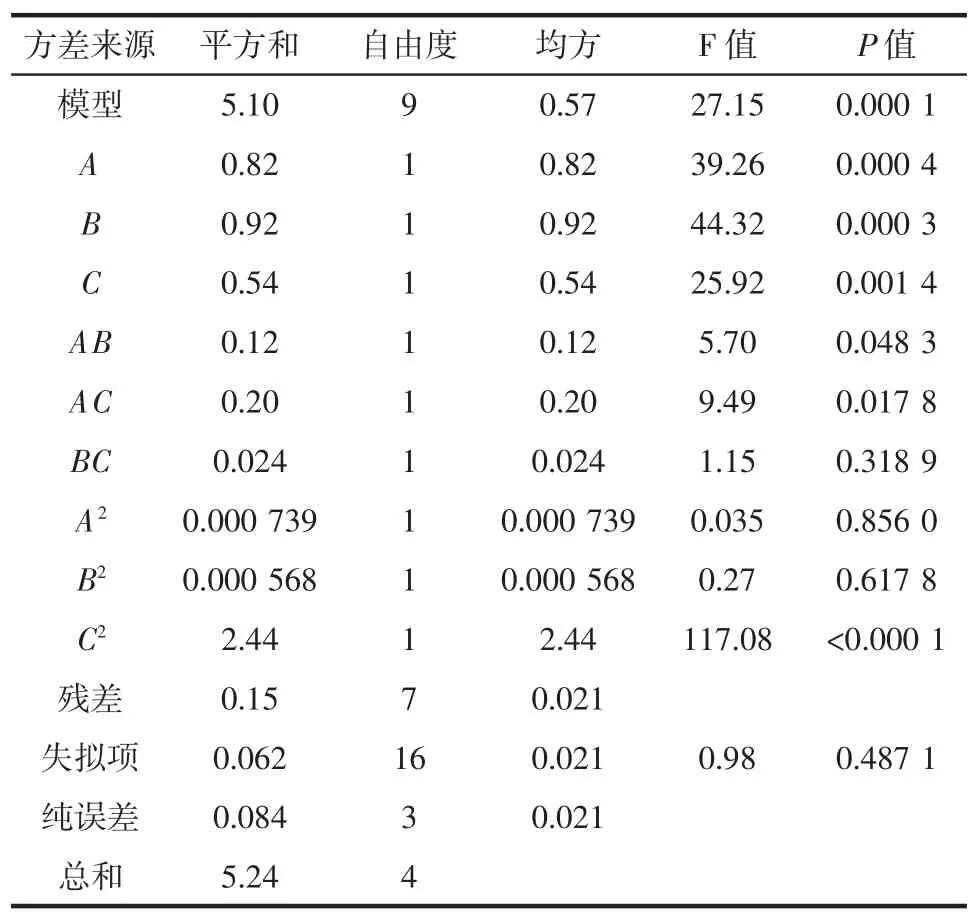
表3 回歸模型各項方差分析Table 3 Variance analysis of regression model
從表3 可以看出,模型的F=27.15、P=0.000 1<0.05,說明本試驗所采用的二次模型是很顯著的。PA、PB、PC、PAB、PAC、PC2均小于 0.05,說明提取時間、甲醇體積分數、超聲功率、時間與甲醇體積分數的交互作用、時間與超聲功率的交互作用及超聲功率的二次項具有顯著影響,而甲醇體積分數與超聲功率的交互作用、甲醇體積分數的二次項和提取時間的二次項的顯著性較差,失擬項不顯著表明試驗誤差小,決定因素R2=0.972 1,也說明模型能夠很好地反應響應值的變化,擬合度好。同時,各因素的效應關系為甲醇體積分數>提取時間>超聲功率。
2.2.3 響應面分析
響應面優化綠原酸提取,得出3D 模型圖,見圖5。
由圖5 可知,當提取時間和超聲功率都固定時,綠原酸含量隨甲醇體積分數的變化幅度較大,而綠原酸含量隨著提取時間以及超聲功率的變化幅度較小,所以,甲醇體積分數的影響較為顯著。通過最優化分析,最佳的提取條件為提取時間75 min,甲醇體積分數70%,超聲功率270 W,提取溫度40 ℃,預測值為2.532%,在此條件下進行試驗驗證,綠原酸的含量為2.529%,與預測值基本相符,證實了該方程的準確性和實用性。
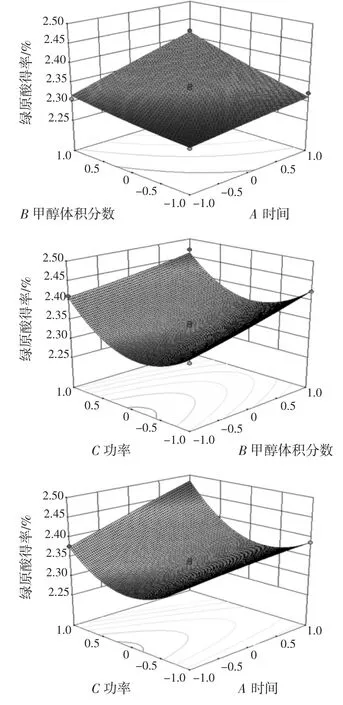
圖5 各兩因素的響應面和等高線圖Fig.5 Response surface and contour plots showing the pairwise interactive effects of three factors on extraction yield of chlorogenic acid
2.2.4 試驗結果驗證
在得出最佳提取條件的情況下,做3 次平行試驗對預測結果進行驗證,驗證結果如圖4 所示。
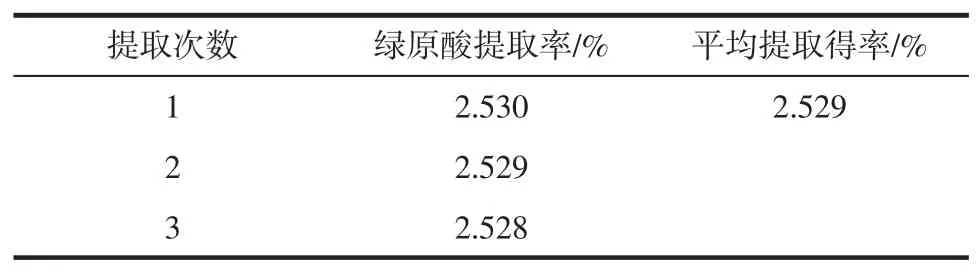
表4 最佳工藝條件及其驗證響應面Table 4 Results of validation experiments under optimized extraction conditions
經過3 次平行試驗,綠原酸實際含量為2.529%,與2.532%相比,相差0.003%,說明此方程與實際情況擬合良好,建立的模型可靠。
3 結論與討論
與傳統的提取溶劑不同的是,本文采用一定體積分數的甲醇作為提取溶劑,將甲醇與水結合作為提取劑,從提取效率和節約成本上來說很有意義。通過單因素試驗及響應面法對超聲輔助提取杜仲葉中的綠原酸的工藝條件進行優化,獲得最佳提取條件為:提取時間75 min,甲醇體積分數70%,超聲功率270 W,提取溫度40 ℃,在此條件下,綠原酸的含量達到2.529%,與預測值相符。
王柏強等[29]利用纖維素酶來提取杜仲葉綠原酸,考察酶解時間、溫度、pH 值等因素對杜仲葉綠原酸提取率的影響,正交試驗優選出最佳提取條件下綠原酸提取得率為2.37%。鄧愛華[30]通過響應面法優化杜仲葉中綠原酸提取工藝,最佳提取參數為:40%的乙醇,料液比 1 ∶11(mg/mL),提取溫度61.4 ℃,提取率為 0.872 8%。魏銳[31]以水為提取劑提取杜仲葉綠原酸,響應面工程數學法優化提取工藝,在最佳提取工藝條件下,杜仲葉綠原酸提取得率為1.67%。與上述文獻相比,本研究杜仲葉綠原酸提取得率最高為2.529%,這當然是假設以上研究的杜仲葉綠原量相同的情況下的比較結果;相較于其他3 種提取溶劑,一定體積分數的甲醇更適合作為杜仲葉綠原酸的提取溶劑,這為杜仲葉綠原酸提取的工業化生產提供了理論依據。

