流動相pH值對離子型物質分離的影響
劉珍 王彥 閆超
(上海交通大學藥學院 上海 200240)
在多物質的液相色譜分離過程中,常常包含有酸堿離子型化合物,除了通過篩選色譜柱、更改流動相種類和比例等方式外,調節流動相的pH值常常是改善該類物質分離度的有效手段。本文從理論上進行分析,并且輔以具體的實例,闡述了這一行為在色譜分離中的應用和注意事項。
1.流動相pH值對分離的影響
流動相的pH值對酸堿離子型的物質影響最為顯著,其保留與pH值的關系有詳細的理論分析[1]。簡單來說,酸性物質在低pH條件下呈分子態,保留較強;在高pH條件下呈離子態,保留較弱。堿性物質在高pH條件下呈分子態,保留較強;在低pH條件下呈離子態,保留較弱。
對于中性物質,保留時間一般不受pH值影響,重現性相對比較好;對于離子型物質,如上所述,在一定的pH值范圍內,保留時間受pH值影響很明顯,特別是臨近pKa附近,微小的pH值波動就可能使保留時間出現較大的變化,導致方法的重現性較差。
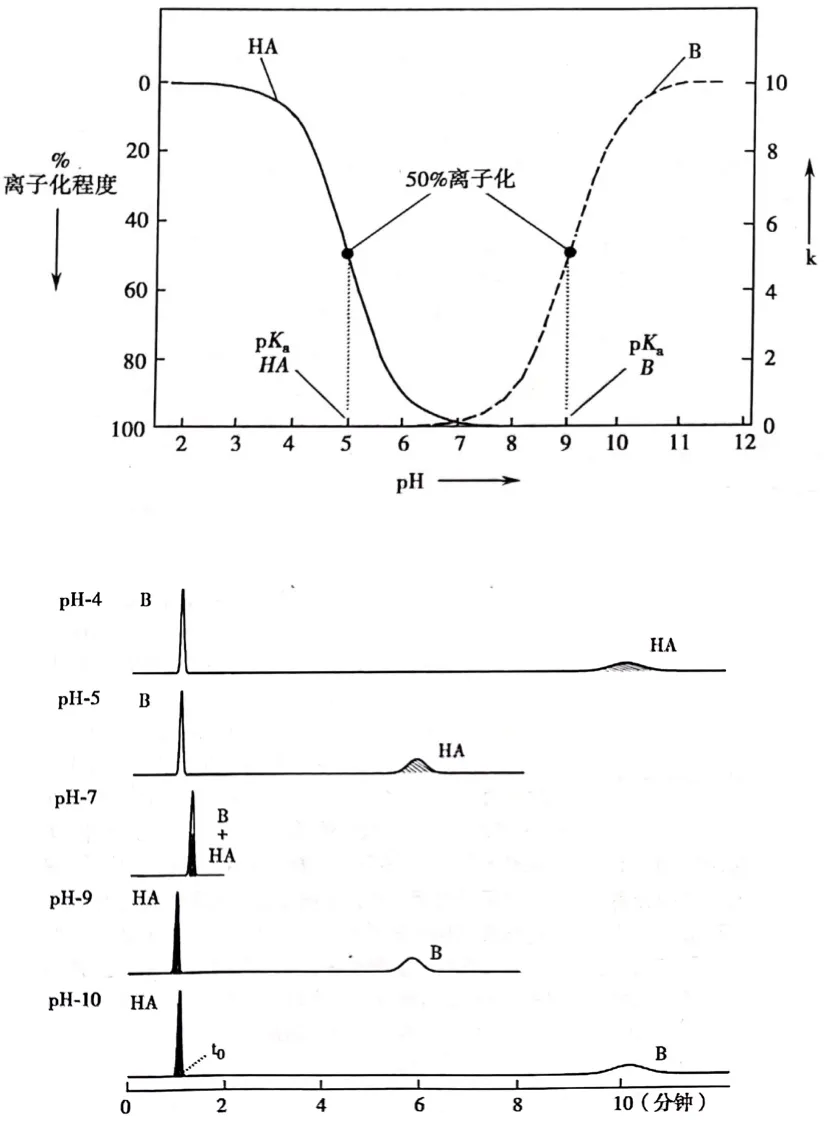
圖1 不同pH值下離子型物質的分子-離子態轉化和保留時間的變化
離子型物質的離子化過程如下:

上圖從微觀和宏觀上很好的描述了這種現象[2]。
pH≤4時,酸性物質HA主要以分子態[HA]形式存在,在色譜圖上表現為較強的保留(10min);堿性物質B以離子態的[BH+]形式存在,色譜圖上表現為幾乎無保留(1min)。
pH=5時,酸性物質HA呈50%離子化狀態,在色譜圖上表現為保留減弱(6min);堿性物質B在此pH下仍舊以離子態[BH+]形式存在,色譜圖上仍無保留。
pH=7時,酸性物質HA和堿性物質B均主要以離子態[A-]和[BH+]形式存在,表現在色譜圖上為兩者均無保留(重合,1min)。
pH=9時,酸性物質HA呈完全離子化狀態,色譜圖上無保留;堿性物質B呈50%離子化狀態,在色譜圖上表現為保留增強(6min)。
pH≥10時,酸性物質HA仍呈完全離子化狀態,色譜圖上無保留;堿性物質B主要以分子態[B]形式存在,在色譜圖上表現為較強的保留(10min)。
2.合理認識流動相pH值在分離中的作用
pKa是一把雙刃劍。我們一方面希望流動相體系的pH值遠離被分離物質的pKa來獲得穩定的保留時間,但對于十余個物質的混合溶液,常常沒法避開所有物質的pKa;從另一個方面來說,正因為有pKa的存在,當酸、堿物質的流動相體系處于pKa附近時,保留時間可以很容易被精細調整,使得分離的可能性大大增加。
在實際的方法開發過程中,我們通過各個待分離物質的化學結構式就能大致判斷哪些物質是pH值敏感型。但這些pH值敏感型物質在哪一個pH值范圍段內敏感?敏感到什么程度?峰型如何?這些數據往往需要通過實驗來系統的了解,我們可以在大范圍的pH值內(如pH值=2,4,6,8,10)進行初篩,然后根據結果進行小范圍的pH微調。
需要注意的是,上述分子-離子態轉化對離子型物質的保留時間有非常顯著的影響,但不同pH環境只是影響該類物質保留的因素之一。對于結構較復雜的離子型物質,對保留行為起主要作用的可能是該物質中其他結構與固定相的作用力,比如芳香族離子型分析物在苯基柱上,起主要作用的可能是π-π作用,不同pH值下分子-離子態對保留時間的敏感程度可能相對較低。因此,進行pH值的篩選,應盡可能減少其他作用力,減少各影響因素。建議在封端的未進行鍵合基團改造的單純C18鍵合相的色譜柱上進行,其色譜行為更加可控。在各因素未能充分研究透徹的情況下,單因素考察是一個非常簡單有效的方式,可以提供規律性更強的信息。
3.pH值調節在色譜分離中的應用
在一種降壓藥中8個雜質與主成份的分離試驗。在8個待研究的雜質中,有2個堿(雜質A和F),1個酸(雜質C),理論上來說,流動相的pH值能顯著影響這些物質的保留。
選用pH值耐受范圍為1-12的Waters XBridge C18色譜柱,磷酸鹽-乙腈體系梯度洗脫。

圖2 8個雜質在流動相pH4.0-pH10.0的色譜圖
上述雜質中,雜質A和雜質F是帶有-NH2結構的堿性物質,在低pH下呈離子態,保留較弱,隨pH升高而保留增強;雜質C是帶-COOH結構的可電離的復雜物質,在高pH下呈離子態,保留較弱,隨pH降低而保留增強。
上圖中可以明顯看出這些酸堿雜質隨流動相pH變化導致保留時間變化的情況,可以收集到如下信息:
(1)堿性雜質F在pH6.0~pH8.0對流動性pH值最敏感。
(2)堿性雜質A在pH6.0以下時,對流動相pH較為敏感,pH在6.0以上,保留時間趨于穩定。
(3)酸性雜質C在pH值6.0以下時,對流動相的pH較為敏感;且在pH6.0以下時,可能因其分子態/離子態同時存在而導致峰形拖尾現象;當pH值在6.0以上時,電離較為完全,保留時間基本固定。
(4)pH8.0~10.0間,雜質F和C分離度較小,且位置互換,應盡量避免此段。
初篩4個pH后,考慮到雜質C的峰形,且雜質F在雜質A和C的空間要大于雜質C和G的空間,最終細篩pH值為7.7,各雜質的分離度和峰型良好。
4.討論
離子型物質的分離還有其他的選擇,如使用離子對試劑增強保留時間和達到分離的目的。但離子對分析方法本身存在很多局限,主要是效率低下,無法兼容質譜,以及會對色譜柱的填料造成難以逆轉的保留行為改變,這在實際應用過程中會帶來諸多不便。此外,通過特殊的色譜柱,如離子交換色譜柱、Hillc等實現離子型物質的保留和分離,也是一種積極的嘗試。

