新型冠狀病毒肺炎并發輕癥急性胰腺炎一例
姚利 盛健 朱琦 劉小玉 蔣鈺輝 戴希勇
1武漢市肺科醫院外科,武漢 430030;2武漢市肺科醫院結核科,武漢 430030
【提要】 新型冠狀病毒肺炎(COVID-19)是由新型冠狀病毒(2019-nCov)引起的急性呼吸道傳染性疾病,是一種新型傳染病。目前對COVID-19及其病原體2019-nCov知之甚少,尚未發現特效治療藥物。國內外尚無COVID-19治療過程中出現AP的報道,本文報道1例COVID-19并發AP的病例并復習相關文獻,以期分析其致病原因,為臨床醫師識別和處理提供參考。
患者女,44歲。因“發熱、嘔吐8 d,活動后胸悶3 d”入院。患者2020年1月17日無明顯誘因出現間斷發熱,最高體溫38℃,伴惡心、嘔吐,嘔吐物為胃內容物。1月21日出現活動后胸悶,無咳嗽、咳痰、腹痛、腹瀉等不適,胸部CT示雙肺散在多發的片狀、斑片狀磨玻璃樣稍高密度影(圖1)。1月24日復查CT示兩肺病灶明顯加重(圖2),咽拭子新型冠狀病毒(2019-nCov)核酸檢測陽性,1月25日以“新型冠狀病毒肺炎(COVID-19)重型”收住入院。既往因膽囊結石行膽囊切除術,有腎結石病史,否認其他病史及藥物過敏史,無煙酒史。入院體檢:體溫36.3℃,脈搏82次/min,呼吸頻率26次/min,血壓112/72 mmHg(1 mmHg=0.133 kPa),雙肺呼吸音清,未聞及明顯干濕啰音,心律齊,未聞及病理性雜音,腹軟,無壓痛、反跳痛,雙下肢無水腫。實驗室檢查:白細胞計數3.63×109/L、淋巴細胞計數0.6×109/L[正常參考值(1.1~3.2)×109/L)],血氣分析(吸氧狀態)、肝腎功能、凝血功能、甲功三項正常,尿、糞常規正常。入院后予吸氧,洛匹那韋/利托那韋、α-干擾素霧化抗病毒,哌拉西林他唑巴坦抗感染,注射用甲潑尼龍琥珀酸鈉抗炎(1月26-29日使用劑量為40 mg/次、2次/d,1月30-31日使用劑量為40 mg/次、1次/d),蘭索拉唑口服預防應激性潰瘍,胸腺五肽提升免疫力,葡萄糖、氨基酸、維生素C補液支持治療。1月27日復查胸部CT,與1月24日CT片相比,兩肺病灶有吸收。1月28日復查生物化學指標:總膽紅素28.62 μmol/L(正常參考值0~21.0 μmol/L)、直接膽紅素8.60 μmol/L(正常參考值0~6.80 μmol/L)、轉氨酶正常,三酰甘油4.37 mmol/L(正常參考值0.5~1.90 mmol/L),給予茵梔黃口服液降黃治療。1月31日早查房患者精神、食納可,訴胸悶、喘氣好轉,無發熱等不適,指氧飽和度98%(高鼻流量吸氧、流速50 L/min、氧濃度36%),復查轉氨酶、膽紅素正常,三酰甘油5.82 mmol/L。復查胸部CT,與1月27日CT片相比,兩肺病灶明顯吸收。1月31日患者突發上腹部疼痛,不能耐受,無畏寒、發熱,無腹瀉、惡心、嘔吐不適,持續約10 min后疼痛稍好轉。體檢:腹軟、劍突下及左上腹壓痛,無明顯反跳痛。急查血淀粉酶311 U/L(正常參考值43~116 U/L),心肌酶譜、心梗3項、心電圖正常。考慮AP,停注射用甲潑尼龍琥珀酸鈉及洛匹那韋/利托那韋,行禁食水、抗感染、補液對癥支持治療。患者仍有間斷腹痛,2月1日復查血淀粉酶505 U/L,尿淀粉酶1 742 U/L,加用奧曲肽抑酶、蘭索拉唑注射液抑酸治療。2月2日患者腹痛緩解,復查血淀粉酶361 U/L。2月5日,腹部CT平掃示胰腺尾部局限性輕度腫脹、增粗,周圍脂肪間隙模糊不清,密度增高(圖3、4)。肝臟形態大小正常,肝內外膽管無明顯擴張,膽囊術后改變,脾臟不大,雙腎多發結節狀高密度影,考慮胰腺炎,雙腎多發性結石。2月6日腹痛完全緩解,復查血淀粉酶正常。2月7日進食清淡流質食物后無腹痛等不適,期間連續2次咽拭子核酸檢測呈陰性,符合出院標準。2月8日出院,回家隔離休養。2月24日電話回訪患者一般情況良好,無發熱、腹痛等不適,復查胸部CT示肺部病灶進一步吸收。
討論AP是消化系統常見的危重疾病,早期發現、及時干預尤為重要。依據AP診斷標準[1],本例患者表現為急性、劇烈、持續上腹部疼痛,連續兩次血淀粉酶高于正常值3倍,腹部CT平掃提示胰腺炎可能,病程中無局部或全身并發癥及器官功能衰竭發生,診斷輕癥AP明確。患者發病時無畏寒、發熱癥狀且肝功能及膽紅素正常,無飲酒史,腹部CT未見膽道結石及膽管擴張,可除外常見的膽源性及酒精性AP[2]。
COVID-19疾病本身或其病原體2019-nCov是否會導致胰腺損傷尚不可知,COVID-19造成的缺氧及炎癥反應等可能導致AP。文獻報道重癥急性呼吸綜合征(severe acute repiratory syndrome,SARS)患者尸檢中明確胰腺有SARS-CoV病毒感染[3]。而2019-nCov病毒與蝙蝠SARS-Cov同源性達85%以上[4],故不排除2019-nCov病毒導致胰腺損傷所致AP。本例患者在病情好轉的情況下出現AP,且發生AP后經治療很快治愈,考慮2019-nCov病毒所致胰腺炎可能性小。藥物性胰腺炎是一種較罕見的胰腺炎類型,是指由于藥物本身或其代謝產物,或機體特異質反應引起的超敏反應導致的胰腺損傷,為藥物的不良反應[5]。目前國內外暫無統一的藥物性胰腺炎診斷標準,有研究[6]建議藥物性胰腺炎的診斷標準包括:(1)符合AP的診斷標準;(2)排除所有其他常見的病因;(3)可疑藥物用藥史;(4)潛伏期與大多數文獻報道一致;(5)停藥后癥狀減輕,血淀粉酶降低;(6)再次使用懷疑的藥物后癥狀復發(激發試驗陽性)。結合文獻報道[5,7]和用藥、停藥時間及AP發生及變化情況,本例患者1月31日突發AP,α-干擾素霧化、哌拉西林他唑巴坦、胸腺五肽、蘭索拉唑停用時間為2月8日,發生AP以后繼續使用病情仍好轉,以上藥物引起AP的可能性很小。茵梔黃口服液說明書中無AP相關不良反應,且未見相關文獻報道,其可能性也很小。注射用甲潑尼龍琥珀酸鈉及洛匹那韋/利托那韋說明書中明確指出可引起胰腺炎,且查閱到相關文獻支持[8-9]。本例患者發生AP前一直使用注射用甲潑尼龍琥珀酸鈉、洛匹那韋/利托那韋治療,停用并治療后患者明顯好轉,綜合分析注射用甲潑尼龍琥珀酸鈉或洛匹那韋/利托那韋導致本例AP可疑。本例患者住院期間三酰甘油均有不同程度升高,但多數<5.65 mmol/L,患者發病前無進食油膩食物誘因,高脂血癥性AP不能排除、但可能性較小[2]。注射用甲潑尼龍琥珀酸鈉及洛匹那韋/利托那韋均可引起血脂水平升高[10-11],本例患者三酰甘油逐漸升高也不排除其所致。綜合分析,考慮注射用甲潑尼龍琥珀酸鈉或洛匹那韋/利托那韋導致本例COVID-19患者治療中出現AP的可能性大,高脂血癥性AP及COVID-19疾病本身或2019-nCov病毒導致的AP的可能性相對較小。
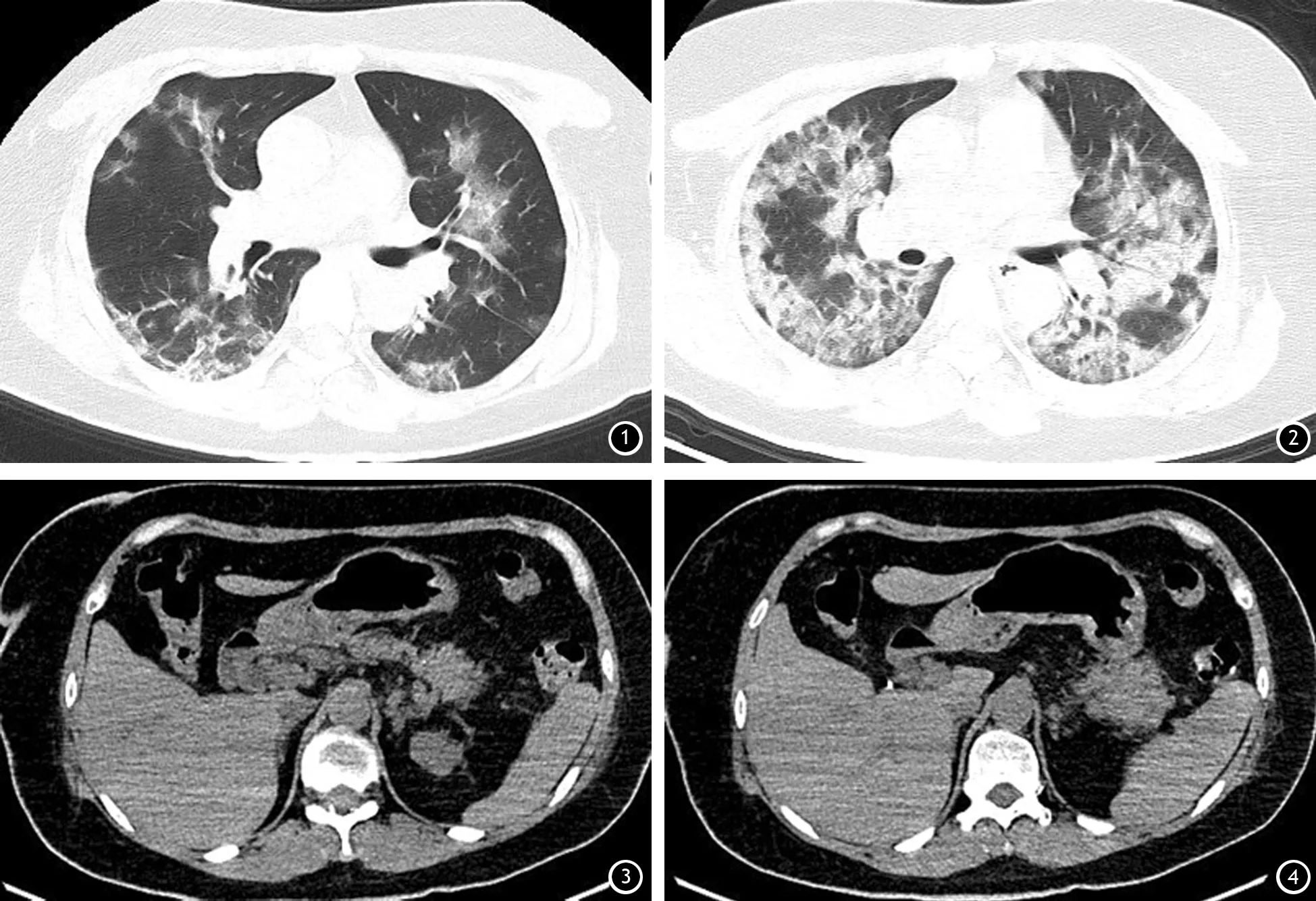
圖1~2 胸部CT示雙肺散在片狀、班片狀磨玻璃樣稍高密度影 圖3~4 腹部CT平掃示胰腺尾部局限性輕度腫脹、增粗,周圍脂肪間隙模糊不清,密度增高
除本病例外,筆者所在病區還發現2例COVID-19治療過程中出現上腹部疼痛及血淀粉酶升高的患者,兩例患者最高血淀粉酶分別為324 U/L、198 U/L,均未達到診斷AP的標準,但在立即停用注射用甲潑尼龍琥珀酸鈉及(或)洛匹那韋/利托那韋,按照AP行常規治療后腹痛均較快緩解,淀粉酶均逐漸恢復正常。目前尚無確定治療 COVID-19的有效藥物,糖皮質激素的使用存在爭議,洛匹那韋/利托那韋治療COVID-19的療效也尚不確定[12-13],兩者均存在導致血脂異常、血糖異常、胰腺炎等諸多不良反應[10-11],臨床使用時需注意監測,當出現AP等嚴重不良反應時應立即停用。
綜上所述,注射用甲潑尼龍琥珀酸鈉或洛匹那韋/利托那韋導致本例COVID-19患者治療中發生AP的可能性較大,臨床醫師在治療COVID-19過程中,對于患者出現的上腹部疼痛等癥狀需警惕發生AP,分析其致病原因并及時處理,以確保患者的治療安全。
利益沖突所有作者均聲明不存在利益沖突

